一种线粒体分裂抑制剂在制备防治危重症器官功能保护药物中的应用
1.本发明涉及医药生物技术领域,具体涉及一种线粒体分裂抑制剂在制备防治危重症器官功能保护药物中的应用。
背景技术:
2.多器官功能损害是covid-19感染、脓毒症和休克等危重症死亡的主要原因,心脏、血管、大脑、肠道等重要器官功能障碍对危重症患者的预后及死亡影响重大。危重症多器官功能损害的机理错综复杂,主要与以下几方面因素有关:低灌流导致的组织缺血缺氧;过度炎症反应导致的组织损伤;缺血再灌注损伤;毒性代谢产物积聚、酸碱平衡紊乱导致的机体内环境紊乱等。针对这些机制也提出了一些防治措施,如针对大量炎性因子释放和毒性产物蓄积采取血液净化和免疫吸附;针对感染清除原发病灶和抗感染;针对微循环功能障碍和组织低灌注采取改善微循环氧供和血流动力学支持等。
3.以上的措施有一定减缓病情及病程的效果,但结局并不理想,危重症患者通过常规液体复苏治疗,存在难以长时间维持血压,导致重要器官功能损害严重和救治时间有限的不足。而线粒体作为细胞有氧呼吸的主要场所,是缺血缺氧后较早发生损害的细胞器之一。因此,在此基础上,本发明提出了基于“线粒体分裂调控”保护危重症多器官功能的措施,线粒体分裂抑制剂mdivi-1 (mitochondrial division inhibitor 1)在制备新型危重症器官功能保护药物中的新用途。
技术实现要素:
4.针对现有技术存在的不足,本发明的目的是提出一种线粒体分裂抑制剂在制备防治危重症器官功能保护药物中的应用,以解决危重症患者通过常规液体复苏治疗,存在难以长时间维持血压,导致重要器官功能损害严重和救治时间有限的问题。
5.为达到上述目的,本发明采用如下技术方案:一种线粒体分裂抑制剂在制备防治危重症器官功能保护药物中的应用,所述线粒体分裂抑制剂为线粒体分裂抑制剂mdivi-1,所述的mdivi-1的化学分子式为c15h10c12n2o2s(3-(2,4-dichloro-5-methoxyphenyl)-2-sulfanyl-4 (3h)
‑ꢀ
quinazolinone),化学结构式为:。
6.采用上述技术方案时,mdivi-1抑制了线粒体分裂蛋白drp1(dynamin-related protein 1)的活性及其线粒体表达,保护了线粒体功能。mdivi-1通过保护危重症后血管收
缩张力,恢复血流动力学,改善血压维持情况,从而保护肝、肾、心脏等重要器官的血流灌注及其功能,改善动物预后及存活。
7.本发明还提供含有mdivi-1(3-(2,4-dichloro-5-methoxyphenyl)-2-sulfanyl-4 (3h)
‑ꢀ
quinazolinone)或以其为基础改造的、仍具有线粒体功能保护作用的化合物的复方药物在制备危重症器官功能保护药物中的应用。
8.与现有技术相比,本方案产生的有益效果是:(1)脓毒症和休克后,危重症模型的血管组织中drp1活性明显上调并大量转位到线粒体上。与常规lr复苏组相比,合并mdivi-1给药后可以明显抑制drp1 ser616位点磷酸化水平,减少其线粒体转位,抑制线粒体过度分裂,包括线粒体形态和线粒体功能。
9.(2)脓毒症和休克后,血管收缩功能明显减弱,与常规lr复苏组相比,合并mdivi-1给药后可明显提高危重症后血管收缩张力。
10.(3)脓毒症和休克后,肝肾血流灌注情况明显不足,使用常规lr复苏虽然可以快速补充肝脏和肾脏中的血流量,但是在复苏后2h肝脏灌注情况开始明显减弱,肾脏灌注情况更是几乎接近于危重症模型。合并mdivi-1给药后,肝肾血流灌注情况明显改善。
11.(4)脓毒症和休克后,心脏收缩功能和射血分数明显减弱,与常规lr复苏组相比,合并mdivi-1给药后可明显改善心脏功能。
附图说明
12.为了更清楚地说明本发明具体实施方式,下面将对具体实施方式中所需要使用的附图作简单地介绍。在所有附图中,各元件或部分并不一定按照实际的比例绘制。
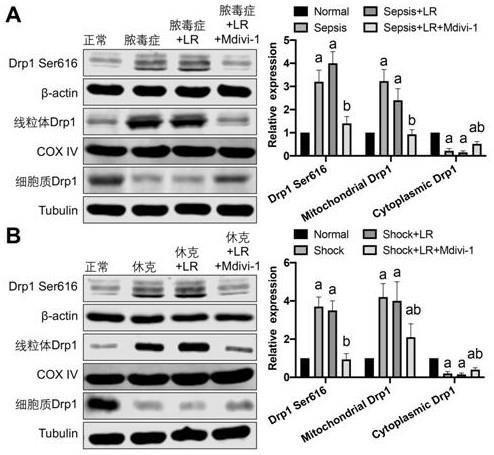
13.图1为本发明中显示mdivi-1给药后对脓毒症和休克大鼠肠系膜上动脉drp1活性及其表达分布的影响。
14.图2为本发明中显示mdivi-1给药后对脓毒症和休克大鼠肠系膜上动脉血管收缩张力的影响。
15.图3为本发明中显示mdivi-1给药后对脓毒症和休克大鼠肝脏和肾脏的血流灌注的影响。
16.图4为本发明中显示mdivi-1给药后对脓毒症和休克大鼠心脏收缩功能的影响。
具体实施方式
17.下面将结合附图对本发明技术方案的实施例进行详细的描述。以下实施例仅用于更加清楚地说明本发明的技术方案,因此只作为示例,而不能以此来限制本发明的保护范围。
18.本实施例中,线粒体分裂抑制剂为线粒体分裂抑制剂mdivi-1,用于在制备防治危重症器官功能保护药物中的应用。同时,含有mdivi-1(3-(2,4-dichloro-5-methoxyphenyl)-2-sulfanyl-4 (3h)
‑ꢀ
quinazolinone)或以其为基础改造的、仍具有线粒体功能保护作用的化合物的复方药物在制备危重症器官功能保护药物中的应用。
19.具体的,mdivi-1的化学分子式:c15h10c12n2o2s,分子量:353.22,化学结构如式i,为白色或卡其色固体,易溶dmso,不溶或难溶于水。
20.。
21.式imdivi-1是一个可穿越细胞膜的喹唑酮类化合物,也是血脑屏障通透性分子,能降低drp1蛋白(dynamin related protein 1)ser616位点磷酸化水平(ic
50
为1-10μm)。可与drp1变构位点结合以阻止drp1自组装和gtp水解。可诱导线粒体融合进一个巢样结构。还可以抑制线粒体外膜通透性,从而阻止凋亡和细胞色素c的释放。
22.动物实验1.动物:本实验选用8周龄健康成年清洁级sprague dawley(sd)大鼠,体重190-210 g,雌雄随机。由陆军特色医学中心动物实验中心提供。所有实验动物的喂养及实验程序均严格遵照实验动物保护条款。动物房内环境安静, 室温25
°
c左右,12h/天光照(7:00-19:00)。
23.2.主要试剂:mdivi
‑ꢀ
1(tocris公司,美国),乳酸林格氏液(lr)(四川科伦药业,中国),去甲肾上腺素(ne)(远大医药,中国),戊巴比妥钠(sigma 公司,美国),戊二醛(sigma 公司,美国),肝素钠(北京酷来搏公司,中国),drpl抗体(abcam公司,美国),phospho-drpl (ser616)抗体(cst公司,美国),cox iv抗体(abcam公司,美国),β-actin抗体(abcam公司,美国),tubulin抗体 (cst公司,美国),线粒体分离提取试剂盒(invent公司,美国)。
24.3.主要实验仪器:激光散斑血流成像仪(perimed公司,瑞典),活体成像显微镜(奥林巴斯公司,日本),恒温离体器官灌流浴槽(letica 公司,西班牙),小动物超声机(迈瑞公司,中国),垂直电泳系统,凝胶成像分析系统(bio-rad公司,美国),odyssey红外激光扫描成像系统(li-cor公司,美国),动静脉管(ad instrument 公司,澳大利亚)。
25.4.实验方法:(1)模型建立脓毒症模型制备:选用8周龄sd大鼠,术前12h禁食,自由饮水,腹腔注射3%戊巴比妥钠(30mg/kg)。将大鼠仰卧固定于手术板上,腹部手术区常规消毒与去毛,无菌条件下用手术刀在腹壁作一长约2cm切口,经切口进腹在回盲瓣远端分离并以3号丝线结扎1/3处盲肠。用18号注射针头于结扎端穿孔,并挤出粪便少许,尽量避免损伤血管,然后用4号丝线间断缝合腹膜及皮肤,然后皮下注射生理盐水(50ml/kg)并按揉腹部,使腹内粪便均匀散布于腹腔中,等待12h腹内感染后即达到脓毒症模型标准。
26.休克模型制备:选用8周龄sd大鼠,术前12h禁食,自由饮水,腹腔注射3%戊巴比妥钠(30mg/kg)。在大鼠股动脉对应皮肤位置剪一切口,用止血钳进行钝性分离,暴露股动脉后进行穿刺插管(导管内径0.58mm,外径0.95mm),经导管注射肝素钠生理盐水(500 u/kg)抗凝后,使用三通旋塞连接水银血压计和注射器,用于血压观察和放血处理,术毕后稳定
10min。使用注射器通过股动脉导管匀速抽血的方式进行失血处理,标准为15min内血压降至40mmhg,放血量大约为整体血量的50%左右(以200g大鼠为例,总血量占体重7%,约为14ml,放血量大约为7ml左右),维持血压40mmhg的休克状态4h。
27.(2)mdivi-1药物治疗将造好模的大鼠分为两组,常规液体复苏组(lr组)是依照临床处理方式采用输液泵进行匀速输注,对于脓毒症模型的复苏方式为在30min内经右侧股静脉按大鼠体重35ml/kg的液体体积输注,对于休克模型的复苏方式为在30min内经右侧股静脉按2倍失血量的液体体积进行输注。mdivi-1给药组(mdivi-1组)是在lr 复苏液基础上按照1mg/kg的剂量加入mdivi-1溶液,混匀后进行输注。
28.(3)蛋白质免疫印迹取休克模型和脓毒症模型血管组织,置于ep管中,在低温液氮下碾碎成粉末,加入ripa裂解液120ul,吹打混匀后于冰上裂解40min,离心,取上清,加入蛋白缓冲液,分别提取总蛋白,细胞质蛋白和线粒体蛋白,吹打均匀后105℃孵育6min,于-80℃保存。蛋白样品进行上样、跑胶、转膜、孵育一抗和二抗,最后显影。odyssey曝片机曝片,总蛋白内参β-actin,线粒体内参cox iv,细胞质内参是tubulin,通过目的蛋白与相应内参比较后反映蛋白表达变化。
29.(4)血管收缩张力检测大鼠模型制备并治疗处理后,用配有 37℃恒温装置的活体成像显微镜下,观察直径在 30-50κm 之间,200κm长无分支,无明显弯曲的肠系膜动脉,用浓度为10-3
mol/l的ne溶液100ul刺激血管收缩。通过连接在显微镜上的ccd 彩色摄像机(olympus,dp21)显示屏上(cellsens entry)观察,记录血管管径变化反映血管收缩张力。
30.(5)肝肾血流量测定大鼠模型制备并治疗处理后,麻醉大鼠并置于鼠板上,剪开腹部,充分暴露肝脏和肾脏。将低能量的氦-氖激光器探头分别置于肝脏和肾脏上14cm处,检测大鼠肝脏和肾脏的血流量。用激光散斑血流成像仪连续监测大鼠肝脏和肾脏血流灌注情况。
31.(6)大鼠心脏超声观察大鼠模型制备并治疗处理后,麻醉大鼠并置于鼠板上,使用小动物超声机经胸超声探查。用m型超声心动图从左胸骨旁长轴切面测量左心室收缩功能。计算左室短轴缩短率(fs)、射血分数(ef)等左心室功能参数。
32.5.主要结果5.1 mdivi-1给药后能够抑制脓毒症和休克大鼠drp1活性,减少其线粒体转位。
33.请参阅图1a,脓毒症后血管组织drp1 ser616活性明显增高,线粒体drp1表达上调,细胞质drp1表达下调,提示脓毒症后drp1发生了线粒体转位。使用常规lr复苏无法有效干预drp1活性及其线粒体转位,合并mdivi-1给药后drp1活性减少65.4%,线粒体drp1表达减少61.3%。
34.请参阅图1b,休克后血管组织drp1 ser616活性明显增高,线粒体drp1表达上调,细胞质drp1表达下调,提示休克后drp1发生了线粒体转位。使用常规lr复苏无法有效干预drp1活性及其线粒体转位,合并mdivi-1给药后drp1活性减少73.2%,线粒体drp1表达减少47.5%。
35.5.2 mdivi-1给药后能够改善脓毒症和休克大鼠血管收缩张力。
36.请一并参阅图2a,在血管活性药物ne的刺激下,使用常规lr复苏的脓毒症大鼠血管管径几乎没有发生变化,提示常规lr复苏无法提高脓毒症血管活性药物的救治效果,而合并mdivi-1给药后,血管管径收缩情况改善73%。
37.请一并参阅图2b,在血管活性药物ne的刺激下,使用常规lr复苏的脓毒症大鼠血管管径几乎没有发生变化,提示常规lr复苏无法提高脓毒症血管活性药物的救治效果,而合并mdivi-1给药后,血管管径收缩情况改善62%。
38.5.3 mdivi-1给药后能够改善脓毒症和休克大鼠肝肾血流灌注。
39.请一并参阅图3,使用常规lr复苏的脓毒症大鼠虽然可以快速补充肝脏和肾脏的血流量,但是在复苏后2h肝脏灌注情况开始明显减弱,肾脏灌注情况更是几乎没有效果,而合并mdivi-1给药后肝肾血流灌注情况明显改善。
40.使用常规lr复苏的休克大鼠在复苏后3h肝脏和肾脏灌注情况开始明显减弱,而合并mdivi-1给药后可以很好地维持肝肾血流灌注情况(图3c-d)。
41.5.4 mdivi-1给药后能够改善脓毒症和休克大鼠心脏收缩功能。
42.请一并参阅图4,使用常规lr复苏的脓毒症和休克大鼠无法有效改善心脏收缩功能,而合并mdivi-1给药后心脏收缩功能和左室射血分数明显增强。
43.以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围,其均应涵盖在本发明的权利要求和说明书的范围当中。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1