泰妙菌素在制备用于治疗银屑病的药物中的应用
1.本发明涉及一种化合物在制备用于治疗皮肤病的药物中的新的应用,特别涉及一种化合物在制备用于治疗银屑病的药物中的应用,属于医药技术领域。
背景技术:
2.银屑病(俗称牛皮癣),是一种常见的慢性炎症性皮肤病,全世界的发病率约为1%,寻常型银屑病是银屑病最常见的亚型,典型的临床表现为鳞屑性红斑或斑块,皮损可局部或广泛分布,其反复发作的临床特点给患者造成巨大的经济和心理压力也给临床医疗造成了很多的困难。
3.传统针对银屑病的局部治疗主要采用外用糖皮质激素进行治疗,然而长期外用糖皮质激素可能导致皮肤出现萎缩、多毛等一系列不良反应。
4.近年来针对银屑病发病的关键炎症因子例如肿瘤坏死因子α(tumor necrosis factor alpha,tnf-α),白介素17(interleukin 17,il-17)的单克隆抗体药物开发取得了进展。然而,如阿达木单抗(adalimumab,tnf-α单克隆抗体)和司库奇尤单抗(il-17单克隆抗体)等药物具有较多固有的缺陷,如价格昂贵、无法口服与外用以及长期使用的严重副作用等。
5.故而针对银屑病的药物开发是目前实验研究和临床实践急待解决的重大问题之一。近年来的研究表明小分子药物具有成本低、给药方法灵活等诸多优点,故而寻找和开发针对银屑病的小分子药物是目前研究的热点。
6.本发明采用咪喹莫特(imiquimod,imq)诱导形成银屑病动物模型,并通过灌胃和外用给药延胡索酸泰妙菌素(tiamulin fumarate,tf),然后检测其对银屑病的治疗效果。实验结果表明灌胃或外用给药泰妙菌素均能显著缓解咪喹莫特诱导的红斑和鳞屑,减少皮肤增殖相关因子ki67的表达,并降低pasi评分和皮肤增厚。免疫印迹结果提示泰妙菌素可以抑制tnf-α诱导的nf-κb(nuclear factor-κgene binding)和mapk(mitogen activated protein kinase)通路激活。以上结果显示,泰妙菌素可以通过抑制tnf-α及其下游炎症通路进而改善imq诱导的银屑病症状,且该小分子可以通过外用给药,所以副作用相对较小,对于全身的影响也小,故其可在银屑病的治疗药物中得到应用。
7.泰妙菌素是一种截短侧耳素类兽用抗生素,于1976年被开发,针对该化合物的研究主要集中在抗菌方面,关于其治疗银屑病的研究,迄今未见报道。本发明主要发现了泰妙菌素对咪喹莫特诱导的小鼠银屑病样模型具有显著的改善作用,免疫印迹实验结果提示泰妙菌素具有拮抗tnf-α及其通路效应,故其可在银屑病的治疗药物中得到应用。
技术实现要素:
8.本发明的目的是针对目前治疗银屑病过程中,现有药物存在诸多不足,生物大分子药物存在无法口服和外用以及长时间使用具有严重的副作用的技术缺陷,提供一种小分子化合物泰妙菌素在制备用于治疗银屑病药物或保健品中的应用,本发明的泰妙菌素能显
著缓解银屑病的红斑和鳞屑,减少皮肤增厚;泰妙菌素可明显抑制tnf-α下游炎症nf-κb、mapk通路,进而改善银屑病症状;而且泰妙菌素还可以通过外用给药发挥作用,鉴于外用给药可显著减少副作用,对于全身的影响更小,可在银屑病的治疗药物中得到更好的应用。
9.为实现本发明的目的,本发明一方面提供一种泰妙菌素或泰妙菌素类似物在制备用于治疗慢性炎症性皮肤病药物或保健品中的应用。
10.其中,所述慢性炎症性皮肤病为银屑病、特异性皮炎,优选为银屑病。
11.特别是,所述银屑病为寻常型银屑病。
12.其中,所述药物由泰妙菌素和药学上可接受的载体组成
13.特别是,药学上可接受的载体通常被保健专家认可用于这一目的且作为药剂的非活性成分。有关药学上可接受的载体的汇编可以在《药物赋形剂手册》(handbook of pharmaceutical excipients,第2版,由a.wade和p.j.weller编辑;american pharmaceutical association出版,washington and the pharmaceutical press,london,1994)等工具书中找到。
14.尤其是,所述的载体包括赋形剂,如淀粉、水等;润滑剂,如硬脂酸镁等;崩解剂,如微晶纤维素等;填充剂,如乳糖等;粘结剂,如预胶化淀粉、糊精等;甜味剂;抗氧化剂;防腐剂、矫味剂、香料等;
15.其中,所述药物是通过经胃肠道给药和非经胃肠道给药途径给药。
16.特别是,所述的非经胃肠道给药途径选择注射给药、呼吸道给药、皮肤给药、粘膜给药或腔道给药。
17.其中,所述药物以片剂、胶囊剂、丸剂、散剂、颗粒剂、糖浆剂、溶液剂、注射剂、喷雾剂、气雾剂、贴剂等形式存在。
18.其中,非经胃肠道给药药剂选择注射剂、喷雾剂、气雾剂、贴剂、酊剂、粉剂、糊剂、洗剂、乳膏剂、霜剂、软膏剂等。
19.特别是,所述的经胃肠道给药制剂选择片剂、胶囊剂、散剂、颗粒剂、丸剂、溶液剂或糖浆剂等。
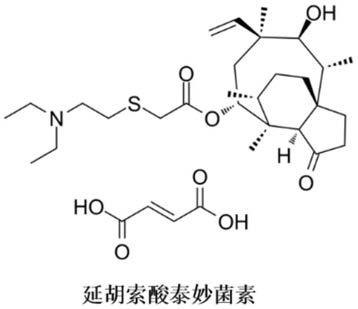
20.尤其是,所述泰妙菌素为延胡索酸泰妙菌素。
21.其中,延胡索酸泰妙菌素的结构如下:
[0022][0023]
本发明另一方面提供一种用于治疗银屑病的药物或保健品,包括泰妙菌素或泰妙菌素类似物。
[0024]
其中,所述药物由泰妙菌素和药学上可接受的载体组成。
[0025]
特别是,所述泰妙菌素为延胡索酸泰妙菌素。
[0026]
特别是,所述的载体包括赋形剂,如淀粉、水等;润滑剂,如硬脂酸镁等;崩解剂,如微晶纤维素等;填充剂,如乳糖等;粘结剂,如预胶化淀粉、糊精等;甜味剂;抗氧化剂;防腐剂、矫味剂、香料等;
[0027]
所述药物可以采用本领域公知的方法制成各种剂型,如片剂、胶囊剂、丸剂、散剂、颗粒剂、糖浆剂、溶液剂、注射剂、喷雾剂、气雾剂、贴剂、酊剂、粉剂、糊剂、洗剂、乳膏剂、霜剂、软膏剂等;
[0028]
本发明还提供一种治疗银屑病的方法,包括给予治疗有效量的泰妙菌素。
[0029]
其中,动物口服治疗有效剂量为100mg-300mg/kg;外用有效浓度为5%。
[0030]
除非另外说明,本文所用的术语“治疗有效量”为需要产生有效作用的药物的用量;“治疗有效量”是可以调整和变化的,最终由医务人员确定,其所考虑的因素包括给药途径和制剂的性质、接受者的体重、年龄等一般情况以及所治疗疾病的性质和严重程度。
[0031]
与现有技术相比,本发明具有如下优点:
[0032]
泰妙菌素可以改善咪喹莫特诱导的小鼠模型的银屑病症状,而且该小分子还可以通过外用给药,副作用相对较小,对于全身的影响也小,故其可在银屑病的治疗中得到应用。
[0033]
本发明对已知化合物泰妙菌素发掘了新的药用价值,将其用于治疗银屑病,并可制备成预防、缓解和治疗银屑病的药物,从而为泰妙菌素的应用开拓了一个新的应用领域。
[0034]
本发明的泰妙菌素治疗银屑病的药理作用强,可以缓解咪喹莫特诱导的银屑病样皮炎,降低银屑病皮损面积及严重程度评分(psoriatic area and severity index,pasi)和皮肤异常增殖,抑制皮肤增殖相关因子ki67的表达。免疫印迹实验提示泰妙菌素可以抑制tnf-α诱导的nf-κb、mapk通路激活,进而达到治疗银屑病。
[0035]
泰妙菌素用于治疗银屑病的功效显著,毒副作用小、安全性好,尤其是可以通过外用给药,具有良好的药用前景。
[0036]
本发明的泰妙菌素临床使用安全,制备工艺简单,可制成口服、外用剂型,使用方便,因此易于推广。
附图说明
[0037]
图1a为实施例1中小鼠背部皮肤变化、皮损he染色图,其中左侧为背部皮肤变化图,右侧为皮损he染色图;
[0038]
图1b为实施例1中小鼠皮肤ki67免疫组织化学染色观察图;
[0039]
图1b-1为实施例1中小鼠皮肤免疫组织化学染色ki67阳性细胞统计图;
[0040]
图1c为实施例1中小鼠背部皮损程度pasi评分曲线图;
[0041]
图1d为实施例1中小鼠背部表皮层厚度测定图;
[0042]
图2a为实施例3中小鼠背部皮肤变化、皮损he染色图,其中左侧为背部皮肤变化图,右侧为皮损he染色图;
[0043]
图2b为实施例3中小鼠皮肤ki67免疫组织化学染色观察图;
[0044]
图2b-1为实施例3中小鼠皮肤免疫组织化学染色ki67阳性细胞的统计图;
[0045]
图2c为实施例3中小鼠背部皮损程度pasi评分曲线图;
[0046]
图2d为实施例3中小鼠背部表皮层厚度测定图;
[0047]
图3为本发明实施例4中泰妙菌素对tnf-α诱导的hacat细胞系的免疫印迹电泳检测图。
具体实施方式
[0048]
下面结合具体实施例来进一步描述本发明,本发明的优点和特点将会随着描述而更为清楚。但这些实施例仅是范例性的,并不对本发明的范围构成任何限制。本领域技术人员应该理解的是,在不偏离本发明的精神和范围下可以对本发明技术方案的细节和形式进行修改或替换,但这些修改和替换均落入本发明的保护范围内。
[0049]
以下通过试验例来进一步阐述本发明所述药物的有益效果,这些试验例包括了本发明药物的药效学试验。
[0050]
实施例1灌胃给药泰妙菌素对咪喹莫特诱导的小鼠银屑病模型的影响
[0051]
1、试验材料
[0052]
1.1实验动物、试剂
[0053]
7-8周龄的balb/c小鼠,雄性,由集萃药康动物生物科技实验中心提供,合格证编号:scxk(苏)2018-0008。
[0054]
延胡索酸泰妙菌素(购自medchemexpress公司)溶解于水中,配制成浓度为25mg/ml的延胡索酸泰妙菌素溶液;
[0055]
左氧氟沙星(levofloxacin,购自medchemexpress公司)溶解于水中,配制成浓度为10mg/ml的左氧氟沙星溶液;
[0056]
5%咪喹莫特乳膏(购自四川明欣药业有限公司);凡士林软膏(购自联合利华公司),ki67抗体(购自abcom公司)。
[0057]
1.2实验方法
[0058]
将30只7-8周龄的雄性balb/c小鼠,随机分为5组,每组6只,背部剃毛(面积:2cm
×
3cm),正常饲养,三天后分别在小鼠剃毛处给予不同处理,具体操作如下:
[0059]
空白对照组(control):小鼠背部皮肤涂抹凡士林62.5mg/只/天,持续5天;
[0060]
模型组(imq):小鼠背部皮肤涂抹imq(咪喹莫特)62.5mg/只/天,持续5天;
[0061]
安慰剂组(imq+placebo(安慰剂:左氧氟沙星)):小鼠背部皮肤涂抹imq 62.5mg/只/天,持续5天;涂抹imq之前,灌胃给予左氧氟沙星10mg/kg;
[0062]
低剂量治疗组(imq+tf 100mg/kg):小鼠背部皮肤涂抹imq 62.5mg/只/天,持续5天;涂抹imq之前,灌胃给予tf 100mg/kg;
[0063]
高剂量治疗组(imq+tf 300mg/kg):小鼠背部皮肤涂抹imq 62.5mg/只/天,持续5天;涂抹imq之前,灌胃给予tf 300mg/kg。
[0064]
上述各组小鼠正常喂食饮水,每天观察小鼠皮肤表现,并给予pasi评分,第6天处死小鼠取小鼠皮损进行he染色并测量表皮厚度、并对皮损皮肤进行免疫组织化学染色。
[0065]
pasi评分设有3个评价指标,根据小鼠背部皮损严重程度,分别给予0-4分,三项评分汇总为pasi评分总分。pasi评分具体如下:
[0066]
1、红斑:对身小鼠背部红斑的评分采用以下评分:
[0067]
无症状0;轻度1;中度2;重度3;极其严重4。
[0068]
2、浸润:对小鼠背部浸润的评分采用以下评分:
[0069]
无症状0;轻度1;中度2;重度3;极其严重4。
[0070]
3、脱屑:对小鼠背部脱屑的评分采用以下评分:
[0071]
无症状0;轻度1;中度2;重度3;极其严重4。
[0072]
第6天处死小鼠,小鼠背部皮肤组织用10%福尔马林固定48h,石蜡包埋;
[0073]
切取5μm厚的石蜡切片进行苏木精和伊红(h&e)染色,然后在40x视野下拍照,并使用软件image j在每张切片的垂直横截面上测量表皮厚度。计算每只小鼠5个随机点平均值即得表皮厚度。
[0074]
切取5μm厚的石蜡切片进行ki67免疫组织化学染色,一抗使用(abcam,ab6721,1:400稀释)。在40x视野下拍照,并使用软件image j在100x视野下对ki67阳性细胞数量进行统计,计算每只小鼠3个随机视野下ki67阳性细胞的平均值。
[0075]
1.3实验结果
[0076]
各组小鼠背部皮肤第6天的变化及皮损he染色(40x),结果如图1a。
[0077]
由图1a可知:与空白对照组相比,模型组(imq)和安慰剂组(imq+placebo)小鼠背部皮肤可见明显的红斑、鳞屑;he染色可见表皮明显的角化过度与角化不全,真皮浅层可见大量炎症细胞浸润。低剂量组治疗(imq+tf 100mg/kg)和高剂量治疗组(imq+tf 300mg/kg)均提示药物灌胃治疗后红斑和鳞屑明显缓解,其中高剂量治疗组皮损缓解更为明显。
[0078]
图1b为不同处理组小鼠皮肤ki67免疫组织化学染色观察图(40x);
[0079]
与空白对照组相比,模型组(imq)的皮肤基底层细胞ki67免疫组织化学染色显著增强,低剂量治疗组(imq+tf 100mg/kg)和高剂量治疗组(imq+tf 300mg/kg)皮肤基底层细胞ki67免疫组织化学染色减弱,其中高剂量治疗组染色减弱更显著。
[0080]
图1b-1为不同处理组小鼠皮肤ki67免疫组织化学染色统计图,即不同处理组小鼠皮肤ki67免疫组织化学染色高倍镜显微镜视野下100x使用软件image j对视野中ki67阳性细胞数量进行计数,计算每只小鼠3个随机视野ki67阳性细胞的平均值,使用独立样本t检验进行统计。
[0081]
空白对照组vs模型组:****p《0.0001;低剂量治疗组vs模型组:*p《0.05;高剂量治疗组vs模型组:**p《0.01。
[0082]
pasi评分结果如图1c,评分结果显示tf药物治疗后评分下降,高剂量组评分下降更明显。使用双因素方差分析(two-way anova)进行统计。低剂量治疗组vs模型组,第四天:*p《0.05,第五天:**p《0.01,第六天:**p《0.01。高剂量治疗组vs模型组,第四天:**p《0.01,第五天:***p《0.001,第六天:****p《0.0001。
[0083]
表皮厚度测定结果如图1d:40x显微镜视野下,使用软件image j在每张切片的垂直横截面上测量表皮层的厚度。计算每只小鼠5个随机点表皮厚度的平均值,使用独立样本t检验进行统计。空白对照组vs模型组:****p《0.0001;低剂量治疗组vs模型组:*p《0.05;高剂量治疗组vs模型组:**p《0.01。
[0084]
实施例1的实验表明,在咪喹莫特诱导的银屑病小鼠模型中,口服泰妙菌素可以缓解咪喹莫特诱导的银屑病样皮炎,表明泰妙菌素具有治疗银屑病的效应。
[0085]
实施例2制备泰妙菌素乳膏剂
[0086]
1)按照如下配方备料:
[0087][0088]
2)制备泰妙菌素乳膏剂
[0089]
称取延胡索酸泰妙菌素(1g)置于烧杯内,加入10g纯化水,超声使泰妙菌素溶解,然后加入液体石蜡、尼泊金乙酯、吐温80、硅油,加热使溶解,再依次加入单硬脂酸甘油酯、十八醇、甘油、平平加,边加热边搅拌,使融化,最后加入纯化水补足至20g,搅拌至凝固,即得泰妙菌素乳膏剂。
[0090]
实施例2a制备安慰剂乳膏
[0091]
1)按照如下配方备料:
[0092][0093][0094]
2)制备安慰剂乳膏
[0095]
将10g纯化水置于烧杯内,接着加入液体石蜡、尼泊金乙酯、吐温80、硅油,加热使溶解,再依次加入单硬脂酸甘油酯、十八醇、甘油、平平加,边加热边搅拌,使融化,最后加入纯化水补足至20g,搅拌至凝固,制得泰妙菌素慰剂,备用。
[0096]
实施例2b制备泰妙菌素软膏剂(油性基质)
[0097]
1)按照如下配方备料:
[0098]
延胡索酸泰妙菌素
ꢀꢀꢀꢀꢀꢀꢀꢀ
1.0g
[0099]
白凡士林
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
17.0g
[0100]
羊毛脂
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
2.0g
[0101]
2)制备泰妙菌素软膏剂
[0102]
将白凡士林和羊毛脂置于烧杯内,加热使其完全融化,加入延胡索酸泰妙菌素(1g)快速搅拌均匀,停止加热后搅拌至凝固,制得泰妙菌软膏剂。
[0103]
实施例2c制备泰妙菌素软膏剂(水性基质)
[0104]
1)按照如下配方备料:
[0105][0106]
2)制备泰妙菌素软膏剂(水性基质)
[0107]
称取延胡索酸泰妙菌素(1g)置于烧杯内,加入10g纯化水,超声使泰妙菌素溶解,然后加入硬脂酸、山梨醇酐单硬脂酸酯、吐温60边加热边搅拌,使融化,最后加入纯化水补足至20g,搅拌至凝固,即得泰妙菌素软膏剂。
[0108]
实施例3局部给药泰妙菌素对咪喹莫特诱导的小鼠银屑病模型的影响
[0109]
1、试验材料
[0110]
1.1实验动物、试剂
[0111]
实施例2、2a制备的泰妙菌素乳膏剂、安慰剂。
[0112]
7-8周龄的balb/c小鼠,雄性,由集萃药康动物生物科技实验中心提供,合格证编号:scxk(苏)2018-0008。
[0113]
咪喹莫特乳膏(购自四川明欣药业有限公司);凡士林软膏(购自联合利华公司),ki67抗体(购自abcom公司)。
[0114]
1.2实验方法
[0115]
将24只7-8周龄的雄性balb/c小鼠,随机分为4组,每组6只,背部剃毛(面积:2cm
×
3cm),正常饲养,三天后分别在小鼠剃毛处给予不同处理,具体操作如下:
[0116]
空白对照组(control):小鼠背部皮肤涂抹凡士林62.5mg/只/天,持续5天;
[0117]
造模组(imq):小鼠背部皮肤涂抹imq 62.5mg/只/天,持续5天;
[0118]
安慰剂组(imq+placebo(实施例2a制备的安慰剂)):小鼠背部皮肤涂抹imq62.5mg/只/天,持续5天;每天涂抹imq 6小时后,再涂抹等剂量安慰剂。
[0119]
治疗组(imq+tf 5%):小鼠背部皮肤涂抹imq 62.5mg/只/天,持续5天;每天涂抹imq 6小时后,再涂抹等剂量的实施例2制备的5%泰妙菌素乳膏。
[0120]
上述各组小鼠正常喂食饮水,每天观察小鼠皮肤表现,并给予pasi评分,第6天处死小鼠取小鼠皮损进行he染色并测量表皮厚度、并对皮损皮肤进行免疫组织化学染色。
[0121]
pasi评分标准与实施例1相同;第6天处死小鼠,小鼠背部皮肤组织用10%福尔马林固定48h,石蜡包埋;苏木精和伊红(h&e)染色方法与实施例1相同;皮损表皮厚度的测定与实施例1相同;ki67免疫组织化学染色与实施例1相同。
[0122]
1.3实验结果
[0123]
各组小鼠背部皮肤第6天的变化及皮损的he染色(40x),结果如图2a。
[0124]
由图2a可知:相比于空白对照组(control)小鼠,造模组(imq)和安慰剂组(imq+palcebo)小鼠背部皮肤可见明显的红斑、鳞屑;he染色可见表皮明显的角化过度与角化不全,真皮浅层可见大量炎症细胞浸润。治疗组(imq+tf 5%)提示药物外用治疗后红斑和鳞屑明显缓解。
[0125]
图2b为不同处理组小鼠皮肤ki67免疫组织化学染色观察图(40x);
[0126]
与空白对照组相比,模型组(imq)的皮肤基底层细胞ki67免疫组织化学染色显著增强,治疗组(tf 5%)皮肤基底层细胞ki67免疫组织化学染色减弱。
[0127]
图2b-1为不同处理组小鼠皮肤ki67免疫组织化学染色统计图,即不同处理组小鼠皮肤ki67免疫组织化学染色高倍镜显微镜视野下(100x)使用软件image j对视野中ki67阳性细胞数量进行计数,计算每只小鼠3个随机视野ki67阳性细胞的平均值,使用独立样本t检验进行统计,空白对照组vs模型组:****p《0.0001;治疗组vs模型组:***p《0.001。
[0128]
pasi评分结果如图2c,评分结果显示tf药物治疗后评分下降。使用双因素方差分析(two-way anova)进行统计。治疗组vs模型组,第三天:**p《0.01,第四天:****p《0.0001,第五天:***p《0.001,第六天:****p《0.0001。
[0129]
不同处理组小鼠的表皮厚度测定结果如图2d:40x显微镜视野下,使用软件image j在每张切片的垂直横截面上测量表皮层的厚度。计算每只小鼠5个随机点表皮厚度的平均值,使用独立样本t检验进行统计。空白对照组vs模型组:****p《0.0001;治疗组vs模型组:****p《0.0001。
[0130]
实施例3的实验表明,在咪喹莫特诱导的银屑病小鼠模型中,外用泰妙菌素可以缓解咪喹莫特诱导的银屑病样皮炎,在皮肤疾病中外用给药更加的高效和便捷。
[0131]
实施例4泰妙菌素对tnf-α刺激的hacat细胞系的影响
[0132]
1、试验材料
[0133]
取对数生长期的人表皮永生化细胞hacat系进行实验;
[0134]
人源的tnf-α溶于纯化水中,浓度为10ng/ml;tf溶于二甲基亚砜中,制成浓度分别为50μm、100μm的tf溶液;adalimumab(阿达木单抗,购买自medchemexpress公司)为阳性对照,溶于纯化水中,浓度为10μg/ml。免疫印迹第一抗体均购自cst(cell signaling technology)公司,分别为:iκbα(#4814),p65(#8242),p-p65(#3033),p-erk(#4370),p-jnk(#4668)。
[0135]
1.2实验方法
[0136]
分为5组,具体操作如下:
[0137]
空白对照组(control,简称k组):hacat细胞系提取蛋白,即以使用ripa裂解液提取的hacat细胞的蛋白作为空白对照;
[0138]
刺激组(tnf-α,简称c组):hacat细胞系予以10ng/ml的tnf-α刺激30分钟,然后使用ripa裂解液提取hacat细胞蛋白;
[0139]
低剂量tf组(tnf-α+tf 50μm,简称d组):使用50μm的tf预处理hacat细胞2小时;接着使用10ng/ml tnf-α刺激hacat细胞30分钟,然后使用ripa裂解液提取hacat细胞蛋白;
[0140]
高剂量tf组(tnf-α+tf 100μm,简称g组):使用100μm的tf预处理hacat细胞2小时,
接着使用10ng/ml tnf-α刺激hacat细胞30分钟,然后使用ripa裂解液提取hacat细胞蛋白;
[0141]
阳性对照组(tnf-α+adalimumab 10μg/ml,简称y组):使用100μg/ml的adalimumab预处理hacat细胞2小时,接着使用10ng/ml tnf-α刺激hacat细胞30分钟,然后使用ripa裂解液提取hacat细胞蛋白;其中使用ripa裂解液提取hacat细胞蛋白的具体方法如下:
[0142]
室温下,向细胞中加入100μl ripa裂解液,裂解2分钟后收集液体至离心管中,高速离心机4℃10000转/min离心10分钟,吸取上清即得蛋白样品。室温下使用恒压法150v和4-20%十二烷基硫酸钠聚丙烯酰胺凝胶(bio-rad)进行电泳分离等量的蛋白样品;使用半干转膜法将蛋白转移到pvdf膜(bio-rad);室温下使用5%的脱脂奶粉封闭pvdf膜1小时;4℃下pvdf膜与一抗(即免疫印迹第一抗体)孵育过夜,随后在室温下与辣根过氧化物酶二抗(abclonal)孵育1小时。使用gel-doc xr成像实验室系统(bio-rad)检测和分析化学发光信号。
[0143]
1.3实验结果
[0144]
nf-κb相关蛋白iκbα、p-p65、p65免疫印迹检测结果如图3,相比于空白对照组和阳性对照组,刺激组可见iκbα显著下调,而p-p65、p-erk和p-jnk显著上调,p65无明显变化,表明tnf-α有效激活nf-κb和mapk通路相关蛋白。
[0145]
tf给药组中,低剂量和高剂量tf均可以显著抑制tnf-α诱导的iκbα下调和p-p65、p-jnk上调,高剂量tf可以抑制tnf-α诱导的p-erk上调。该结果提示在hacat细胞系中,tf可以显著抑制tnf-α对其下游nf-κb、mapk通路的激活。
[0146]
实施例4结果表明在体外实验中tf可以直接抑制tnf-α所激活的mapk、nf-κb炎症通路。而mapk和nf-κb银屑病中均显著上调。故而tf可以抑制mapk、nf-κb的激活,最终达到对银屑病的治疗作用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1