一种NLRP3抑制剂
一种nlrp3抑制剂
技术领域
1.本发明属于小分子药物领域,特别涉及一种nlrp3抑制剂。
背景技术:
2.nlrp3炎症小体是由感受器分子nlrp3、衔接蛋白asc和效应蛋白前体procaspase-1三个部分组成一种蛋白复合物体,其可感受机体内各种危险信号而被激活,进而剪切细胞因子il-1β和il-18,以及打孔蛋白gasdermin d,促进炎症反应和引起细胞凋亡。自从于2002年被发现以来,大量研究表明nlpr3炎症小体与阿尔茨海默病、帕金森、动脉粥样硬化、痛风、风湿性疾病、感染性疾病、哮喘等多种疾病有着密切的关系。因此,研发能够特异性抑制nlrp3的药物有望为治疗这些疾病提供新的手段,也是全球各大制药公司竞争的焦点。尽管目前已经报道了一些nlrp3的小分子抑制剂,但是目前均停留在基础研究或临床1/2期研究中,尚无药物用到临床,这些小分子的效果亦不明。因此,研发新的、能够特异性抑制nlrp3的小分子抑制剂有着重要的科学意义和临床应用价值。
技术实现要素:
3.本发明所要解决的技术问题是提供一种nlrp3抑制剂,通过体内、体外实验证明了uk5099可特异性抑制nlrp3炎症小体激活,为临床治疗nlrp3相关的疾病提供新的方法。
4.本发明提供了一种nlrp3抑制剂,所述抑制剂有效成分为小分子化合物uk5099。
5.所述uk5099的结构式为:
[0006][0007]
所述uk5099对nlrp3的抑制作用独立于其对线粒体丙酮酸转运体(mpc)的效应。
[0008]
所述uk5099以nlrp3为靶点,制备治疗阿尔茨海默病、帕金森、动脉粥样硬化、痛风、风湿性疾病、感染性疾病或哮喘或其他与nlrp3炎症小体相关疾病的药物。
[0009]
所述药物配以药学上可接受的辅料或辅助性成分制备成制剂使用。
[0010]
所述制剂选自片剂、粉剂、颗粒剂、胶囊、口服液、缓释剂中的一种。
[0011]
有益效果
[0012]
本发明通过体内、体外实验证明了uk5099可特异性抑制nlrp3炎症小体激活,为临床治疗nlrp3相关的疾病提供新的方法。
附图说明
[0013]
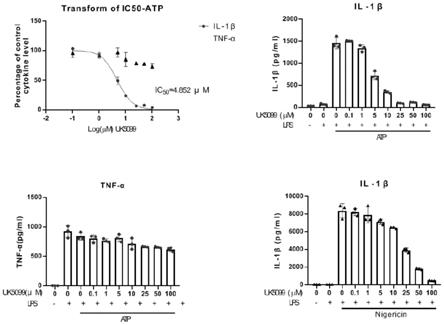
图1为uk5099抑制促炎细胞因子il-1β和tnf-α分泌的浓度梯度试验;
[0014]
图2为uk5099对nlrp3、csaspase-1和gasdermin d的作用图;
[0015]
图3为uk5099对野生型和缺失mpc表达bmdms分泌il-1β的抑制作用图;
[0016]
图4为uk5099对野生型和缺失mpc表达bmdms中的nlrp3、csaspase-1和gasdermin d的作用图;
[0017]
图5为uk5099降低内毒素诱导的脓毒症小鼠模型体内细胞因子水平,并改善其生存率。
具体实施方式
[0018]
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本技术所附权利要求书所限定的范围。
[0019]
实施例1
[0020]
以下实施案例中的实验方法,如无特殊说明,均为常规实验方法。实验中所用试剂和耗材如无特殊说明,均来自于sigma、invivogene、r&d、corning、biolegend等本研究领域的主流供应商。
[0021]
1.小鼠骨髓来源的巨噬细胞(bmdms)的获取
[0022]
使用6-8周龄的小鼠提取骨髓细胞,在含有10ng/ml的m-csf培养液中培养7天,其中第四天加入一半的新鲜培养液,得到bmdms。收集bmdms并重新种在细胞培养板中(1*106/ml)过夜,进行下一阶段的实验。
[0023]
2.炎症小体的激活
[0024]
(1)nlrp3炎症小体的激活:使用lps预处理bmdms三小时,然后将原培养液替换为不含血清的培养液,并加入不同浓度的uk5099 30分钟,再使用atp或nigericin刺激30和60分钟,收集上清液和蛋白,用于之后的elisa和western blot实验。
[0025]
(2)nlrc4炎症小体的激活:使用lps预处理bmdms三小时,然后将原培养液替换为不含血清的培养液,并加入不同浓度的uk509930分钟,再使用flagellin+lipo2000刺激6小时,收集上清液和蛋白,用于之后的elisa和western blot实验。
[0026]
(3)aim2炎症小体的激活:使用lps预处理bmdms三小时,然后将原培养液替换为不含血清的培养液,并加入不同浓度的uk509930分钟,再使用dsdna+lipo2000刺激6小时,收集上清液和蛋白,用于之后的elisa和western blot实验。
[0027]
3.小鼠体内实验(脓毒症模型)
[0028]
使用uk5099(50mg/kg)腹腔注射预处理小鼠1小时,然后使用lps(15mg/kg)腹腔注射造成脓毒症模型,一批小鼠于6小时后处死并提取血清用于细胞因子检测,另一批小鼠用于观察生存率。
[0029]
由图1所示,使用小鼠骨髓来源的巨噬细胞(bmdms)作为研究对象,采用lps+atp诱导nlrp3炎症小体激活模型,uk5099可显著抑制il-1β的产生,并呈剂量依赖型,其ic50=4.852μm。uk5099对tnf-α的抑制作用不明显,说明其可特异性抑制nlrp3炎症小体激活。
uk5099同样可以抑制其它激活剂(lps+nigericin)诱导的nlrp3炎症小体激活。
[0030]
由图2所示,western blot显示uk5099不影响pro-il-1β的表达,但可以抑制nlrp3下游caspase-1和gasdermin d的剪切,说明uk5099的作用靶点在nlrp3。
[0031]
由图3所示,uk5099数十年来一直被认为是线粒体丙酮酸转运体(mpc)的特异性抑制剂,但是本发明发现其不但可以在野生型bmdms抑制il-1β的产生,在缺乏mpc表达的bmdms同样存在这样的作用,说明其对nlrp3的抑制作用独立于mpc,nlrp3是其作用新靶点。
[0032]
由图4所示,uk5099在对照和缺失mpc表达的bmdms上均可抑制nlrp3下游caspase-1和gasdermin d的剪切,说明uk5099的作用于nlrp3而抑制nlrp3炎症小体的激活,这一效应与mpc无关。
[0033]
由图5所示,使用uk5099预处理小鼠后通过内毒素腹腔内注射诱导脓毒症模型,uk5099可以显著降低小鼠血清il-1β、tnf-α、il-6和il-12的水平,并大幅提高小鼠的生存率,说明uk5099在体内亦存在显著的抑制nlrp3的作用,可以作为一种潜在的药物来治疗脓毒症等炎症性疾病。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1