内腔装载小核酸药物的铁蛋白纳米笼载体及应用的制作方法
本发明属于铁蛋白生物纳米材料领域,涉及内腔装载小核酸药物的铁蛋白纳米笼载体的制备方法及应用。
背景技术:
1、核酸药物(nucleic acid drug)可特异性针对致病基因,在基因水平上精准靶向调控治疗疾病,近年来在精准和个性化治疗领域受到了广泛关注。然而,游离的核酸药物在应用中存在着稳定差和生物利用率低的问题,进入血液之后裸核酸极易被核酸酶降解,且容易通过肾脏清除,半衰期短。同时外源核酸分子具有免疫原性,容易引起人体的免疫反应。此外,核酸药物大多为带负电的亲水性分子,难以透过细胞质膜被细胞摄取。如果不能进入细胞实现胞吞,小核酸药物将无法发挥作用。因此,亟需开发一个安全高效的核酸药物体内递送载体。
2、笼形蛋白广泛存在于自然界中,如病毒衣壳,铁蛋白、小热激蛋白和dps蛋白等,其独特的水溶性、高分散性、对称性、均一性使其在药物载体材料领域受到广泛的关注。例如,铁蛋白是一类具有代表性的天然笼状蛋白,其24个亚基可以通过可逆自组装过程形成内径为8nm,外径为12nm的空心球形纳米蛋白笼。天然的蛋白笼作为药物载体具有众多优点,包括:1、具有均一的纳米尺寸和中空的笼状结构;2、高稳定性、低免疫原性和高生物相容性;3、可逆的自组装性质,可简单地通过调节缓冲液的酸碱或添加变性剂介导蛋白笼的解组装和自组装,进而实现药物的内腔装载;4、易于通过基因工程手段和化学修饰方法对其进行性质及功能改造;5、某些笼状蛋白(如铁蛋白)还具有受体介导的细胞内吞作用和固有肿瘤靶向性;目前笼状蛋白已经被广泛应用于装载小分子药物。但是由于天然蛋白笼内腔性质的限制,其核酸装载表现不尽人意,如铁蛋白内腔电荷分布以负电为主导,难以有效装载同样带负电的核酸药物。
3、虽然目前存在少数研究对笼状蛋白进行改造以实现核酸装载的目的,包括在蛋白笼外表面融合正电肽或阳离子聚合物以借助静电作用来吸附核酸药物。但是在复杂的血液循环环境,存在血浆剪切力会提前剥离外部装载的核酸及血浆蛋白干扰的问题。因此,如何将带负电的核酸药物装载至蛋白笼内腔以进一步提高其稳定性和安全性是领域目前面临的一大瓶颈难题。
技术实现思路
1、本发明要解决的技术问题在于如何高效地将小核酸药物装载至笼状蛋白内腔。针对现有笼状蛋白变体的缺陷,本发明提供了更加安全高效的内部正电突变的铁蛋白笼纳米载体用于内腔装载小核酸药物,并进一步提供其设计方法和应用。
2、本发明第一方面,提供了一种小核酸药物递送铁蛋白笼纳米载体的制备方法,所述方法包括将所述铁蛋白笼内腔电荷性进行由负转正的改变。
3、本发明所述铁蛋白“hfn”是指可以形成笼状结构的任何铁蛋白,其可以是天然来源的铁蛋白,也可以是重组表达的铁蛋白,或其突变体,其可以来源于原核生物、原生生物、真菌、植物或动物,例如来源于细菌、真菌、昆虫、爬行动物、禽类、两栖动物、鱼类、哺乳动物,例如来源于啮齿类动物、反刍动物、非人灵长类动物或人类,例如小鼠、大鼠、豚鼠、犬类、猫、牛、马、羊、猴、大猩猩、人。从细菌到人类,尽管不同生物的铁蛋白氨基酸序列具有极大的差别,但其结构相似,均可以形成蛋白壳结构。
4、在某些实施例中,所述铁蛋白为人重链铁蛋白hfn,其氨基酸序列为seq id no.1。
5、在某些实施例中,所述改变包括以下步骤,
6、(a)将空间上分布于所述铁蛋白内表面的带负电或不带电氨基酸突变为带正电氨基酸,和/或,
7、(b)将铁蛋白c端的e螺旋替换为具有核酸亲和力的功能肽。
8、在某些实施例中,所述步骤(a)中突变位点为glu61,glu64,gl u140和glu147。
9、在某些实施例中,所述步骤(a)中带正电氨基酸选自精氨酸、赖氨酸和组氨酸的任一种。
10、在某些实施例中,所述步骤(b)中的替换为以下任意一种或多种,
11、(a)将所述铁蛋白c端的e螺旋替换为带有正电肽的功能性基序,
12、(b)将所述铁蛋白c端的e螺旋替换为带有核酸结合肽的功能性基序,
13、(c)将所述铁蛋白c端的e螺旋替换为带有细胞穿透肽的功能性基序。
14、在某些实施例中,所述带有正电肽的功能性基序序列如seq id no.7(grkkrrqrrr)所示。
15、在某些实施例中,所述带有核酸结合肽的功能性基序序列如seq id no.8(qstekgaadkarrksa)所示。
16、在某些实施例中,带有细胞穿透肽的功能性基序序列如seq id no.9(ywhhhhh)或seq id no.10(khhhkhhhkhhhkhhh)所示。
17、本发明第二方面,提供了一种由本发明第一方面的制备方法制备获得的小核酸药物递送铁蛋白笼纳米载体,所述铁蛋白笼纳米载体内腔带正电。
18、在某些实施例中,所述铁蛋白笼纳米载体含有突变位点为glu61,glu64,glu140和glu147。
19、在某些实施例中,所述铁蛋白笼纳米载体含有氨基酸序列seq id no.7-10中任意一种。
20、在某些实施例中,所述小核酸药物为包括但不限于ssdna、as o、sirna、shrna、mirna、mrna、incrna、核酸适配体等。
21、在某些实施例中,所述铁蛋白笼纳米载体的氨基酸序列为seq id no.2-6中任意一种或多种。
22、在某些实施例中,所述铁蛋白笼纳米载体的小核酸药物装载量为2-8个核酸分子/每个蛋白笼。
23、在某些实施例中,所述铁蛋白笼纳米载体的小核酸药物装载量为5-6个核酸分子/每个蛋白笼。
24、本发明第三方面,提供了一种小核酸药物递送系统,所述小核酸药物递送系统包括本发明第二方面提供的小核酸递送铁蛋白笼纳米载体和小核酸药物。
25、在某些实施例中,所述所述铁蛋白笼纳米载体与小核酸药物的摩尔质量比为1:2~1:10,优选的,摩尔质量比为1:5。
26、本发明第四方面,提供了一种采用本发明第三方面提供的小核酸药物递送系统包载小核酸药物的方法,包括以下步骤,
27、步骤s1、制备并纯化权利要求15所述的小核酸药物递送系统中的铁蛋白笼纳米载体;
28、步骤s2、将所述小核酸药物溶解于depc水,稀释成一定浓度;
29、步骤s3、将步骤s1获得的铁蛋白笼纳米载体加入ph 1-3的酸性缓冲液中,4℃共孵育30-45分钟,获得酸解聚体系;
30、步骤s4、将步骤s2配置的小核酸药物溶液加入ph 9-11的碱性缓冲液中,混合均匀后,加入步骤s3所得的酸解聚体系,4℃共孵育1-3小时,以重组装内腔包载有小核酸药物的铁蛋白纳米笼,即得。
31、在某些实施例中,步骤s3中所述的酸性缓冲液为hcl溶液,优选为ph 1.5-1.6的hcl溶液。
32、在某些实施例中,步骤s4中所述的碱性缓冲液包括但不限于na2co3/nahco3、na2co3、nahco3、tris、naoh溶液等,优选的,碱性缓冲液为ph 9-10的na2co3/nahco3溶液。
33、在某些实施例中,步骤s4中的蛋白笼纳米载体与小核酸药物制备的投料摩尔质量比为1:2~1:10,优选的,摩尔质量比为1:5。
34、本发明第五方面,提供了本发明第二方面所述的小核酸药物递送铁蛋白笼纳米载体、本发明第三方面所述的小核酸药物递送系统在药物递送中的应用。
35、在某些实施例中,所述药物为小核酸药物。
36、在某些实施例中,所述小核酸药物包括但不限于ssdna、aso、sirna、shrna、mirna、mrna、incrna、核酸适配体等。
37、本发明第六方面,本发明还提供了所述的小核酸药物递送铁蛋白笼纳米载体、所述的小核酸药物递送系统在制备抗肿瘤、抗病毒及相关基因疾病治疗的药物中的应用。
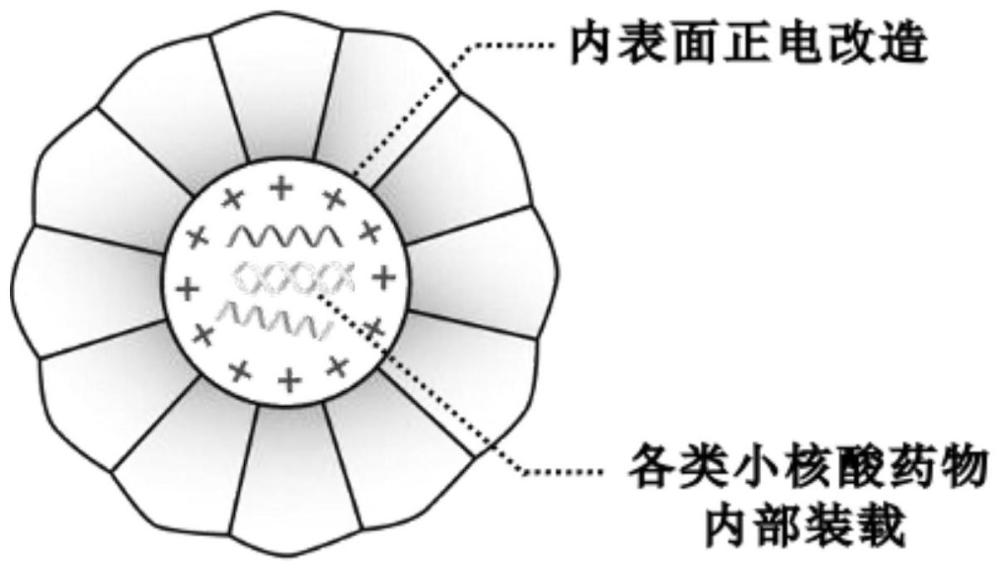
38、本发明对于现有技术而言,通过基因工程手段,将铁蛋白的负电内腔改造为正电(包括基于其内表面氨基酸突变或在c端融合功能肽)构建新型载核酸蛋白纳米笼载体。通过静电吸附作用,呈负电性的小核酸药物可被高效装载至铁蛋白纳米笼内部,显著提升小核酸药物的体内外递送稳定性、细胞摄取效率和靶向治疗疗效。本发明构建的铁蛋白笼纳米载体可作为一种普适性的小核酸药物装载平台广泛应用于抗肿瘤、抗病毒及相关基因疾病治疗。
- 还没有人留言评论。精彩留言会获得点赞!