应用于临床手术的注射取样装置
1.本公开涉及医疗器械技术领域,尤其涉及一种应用于临床手术的注射取样装置。
背景技术:
2.临床手术一般是指医生利用医疗手术器械对患者身体局部进行切除、缝合、注射以及检查等与医治相关的操作,以期实现对患者进行精确地诊断和治疗。随着科学技术的发展,当前临床手术器械基本上能够满足在人体任何部位进行手术的需求。但是,在现今部分人体部位的手术过程中,仍然缺乏结构简单、易于实现精准手术操作且能够减少患者手术痛苦的手术器械。例如,在妇产科领域中会存在对患者阴道内壁进行手术麻醉(如穿刺和麻醉药物注射)的情况,传统的手术过程一般是利用扩张器实现阴道扩张,借助扩张产生的空间,医生会手持注射器对阴道内壁上相应的麻醉位置进行麻醉注射,这就造成患者会因扩张器的扩张作用产生强烈不适感,关键是,由于阴道内部扩张空间有限,在伸入麻醉注射器过程中往往会因组织遮挡使得医生对麻醉位置不可视,对麻醉位置的判断不准确,不仅易于造成划伤、刺伤患者阴道内壁组织的情况,且可能会因麻醉不到位而需要重复执行麻醉,无论是对患者本身抑或是对手术过程均会产生不利的影响。
技术实现要素:
3.(一)要解决的技术问题
4.为解决现有技术中存在的上述技术问题至少之一,本公开提供了一种应用于临床手术的注射取样装置。
5.(二)技术方案
6.本公开提供了一种应用于临床手术的注射取样装置,其中,包括壳体部、驱动部、注射取样部、弹性缓冲部和发光成像部。壳体部为注射取样装置的外部壳体,用于形成容置空间;驱动部位于壳体部的后端的容置空间中;注射取样部活动设置于壳体部的容置空间中,与驱动部的前端相接触;弹性缓冲部位于壳体部的前端的容置空间中,弹性缓冲部的后端与注射取样部的前端相抵,弹性缓冲部的前端与壳体部的前端的容置空间的内壁相抵;发光成像部固定连接于壳体部的前端的端面上。
7.根据本公开实施例,壳体部包括外壳和顶板。外壳为中空圆柱形结构,作为壳体部的主体,形成容置空间;顶板为一板状结构,设置于外壳的一端,封堵外壳在壳体部前端的开口。
8.根据本公开实施例,驱动部包括转动柱、间隔板、旋动柱和旋杆。转动柱为一中空圆柱状结构,位于壳体部的后端的容置空间中,转动柱相对于外壳的圆柱形容置空间的内壁可作前后方向的移动;间隔板为一中间通孔的板状结构,设置于驱动部的顶端并与转动柱对应接触,间隔板位于转动柱与注射取样部之间;旋动柱为一中间通孔的柱状结构,位于转动柱中空的中部空间中,转动柱相对于旋动柱可作前后方向的移动;旋杆为一长条形杆状结构,一端与注射取样部相连且主体穿设间隔板中间通孔和旋动柱的中间通孔,旋杆相
对于旋动柱可作前后方向的移动;其中,旋动柱的中间通孔的内壁与旋杆的外侧表面之间通过螺纹匹配接触。
9.根据本公开实施例,转动柱包括基柱和撑柱。基柱与外壳的容置空间的内壁之间通过螺纹匹配接触,作为转动柱的主体,位于壳体部的后端的容置空间中;撑柱设置于基柱上与基柱一体成型,顶端与间隔板接触且外侧表面与容置空间的内壁之间具有间隙。
10.根据本公开实施例,转动柱还包括至少两个限位孔,至少两个限位孔均匀分布设置在转动柱的中部空间的内壁面上;旋动柱还包括至少两个限位凸,至少两个限位凸与至少两个限位孔对应设置,均匀分布凹设在旋动柱与转动柱相接触的外壁面上。
11.根据本公开实施例,注射取样部为一方柱形结构,包括推板、推柱、推塞和推筒。推板为一板状结构,位于注射取样部主体和驱动部的间隔板之间,与驱动部的旋杆一端相连;推柱与推板相连,位于推板和注射取样部主体之间;推塞为注射取样部主体结构,与推柱相连;推筒为一中空的套筒结构,容置推板、推柱和推塞,套筒结构的后端开口朝向驱动部的间隔板,前端的边缘朝向发光成像部方向开设有微孔,微孔贯穿推筒前端;其中,推板在受到驱动部的旋杆的驱动力之后,通过推柱带动推塞在推筒中相对推筒作前后移动。
12.根据本公开实施例,推塞为一方柱形结构,包括斜向顶面,斜向顶面位于推塞的顶端,自推塞的上端朝向推筒的前端的边缘的微孔外倾斜第一角度。
13.根据本公开实施例,推筒包括斜向底面,斜向底面位于推筒的前端,为推筒的底壁面,对应推塞的斜向顶面,自推筒的上端朝向推筒的前端的边缘的微孔内倾斜第二角度;其中,第一角度小于第二角度。
14.根据本公开实施例,推筒还包括推凸和推针。推凸为一柱形体,沿推筒的微孔朝向发光成像部垂直固定于推筒的前端端面边缘;推针为一中空注射针体,垂直推筒的前端端面穿设推凸并贯穿微孔连通推筒内部。
15.根据本公开实施例,弹性缓冲部包括弹力件和抵接板。弹力件为一可变形恢复并提供弹性力的结构,位于注射取样部和壳体部的顶板之间,弹力件一端固定于顶板的内壁面上;抵接板为一板状结构,背向发光成像部的侧面与注射取样部的前端端面抵接,朝向发光成像部的侧面与弹力件的另一端固定连接;其中,抵接板的边缘具有一与注射取样部的推筒的推凸相匹配的开孔。
16.根据本公开实施例,发光成像部包括基体、电路区、发光区、成像区、电源、透明层、穿孔和覆盖层。基体固定在壳体部的顶板的外端面上,为发光成像部的主体结构;电路区设置于基体的内部;发光区对应基体的前端端面的中心设置于电路区和基体的前端端面之间,并与电路区电连接;成像区对应于基体的前端端面的边缘设置于电路区和基体的前端端面之间,并与电路区电连接;电源设置于电路区中,与发光区和成像区电连接;透明层设置于基体的前端端面上,覆盖发光区和成像区;穿孔对应于壳体部的顶板的边缘的通孔和注射取样部的推筒的推针,穿设基体的边缘,并相对于发光区为中心与成像区中心对称设置;覆盖层为一柔性层状结构,包设基体、发光区、成像区、穿孔;其中,成像区的成像表面与透明层的外表面之间具有第三角度的倾斜角。
17.根据本公开实施例,注射取样装置还包括延伸部,延伸部与壳体部的后端固定连接。
18.(三)有益效果
19.本公开提供了一种应用于临床手术的注射取样装置,其中,包括壳体部、驱动部、注射取样部、弹性缓冲部和发光成像部。壳体部为注射取样装置的外部壳体,用于形成容置空间;驱动部位于壳体部的后端的容置空间中;注射取样部活动设置于壳体部的容置空间中,与驱动部的前端接触;弹性缓冲部位于壳体部的前端的容置空间中,弹性缓冲部的后端与注射取样部的前端相抵,弹性缓冲部的前端与壳体部的前端的容置空间的内壁相抵;发光成像部固定连接于壳体部的前端的端面上。因此,通过上述简单的装置结构,在对阴道等人体组织实施注射取样过程中,可以不再需要使用扩张器等组织扩张工具,降低患者的手术痛苦和不适感,实现对组织内部的可视化,极大提高注射或取样准确性,同时避免在注射或者取样过程中对其他位置造成的意外刺伤或划伤,提高注射或取样效率,防止重复取样或注射,降低患者的手术痛苦和不适感。
附图说明
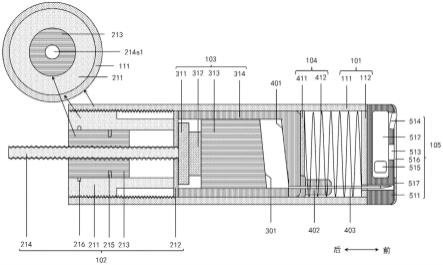
20.图1a示意性示出了根据本公开实施例的应用于临床手术的注射取样装置在起始状态下对应前后方向的剖视结构组成图及其壳体部的后视平面图;
21.图1b示意性示出了对应图1a的根据本公开实施例的应用于临床手术的注射取样装置在推筒状态下对应前后方向的剖视结构组成图及其驱动部的间隔板的后视平面图;
22.图1c示意性示出了对应图1b的根据本公开实施例的应用于临床手术的注射取样装置在推针状态下对应前后方向的剖视结构组成图及其弹性缓冲部的抵接板的后视平面图;
23.图2a示意性示出了对应图1a的根据本公开实施例的应用于临床手术的注射取样装置在推筒状态下对应驱动部的剖视结构组成图;
24.图2b示意性示出了对应图1b的根据本公开实施例的应用于临床手术的注射取样装置在推筒状态下对应注射取样部的第一角度θ1和第二角度θ2的剖视结构组成图;
25.图3示意性示出了对应图1a-图1c的根据本公开实施例的应用于临床手术的注射取样装置中发光成像部的对应前后方向的剖视结构组成图及其前视平面图;
26.图4示意性示出了对应图3的根据本公开实施例的应用于临床手术的注射取样装置中对应发光成像部的成像区、透明层与推针之间的结构关系图;
27.图5示意性示出了对应图3的根据本公开实施例的应用于临床手术的注射取样装置中。
28.附图标记说明:
29.壳体部101:外壳111,顶板112;
30.驱动部102:转动柱211,间隔板212,旋动柱213,旋杆214,限位凸215,限位孔216,旋动柱的中间通孔214s1,间隔板的中间通孔214s2;
31.注射取样部103:推板311,推,312,推,313,推筒314,推塞的斜向顶面301,推筒的斜向底面401,推凸402,推针403,第一角度θ1,第二角度θ2;
32.弹性缓冲部104:抵接板411,弹力件412,抵接板的开孔402s;
33.发光成像部105:基体511、电路区512、发光区513、成像区514、电源515、透明层516、覆盖层517,穿孔403s,入射角α,折射角β,第三角度γ;
具体实施方式
34.为使本发明的目的、技术方案和优点更加清楚明白,以下结合具体实施例,并参照附图,对本发明进一步详细说明。
35.需要说明的是,在附图或说明书正文中,未绘示或描述的实现方式,均为所属技术领域中普通技术人员所知的形式,并未进行详细说明。此外,上述对各元件和方法的定义并不仅限于实施例中提到的各种具体结构、形状或方式,本领域普通技术人员可对其进行简单地更改或替换。
36.还需要说明的是,实施例中提到的方向用语,例如“上”、“下”、“前”、“后”、“左”、“右”等,仅是参考附图的方向,并非用来限制本公开的保护范围。贯穿附图,相同的元素由相同或相近的附图标记来表示。在可能导致对本公开的理解造成混淆时,将省略常规结构或构造。
37.并且图中各部件的形状和尺寸不反映真实大小和比例,而仅示意本公开实施例的内容。另外,在权利要求中,不应将位于括号之间的任何参考符号构造成对权利要求的限制。
38.再者,单词“包含”不排除存在未列在权利要求中的元件或步骤。位于元件之前的单词“一”或“一个”不排除存在多个这样的元件。
39.说明书与权利要求中所使用的序数例如“第一”、“第二”、“第三”等的用词,以修饰相应的元件,其本身并不意味着该元件有任何的序数,也不代表某一元件与另一元件的顺序或是制造方法上的顺序,这些序数的使用仅用来使具有某命名的一元件得以和另一具有相同命名的元件能做出清楚区分。
40.本领域那些技术人员可以理解,可以对实施例中的设备中的模块进行自适应性地改变并且把他们设置在与该实施例不同的一个或多个设备中。可以把实施例中的模块或单元或组件组合成一个模块或单元或组件,以及此外可以把他们分成多个子模块或子单元或子组件。除了这样的特征和/或过程或者单元中的至少一些是相互排斥之外,可以采用任何组合对本说明书(包括伴随的权利要求、摘要和附图)中公开的所有特征以及如此公开的任何方法或者设备的所有过程或单元进行组合。除非另外明确陈述,本说明书(包括伴随的权利要求、摘要和附图)中公开的每个特征可以由提供相同、等同或相似目的的代替特征来代替。并且,在列举了若干装置的单元权利要求中,这些装置中的若干个可以是通过同一个硬件项来具体体现。
41.类似地,应当理解,为了精简本公开并帮助理解各个公开方面的一个或多个,在上面对本公开的示例性实施例的描述中,本公开的各个特征有时被一起分组到单个实施例、图、或者对其的描述中。然而,并不应将该公开的方法解释成反映如下意图:即所要求保护的本公开要求比在每个权利要求中所明确记载的特征更多的特征。更确切地说,如下面的权利要求书所反映的那样,公开方面在于少于前面公开的单个实施例的所有特征。因此,遵循具体实施方式的权利要求书由此明确地并入该具体实施方式,其中每个权利要求本身都作为本公开的单独实施例。
42.为解决现有技术中所存在的传统人体组织临床手术过程中所使用的手术器械或者手术设备结构过于笨重复杂、注射取样等手术操作难度大同时难以有效避免患者手术痛苦的技术问题至少之一,本公开实施例提供了一种应用于临床手术的注射取样装置,以期
达到简化手术器械结构、便于临床手术操作且保证患者手术体感较低的效果,从而实现手术器械结构集成化、电控化、微型化以及智能化,在保证临床手术操作精度的情况下,尽可能地降低手术操作难度,极大降低患者在手术过程中的不适感。
43.如图1a-图1c所示,本公开提供了一种应用于临床手术的注射取样装置,其中,包括壳体部101、驱动部102、注射取样部103、弹性缓冲部104和发光成像部105。其中,本公开实施例的注射取样装置可以应用于临床手术操作过程中在人体组织内部的注射操作或者取样操作,该人体组织可以是口腔、食道、胃、结肠、直肠、气管、阴道甚至子宫等相对开放的组织环境,也可以是主要的静脉血管等非开放环境的组织环境。
44.壳体部101为注射取样装置的外部壳体,用于形成容置空间。壳体部101可以为该装置的中空壳体结构的主体组成,其他组成部分主要都基于该壳体部101的外部壳体及其形成的容置空间进行设置,从而保证整体装置的高度集成化和微型化。其中,壳体部101的外部壳体的表面还需要与人体组织进行接触,即该装置进入人体之后,会在人体组织之间来回移动,并到达指定的病灶处,以便于对相应的病灶实现注射操作或者取样操作,以配合完成临床手术,可以有效保证微创效果,降低病人术后恢复时间和手术期间或手术之后的痛苦。
45.驱动部102位于壳体部101的后端的容置空间中。其中,对于本公开的实施例而言,相对壳体部101的整体结构,驱动部102所处的位置位于壳体部101的后端(即装置后端),相反,另一端则位于壳体部101的前端(即装置前端)。驱动部102主要用于为注射取样部103提供驱动力,使得注射取样部能够顺利完成注射或者取样的操作过程。
46.注射取样部103活动设置于壳体部101的容置空间中,与驱动部102的前端相接触。注射取样部103位于容置空间中的中部、驱动部102的前部,用于在执行注射操作时,受到驱动部102提供的驱动力,实现注射液抽取和向病灶组织进行注射的操作,在执行取样操作时,受到驱动部102提供的驱动力,实现向病灶组织进行抽取组织样本的取样操作。其中,在非注射和取样操作期间,一般注射取样部103的注射取样端,如注射针头或者取样针头等尖端取样结构不会突出壳体部101的前端之外。换言之,在该装置进入人体组织并在其中进行移动的过程中,注射取样部103不会伸出壳体部101之外,以防止对非目标病灶组织的破坏,只有在面对目标病灶组织时注射取样部103才会因受到驱动部102驱动力的作用,突破壳体部101的束缚。其中,注射取样部103可以在容置空间中相对于壳体部101、驱动部102等结构进行前后移动。
47.弹性缓冲部104位于壳体部101的前端的容置空间中,弹性缓冲部103的后端与注射取样部103的前端相抵,弹性缓冲部104的前端与壳体部101的前端的容置空间的内壁相抵。弹性缓冲部104主要位于壳体部101的前端,用于对位于驱动部102和壳体部101的前端的端壁之间的注射取样部103进行弹性缓冲。具体地,在非注射取样操作的期间,驱动部102不会产生驱动力,弹性缓冲部104利用自身的弹性力将注射取样部103的主体结构顶在驱动部102的前端,使得其与驱动部102的前端相接触,防止因装置进入人体组织之后,注射取样部103的尖端取样结构不会因意外的惯性或者重力等原因导致突破壳体部101的束缚,延伸到壳体部101外侧对非目标病灶组织产生意外破坏,如对正常的组织粘膜、气道等造成划伤甚至穿孔。此外,在注射取样结束之后,需要将装置从人体组织中退出时,弹性缓冲部104还可以配合驱动部102的驱动力,确保注射取样部103缩回到壳体部101的容置空间中,防止意
外破坏非目标病灶组织,如对正常的组织粘膜、气道等造成划伤甚至穿孔。此外,弹性缓冲部104还可以在原始状态下(如图1a所示),始终将注射取样部103推压在驱动部102上,防止容置空间内发生结构部分晃动,而且能够充分实现对容置空间的空间利用。
48.发光成像部105固定连接于壳体部101的前端的端面上。发光成像部105可以在该装置进入人体组织之后,可以对人体组织内部进行成像发光提供可视环境,同时进行成像并对成像结果进行实时回传,从而能够实现人体组织内部的可视化操作,在具有光源和实时成像情况下,对注射或取样操作进行精准的定位操作,而不需要任何如阴道扩张器等扩张辅助器械,在提高操作精准性的情况下,极大地降低了如阴道注射取样的操作难度和患者的手术不适感,避免手术重复操作的情况,改善患者的抵触心理。
49.具体地,在执行装置进入人体组织或者自人体组织退出过程中,发光成像部105能够实现光感检测,在人体组织内部自动光感同时打开(或者维持)发光和成像,实现人体组织内部环境可视化,实时回传内部环境;此时,驱动部102不会被控制产生驱动力,弹性缓冲部104能够对注射取样部103施加弹性力,使得注射取样部103的尖端注射取样结构能够稳定保持在壳体部101的内部容置空间中、且与驱动部102的前端相接触而不会外露,以防止其意外划伤组织。
50.在执行注射过程中,通过发光成像部105的发光成像可以准确找到相应的目标病灶组织,之后可以对驱动部102发送第一控制指令,使得驱动部102接收到该第一控制指令后提供第一驱动力,使得受到该第一驱动力的注射取样部103朝向壳体部101的前端移动,并最终突破弹性缓冲部104的弹性力,将尖端注射取样结构伸出到壳体部101的前端外部,将尖端注射取样结构对目标病灶组织进行刺入;之后,对驱动部102发送第二控制指令,使得驱动部102接收到该第二控制指令后提供第二驱动力,使得受到该第二驱动力的注射取样部103执行注射操作。
51.在执行取样过程中,在执行上述尖端注射取样结构的刺入之后,还可以对驱动部10发送第三控制指令,使得驱动部102接收到该第三控制指令后,提供与第二驱动力反向的第三驱动力,使得受到该第三驱动力的注射取样部103吸取病灶组织的组织样本进入注射取样部103内,实现取样。
52.无论是执行注射还是执行取样操作,完成注射或者取样操作之后,对驱动部102发送第四控制指令,使得驱动部102接收到该第四控制指令后,撤除第一驱动力,使得受到弹性缓冲部104的弹性力的注射取样部103向壳体部101的后端移动,将尖端注射取样结构收回至壳体部101的容置空间内。
53.因此,当该装置被置入阴道等人体组织时,弹性缓冲部104可以保证注射取样部103的尖端注射取样结构不会因意外受力伸出壳体部101前端造成划伤或刺伤组织,同时发光成像部105可以有效实时传回阴道等组织内部图像,使得临床手术医生可以通过手机等终端设备实时获取阴道等组织内部影像,准确判断注射或者取样位置。当执行注射或者取样时,可以通过驱动部102推动注射取样部103压缩弹性缓冲部104,使得注射或取样针头等尖端注射取样结构外露出壳体101,并对注射位置进行精确地注射(如麻醉)或者对取样位置进行精确地吸取取样。因此,通过上述简单的装置结构,在对阴道等人体组织实施注射取样过程中,可以不再需要使用扩张器等组织扩张工具,降低患者的手术痛苦和不适感,实现对组织内部的可视化,极大提高注射或取样准确性,同时避免在注射或者取样过程中对其
他位置造成的意外刺伤或划伤,提高注射或取样效率,防止重复取样或注射,降低患者的手术痛苦和不适感。
54.如图1a-图1c所示,根据本公开实施例,壳体部101包括外壳111和顶板112。
55.外壳111为中空圆柱形结构,作为壳体部101的主体,形成容置空间;其中,外壳111外表面还需要与人体组织进行接触,即该装置进入人体之后,会在人体组织之间来回移动,并到达指定的病灶处,以便于对相应的病灶实现注射操作或者取样操作,以配合完成临床手术,可以有效保证微创效果,降低病人术后恢复时间和手术期间或手术之后的痛苦。外壳111的中空圆柱形结构有利于进入人体组织时降低组织摩擦力,减少患者不适感和痛苦感。此外,外壳111的材料可以选择具有一定韧性的塑质或树脂材料,如氟树脂与聚酰亚胺系树脂的复合材料等,在维持一定强度不易变形或毁坏的情况下,避免金属材料一般温度过低导致患者不适感的情况。
56.顶板112为一板状结构,设置于外壳111的一端,封堵外壳111在壳体部前端的开口。外壳111为一前端和后端开口的中空圆柱形结构,顶板112可以垂直于前后方向与外壳111的前端固定连接,对前端开口封堵,形成中间的容置空间。顶板112一般还用于设置发光成像部105,一般可以不与人体组织相接触。顶板112的材料可以选用与外壳111相同或者性质接近的材料,甚至顶板112可以与外壳111一体成型。
57.因此,外壳111可以保证容置空间能够提供该装置高度集成化和微型化的安装位置,同时与人体组织进行接触,配合完成临床手术,保证微创效果的情况下,就可以实现对患者的注射取样操作,降低病人对装置进入和退出时的不适感,减少手术痛苦。
58.如图1a-图2a所示,根据本公开实施例,驱动部102包括转动柱211、间隔板212、旋动柱213和旋杆214。
59.转动柱211为一中空圆柱状结构,位于壳体部101的后端的容置空间中,转动柱211相对于外壳111的圆柱形容置空间的内壁可作前后方向的移动。在驱动力接到第一控制指令或者第四控制指令时,转动柱211的柱体外表面与外壳111的后端的内圆柱形壁面相互配合进行转动,可以使得转动柱211可以沿容置空间作向前或者向后移动,从而能够带动与之相接触的间隔板212在容置空间中作向前或者向后移动,从而给与间隔板212相接触的注射取样部103施加向前的第一驱动力,或者撤除第一驱动力使得注射取样部103受到弹性缓冲部104的弹性力向容置空间的后端移动,收回到外壳111内。
60.转动柱211对应的容置空间的内壁表面为圆柱形环面,以利于转动柱211相对于外壳111转动,同时可以借此进行在容置空间中前后的移动。
61.间隔板212为一中间通孔214s2的板状结构,设置于驱动部102的顶端并与转动柱214对应接触,间隔板212位于转动柱211与注射取样部103之间。间隔板212的中间通孔214s位于间隔板212的中心位置,且间隔板212为非圆形的板状结构,其形状与注射取样部103的后视平面形状结构相同,例如为四角为弧形角没计的方形板。如此,可以在实现间隔板212在容置空间中前后移动的同时,不易于因接触的转动柱211转动而发生相对的转动。因此,间隔板212的两侧表面均未光滑的平坦设计,以尽可能降低摩擦力。间隔板212可以便于驱动部102的转动柱211向注射取样部103均匀传递驱动力,防止注射取样部受力不均的情况。而且,间隔板212还可以将注射取样部103和驱动部102间隔开来,防止二者之间收到相互的影响。
62.其中,间隔板212的中间通孔214s用于旋杆214的穿设,具体参见下文描述。
63.旋动柱213为一中间通孔214s1的圆柱状结构,位于转动柱211中空的中部空间中,转动柱211相对于旋动柱213可作前后方向的移动。其中,旋动柱213可以与相应的伺服电机或者步进电机等驱动电机结构(可以包括齿轮转换组件等)相连且固定,换言之,旋动柱213并不会沿容置空间作前后的移动。旋动柱213的圆柱体结构外表面光滑,且与转动柱211的中部空间的光滑内壁表面相接触,二者通过光滑表面可以作相对的前后移动。此外,转动柱211也可以与相应的伺服电机或者步进电机等驱动电机结构(可以包括齿轮转换组件等)相连,从而可以受到外力驱动相对旋动柱213和外壳111发生转动,并前后移动。
64.其中,旋动柱213保持不动,转动柱211在受力旋转时,可以相对该旋动柱213向前后移动,如收到第一控制指令和第四控制指令,转动柱213向前后移动可以通过间隔板212实现向注射取样部103施加第一驱动力或者撤除第一驱动力。
65.旋杆214为一长条形杆状结构,一端与注射取样部103相连且主体穿设间隔板212中间通孔214s2和旋动柱213的中间通孔214s1,旋杆214相对于旋动柱213可作前后方向的移动。其中,旋动柱213的中间通孔214s1的内壁与旋杆214的外侧表面之间通过螺纹匹配接触。
66.其中,当转动柱211保持不动,旋动柱213在受外力相对于转动柱211的内壁面旋转时,由于旋动柱213位置固定,旋动柱213可以相对于使得与之具有螺纹匹配接触关系的旋杆214作前后移动,而且由于旋杆214的一端与注射取样部103相连,从而在旋杆214向前移动时,能够给注射取样部103提供第二驱动力或者与第二驱动力相反的第三驱动力。旋杆214整体为柱状结构,外表面为螺纹凸起面,与之相匹配的旋动柱213的中间通孔214s1的内壁表面为与该旋杆214的螺纹凸起表面相匹配的螺纹凹陷面,二者相对旋转,使得二者发生相对的前后移动,具体不作赘述。
67.因此,通过驱动部102的上述转动柱211、间隔板212、旋动柱213和旋杆214能够使得驱动部102给注射取样部103提供稳定均匀的输出力,使得注射取样部103可以在受到相应的驱动力时,灵活地实现相应的注射或取样操作。
68.如图1a-图2a所示,根据本公开实施例,转动柱211包括基柱211a和撑柱211b。
69.基柱211a与外壳111的容置空间的内壁之间通过螺纹匹配接触,作为转动柱211的主体,位于壳体部101的后端的容置空间中;基柱211a整体为圆柱状结构,外表面为螺纹凸起面,与之相匹配的外壳111的容置空间的内壁表面为与该基柱211a的螺纹凸起表面相匹配的螺纹凹陷面,二者相对旋转,使得二者发生相对的前后移动,具体不作赘述。
70.撑柱211b设置于基柱211a上与基柱211a一体成型,顶端与间隔板212相接触且外侧表面与容置空间的内壁之间具有间隙。撑柱211b可以同样为圆柱形的结构,与基柱211a一体成型设计,且与容置空间的内壁之间保持间距,从而确保二者不会发生接触,有效降低转动柱211与容置空间内壁之间的接触摩擦力,使得转动柱211的基柱211a能够更好地与容置空间内壁发生相对转动。同时,撑柱211b还用于作为驱动部102的驱动力传递中间件,向间隔板212传递驱动输出力给注射取样部103。
71.在驱动力接到第一控制指令或者第四控制指令时,基柱211a的柱体外表面与外壳111的后端的内圆柱形螺纹壁面相互配合进行转动,可以使得基柱211a可以沿容置空间作向前或者向后移动,从而能够带动与之一体成型的撑柱211b推动接触的间隔板212在容置
空间中作向前或者向后移动,从而给与间隔板212相接触的注射取样部103施加向前的第一驱动力,或者撤除第一驱动力使得注射取样部103受到弹性缓冲部104的弹性力向容置空间的后端移动,收回到外壳111内。此外,基柱211a和撑柱211b中用于容置旋动柱213的中部空间相连通,且该旋动柱213在前后方向的长度要大于基柱211a的前后方向上的长度,从而加强基柱211a和撑柱211b的转动柱211的整体强度,防止撑柱211b发生断裂或者损坏。
72.如图1a-图2a所示,根据本公开实施例,转动柱211还包括至少两个限位孔216,至少两个限位孔216均匀分布设置在转动柱211的中部空间的内壁面上;
73.旋动柱213还包括至少两个限位凸215,至少两个限位凸215与至少两个限位孔216对应设置,均匀分布凹设在旋动柱213与转动柱211相接触的外壁面上。
74.限位凸215与限位孔216的数量一致,分布位置在满足前后移动特定距离的基础上对应,基限位凸215可以直接嵌入限位孔216中,从而将旋动柱213和转动柱211固定住,防止二者再次发生相对的转动。具体地,当旋动柱213固定不动,转动柱211相对于旋动柱213转动,同时借助与外壳111的内壁之间螺纹匹配发生转动,相对于旋动柱213发生向前的移动,当自原始位置移动如图2a所示l1的间距时,转动柱211a的撑柱211b带动间隔板212向注射取样部103施加第一驱动力,并推动注射取样部103至最后的位置(即第一驱动力再次加大,也无法推动注射取样部103继续移动)的情况下,进一步地,转动柱211保持不动,旋动柱213发生相对于转动柱211的旋转,同时由于旋动柱213固定,会带动与之螺纹匹配的旋杆214发生向前的移动,并且旋杆214向注射取样部103的后文所提推塞提供第二驱动力使之继续向前移动,直至其移动至最后位置(即第二驱动力再次加大,也无法推动推塞继续移动)的情况下,限位凸215敲好嵌入对应匹配的限位孔216,使得旋动柱213、转动柱211与外壳111三者连为一体,使得整个驱动部102和壳体部101相对于注射取样部103保持稳定,借助间隔板212确保旋杆214的第一驱动力和第二驱动力的输出均匀性和稳定性,防止因电机控制意外造成的注射取样部103的退回情况出现,实现了二次保险的效果。
75.其中,限位凸215可以是限位用的弹针或弹珠,可以受到电控作用弹起,并嵌入到与之形状匹配的限位孔216中,具体不作赘述。
76.如图1a-图2b所示,根据本公开实施例,注射取样部103为一方柱形结构,包括推板311、推柱312、推塞313和推筒314。
77.推板311为一板状结构,位于注射取样部103主体和驱动部102的间隔板212之间,与驱动部102的旋杆214一端相连;
78.推柱312与推板311相连,位于推板311和注射取样部103主体之间;
79.推塞313为注射取样部103主体结构,与推柱312相连;
80.推筒314为一中空的套筒结构,容置推板311、推柱312和推塞313,套筒结构的后端开口朝向驱动部102的间隔板212,前端的边缘朝向发光成像部105方向开设有微孔,微孔贯穿推筒314前端;
81.其中,推板311在受到驱动部102的旋杆214的驱动力之后,通过推柱312带动推塞313在推筒314中相对推筒314作前后移动。
82.在原始状态下,受到弹性缓冲部104的弹性力作用,整个注射取样部103始终被推压在驱动部102上,防止容置空间内发生结构部分晃动,而且能够充分实现对容置空间的空间利用,确保装置结构的高度微型化和集成化。推板311与旋杆314相连,使得在注射取样部
103在受到第一驱动力之后,旋杆314可以在前后移动时带动推板311前后移动。从而使得推板311能够给予推柱312施加推力,不能够通过推柱312向推塞313施加推力,最终实现推塞313相对于推筒314的前后移动。其中,由于旋杆214会发生旋转动作,所以旋杆214和推板311之间的相连可以是球形相连,如三脚架的球接结构,具体不作赘述。如此,可以防止旋杆214带动推板311发生旋转,给注射取样部103带来损害。
83.推柱312为柱形体可与推板311一体成型,一端固定在推板311的侧壁上,一端固定在推塞313的后端面上,从而起到受力时带动推塞有效实现相对推筒的推拉效果。
84.其中,推板311与推柱312均与推筒314的内壁面保持间隙,以防止与推筒314的内壁面的摩擦力过大,影响推塞313相对推筒314的推拉效果。其中,推板311和推柱312可以为一体成型的塑质材料。
85.推塞313为非圆形柱状体,截面形状为非圆形,如四角弧形设计的正方形柱体结构,从而区别于传统的圆柱形推塞,在保证受力前后移动的情况下,有效的防止其在推筒314中发生旋转,避免产生较大的摩擦力,防止注射或者取样过程中不必要的漏液等情况出现。其中推塞313主体可以具有一定硬度的塑料材料,并作外围包覆塑胶层,具体可以是橡胶层。
86.推筒314为与推塞313相匹配的非圆形柱状体,如四角弧形设计的正方形柱状体结构,且推筒314可以为金属材料制成,从而保证内壁光滑,降低推塞313与推筒314之间的前后移动的摩擦力,防止推筒314受力发生相对于外壳111的旋转造成后文推针的断裂。此外,推筒314与推塞313的非圆柱形结构设计,还可以有利于后文所提及的斜向顶面和斜向底面的设计,从而有利于实现更好的注射效果。因此,与容置空间后半段对应驱动部102的圆柱形内壁表面不同,对应注射取样部103的容置空间的内壁表面为匹配推筒314柱体形状的非圆柱形,换言之,在注射取样部103的位置,注射取样部103只能作前后移动,不能旋转,从而保证后续的注射取样的稳定性。
87.其中,推筒314的前端因受到弹性缓冲部104的弹性力,使得推筒312的后端与间隔板212之间存在受力接触,即柱形中空的推筒314的后端开口顶在间隔板212的表面上,使得推板311与间隔板212之间恰好能够无力接触,从而有效保证整个结构的紧凑性,实现高度的集成化效果。
88.如图1a-图2b所示,根据本公开实施例,推塞313为一方柱形结构,包括斜向顶面301,斜向顶面301位于推塞313的顶端,自推塞313的上端朝向推筒314的前端的边缘的微孔外倾斜第一角度θ1。
89.如图1a-图2b所示,根据本公开实施例,推筒314包括斜向底面401,斜向底面401位于推筒314的前端,为推筒314的底壁面,对应推塞313的斜向顶面301,自推筒314的上端朝向推筒314的前端的边缘的微孔内倾斜第二角度θ2;其中,第一角度θ1小于第二角度θ2。
90.相对于现有技术中推塞普遍设计为中心朝向推筒底面凸起的锥形柱结构,本公开实施例的推塞313借助于上述斜向顶面301和相匹配推筒314的斜向底面401及推筒314前端下边缘设计的注射液或样本组织进出用微孔,使得本公开的推塞313和推筒314在推出注射液或者样本组织时能够尽可能地将其完全推出,基本不会留下残存。
91.其中,斜向顶面301的第一角度θ1小于推筒314的斜向底面的第二角度θ2,使得推塞313的斜向顶面301与推筒314的斜向底面自上方先行接触,从而能够直接实现对注射液
或样本组织自微孔的退出。相应地,斜向顶面301和斜向底面401在保持上述角度关系的同时可以进一步设计为相互匹配的凹凸面,凹凸面的中心朝向微孔,以进一步提供注射液和样本组织的推出。因此,即便对于本公开实施例微型化的注射取样装置,推筒314和推塞313之间的容置注射液和样本组织的空间非常狭小,也能够充分实现利用,确保推出注射液和组织样本时基本不残留。
92.如图1a-图1c所示,根据本公开实施例,推筒314还包括推凸402和推针403。
93.推凸402为一柱形体,沿推筒314的微孔朝向发光成像部105垂直固定于推筒314的前端端面边缘;
94.推针403为一中空注射针体,垂直推筒314的前端端面穿设推凸402并贯穿微孔连通推筒314内部。
95.推凸402为推针403能够固定连接在推筒314的微孔位置处前端端面上的柱体结构,起到稳固推针的效果,防止推针403歪斜,甚至发生断裂,具体可以为一圆台结构或者圆柱结构。推针403为一注射针,一端尖锐用于刺入组织并实现注射或者取样,另一端固定在推凸402中并穿设在推筒314的微孔中,连通推筒314内部。
96.因此,推针403能够对应微孔设置在推筒314的前端的端面的边缘上,使得推针403能够在伸出壳体部101的前端之后保持在壳体部101的前端边缘上,从而能够确保推针403能够相对于壳体部101的前端中心保持一定距离,更有利于在找到确切的病灶组织后对病灶组织进行更为精准的注射或者取样,不容易出现现有技术中因推针处于外壳的前端中心,被外壳的中心至边缘之间的结构所遮挡,无法有效对准微小病灶组织的情况出现。换言之,无论对于何种微型病灶组织都可以实现快速精准的定位刺入操作。
97.进一步地,配合上述推塞313和推筒314的斜向顶面301和斜向地面401的设计,该推针403设计在微孔位置,也能够有利于注射液或者样本组织的尽量退出,避免残存在推筒314中,可谓一举两得。而对于处于非推筒314前端端面中心的推针403和推凸402,由于推筒314的整体结构为方柱体,使得推筒314不会相对容置空间发生旋转动作,从而有效地防止推针403和推凸402因发生旋转干涉断裂。
98.如图1a-图2b所示,根据本公开实施例,弹性缓冲部104包括弹力件412和抵接板411。
99.弹力件412为一可变形恢复并提供弹性力的结构,位于注射取样部103和壳体部101的顶板112之间,弹力件412一端固定于顶板112的内壁面上;
100.抵接板411为一板状结构,背向发光成像部105的侧面与注射取样部103的前端端面抵接,朝向发光成像部105的侧面与弹力件412的另一端固定连接;
101.其中,抵接板411的边缘具有一与注射取样部103的推筒314的推凸402相匹配的开孔402s。
102.弹力件412可以是弹簧等能够因变形而产生弹性力且可恢复的结构元件,一端连接固定在顶板112的内壁面上,另一端固定在抵接板411的侧表面上。其中,抵接板411整体上平贴在推筒314的前端端面上,实现将弹簧的弹性力均匀地施加在推筒314的前端端面上,使得整个注射取样部103的弹性力受力保持均匀一致。开孔402s专门用于穿设推凸402,使得推凸402在前后方向上不会产生多余的占用空间,从而进一步实现对容置空间的充分利用,实现高度集成化。此外,对于弹力件412为弹簧的情况下,由于推凸402在穿设402s之
后位于推筒314和顶板112之间的空间时,推凸402与外壳111的内壁面保持间隙,使得推凸402能够位于弹簧的中间,从而进一步确保推凸402不会占用容置空间,实现与弹力件412的空间的充分共用,进一步实现对容置空间的充分利用,实现高度集成化。
103.由于弹力件412一直保持受到推筒314和顶板112之间的挤压力的状态,使得推筒314在原始状态下一直被弹力件412紧紧压在驱动部102的间隔板212上,能够给予推筒314为主体的注射取样部103提供更为稳定的缓冲力,防止推筒314发生前后晃动,充分利用容置空间,实现微型化和集成化,避免推筒314因意外将推针403非正常向前推出壳体部101。
104.可见,弹性缓冲部即可以在保证充分的空间利用的情况下,提高注射取样部103和驱动部102的稳定性,防止意外出针造成人体组织的划伤和刺伤情况出现。
105.如图1a-图4所示,根据本公开实施例,发光成像部105包括基体511、电路区512、发光区513、成像区514、电源515、透明层516、穿孔403s和覆盖层517。
106.基体511固定在壳体部101的顶板112的外端面上,为发光成像部105的主体结构;基体511构成发光成像部105的主要结构组成设置位置,实现对发光成像部105的高度结构集成。
107.电路区512设置于基体511的内部;电路区512为基体511的内部的一个空间位置,用于容置控制电路板、电路控制线以及相应的设置位。电路区512还可以包括蓝牙或者类似的视频数据无线传输电路板,以及用于存储特定时间段的存储模块的设置位等。其中,无线传输电路板还可以作为传输模块与存储模块一并集成在控制电路板上。从而能够实现对发光成像部的控制电路结构的高度集成。
108.发光区513对应基体511的前端端面的中心设置于电路区512和基体511的前端端面之间,并与电路区512电连接。发光区513可以包括光感传感器以及发光元件,光感传感器可以是微型的光感元件,在接收不到外界光线时,电阻发生变化产生电流变化,并通过控制电路板的控制处理将电流变化转换为控制指令,控制对发光元件的发光控制。发光元件可以是led灯等普通的发光元器件,在接收到相应的发光控制的电流时,发出光线,在电流中断时,停止发光。从而,能够通过发光区513的光感检测,使得装置进入人体组织时,能够自动发光,起到能源节约的效果。
109.其中,发光区513的光感传感器和发光元件尽可能设置在基体511的前端端面中心位置上,从而能够确保光感传感器的光感检测准确性,防止出现误监测从而浪费电能的情况。而且对于发光元件而言,处于中心能够实现中心发光,从而确保发光效果能够覆盖装置前端的人体组织,且照射到人体组织内壁面的光线不容易被反射进入成像区514,给成像带来干扰。具体地,由于装置进入人体组织时,如进入阴道内部,由于发光区513处于装置前端中心,人体组织处于该中心的相对两侧,发光区513中心的强光不容易照射到人体组织两侧,而发光区边缘的柔光更容易照射到人体组织两侧,且成像更好。其中,发光区513中心的强光不容易反射到成像区514的成像面上,防止对成像造成干扰。可见,发光区513的发光元件可以采用成本较低的光电器件即可,可有效降低发光成本。
110.成像区514对应于基体511的前端端面的边缘设置于电路区512和基体511的前端端面之间,并与电路区512电连接。成像区514处在基体511前端端面的边缘位置,用于为装置进行发光成像。成像区514可以是高清微型摄像头,如针孔摄像头等,可以实现实时的视频拍摄成像。
111.电源515设置于电路区512中,与发光区513和成像区514电连接;电源515可以是独立的微型纽扣锂电池,电源515也还可以通过可以埋设在壳体部101的外壳111中的电线与外界直接电连,由外界直接有线供电。电源515主要用于为上述的电路区512的控制电路板、发光区513的光感传感器和发光元件、成像区514等进行供电。
112.透明层516设置于基体511的前端端面上,覆盖发光区513和成像区514;其中,如图3和图4所示,成像区514的成像表面与透明层516的外表面之间具有第三角度γ的倾斜角。成像区514的上述第三角度γ,能够有效防止发光区513中心发出的强光被反射也不会被反射至成像区514的成像表面上被成像区514成像。从而有效地防止了成像干扰。透明层516可以有效地使得发光区513的光线发出,同时即使成像区514相对于透明层516倾斜第三角度γ,透明层516也可以保证发光成像部105的前端端面能够平整光滑,降低其在进入人体组织时的顺滑度,防止因不平整刮伤人体组织,或者造成人体组织液、血液等囤积在发光成像部105的前端表面上,从而影响发光成像。
113.在本公开的另一实施例中,透明层516相对于基体511的外侧表面沿中心向前微凸设计,从而使得透明层516具有平凸透镜的效果,一定程度上有助于普通的发光区513的发光元件的发光更为均匀分散,而且对于成像区514有一定的放大效果。
114.穿孔403s对应于壳体部101的顶板112的边缘的通孔和注射取样部103的推筒314的推针403,穿设基体511的边缘,并相对于发光区513为中心与成像区514中心对称设置。如图3和图4所示,因此,当成像区514与透明层516之间构成第三角度的倾斜角γ时,同时成像区514相对于上述穿孔403s相对于中心的发光区513中心对称设置时,且推筒314受到第一驱动力将推针403自穿孔403s穿出时,推针403的针尖尖端位置在成像区514中的成像原理满足图4所示的光路图。
115.具体地,以推针403的针尖尖端位置为成像点,相对于空气(折射率为n0)为光密介质材料的透明层416的折射率为n1,且n1满足:n1sinβ=n0sinα。其中,α为成像点相对于人体组织中空气在透明层416上的入射角,β为该成像点相对于透明层416内部的折射角,同时经折射之后成像点的光路直接沿与透明层416表面呈第三角度γ的成像区514的成像平面的法线入射到成像区514中,从而实现了成像区514能够对处于前端边缘位置的推针的准确性成像,基本不会出现现有技术中的成像扭曲现象,避免对成像造成干扰,尽可能地确保精准化的注射或取样操作。
116.因此,可见,通过上述注射取样部的推塞313、推筒314、处于边缘位置的推针403和与该推针403位置中心对称的成像区514,且成像区514与透明层516之间具有夹角伽马,从而实现了在推针403精准化实现注射取样的情况下,确保能够对注射液和样本组织的尽可能排出推筒,防止在推筒残留,从而有效利用微小推筒空间。
117.可见,上述的壳体部101、驱动部102、注射取样部103、弹性缓冲部104、发光成像部105的结构为相互配合的结构形式,而非是单一的技术组合,能顾实现恰到好处的结构组成关系,力求在实现相应精准化的注射取样效果的同时,确保注射取样操作过程的安全性、稳定性,同时实现对整体装置结构的高度集成化和微型化,降低病患的手术痛苦,提高手术操作性,实现对结构的简化同时,降低手术操作难度,有利于改善病患对手术的抵触感心理。
118.覆盖层517为一柔性层状结构,包设基体511、发光区513、成像区514、穿孔403s。覆盖层517可以为一橡胶材料层,可以对基体511的前端的端面除透明层516之外的表面进行
覆盖,同时将透明层516紧密的贴覆在基体511的前端端面上。此外,由于覆盖层517为橡胶材料层,具有柔性结构性质,因此,其在被推针403扎破之后,基本不会出现碎渣,而是会出现一个可在推针403收回到外壳111内部之后可恢复并吻合的裂缝。借此,在推针403没有受到第一驱动力扎破该覆盖层517之前,装置进入人体组织的过程中,并不会像传统结构那样在基体穿孔403s中积存组织液或者血液,甚至进入外壳111内部;而在推针403扎破该覆盖层517之后并退回至外壳111内部中时,由于覆盖层517仅留下一吻合缝隙,在装置从人体组织的退出过程中,也不会像传统结构那样在基体穿孔403s中积存组织液或者血液。换言之,覆盖层517作为一结构保护层,可以有效保证外壳111与外界人体组织液和血液等之间的接触,防止内部被液体污染,影响注射或者取样操作。
119.如图1a-图5所示,根据本公开实施例,注射取样装置还包括延伸部106,延伸部106与壳体部101的后端固定连接。
120.延伸部106的前端开口与壳体部101的外壳111的后端开口连接固定,从而能够使得整个注射取样装置能够尺寸延长,从而适应于口腔、食道、胃、结肠、直肠、气管、阴道甚至子宫等相对开放的组织环境,也可以是主要的静脉血管等非开放环境的组织环境,从而极大地增强该装置的适用范围。其中延伸部106可以是柔性可弯曲的的复合材料管,为圆柱形结构,其与壳体部101的外壳111的后端开口连接,同时提供驱动部102的设置位置,使得驱动部102能够依托该延伸部106的内部结构实现驱动效果。具体地,延伸部106可以具有与驱动部102的转动柱211和旋动柱213相互连接或者固定的电机结构。
121.其中,在延伸部106的后端则可以连接到相应的操作柄上,该操作柄具有相应的控制按键、旋钮等控制用结构,以用于间隔延伸部106控制壳体部101及其内部的驱动部102、注射取样部103、弹性缓冲部104以及发光成像部105等组成部分,从而实现相应的注射或取样操作。
122.至此,已经结合附图对本公开实施例进行了详细描述。
123.以上所述的具体实施例,对本发明的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上所述仅为本发明的具体实施例而已,并不用于限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1