Desotamide在制备具有抗鸡球虫病功效的药物或饲料添加剂中的应用
desotamide在制备具有抗鸡球虫病功效的药物或饲料添加剂中的应用
技术领域
1.本发明涉及药物技术领域,特别是涉及一种desotamide在制备具有抗鸡球虫病功效的药物或饲料添加剂中的应用。
背景技术:
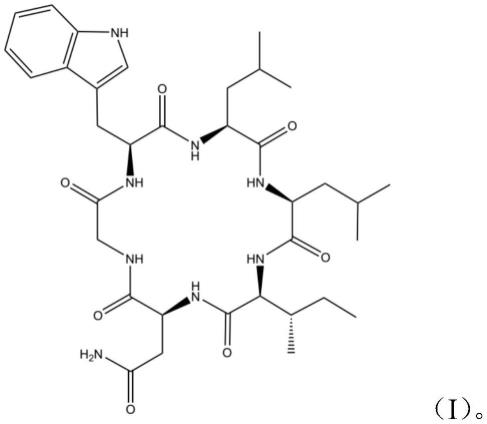
2.desotamide是深海放线菌(streptomyces sp.)天然代谢产物,为环六肽化合物,其分子式为c
35h52
n8o7,分子量为696.8,cas号为194660-14-5,化学结构如下式所示:
[0003][0004]
已有研究表明,desotamide具有抗菌的药理活性,以及较好的透膜活性与稳定性。
[0005]
鸡球虫病是一种严重危害养鸡业发展的肠道寄生虫病,能引起严重的经济损失。该病由一种或多种艾美耳球虫感染引起,具体为顶复门、孢子虫纲、真球虫目、艾美耳科、艾美耳属的原虫。鸡球虫有7个种,包括柔嫩艾美耳球虫(eimeria tenella)、毒害艾美耳球虫(e.necatrix)、布氏艾美耳球虫(e.brunetti)、堆型艾美耳球虫(e.acervulina)、巨型艾美耳球虫(e.maxima)、缓艾美耳球虫(e.mitis)和早熟艾美耳球虫(e.praecox)。鸡感染球虫后,因球虫在肠道的大量增殖损伤肠粘膜,引起大量出血,生产性能严重下降,饲料报酬降低,甚至造成鸡只死亡。柔嫩艾美耳球虫(e.tenella)是危害最为严重的虫种之一,其寄生于盲肠,可引起鸡只血便、精神萎顿、食欲减退、消瘦等临床症状。
[0006]
目前,鸡球虫病的防治仍主要依靠药物。已报道的抗球虫药多达40余种,现今广泛使用的有20种。由于抗球虫药物的长期和大量使用,鸡球虫临床野毒虫株对传统抗球虫药物产生严重的抗药性,致使现有抗球虫药物作用效果明显降低,临床缺乏有效的抗球虫药物。
技术实现要素:
[0007]
基于此,本发明提供式(i)所示结构特征的化合物在制备具有抗鸡球虫病功效的
药物或饲料添加剂中的应用。
[0008]
本发明的第一方面,提供具有如下式(i)所示结构特征的化合物在制备具有抗鸡球虫病功效的药物中的应用:
[0009][0010]
在其中一个实施例中,所述鸡球虫病为柔嫩艾美耳球虫病。
[0011]
在其中一个实施例中,所述抗鸡球虫病是指抑制鸡球虫的繁殖。
[0012]
在其中一个实施例中,所述药物包括式(i)所示结构特征的化合物以及药物上可接受的辅料。
[0013]
在其中一个实施例中,所述药物的剂型为散剂。
[0014]
本发明的第二方面,提供具有如下式(i)所示结构特征的化合物在制备具有抗鸡球虫病功效的饲料添加剂中的应用:
[0015][0016]
在其中一个实施例中,所述鸡球虫病为柔嫩艾美耳球虫病。
[0017]
在其中一个实施例中,所述抗鸡球虫病是指抑制鸡球虫的繁殖。
[0018]
在其中一个实施例中,所述饲料添加剂包括式(i)所示结构特征的化合物以及辅料。
[0019]
在其中一个实施例中,所述饲料添加剂的剂型为散剂。
[0020]
本发明通过研究发现,式(i)所示结构特征的化合物能够有效抑制鸡球虫,特别是柔嫩艾美耳球虫的繁殖,发挥优异的抗鸡球虫作用,且治疗效果明显优于对照药物磺胺氯吡嗪钠,能够为鸡球虫病的治疗提供新的解决方案,可具体应用于抗鸡球虫病的药物或饲料添加剂。
附图说明
[0021]
图1为本发明一个实施例中desotamide对柔嫩艾美耳球虫(e.tenella)繁殖的影响;图中,横坐标是desotamide的浓度,纵坐标是desotamide对柔嫩艾美耳球虫(e.tenella)繁殖的抑制率;
[0022]
图2为本发明一个实施例中阳性对照药物磺胺氯吡嗪钠对柔嫩艾美耳球虫(e.tenella)繁殖的影响;图中,横坐标是磺胺氯吡嗪钠浓度,纵坐标是磺胺氯吡嗪钠对柔嫩艾美耳球虫(e.tenella)繁殖的抑制率。
具体实施方式
[0023]
以下结合具体实施例对本发明的desotamide在制备具有抗鸡球虫病功效的药物或饲料添加剂中的应用作进一步详细的说明。本发明可以以许多不同的形式来实现,并不限于本文所描述的实施方式。相反地,提供这些实施方式的目的是使对本发明公开内容理解更加透彻全面。
[0024]
除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施例的目的,不是旨在于限制本发明。
[0025]
本发明中,“第一方面”、“第二方面”等仅用于描述目的,不能理解为指示或暗示相对重要性或数量,也不能理解为隐含指明所指示的技术特征的重要性或数量。而且“第一”、“第二”等仅起到非穷举式的列举描述目的,应当理解并不构成对数量的封闭式限定。
[0026]
本发明中,以开放式描述的技术特征中,包括所列举特征组成的封闭式技术方案,也包括包含所列举特征的开放式技术方案。
[0027]
本发明中,涉及到数值区间,如无特别说明,上述数值区间内视为连续,且包括该范围的最小值及最大值,以及这种最小值与最大值之间的每一个值。进一步地,当范围是指整数时,包括该范围的最小值与最大值之间的每一个整数。此外,当提供多个范围描述特征或特性时,可以合并该范围。换言之,除非另有指明,否则本文中所公开之所有范围应理解为包括其中所归入的任何及所有的子范围。
[0028]
本发明中涉及的百分比含量,如无特别说明,对于固液混合和固相-固相混合均指质量百分比,对于液相-液相混合指体积百分比。
[0029]
本发明中涉及的百分比浓度,如无特别说明,均指终浓度。所述终浓度,指添加成分在添加该成分后的体系中的占比。
[0030]
本发明中的温度参数,如无特别限定,既允许为恒温处理,也允许在一定温度区间内进行处理。所述的恒温处理允许温度在仪器控制的精度范围内进行波动。
[0031]
本发明提供具有如下式(i)所示结构特征的化合物在制备具有抗鸡球虫病功效的药物中的应用:
[0032][0033]
本发明通过研究发现,式(i)所示结构特征的化合物能够有效抑制鸡球虫,特别是柔嫩艾美耳球虫的繁殖,该抑制作用体现在式(i)所示结构特征的化合物在柔嫩艾美耳球虫的细胞培养(例如mdbk细胞)模型上能有效抑制柔嫩艾美耳球虫的繁殖,并且该抑制作用通过动物试验得以验证。因此证实式(i)所示结构特征的化合物能够发挥优异的抗鸡球虫作用,且治疗效果明显优于对照药物磺胺氯吡嗪钠,能够为鸡球虫病的治疗提供新的解决方案,可应用于抗鸡球虫病的药物,同时也拓展了式(i)所示结构特征的化合物的应用范围。
[0034]
在其中一个具体的示例中,提供desotamide在制备具有抗鸡球虫病功效的药物中的应用。
[0035]
在其中一个具体的示例中,所述鸡球虫为柔嫩艾美耳球虫(eimeria tenella)、毒害艾美耳球虫(e.necatrix)、布氏艾美耳球虫(e.brunetti)、堆型艾美耳球虫(e.acervulina)、巨型艾美耳球虫(e.maxima)、缓艾美耳球虫(e.mitis)或早熟艾美耳球虫(e.praecox)。
[0036]
在其中一个具体的示例中,所述鸡球虫为柔嫩艾美耳球虫。
[0037]
在其中一个具体的示例中,所述鸡球虫病为柔嫩艾美耳球虫(eimeria tenella)病、毒害艾美耳球虫(e.necatrix)病、布氏艾美耳球虫(e.brunetti)病、堆型艾美耳球虫(e.acervulina)病、巨型艾美耳球虫(e.maxima)病、缓艾美耳球虫(e.mitis)病或早熟艾美耳球虫(e.praecox)病。
[0038]
在其中一个具体的示例中,所述鸡球虫病为柔嫩艾美耳球虫病。
[0039]
在其中一个具体的示例中,所述抗鸡球虫病是指抑制鸡球虫的繁殖。
[0040]
在其中一个具体的示例中,所述药物包括式(i)所示结构特征的化合物以及药物上可接受的辅料。
[0041]
在其中一个具体的示例中,所述药物的剂型为散剂。
[0042]
本发明还提供具有如下式(i)所示结构特征的化合物在制备具有抗鸡球虫病功效的饲料添加剂中的应用:
[0043][0044]
本发明通过研究发现,式(i)所示结构特征的化合物能够有效抑制鸡球虫,特别是柔嫩艾美耳球虫的繁殖,该抑制作用体现在式(i)所示结构特征的化合物在柔嫩艾美耳球虫的细胞培养(例如mdbk细胞)模型上能有效抑制柔嫩艾美耳球虫的繁殖,并且该抑制作用通过动物试验得以验证。因此证实式(i)所示结构特征的化合物能够发挥优异的抗鸡球虫作用,且治疗效果明显优于对照药物磺胺氯吡嗪钠,能够为鸡球虫病的治疗提供新的解决方案,可应用于抗鸡球虫病的饲料添加剂,同时也拓展了式(i)所示结构特征的化合物的应用范围。
[0045]
在其中一个具体的示例中,提供desotamide在制备具有抗鸡球虫病功效的饲料添加剂中的应用。
[0046]
在其中一个具体的示例中,所述鸡球虫为柔嫩艾美耳球虫(eimeria tenella)、毒害艾美耳球虫(e.necatrix)、布氏艾美耳球虫(e.brunetti)、堆型艾美耳球虫(e.acervulina)、巨型艾美耳球虫(e.maxima)、缓艾美耳球虫(e.mitis)或早熟艾美耳球虫(e.praecox)。
[0047]
在其中一个具体的示例中,所述鸡球虫为柔嫩艾美耳球虫。
[0048]
在其中一个具体的示例中,所述鸡球虫病为柔嫩艾美耳球虫(eimeria tenella)病、毒害艾美耳球虫(e.necatrix)病、布氏艾美耳球虫(e.brunetti)病、堆型艾美耳球虫(e.acervulina)病、巨型艾美耳球虫(e.maxima)病、缓艾美耳球虫(e.mitis)病或早熟艾美耳球虫(e.praecox)病。
[0049]
在其中一个具体的示例中,所述鸡球虫病为柔嫩艾美耳球虫病。
[0050]
在其中一个具体的示例中,所述抗鸡球虫病是指抑制鸡球虫的繁殖。
[0051]
在其中一个具体的示例中,所述饲料添加剂包括式(i)所示结构特征的化合物以及辅料。
[0052]
在其中一个具体的示例中,所述饲料添加剂的剂型为散剂。
[0053]
以下为具体的实施例。
[0054]
实施例1
[0055]
一、实验材料
[0056]
(1)desotamide购自阿拉丁生化科技公司,磺胺氯吡嗪钠购自merck公司。
[0057]
(2)球虫卵囊:柔嫩艾美耳球虫(e.tenella)广东株孢子化卵囊,由广东省农业科学院动物卫生研究所保存,使用前在无球虫雏鸡体内复壮。
[0058]
(3)细胞:mdbk细胞(即牛肾细胞),由广东省农业科学院动物卫生研究所保存。
[0059]
二、实验方法:
[0060]
以e.tenella mdbk细胞培养模型评价抗球虫效果,具体评价步骤包括:
[0061]
(1)用0.25%的胰蛋白酶消化液消化生长至融合状态达到80%以上的mdbk细胞,以4
×
105个/孔的细胞浓度铺板12孔细胞培养板,置于37℃含5%co2的培养箱中培养24h。
[0062]
(2)待12孔培养板的细胞生长至融合状态达80%及以上时,每孔接种10
×
104个子孢子/ml,4h后弃去培养基,以pbs洗涤3次,洗掉悬浮的子孢子,每孔加入5%胎牛血清的mem培养基。
[0063]
(3)试验分组:
[0064]
参照待测药物(desotamide)组,设5个药物浓度梯度,具体为0.01μm、0.1μm、1μm、10μm、100μm,每个浓度梯度设3个重复;
[0065]
阳性对照(磺胺氯吡嗪钠)组,设5个药物浓度梯度,具体为0.01μm、0.1μm、1μm、10μm、100μm,每个浓度梯度设3个重复;
[0066]
空白对照组:参照待测药物组(即desotamide组)和阳性对照组(即磺胺氯吡嗪钠组)加入待测药物和阳性对照药物的体积,添加等体积的培养基,该培养基为5%胎牛血清的mem培养基,设3个重复。
[0067]
(4)置于37℃含5%co2的培养箱中继续培养,培养48h后弃去培养基,pbs洗涤3次,提取各孔样品的总rna。以real-time pcr(rt-pcr)检测各试验药物对柔嫩艾美耳球虫(e.tenella)繁殖的影响。
[0068]
real-time pcr引物如下。
[0069]
特异性扩增柔嫩艾美耳球虫(e.tenella)actin引物,
[0070]
etactin-f:5
’‑
caccaccgccgagaaaga-3’(seq id no.1),
[0071]
etactin-r:5
’‑
gaacaacattg-ccgtagagg-3’(seq id no.2);
[0072]
特异性扩增宿主细胞actin引物,
[0073]
bactin-f:5
’‑
ggatgaggctcagagcaagaga-3’(seq id no.3),
[0074]
bactin-r:5
’‑
tcgtcccagttggtg-acgat-3’(seq id no.4)。
[0075]
以δδc
t
方法计算各试验药物对细胞培养水平上柔嫩艾美耳球虫(e.tenella)生长发育的抑制效果。
[0076]
real-time pcr反应体系和反应程序如表1和表2所示。
[0077]
表1 real-time rt-pcr反应体系
[0078][0079]
表2 real-time pcr反应程序
[0080][0081]
评价指标:通过real-time pcr获得实验组和对照组的δc
t
=c
t
[et actin]-c
t
[h actin],δδc
t
=δc
t[exp]-δc
t[ref]
,最终获得待筛选药物的抗球虫作用效果:inhibition(%)=100
×
(1-2-δδct
)。
[0082]
三、实验结果:
[0083]
结果见图1和图2,图1为待测药物desotamide对柔嫩艾美耳球虫(e.tenella)繁殖的影响;图中,横坐标是desotamide的浓度,纵坐标是desotamide对柔嫩艾美耳球虫(e.tenella)繁殖的抑制率;图2为阳性对照药物磺胺氯吡嗪钠对柔嫩艾美耳球虫(e.tenella)繁殖的影响;图中,横坐标是磺胺氯吡嗪钠浓度,纵坐标是磺胺氯吡嗪钠对柔嫩艾美耳球虫(e.tenella)繁殖的抑制率。
[0084]
分别计算各组药物对柔嫩艾美耳球虫(e.tenella)的抑制作用,待测药物desotamide对柔嫩艾美耳球虫(e.tenella)的繁殖具有明显的抑制效果,其mic
50
值为44.63μm;阳性对照药物磺胺氯吡嗪钠对柔嫩艾美耳球虫(e.tenella)具有抑制效果,其mic
50
值为65.48μm。上述结果表明,待测药物desotamide具有良好的抗柔嫩艾美耳球虫(e.tenella)作用,且明显优于阳性对照药物磺胺氯吡嗪钠。
[0085]
同时,根据图1还可知,随着desotamide浓度的增加,其抑制柔嫩艾美耳球虫(e.tenella)繁殖的作用增强,抑制作用具有浓度依赖性。
[0086]
实施例2
[0087]
一、实验材料:
[0088]
(1)散剂型的制备:取1gdesotamide(含量不低于98%)和99g淀粉混匀,制备desotamide散剂型;
[0089]
(2)对照药物:市售抗球虫药物三字球虫粉(30%磺胺氯吡嗪钠),由上海诺华动物保健有限公司生产。
[0090]
(3)球虫卵囊:柔嫩艾美耳球虫(e.tenella)广东株孢子化卵囊,由广东省农业科学院动物卫生研究所保存,使用前在无球虫雏鸡体内复壮。
[0091]
(4)雏鸡:岭南黄肉鸡,由广东省农业科学院动物科学研究所提供,饲养于已消毒的专用动物房内;鸡笼和所用器皿均严格消毒,自由采食和饮用纯净水;试验前观察雏鸡有无临床症状及连续2天检查粪便有无球虫卵囊,备用。
[0092]
(5)饲料:由广东省新南都饲料科技有限公司定制育雏料,不含任何抗球虫药物。
[0093]
二、实验方法:
[0094]
(1)分组:按试验分组及处理将150只岭南黄肉鸡饲养至14日龄,逐只称重,淘汰弱雏和体重过大者,将剩余雏鸡随机分成4组,每组30只,并适当调整使每组雏鸡总体重大致相等。
[0095]
(2)处理:除第1组(空白对照组)外,第2~4组雏鸡一次性经口灌服柔嫩艾美耳球虫(e.tenella)孢子化卵囊l
×
105个/羽;攻虫当天,第3~4组分别饲喂含抗球虫药物的饲料7天。试验鸡的分组情况及药物的用法用量见表3。
[0096]
表3实验分组情况
[0097][0098]
备注:表中“g/kg”指每1kg饲料含有的药物重量。
[0099]
每天观察并记录鸡群的精神状况、采食量、粪便情况等;对死亡雏鸡称重,剖检,若为柔嫩艾美耳球虫(e.tenella)感染引起死亡则病变记分为+4分;所有雏鸡于感染后第7天逐只称重,剖检,进行盲肠病变记分;最后计算各组雏鸡的增重和饲料报酬。
[0100]
药效判定方法及标准抗球虫指数(aci)按美国默克公司推荐的公式计算:
[0101]
aci=(相对增重率+存活率)-(卵囊值+病变值);
[0102]
相对增重率(%)=(试验组增重
÷
空白对照组增重)
×
100%;
[0103]
存活率(%)=(各组存活雏鸡数
÷
各组雏鸡总数)
×
100%。
[0104]
病变按五级记分:
[0105]
①
无卵囊,盲肠正常,为0分;
[0106]
②
有卵囊,盲肠黏膜稍增厚,有少量散在出血或少量血样肠内容物,为+1分;
[0107]
③
有卵囊,盲肠黏膜增厚,有明显出血或明显血样肠内容物,为+2分;
[0108]
④
有卵囊,盲肠黏膜增厚,有大量凝血块或血样肠芯,为+3分;
[0109]
⑤
雏鸡因球虫病死亡或有大量卵囊,盲肠外观呈酱油色(或小肠中部有点状坏死灶,黏膜面呈绯红色),肠管明显肿大,内容物形成明显的血样肠芯,为+4分;
[0110]
病变值=每组平均病变记分
×
10;
[0111]
卵囊值由盲肠内容物克粪便卵囊数(opg)换算而来。
[0112]
药效判定标准是aci《120为无效,120~160为弱效,160~180为中效,180以上为强效。
[0113]
三、实验结果:
[0114]
临床症状观察:接种柔嫩艾美耳球虫(e.tenella)孢子化卵囊的对照组(试验组2)第2天,病鸡出现精神沉郁,采食量下降;第5天出现明显血便,随后血便逐渐减少。
[0115]
分别计算各组的抗球虫指数,结果见表4。待测药物组(试验组4)的抗球虫指数(aci)为172.2,明显高于对照药物组(试验组3)的162.7,具有良好的抗柔嫩艾美耳球虫(e.tenella)作用,且优于市售抗球虫药物三字球虫粉。
[0116]
表4各组抗球虫指数
[0117][0118]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0119]
以上所述实施例仅表达了本发明的几种实施方式,便于具体和详细地理解本发明的技术方案,但并不能因此而理解为对发明专利保护范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。应当理解,本领域技术人员在本发明提供的技术方案的基础上,通过合乎逻辑的分析、推理或者有限的试验得到的技术方案,均在本发明所附权利要求的保护范围内。因此,本发明专利的保护范围应以所附权利要求的内容为准,说明书及附图可以用于解释权利要求的内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1