放射核素标记的过氧化氢酶及其应用
1.本发明涉及放射治疗、临床核医学技术领域,具体地说,涉及一种放射核素标记的过氧化氢酶及其应用。
背景技术:
2.癌症的传统治疗方式主要包括:手术,化学治疗和放射治疗。核素靶向治疗是介于化学治疗和放射治疗之间的一种独特的治疗方式。核素靶向治疗原理是利用核素发射出的α、β射线、俄歇电子或内转换电子在病变组织中产生一系列的电离辐射生物效应,导致细胞增殖功能丧失、代谢紊乱失调、细胞衰老或凋亡,从而达到治疗的目的。与传统的放射治疗不同,核素靶向治疗的靶点是细胞水平的疾病,并非解剖水平的疾病。核素靶向治疗包括放射性同位素和靶向载体两部分,结合了同位素的电离辐射和分子靶向的特异性,它们自然地聚集在或被设计成靶向肿瘤,通过向特定靶点输送高剂量的电离辐射,选择性地杀死肿瘤细胞,同时尽量减少对正常细胞的损伤。放射性核素治疗是一种近年来发展迅速的治疗方法,其能够近距离利用电离辐射杀伤肿瘤细胞,在肿瘤治疗中已展现出选择性高、治疗响应率高、副作用小等优势,能够有效治疗全身转移灶,解决肿瘤异质性问题,改善生活质量。
3.肿瘤介入治疗是一项微创治疗技术,是指通过影像设备的监视及引导作用,借助导管及穿刺针等介入器械,经由身体的微小创口或自然孔道将药物或器械置入肿瘤部位。肿瘤介入治疗具备高效、安全、微创、靶向等优点,属于肿瘤疾病综合治疗方案的重要组成部分。肿瘤介入治疗包含非血管介入治疗及血管介入治疗两种模式,前者主要为经皮穿刺肿瘤消融术,后者包含栓塞治疗及经导管动脉灌注化疗。肿瘤消融包含物理消融及化学消融两种模式。物理消融包含微波消融及射频消融等多种模式。在化学消融方案中,将借助穿刺针直接将乙酸或无水乙醇注入肿瘤内,从而加速肿瘤的坏死进程,操作过程相对便捷,经济价值较高,疗效显著,不过消融的体积相对较小,仅适用于治疗小肝癌及少数因部位特殊难以进行物理消融处理的病例经放疗栓塞处理后。
4.核素内照射治疗是一种很有前景的核素靶向治疗手段。与化疗和外照射放疗相比,内照射治疗具有独特的优点,它以能高度选择性聚集在肿瘤组织的物质作为载体,如单克隆抗体、生物活性肽等,将放射性核素靶向运送到病灶内,或某些肿瘤细胞能直接摄取放射性核素(如
131
i治疗甲状腺癌),而后核素发出的射线粒子(α粒子、β射线、内转换电子及俄歇电子)通过电离辐射生物效应发挥最大的肿瘤杀伤作用,而对正常组织产生尽可能小的损伤。
5.目前,多种放射性核素治疗药物已被fda批准应用于临床肿瘤治疗,包括:
177
lu-dotatate治疗神经内分泌肿瘤、
90
y-ibritumomab tiuxetan(
90
y-it)治疗非霍奇金淋巴瘤、
177
lu-psma-617治疗转移性去势抵抗性前列腺癌。放射性核素靶向治疗在临床上的成功应用,为开展放射核素靶向治理研究提供了新思路。
6.对于放射性同位素疗法而言,临床目前使用的如碘-125粒子源植入技术和钇-90 微球经动脉介入栓塞技术对于肿瘤有很好的杀伤作用,但两种技术都无法改善肿瘤部位的
乏氧环境。
技术实现要素:
7.本发明的目的是提供一种放射核素标记的过氧化氢酶及其应用。
8.本发明构思如下:提供一种放射核素内治疗的方法,过氧化氢酶(catalase,cat)通过双功能偶联剂修饰之后,进行放射性治疗核素(包括但不限于
90
y、
177
lu、
225
ac或
213
bi)标记,得到放射性核素治疗探针
90
y/
177
lu/
225
ac/
213
bi-cat等,与海藻酸钠混合之后,局部注射于肿瘤内,以期用于肿瘤的放射核素治疗。
9.过氧化氢酶是一种内源性抗氧化酶,在人体内,编码过氧化氢酶的基因定位至染色体11p13,由12个内含子和13个外显子所组成。先将过氧化氢酶进行双功能偶联剂dota(1,4,7,10-四氮杂环十二烷-1,4,7,10-四羧酸),双功能偶联剂dtpa(二乙烯三胺五乙酸)或者双峰双功能配体3pc-neta-ncs修饰之后,进行治疗性放射性核素(
90
y/
177
lu/
225
ac/
213
bi等)标记得到相应的治疗性放射性分子探针,评价
90
y/
177
lu/
225
ac/
213
bi-cat分子探针的放射化学与生物学性质,评估分子探针的亲和力、特异性和靶向性。
10.为了实现本发明目的,第一方面,本发明提供一种放射核素标记的过氧化氢酶,其是将过氧化物酶经双功能偶联剂修饰后,进行放射性核素标记得到的。
11.所述双功能偶联剂包括但不限于dota、dtpa或3pc-neta-ncs等。
12.3pc-neta-ncs可参见文献chong hs, song ha, ma x, milenic de, brady ed, lim s, lee h, baidoo k, cheng d, brechbiel mw. novel bimodal bifunctional ligands for radioimmunotherapy and targeted mri. bioconjug chem. 2008 jul;19(7):1439-47. doi: 10.1021/bc800050x. epub 2008 jun 20. pmid: 18564868; pmcid: pmc2497452.所述放射性核素包括但不限于
90
y、
177
lu、
225
ac或
213
bi等β核素和α核素(
90
y、
177
lu属于β核素,
225
ac、
213
bi属于α核素)。第二方面,本发明提供
177
lu标记的过氧化氢酶的制备方法,包括以下步骤:(1)过氧化氢酶经dota修饰,得到标记前体dota-cat;(2)标记前体dota-cat经
177
lu标记,得到
177
lu-dota-cat。
13.进一步地,步骤(1)包括:a、pd-10预装凝胶柱的活化:将pd-10柱(脱盐层析柱)的上端帽取下,倒出保护液,沿末端冲压痕剪去保护塑封。将pd-10柱体垂直固定于铁架台,下面放置烧杯,接淋洗液。用ph 7.4的0.01m pbs平衡柱体,每次加5 ml,重力流速,重复5次;b、取2 mg过氧化氢酶与5-10倍摩尔量的双功能螯合剂dota,用0.1m nahco3调节ph至9.0-9.3,于室温下振荡反应(过氧化氢酶氨基酸上游离的氨基与dota-nhs发生缩合反应)2h;c、将步骤b得到的反应混合物用步骤a平衡后的pd-10柱进行纯化,得到标记前体dota-cat(2-5 mg/ml)。
14.步骤(2)包括:将1 ml 0.05m hcl和65 ul 1m naac混匀作为标记缓冲液;向100 ul或100 ug标记前体dota-cat中加入100-150 ul标记缓冲液,然后加入
177
lu;将体系ph调至5.5,于22oc-40oc反应30-60 min,用脱盐柱pd-10分离纯化,得到
177
lu-dota-cat。
15.第三方面,本发明提供按照所述方法制备得到的
177
lu标记的过氧化氢酶。
16.第四方面,本发明提供一种组合物,由所述放射核素标记的过氧化氢酶或所述
177
lu标记的过氧化氢酶以及可溶性海藻酸盐组成。
17.可选地,所述组合物包含免疫佐剂cpg。
18.组合物中过氧化氢酶的浓度为2-10 mg/ml,海藻酸盐的浓度为2-10 mg/ml,放射核素的剂量为5-20 mci。
19.进一步地,海藻酸盐为海藻酸钠、海藻酸钾或其混合物,优选海藻酸钠。
20.第五方面,本发明提供所述放射核素标记的过氧化氢酶、所述
177
lu标记的过氧化氢酶或所述组合物的以下任一应用:1)用于制备抗肿瘤药剂;2)用于肿瘤(介入)内治疗。
21.所述肿瘤包括原位肿瘤和转移瘤,在治疗原位肿瘤的同时实现治疗远端或转移瘤的目的。
22.本发明中,过氧化氢酶可以高效地分解肿瘤组织间的内源性过氧化氢产生氧气,通过改善肿瘤乏氧以增强放疗疗效;cpg作为免疫佐剂,可以与内放疗摧毁肿瘤后其残留物中肿瘤相关性抗原相互作用,产生肿瘤特异性的免疫反应;而海藻酸钠在局部注射到肿瘤内后,可以与肿瘤细胞间隙液中的钙离子结合能快速形成凝胶,将放射性治疗核素(
90
y/
177
lu/
225
ac/
213
bi等)标记的过氧化氢酶滞留于肿瘤内,从而增强其效果并且降低对正常器官的辐射副作用。
23.90
y和
177
lu是β放射性核素,
90
y的能量较高(2,280 kev)穿透能力较强(12 mm),对于肿瘤细胞或异常增殖组织等具有较强的杀灭作用。与
90
y相比,
177
lu能发射出小离子范围的β-射线(0.5 mev),这样不仅能够保证射线能量传输到肿瘤区域,还能减少对周边正常组织的伤害。
225
ac和
213
bi是α放射性核素,与β放射性核素相比,
225
ac(6000-8000 kev)和
213
bi(》6000 kev)的电离作用更强,穿透能力较弱(
225
ac max range:0.06-0.09 mm; 213
bi max range:84 μm),所以α放射性核素比β放射性核素的细胞毒性作用更强。因此,
90
y/
177
lu/
225
ac/
213
bi-cat治疗用放射性分子探针为肝癌,乳腺癌、宫颈癌,肾癌等患者的较大肿瘤的治疗提供新思路。
24.本发明提供的
90
y/
177
lu/
225
ac/
213
bi-cat探针能较长时间滞留在肿瘤中,全身分布较低,安全性良好,能够明显抑制动物模型肿瘤的生长,以期用于肿瘤患者的局部放射核素治疗。
附图说明
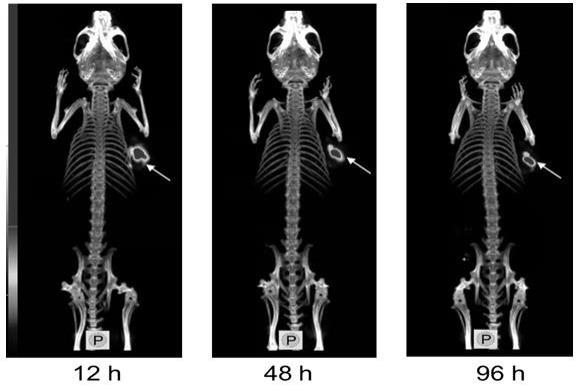
25.图1为本发明较佳实施例中人源结直肠癌ls174t皮下瘤模型在注射
177
lu-dota-cat之后12 h、48 h和96 h的micro-spect显像。
26.图2为本发明较佳实施例中小鼠结肠癌细胞ct26皮下瘤模型的
177
lu-dota-cat治疗实验的肿瘤生长曲线。
27.图3为本发明较佳实施例中人源结直肠癌ls174t皮下瘤模型的
177
lu-dota-cat治疗实验的肿瘤生长曲线。
28.图4为本发明较佳实施例中人源肺癌a549皮下瘤模型的
177
lu-dota-cat治疗实验
的肿瘤生长曲线。
29.图5为本发明较佳实施例中治疗组和对照组小鼠主要器官的切片图。
具体实施方式
30.本发明提供一种肿瘤核素靶向治疗药物,过氧化物酶经双功能偶联剂dota、dtpa、3pc-neta-ncs修饰之后,进行治疗性放射性核素
90
y、
177
lu、
225
ac或
213
bi标记。其中,双功能偶联剂包括但不限于dota、dtpa或3pc-neta-ncs。
31.本发明采用如下技术方案:
90
y、
177
lu、
225
ac或
213
bi对cat标记:cat进行双功能螯合剂dota、dtpa或3pc-neta-ncs修饰后,对制备得到的前体进行
90
y (β-emitter;t
1/2
=64 h; emax: 2,280 kev; max range: 12 mm),
177
lu(β-emitter;t
1/2
=6.7 d;emax: 496 kev; max range: 1.5 mm),
225
ac (α-emitter;t
1/2
=10.0 d;emax: 6,000-8,000 kev; max range: 0.06-0.09 mm),
213
bi (α-emitter;t
1/2
=46 min;emax: 》6,000 kev; max range: 84 μm)等治疗性放射性核素标记。
32.以放射性核素
177
lu为例,具体标记方法如下:cat进行双功能螯合剂dota、dtpa或3pc-neta-ncs修饰后,得到相应的标记前体。按照1 ml 0.05m hcl对应65 ul 1m naac来配置标记缓冲液,待用;100 ul(100ug)标记前体dota-cat中,加入100-150 ul标记缓冲液,然后加入
177
lu;将ph调至5.5,于22℃-40oc反应30-60 min,用脱盐柱pd-10分离纯化,得到
177
lu-dota-cat。纯化得到的
177
lu-dota-cat放射性化学纯度大于90%。取适量经无菌过滤的产品制剂进行质量控制检验,所有检测项目均合格后进行后期研究。
33.将
90
y/
177
lu/
225
ac/
213
bi-cat与海藻酸钠混合之后,局部注射于肿瘤区域,用于肿瘤放射核素内治疗。
34.以下实施例用于说明本发明,但不用来限制本发明的范围。若未特别指明,实施例中所用的技术手段为本领域技术人员所熟知的常规手段,所用原料均为市售商品。
35.以下实施例中使用的cat(genbank:np_001743.1)经过蛋白表达纯化合成。
36.dota、dtpa、3pc-neta-ncs购自sigma-aldrich公司。
37.核素
177
lu购自德国tlg公司。
38.脱盐层析柱pd-10购自ge公司。
39.实施例1 放射核素标记的过氧化氢酶的制备及肿瘤治疗用途1、利用放射核素
177
lu标记cat(1)制备标记前体:将pd-10柱子上端帽取下,倒出保护液,沿末端冲压痕剪去保护塑封。将pd-10柱体垂直固定于铁架台,下面放置烧杯,接淋洗液。用ph 7.4的0.01m pbs平衡柱体,每次加5 ml,重力流速,重复5次;取2 mg过氧化氢酶与5倍摩尔量的双功能螯合剂dota反应,用0.1m nahco3调节ph至9.0-9.3,于室温下振荡反应2 h,通过脱盐柱pd-10纯化,得到标记前体dota-cat(2-5 mg/ml)。
40.(2)放射核素
177
lu标记cat:按照1 ml 0.05m hcl对应65 ul 1m naac来配置标记缓冲液,待用;100 ul(100ug)标记前体dota-cat中,加入100-150 ul标记缓冲液,然后加入
177
lu;然后加入
177
lu;将ph调至5.5,于37 o
c反应30 min,用脱盐柱pd-10分离纯化,得到
177
lu-dota-cat。纯化得到的
177
lu-dota-cat放射性化学纯度大于90%。取适量经无菌过滤的产品制剂进行质量控制检验,所有项目均合格后进行后期研究。用radio-tlc测定标记率及放射化学纯度。tlc展开剂:甲醇与1 m醋酸铵按照1:1体积比混合。
41.2、抗肿瘤药剂的制备纯化后的
177
lu-dota-cat与海藻酸钠(10 mg/ml)混合,终产品的浓度为
177
lu-dota-cat 37 mbq/ml,海藻酸钠5 mg/ml。
42.3、在balb/c(雌性,5-6周,体重18-20 g)小鼠腋下接种ls174t肿瘤细胞建立小鼠皮下肿瘤模型在人源结直肠癌ls174t皮下瘤模型在注射
177
lu-dota-cat后12 h、48 h和96 h的micro-spect显像。准备5只ls174t动物模型,每只小鼠肿瘤局部注射方式(肿瘤上、下、左、右四个方位分点注射)注射1.85 mbq(50
ꢀµ
l)
177
lu-dota-cat(alg);分别在注射标记产物之后12 h、48 h和96 h的进行micro-spect显像。采用静态扫描模式扫描小鼠,能量窗350-700 kev,扫描时间为20 min,扫描过程中以1 l/min的异氟烷气体维持麻醉小鼠,采用有序子集最大期望值(ordered subsets expectation maximization,osem)软件进行图像重建,并在进行衰减校正后采用mmwks软件进行图像分析处理。
177
lu-dota-cat(alg)具有良好的肿瘤滞留能力,实验结果见图1。
43.4、在balb/c(雌性,5-6周,体重18-20 g)小鼠背部接种ct26肿瘤细胞建立小鼠皮下肿瘤模型,并将小鼠随机分配为3组,其中一组小鼠为空白对照组,另外两组小鼠分别以肿瘤局部注射方式(肿瘤上、下、左、右四个方位分点注射)注射1.85 mbq(50
ꢀµ
l)
177
lu-dota-cat(alg)和1.85 mbq(50
ꢀµ
l)
177
lu-dota-hsa,注射后每2天记录一次小鼠肿瘤尺寸。
177
lu-dota-cat(alg)可以有效改善肿瘤组织的乏氧微环境,且显著抑制肿瘤生长,实验结果见图2。
44.5、建立人结肠腺癌细胞ls174t皮下荷瘤鼠模型和肺癌a549皮下荷瘤鼠模型,并将小鼠随机分配为实验组和对照组(50
ꢀµ
l生理盐水),每组各5只。实验组瘤内注射
177
lu-dota-cat(alg),注射后于1,3,5,7,10,14,21天测量荷瘤鼠的肿瘤尺寸和重量。
177
lu-dota-cat(alg)可以有效抑制肿瘤生长,实验结果见图3和图4。
45.治疗后分别取出实验组和对照组的心脏、肝脏、脾脏、肺、肾脏等主要器官,进行he染色,验证组织是否存在病理改变。小鼠在整个治疗过程中,皮肤状态良好,体重稍微,行为正常,he结果出现异常,说明
177
lu-dota-cat(alg)在有效剂量范围内无明显毒副作用,实验结果见图5。
46.图1是
177
lu-dota-cat在人结直肠腺癌ls174动物模型中12 h、48 h和96 h的micro-spect显像,来监测动物模型体内
177
lu-dota-cat分布的。图像结果显示
177
lu-dota-cat主要滞留在肿瘤区域,在12 h、48 h和96 h的肿瘤区域有较高的放射性摄取,全身非特异性摄取较低。直至96 h 时,
177
lu-dota-cat仍主要滞留在动物模型的肿瘤区域,全身其他组织低摄取,可大幅度减少放射性元素对正常器官和组织的毒副作用。
47.图2是小鼠结肠癌细胞ct26皮下瘤模型的
177
lu-dota-cat治疗实验的肿瘤生长曲线。与空白组小鼠相比,经放疗的小鼠肿瘤生长较慢,其中
177
lu-dota-cat含有过氧化氢酶,具有改善肿瘤乏氧微环境的效果,与没有乏氧改善效果的
177
lu-dota-hsa相比,经
177
lu-dota-hsa治疗的小鼠,肿瘤生长曲线明显变缓,说明肿瘤生长得到了抑制。我们的制剂通过单次瘤内注射,达到了抑制肿瘤生长的效果,显著减缓了肿瘤进程,初步验证了该制剂的疗
效。
48.图3是人源结直肠癌ls174t皮下瘤模型的
177
lu-dota-cat治疗实验的肿瘤生长曲线;与空白组小鼠相比,经
177
lu-dota-cat治疗的小鼠肿瘤生长较慢,显著减缓了肿瘤增长。
49.图4是人源肺癌a549皮下瘤模型的
177
lu-dota-cat治疗实验的肿瘤生长曲线;与空白组小鼠相比,经
177
lu-dota-cat治疗的小鼠肿瘤生长较慢,显著减缓了肿瘤增长。
50.图5是治疗组和对照组小鼠主要器官的切片图。he结果未出现异常。小鼠内放疗治疗实验过程中,也未观察到小鼠出现任何明显的不良反应,体重正常,行为正常,说明
177
lu-dota-cat在有效剂量范围内无明显毒副作用。
51.利用
90
y/
177
lu/
225
ac/
213
bi-cat等核素靶向治疗,为局部肿瘤治疗提供新的治疗手段。
52.虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之做一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1