羊肚菌菌丝体提取物的制备方法及作为紫外吸收剂的应用
1.本发明属于生物化工领域,更具体地,涉及一种羊肚菌菌丝体提取物的制备方法及作为紫外吸收剂的应用。
背景技术:
2.羊肚菌是一类珍稀的药食两用真菌,已有研究发现羊肚菌不仅在医药、保健品上具有降血脂、抗疲劳、抗肿瘤、抗放射以及调节免疫力作用;在化妆品领域也具有美容和抗衰老的功能。羊肚菌也一直是一热门研究,现有研究主要集中在菌丝体发酵培育和发酵条件优化,以提高羊肚菌多糖的含量,从而提高羊肚菌的食用价值。
3.紫外线照射皮肤会使大量表皮细胞死亡,人体也会产生一种黑色素来保护皮肤,随着黑色素在人体皮肤表层的积累和沉淀会导致皮肤变黑,通常导致人体皮肤变黑的紫外线波长在290-320nm,因此,防止紫外线被人体表皮细胞吸收是防晒的关键和根本。
4.现有防晒品主要分为化学防晒型、物理防晒型和物理化学结合防晒型,其中化学防晒主要是利用吸收紫外的原理,通常利用透光物质吸收紫外线,使其转化为分子振动能或热能达到防晒的功效,但容易引起敏感肌人群过敏的现象;物理防晒是利用形成的保护膜反射阳光,防止紫外线穿透皮肤表面,但容易出现毛孔堵塞,且其滋润性差,使用受到一定局限。
技术实现要素:
5.针对现有技术的以上缺陷或改进需求,本发明提供了一种羊肚菌菌丝体提取物的制备方法及作为紫外吸收剂的应用,其目的在于发现并证实羊肚菌菌丝体发酵液提取物的紫外吸收作用,由此解决现有防晒技术难以有效防止紫外线穿透皮肤表面的技术问题。
6.为实现上述目的,按照本发明的一个方面,提供了一种羊肚菌菌丝体发酵液提取物的制备方法,其包括以下步骤:
7.(1)将发酵完成的羊肚菌菌丝体发酵液提取物和菌丝球共同匀浆后,50-80℃水浴加热15-30min,获得羊肚菌菌丝体匀浆;
8.(2)将步骤(1)经过固液分离获得澄清的液相,冻干制成粉末状,即为所述羊肚菌菌丝体发酵液提取物。
9.优选地,所述羊肚菌菌丝体发酵液提取物的制备方法,其所述发酵完成的羊肚菌菌丝体发酵液,按照如下方法制备:
10.将羊肚菌菌丝体接种至液体发酵培养基,发酵至菌丝体由丝状长成小球状的菌丝球,直至菌丝球不再变大且液体发酵培养基由白色浑浊液体变为黄褐色澄清液体为止;所述液体发酵培养基,包括0.25%-1%土豆淀粉、3-5%大豆蛋白、ph值为5-6。
11.按照本发明的另一个方面,提供了一种羊肚菌菌丝体发酵液提取物,其所述发酵液提取物,包括发酵液和菌丝体内的热稳定性物质,按照本发明所述的制备方法制备。
12.按照本发明的另一个方面,还提供了一种本发明所述的羊肚菌菌丝体发酵液提取
物在制备紫外吸收剂中的应用。
13.优选地,所述羊肚菌菌丝体发酵液提取物在制备紫外吸收剂中的应用,其应用于制备吸收290-320nm波段的紫外吸收剂。
14.按照本发明的另一个方面,还提供了一种紫外吸收剂,其包括本发明所述羊肚菌菌丝体发酵液提取物。
15.优选地,所述紫外吸收剂,其还包括,抗坏血酸、抗坏血酸衍生物中一种或组合。
16.优选地,所述紫外吸收剂,其按照重量份数计,包括1-5份羊肚菌菌丝体发酵液提取物和10-15份抗坏血酸。
17.按照本发明的另一个方面,还提供了一种防晒制剂,其包括本发明所述的羊肚菌丝体发酵液提取物或者紫外吸收剂。
18.优选地,所述防晒制剂,其所述羊肚菌菌丝体发酵液提取物或者紫外吸收剂添加量在100μg/ml以上,其中羊肚菌菌丝体发酵提取物更优选5mg/ml以上。
19.总体而言,通过本发明所构思的以上技术方案与现有技术相比,能够取得下列有益效果:
20.本发明提供的羊肚菌菌丝体提取物是一种具有天然抗紫外功效,紫外线吸收效果和紫外稳定性良好、具有较高的安全性,并且长期接触实验显示其对皮肤表面无过敏反应,其对新型防晒品的研发具有重要指导意义。
21.通过羊肚菌菌丝体的液体发酵,将发酵液和菌球共同匀浆后灭活,固液分离获得澄清的液相,冻干制成粉末状,即得到羊肚菌菌丝体发酵液提取物,对此提取物利用紫外分光光度法测定spf值,并通过细胞实验确定其毒性及抗紫外活性,之后测定样品紫外吸收的稳定性,从而证明羊肚菌菌丝体发酵液提取物作为防晒化妆品原料的可能性。
附图说明
22.图1不同浓度的提取物样品对hepg 2细胞存活率;
23.图2羊肚菌菌丝体发酵液提取物成分含量测定;
24.图3提取物和茶多酚在290-320nm之间的吸光度;
25.图4提取物、抗坏血酸和茶多酚在日光照射下的稳定性;
26.图5细胞紫外损伤的造模实验结果;
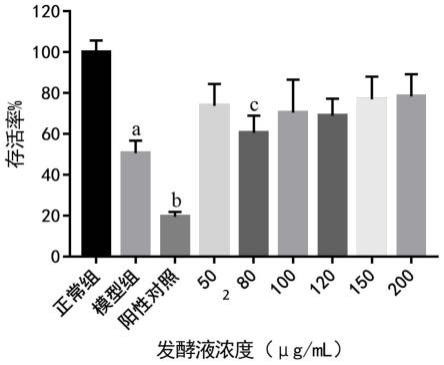
27.图6羊肚菌菌丝体发酵液提取物与茶多酚对细胞光损伤的保护效果比较。
具体实施方式
28.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅用以解释本发明,并不用于限定本发明。此外,下面所描述的本发明各个实施方式中所涉及到的技术特征只要彼此之间未构成冲突就可以相互组合。
29.我们经试验发现羊肚菌菌丝体提取物对紫外有着明显的吸收作用,其抗紫外活性较强,尤其是在uvb区290-320nm具有明显的紫外吸收效果,进一步实验表明,羊肚菌菌丝体发酵液提取物的抗紫外活性与其浓度有着良好的量效关系,添加600μg/ml羊肚菌菌丝体发酵液提取物,测定spf值达6.32,其与100μg/ml茶多酚标准品的spf值相当;当添加量同为
1mg/ml,羊肚菌菌丝体发酵液提取物的spf约为10,而抗坏血酸(vc)的spf约为2,另外,实验结果显示,羊肚菌菌丝体发酵液提取物和抗坏血酸组合物稳定性提高,且羊肚菌菌丝体发酵液提取物和抗坏血酸组所覆盖的紫外波段不同,其组合物能更有效地对抗宽波谱范围的紫外线造成的伤害,说明羊肚菌菌丝体发酵液提取物的抗紫外持续时间显著优于抗坏血酸;另外,抗紫外稳定性实验结果显示,羊肚菌菌丝体发酵液提取物在持续24小时日光照射条件下,spf没有表现出下降反而有上升趋势,而茶多酚有着明显下降,已有研究表明茶多酚具有吸收紫外的作用,说明羊肚菌菌丝体发酵液提取物抗紫外稳定性明显优于茶多酚,可用作防晒制剂的原料。
30.而现有紫外吸收剂主要是化学品类,如水杨酸酯类、苯酮类、苯并三唑类、取代丙烯腈类、三嗪类和受阻胺类,这些紫外吸收剂通常用作光稳定剂,主要是为了防止物体退色,本发明所述的紫外吸收剂是指能够吸收uvb区290-320nm紫外线的物质,主要是为了防止皮肤黑色素的形成。
31.另外,在体外法评价羊肚菌菌丝体发酵液提取物的防晒效果实验中,结果表明羊肚菌菌丝体发酵液提取物的吸光度a为1.77,满足1<a<2.0
±
0.2,符合中级防晒的标准,说明其可用于制备防晒制剂。
32.本发明提供了一种羊肚菌菌丝体发酵液提取物的制备方法,其特征在于,包括以下步骤:
33.(1)将发酵完成的羊肚菌菌丝体发酵液和菌球共同匀浆后,50-80℃水浴加热15-30min,使菌丝体结构破坏,释放其体内的活性物质,获得羊肚菌菌丝体匀浆;所述水浴加热,优选80℃,30min;所述发酵完成的羊肚菌菌丝体发酵液,按照如下方法制备:
34.将羊肚菌菌丝体接种于液体发酵培养基,发酵至菌丝体由丝状长成小球状,且不再变大,液体发酵培养基由白色浑浊液体变为黄褐色澄清液体,即为发酵结束;所述液体发酵培养基包括0.25%-1%土豆淀粉、3-5%大豆蛋白、ph值为5-6,优选添加0.2%-0.4%磷酸二氢钾调节ph。
35.(2)将步骤(1)经过固液分离获得澄清的液相,冻干制成粉末状,即为所述羊肚菌菌丝体提取物,冻干制备成干粉制品,利于发酵活性物质的保存。
36.另一方面,本发明还提供了一种羊肚菌菌丝体发酵液提取物,所述发酵液提取物包括发酵液内和菌丝体内热稳定的防晒活性物质,其按照本发明所述的制备方法制备。
37.另一方面,本发明还提供了一种羊肚菌菌丝体发酵液提取物在制备紫外吸收剂中的应用;所述的羊肚菌菌丝体发酵液提取物按照本发明所述的制备方法制备,其应用于制备吸收290-320波段的紫外吸收剂。
38.另外,本发明还提供了一种紫外吸收剂,其包括本发明所述的羊肚菌菌丝体发酵液提取物;优选还包括抗坏血酸、抗坏血酸衍生物中一种或组合;更优选,1-5份羊肚菌菌丝体发酵液提取物和10-15份抗坏血酸。
39.本发明还提供了一种防晒制剂,其包括本发明所述的羊肚菌菌丝体发酵液提取物或者本发明所述的紫外吸收剂,优选羊肚菌菌丝体发酵液提取物或者紫外吸收剂添加量在100μg/ml以上,其中羊肚菌菌丝体发酵提取物更优选5mg/ml以上,实验结果显示,浓度为5mg/ml羊肚菌菌丝体发酵液提取物的spf值可达30。
40.以下为实施例:
41.以下实施例或附图中“发酵液”均表示本发明所述的羊肚菌菌丝体发酵液提取物。
42.实施例1制备羊肚菌菌丝体发酵液提取物及安全性评价
43.(1)羊肚菌菌丝体发酵液提取物的制备
44.本实施例中采用的液体发酵培养基为0.5%土豆淀粉、4%大豆蛋白、0.3%磷酸二氢钾,溶剂为蒸馏水,羊肚菌菌丝体接种量为10%,发酵培养温度为25℃,设置摇床转速120r/min,震荡发酵7d,此时菌丝体由丝状长成小球状,且不再变大,培养基由白色浑浊液体变为黄褐色澄清液体,即发酵培养结束。将发酵完成后获得的羊肚菌菌丝体发酵液与菌丝球一同匀浆后,80℃条件下水浴加热30min,经过离心、抽滤等步骤获得澄清的羊肚菌菌丝体发酵液,冻干制成粉末状后,作为后续实验原料。
45.(2)安全性评价
46.测定不同浓度的提取物样品对hepg 2细胞存活率,结果见图1。
47.实验结果显示羊肚菌菌丝体发酵液提取物浓度在20-200μg/ml,hepg2细胞存活率在90%以上,400μg/mlhepg 2细胞存活率约为85%,由图1可知,不同浓度羊肚菌菌丝体发酵液提取物对hepg 2细胞存活率影响小,说明其安全性评价高,hepg 2细胞与发酵液提取物直接接触,而皮肤最外层为角质层,它是由20层扁平、相互交织的角质细胞所组成,其表面还有一层由汗液及皮脂组成的保护膜(水脂膜),共同构成了皮肤的屏障,由此可见,羊肚菌菌丝体发酵液提取物对皮肤表皮细胞而言其安全性也高。
48.实施例2羊肚菌菌丝体发酵液提取物成分测定
49.(1)多酚含量测定
50.folin-ciocalteus法测定多酚含量,在10ml离心管中加入1ml的提取物样品,5ml的蒸馏水,3ml的7.5%碳酸钠溶和1ml的福林酚试剂,在室温避光处反应2h后,取200μl加入96孔板中,用酶标仪于765nm下测定吸光度,以没食子酸(0、5、10、15、25、30μg/ml)为对照品绘制标准曲线,羊肚菌菌丝体发酵液提取物多酚含量测定结果见图2。
51.(2)多糖含量测定
52.采用苯酚-硫酸法测定多糖含量,在10ml试管中加入2ml的提取物样品,1ml的5%苯酚溶液,摇匀后迅速加入5ml浓硫酸,摇匀后于室温反应30min,取200μl加入96孔板中,用酶标仪于490nm下测定吸光度,以105℃干燥的葡萄糖(0、0.005、0.01、0.02、0.03、0.04、0.05mg/ml)为对照品绘制标准曲线,羊肚菌菌丝体发酵液提取物多糖含量测定结果见图2。
53.由图2可知,羊肚菌菌丝体发酵液提取物中多酚含量在10%左右,多糖含量在15%左右,说明在发酵液的提取物经冻干后的粉末发酵液提取物中,大分子物质中的多糖和多酚占总物质含量的25%左右,其余的小分子物质因种类复杂,未测定具体成分。
54.实施例3羊肚菌菌丝体发酵液提取物与吸光度之间的关系
55.分别配置100μg/ml、200μg/ml、400μg/ml、600μg/ml、800μg/ml、1000μg/ml的茶多酚溶液和羊肚菌菌丝体发酵液提取物,测定290-320nm之间的吸光度,结果见图3所示,其中图3(左)为茶多酚,图3(右)为羊肚菌菌丝体发酵液提取物。
56.由图3可知,茶多酚浓度在600-1000μg/ml,其在290-310nm之间的吸光度差异不明显,吸光度呈现较平稳状态,说明在290-310nm茶多酚与吸光度没有体现出量效关系;而羊肚菌菌丝体发酵液提取物在290-320nm之间同一波长条件下,随着浓度的增加,吸光度呈现规律性的增加,说明羊肚菌菌丝体发酵液提取物浓度与吸光度有着良好的量效关系。
57.实施例4不同浓度羊肚菌菌丝体发酵液提取物的spf值
58.以100μg/ml的茶多酚标准品作为阳性对照,测定计算羊肚菌菌丝体发酵液提取物100-1000μg/ml浓度范围的spf值,结果见表2。
59.spf值计算:
60.根据mansur的研究表明,spf值可由下列公式进行计算:
[0061][0062]
其中:cf为校正因子,值为10;ee
λ
为波长λ下辐射出的红斑效应;i
λ
为太阳光谱强度;a
λ
为波长λ下的吸光系数。
[0063]
公式中ee
λ
×iλ
可以参考由sayre测得的spf计算规范系数,见表1,该表各波长所对应的系数之和为1。
[0064]
表1 spf计算规范系数
[0065]
波长/nm290295300305310315320ee
λ
×iλ
0.01500.08170.28740.32780.18640.08390.0180
[0066]
表2不同浓度羊肚菌菌丝体发酵液提取物的spf值
[0067][0068]
由表2可知,以100μg/ml的茶多酚标准品作为阳性对照,当羊肚菌菌丝体发酵液提取物浓度为600μg/ml时,其防晒效果与100μg/ml的茶多酚标准品相当,虽然同为天然来源的物质,但茶多酚标准品的工艺复杂、产量有限且价格贵,而羊肚菌菌丝体发酵液提取物的来源广泛,且工艺简单、成本低,可见,羊肚菌菌丝体发酵液提取物作为防晒化妆品的原料具有更高的性价比。
[0069]
实施例5评价羊肚菌菌丝体发酵液提取物抗紫外稳定性
[0070]
将提取物样品、抗坏血酸(vc)和茶多酚分别配制为1mg/ml的浓度,各自再分为两组,一组避光处理,作为对照组,另一组不避光处理,作为实验组。将对照组和实验组同时放在室外环境中进行日光照射,分别测定在室外日光照射0h、2h、4h、6h、8h、10h、12h、24h的紫外吸光度,计算不同时间点的spf值,根据spf值的变化判断不同样品在日光照射下的稳定性,结果见图4。
[0071]
由图4可知,在日光照射的条件下照射24h,茶多酚标准品的spf值有明显下降,而羊肚菌菌丝体发酵液提取物和vc在24h内的spf值略有上升,这可能是由于在一天的日光照射下,有一定的水蒸发,使样品和vc溶液的浓度有一定的变化。综合来说,羊肚菌菌丝体发
酵液提取物样品在24h内的抗紫外活性较为稳定。
[0072]
实施例6细胞紫外损伤的造模实验
[0073]
将hepg-2细胞以2
×
105/孔浓度铺于96孔板,于37℃的恒温培养箱中培养24h后,细胞贴壁生长。将细胞分为10个组,每组设6个复孔,重复三次,分别为阴性对照组(无uv照射)、15mj/cm2组、30mj/cm2组、60mj/cm2组、90mj/cm2组、120mj/cm2组、150mj/cm2组、200mj/cm2组、300mj/cm2组,照射垂直高度为10cm,对于不需照射的细胞用铝箔纸遮蔽进行避光处理。照射结束后,弃去培养液,加100μl/孔细胞基础培养基,置于恒温培养箱培养24h,用mtt法测定细胞存活率,结果如图5所示。
[0074]
由图5可知,以未经辐照的正常组细胞存活率作为100%,在15mj/cm
2-60mj/cm2辐照剂量内,对hepg-2细胞具有增殖作用,而随着辐照剂量的增大,会导致细胞凋亡,使细胞存活率明显下降,当辐照剂量为120mj/cm2时,细胞存活率在50%左右,说明细胞紫外损伤模型建立成功,故之后的实验选用紫外辐照剂量为120mj/cm2。
[0075]
实施例7羊肚菌菌丝体发酵液提取物对uvb致细胞损伤的保护作用
[0076]
实验组别:正常组、模型组(mem基础培养基)、阳性对照组(茶多酚标准品,浓度为100μg/ml),羊肚菌菌丝体发酵液提取物组(浓度为50μg/ml、80μg/ml、100μg/ml、120μg/ml、150μg/ml、200μg/ml);
[0077]
实验方法:
[0078]
将hepg-2细胞以2
×
105/孔浓度接种于96孔板,于37℃的恒温培养箱中培养22h后,弃去原培养基,按照实验组别进行加药,预保护2h后将其置于uvb灯管下,照射高度为10cm,照射时间为1500s,照射剂量为120mj/cm2,对于不需照射的细胞用铝箔纸遮蔽进行避光处理。照射结束后,弃去发酵液提取物,加100μl/孔细胞基础培养基,置于恒温培养箱培养24h,用mtt法测定细胞存活率,测定结果见图6。
[0079]
由图6可知,与模型组相比,浓度为50μg/ml以上的发酵液提取物对uvb致细胞光损伤的均具有明显保护作用,同浓度条件下(100μg/ml)其对细胞的保护效果明显优于茶多酚。
[0080]
实施例8体外法评判羊肚菌菌丝体发酵液提取物的防晒效果
[0081]
用国家标准qb/t 2410-1998方法测定羊肚菌菌丝体发酵液提取物的防晒效果,根据标准中的方法,需将羊肚菌菌丝体发酵液提取物冻干成粉末,之后按照以下步骤进行测定:
[0082]
(a)将规格为transpore tm1527型号的3m胶带剪成1cm
×
4cm大小,粘贴在石英比色皿透光侧表面上;
[0083]
(b)接通紫外风光光度计电源,设定uvb区的检测波长在290-320nm之间;
[0084]
(c)将贴有胶带的石英比色皿置于样品光路和参比光路中,调整仪器零点;
[0085]
(d)精确称取待测样品8mg,将样品均匀涂抹在石英比色皿3m胶带上;
[0086]
(e)将制备好的样品比色皿放置于35℃干燥箱中,干燥30min;
[0087]
(f)将待测样品比色皿置于样品光路中,另取一贴有3m胶带的石英比色皿置于参比光路中,在uvb区进行波长扫描,记录290nm、295nm、300nm、305nm、310nm、315nm、320nm处的吸光度,计算七个波长下吸光度的算术平均值;
[0088]
(g)重复三次取其平均值,根据平均值的结果判断其防晒效果,判断标准见表3,吸
光值测定结果见表4。
[0089]
表3防晒效果评价标准
[0090][0091]
表4羊肚菌菌丝体发酵液提取物和茶多酚标准品在uvb区吸光度的平均值
[0092][0093]
根据表3的防晒判断标准,表4显示羊肚菌菌丝体发酵液提取物的吸光度为1.77,满足1<a<2.0
±
0.2,符合中级防晒的标准,可用作天然防晒原料,用于制备防晒化妆品。
[0094]
本领域的技术人员容易理解,以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1