具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体及其制备方法与流程
1.本发明属于医药制剂领域,涉及一种具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体及其制备方法。
背景技术:
2.去甲斑蝥素为斑蝥虫体内斑蝥素的去甲基衍生物,是我国首先自行研制的抗肿瘤药物,主要用于原发性肝癌的治疗,可通过各种途径破坏、抑制癌细胞,也是国际上第一个具有升高白细胞作用的抗肿瘤药物,其独特的治疗机制使其具有广阔的应用前景。但去甲斑蝥素难溶于水,在体内消除迅速,生物利用度低,且肿瘤靶向性差,有严重的脏器毒性等缺点制约了其在临床上的广泛应用。去甲斑蝥素的递送载体,如微球、壳聚糖纳米粒、微乳、脂质体及胶束等已有研究报道。例如,文献《去甲斑蝥素固体脂质纳米粒的研究》(田海燕.去甲斑蝥素固体脂质纳米粒的研究[d].山东大学,2007.)采用薄膜-分散法制备了包封率为55.4
±
1.2%的去甲斑蝥素固体脂质纳米粒。
[0003]
纳米结构脂质载体作为一种改进的脂质纳米粒子,是在固体脂质纳米粒的基础上发展起来的第二代固体脂质纳米粒,是一种新型的纳米结构递送系统。纳米结构脂质载体为通过向固态脂质中加入与之化学性质差异很大的液态油,使纳米粒以结晶缺陷型或无定型结构存在,常采用混合类脂为载体材料,将液态脂质混合到固体脂质中制备而得。纳米结构脂质载体的制备方法主要有融熔-乳化法、高压乳匀法、溶剂扩散法、薄膜分散-超声法等。由于去甲斑蝥素水溶性较差,采用常规方法制备的纳米结构脂质载体包封率较低,现有纳米结构脂质载体的制备方法不适用于去甲斑蝥素。
[0004]
目前,尚无去甲斑蝥素的纳米结构脂质载体及其制备方法的现有技术以及研究报道,尚无具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体的任何研究报道。因此,研究一种新型去甲斑蝥素纳米结构脂质载体及其制备方法很有必要。
技术实现要素:
[0005]
本发明所要解决的技术问题是现有去甲斑蝥素的递送载体生物利用度低、肿瘤靶向性差的问题。
[0006]
本发明解决其技术问题所采用的技术方案是:具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体,其制备原料各组分按重量比计为:去甲斑蝥素0.1-6份,聚乙二醇-4005-15份,聚氧乙烯蓖麻油8-16份,油酸乙酯20-50份,三棕榈酸甘油酯0.4-2份,磷脂1-5份,单硬脂酸甘油酯2-5份,吐温-801-5份,水相72-308份。
[0007]
进一步的是,上述制备原料各组分按重量比计为:去甲斑蝥素0.1-1份,聚乙二醇-4006-12份,聚氧乙烯蓖麻油9-15份,油酸乙酯25-40份,三棕榈酸甘油酯0.5-1.5份,磷脂1-3份,单硬脂酸甘油酯2-4份,吐温-801.5-3.5份,水相72-206份。
[0008]
上述具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体呈圆形或椭圆形,平均粒径
<100nm。
[0009]
上述具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体的包封率为(87.41
±
0.16)%。
[0010]
上述具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体的制备方法,包括如下步骤:
[0011]
a.去甲斑蝥素纳米乳的制备:按原料各组分重量比将去甲斑蝥素、油酸乙酯、聚乙二醇-400及聚氧乙烯蓖麻油混合后于水浴中避光搅拌,然后滴加水相2-8份继续搅拌至充分乳化,得到去甲斑蝥素纳米乳;
[0012]
脂质薄膜的制备:按原料各组分重量比将单硬脂酸甘油酯、磷脂、三棕榈酸甘油酯置于反应容器中,并加入有机溶剂使其充分溶解后,于水浴中旋转蒸发除去有机溶剂,在反应容器内壁得到脂质薄膜;
[0013]
吐温-80溶液的制备:按原料组分重量比将吐温-80和水相70-300份混合后超声使其充分溶解,得到吐温-80溶液;
[0014]
b.向步骤a得到脂质薄膜的反应容器中加入去甲斑蝥素纳米乳和吐温-80溶液,然后于冰浴中超声使反应容器内壁的脂质薄膜脱落,得到具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体。
[0015]
进一步的是,当制备原料中水相为72-206份时,步骤a去甲斑蝥素纳米乳的制备中滴加水相2-6份,吐温-80溶液的制备中水相为70-200份。
[0016]
上述步骤a去甲斑蝥素纳米乳的制备中,所述水浴温度为35-45℃,避光搅拌时间为3-4h,继续搅拌时间为10-30min。
[0017]
上述步骤a脂质薄膜的制备中,所述有机溶剂的加入量为260-1100份。
[0018]
进一步的是,所述有机溶剂为无水乙醇、二氯甲烷、三氯甲烷、乙酸乙酯、丙酮中至少一种。
[0019]
上述步骤a脂质薄膜的制备中,所述反应容器为圆底烧瓶,水浴温度为35-45℃。
[0020]
上述步骤a吐温-80溶液的制备中,超声时间为10-30min。
[0021]
上述步骤b中,超声时间为10-15min。
[0022]
本发明的有益效果是:本发明提供一种具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体及其制备方法。本发明将纳米结构脂质载体作为去甲斑蝥素的载体,制备得到的载体平均粒径小于100nm。粒径小于100nm的纳米递送载体可渗出肿瘤血管,滞留在肿瘤组织,而不到正常组织。因此,本发明的去甲斑蝥素纳米结构脂质载体有效提高了去甲斑蝥素对肝癌组织(肝脏和肿瘤)的靶向性。
[0023]
本发明的具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体克服了去甲斑蝥素难溶于水,消除速度快,生物利用度低,严重脏器毒性等缺点;本发明具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体增加了去甲斑蝥素的溶解性,延长了去甲斑蝥素在血液循环中的滞留时间,提高其生物利用度,保持其较长时间的有效血药浓度,能减少给药次数,提高患者的顺应性,降低毒副作用;同时,有效增加其在肿瘤组织的靶向性,并通过纳米结构脂质载体的长循环能力和被动靶向特性使纳米制剂在肿瘤部位蓄积,增强对癌细胞的损伤,可以用于肝癌治疗。
[0024]
本发明制备的纳米结构脂质载体作为药物载体,结合了含药微乳和脂质体的特
点,使纳米粒以结晶缺陷型或无定型结构存在,增加了辅料对药物的包容性,避免了药物在放置过程中的泄漏和因此导致包封率下降的缺陷。本发明通过以微乳作为递药方式,可最大限度将药物包裹于液态脂质中,再通过薄膜分散-超声的方法,使部分含药液态脂质及游离药物混合于固体脂质中,增加了纳米粒结构中去甲斑蝥素不规则晶型的比例,使承载脂溶性药物的空间容量增加,从而提高载体的载药能力,可制备得到包封率为(87.41
±
0.16)%的去甲斑蝥素纳米结构脂质载体,防止了去甲斑蝥素在放置中泄漏,增强了制剂稳定性。
[0025]
本发明制备的具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体在肿瘤组织内具有特异性、快速、高效的累积能力,为去甲斑蝥素提供了可供选择的新型递送系统,具有重要意义;本发明提供的制备工艺简单,成本较低,易于控制,易于工业化生产;本发明的去甲斑蝥素纳米结构脂质载体及其制备方法具有广阔的应用前景。
附图说明
[0026]
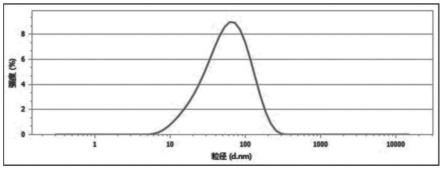
图1为本发明制备的具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体的粒径图;
[0027]
图2为本发明制备的具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体的电镜图;
[0028]
图3为本发明制备的具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体在荷瘤小鼠中的组织分布图;
[0029]
图4为本发明制备的具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体在大鼠体内的血药浓度时间曲线图;
[0030]
图5为本发明制备的具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体在荷瘤小鼠中的肿瘤形成抑制图。
具体实施方式
[0031]
本发明的技术方案,具体可以按照以下方式实施。
[0032]
具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体,其制备原料各组分按重量比计为:去甲斑蝥素0.1-6份,聚乙二醇-4005-15份,聚氧乙烯蓖麻油8-16份,油酸乙酯20-50份,三棕榈酸甘油酯0.4-2份,磷脂1-5份,单硬脂酸甘油酯2-5份,吐温-801-5份,水相72-308份。
[0033]
优选的,上述制备原料各组分按重量比计为:去甲斑蝥素0.1-1份,聚乙二醇-4006-12份,聚氧乙烯蓖麻油9-15份,油酸乙酯25-40份,三棕榈酸甘油酯0.5-1.5份,磷脂1-3份,单硬脂酸甘油酯2-4份,吐温-801.5-3.5份,水相72-206份。
[0034]
上述具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体呈圆形或椭圆形,平均粒径<100nm,具有肿瘤靶向性,其包封率为(87.41
±
0.16)%。
[0035]
上述具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体的制备方法,包括如下步骤:
[0036]
a.去甲斑蝥素纳米乳的制备:按原料各组分重量比将去甲斑蝥素、油酸乙酯、聚乙二醇-400及聚氧乙烯蓖麻油混合后于水浴中避光搅拌,然后滴加水相2-8份继续搅拌至充分乳化,得到去甲斑蝥素纳米乳;
[0037]
脂质薄膜的制备:按原料各组分重量比将单硬脂酸甘油酯、磷脂、三棕榈酸甘油酯
置于反应容器中,并加入有机溶剂使其充分溶解后,于水浴中旋转蒸发除去有机溶剂,在反应容器内壁得到脂质薄膜;
[0038]
吐温-80溶液的制备:按原料组分重量比将吐温-80和水相70-300份混合后超声使其充分溶解,得到吐温-80溶液;
[0039]
b.向步骤a得到脂质薄膜的反应容器中加入去甲斑蝥素纳米乳和吐温-80溶液,然后于冰浴中超声使反应容器内壁的脂质薄膜脱落,得到具有肿瘤靶向性的去甲斑蝥素纳米结构脂质载体。
[0040]
优选的是,当制备原料中水相为72-206份时,步骤a去甲斑蝥素纳米乳的制备中滴加水相2-6份,吐温-80溶液的制备中水相为70-200份。
[0041]
为保证反应成分,因此优选的是,上述步骤a去甲斑蝥素纳米乳的制备中,所述水浴温度为35-45℃,避光搅拌时间为3-4h,继续搅拌时间为10-30min。
[0042]
为了保证实验效果,因此优选的是,上述步骤a脂质薄膜的制备中,所述有机溶剂的加入量为260-1100份,所述反应容器为圆底烧瓶,水浴温度为35-45℃;更优选的是,所述有机溶剂为无水乙醇、二氯甲烷、三氯甲烷、乙酸乙酯、丙酮中至少一种。
[0043]
为了达到技术目的,因此优选的是,上述步骤a吐温-80溶液的制备中,超声时间为10-30min;步骤b中,超声时间为10-15min。
[0044]
本发明提供的去甲斑蝥素纳米结构脂质载体的平均粒径小于100nm,提高了去甲斑蝥素对肝癌组织(肝脏和肿瘤)的靶向性,其主要原因为:肿瘤epr效应,即肿瘤组织的毛细管有很大间隙,小于100nm的纳米递送载体易从血管中溢出,从而在肿瘤组织被动聚集,使其具有一定的肿瘤靶向性。纳米结构脂质载体的这种被动靶向在一定程度上减少了去甲斑蝥素对正常组织的毒副作用,提高了对肿瘤的特异性治疗效果。
[0045]
本发明提供的去甲斑蝥素纳米结构脂质载体抗肿瘤活性有明显,其主要原因为:(1)纳米结构脂质载体包封药物,增强了制剂稳定性,可延长药物生物半衰期,延长作用时间;(2)制剂可增加药物的体内吸收,提高其生物利用度;(3)肿瘤epr效应,制剂具有一定的肿瘤靶向性。
[0046]
下面通过实际的例子对本发明的技术方案和效果做进一步的说明。
[0047]
实施例
[0048]
一、去甲斑蝥素纳米结构脂质载体的制备
[0049]
本发明提供6组采用本发明制备方法制备去甲斑蝥素纳米结构脂质载体的实施例,实施例1-6的原料组分具体质量比如表1所示,具体工艺参数参数如表2所示,制备过程如下:
[0050]
a.去甲斑蝥素纳米乳的制备:将处方量的去甲斑蝥素、油酸乙酯、聚乙二醇-400及聚氧乙烯蓖麻油混合后于40℃水浴中避光搅拌3-4h,然后滴加水相1继续搅拌10-30min,得到去甲斑蝥素纳米乳;
[0051]
b.脂质薄膜的制备:将处方量的单硬脂酸甘油酯、磷脂、三棕榈酸甘油酯置于圆底烧瓶中,并加入260-1100份的有机溶剂使其充分溶解后,于40℃水浴中旋转蒸发除去有机溶剂,在圆底烧瓶内壁得到脂质薄膜;
[0052]
c.将处方量的吐温-80和水相2混合后超声10-30min,得到吐温-80溶液;
[0053]
d.向步骤b得到脂质薄膜的圆底烧瓶中加入步骤a得到的去甲斑蝥素纳米乳和步
骤c得到的吐温-80溶液,然后于冰浴中超声10-15min使圆底烧瓶内壁的脂质薄膜脱落,得到去甲斑蝥素纳米结构脂质载体。
[0054]
表1实施例1-6原料组分质量比/份
[0055][0056][0057]
表2实施例1-6制备工艺参数
[0058][0059]
二、去甲斑蝥素纳米结构脂质载体的理化性质研究
[0060]
对本发明制备得到的去甲斑蝥素纳米结构脂质载体进行理化性质研究,具体如下:
[0061]
1、粒径
[0062]
采用马尔文激光粒度仪测定去甲斑蝥素纳米结构脂质载体的粒径,如图1所示。
[0063]
由图1可知,本发明制备的去甲斑蝥素纳米结构脂质载体平均粒径为(90.97
±
2.58)nm,pdi为0.618
±
0.068。
[0064]
2、包封率
[0065]
采用葡聚糖凝胶g-50柱测定去甲斑蝥素纳米结构脂质载体的包封率进行了测定。
[0066]
经计算得到,本发明制备的去甲斑蝥素纳米结构脂质载体包封率为(87.41
±
0.16)%。
[0067]
3、形貌
[0068]
采用透射电镜测定去甲斑蝥素纳米结构脂质载体混合样的外观形态,如图2所示。
[0069]
由图2可知,透射电镜下观察到去甲斑蝥素纳米结构脂质载体呈均匀分布的圆形或椭圆形,分散均匀,无黏连。
[0070]
4、组织分布
[0071]
12只肝癌hepg2荷瘤小鼠(在给药前禁食12小时,但不禁水),随机分为2组,每组6只,分别尾静脉注射去甲斑蝥素、本发明制备的去甲斑蝥素纳米结构脂质载体混合样,给药剂量相同(以去甲斑蝥素计)。给药一定时间后脱颈处死,迅速摘取心、肝、脾、肺、肾、肿瘤,进行组织分布研究,结果如图3所示。
[0072]
由图3可知,去甲斑蝥素纳米结构脂质载体能明显改变去甲斑蝥素在荷瘤小鼠体内的分布,使去甲斑蝥素浓聚于肝和肿瘤,并明显减少去甲斑蝥素在脾、肺、肾的分布。研究结果说明去甲斑蝥素纳米结构脂质载体具有一定的肝组织和肿瘤组织靶向性。
[0073]
5、药代动力学
[0074]
12只sd大鼠(在给药前禁食12小时,但不禁水),随机分为2组,每组6只,分别灌胃给予去甲斑蝥素、本发明制备的去甲斑蝥素纳米结构脂质载体混合样,给药剂量相同(以去甲斑蝥素计)。给药后定时采血,进行药代动力学研究,结果如图4所示。
[0075]
由图4可知,游离去甲斑蝥素在大鼠体内快速消除,在约6小时浓度趋近于0,去甲斑蝥素纳米结构脂质载体消除速度明显比游离药更慢,在12小时浓度趋近于0,体内的平均滞留时间是游离药物的3.08倍;并且,去甲斑蝥素纳米结构脂质载体消除速度明显比游离药物更慢,消除率减慢至游离药物的60.04%;去甲斑蝥素纳米结构脂质载体的血药浓度-时间曲线图下面积相对于游离去甲斑蝥素有明显提高,是游离去甲斑蝥素的2.08倍。研究表明将去甲斑蝥素制备成去甲斑蝥素纳米结构脂质载体后可延长药物在血液循环保留时间,延缓药物体内消除速度,增加其体内的生物半衰期,能显著提高去甲斑蝥素的生物利用度,
[0076]
6、肿瘤形成抑制情况
[0077]
24只肝癌hepg2荷瘤小鼠(在给药前禁食12小时,但不禁水),随机分为4组,每组6只,分别尾静脉注射和灌胃给予去甲斑蝥素、本发明制备的去甲斑蝥素纳米结构脂质载体混合样,给药剂量相同(以去甲斑蝥素计)。给药一定时间后脱颈处死,迅速摘取肿瘤,对肿瘤形成抑制情况进行研究,结果如图5所示。
[0078]
由图5可知,与游离去甲斑蝥素相比,不同给药途径的去甲斑蝥素纳米结构脂质载体均能明显抑制荷瘤小鼠肿瘤形成,且尾静脉注射给药对肿瘤的抑制效果最佳。研究结果说明去甲斑蝥素纳米结构脂质载体提高了去甲斑蝥素的抗肿瘤活性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1