用于预防和阻断继发龋的抗生物膜-再矿化材料及其制备方法和应用
1.本发明属于防龋材料技术领域,具体涉及一种抗致龋菌生物膜形成、介导牙体组织及修复材料表面矿化以及降低充填修复术后微渗漏的预防和阻断继发龋的材料及其制备方法和应用。
背景技术:
2.充填修复是预防窝沟龋和治疗龋病的主要方法,但充填修复材料的使用寿命约5~7年,70%的修复体需再次干预治疗。由继发龋造成的修复年失败率约12.9%,继发龋的发生主要与生物降解、应力、细菌生物膜造成的牙体组织-修复材料间微渗漏密切相关,预防和阻断继发龋的研究多集中于将抗菌剂和/或矿化剂添加至修复材料或粘接剂,较难实现临床转化,而传统的氟化物在预防继发龋方面未取得良好的临床效果,尤其在龋高风险人群中,且存在一定的安全隐患。目前仍缺乏一种安全、高效、稳定的预防和阻断继发龋的材料。
3.防龋及再矿化材料国际会议明确提出再矿化材料需联合抗菌剂达到防龋目的。将牛血清白蛋白制备成具有淀粉样蛋白特性的涂层,该涂层可稳定粘附于基材表面且易于二次改性,有望成为防龋材料的载体。奥替尼啶是一种广谱抗菌剂,局部使用时可提高浓度且不产生耐药性、操作简单、化学性质稳定、对人体及环境毒性极低,对革兰氏阳性菌、革兰氏阴性菌、真菌等均具有稳定的抗菌活性。
技术实现要素:
4.鉴于此,本发明旨在提供一种用于预防和阻断继发龋的抗生物膜-再矿化材料及其制备方法,以克服目前继发龋预防的技术难点,该材料可同时在牙体组织及充填修复材料表面快速形成薄膜,该薄膜粘附稳定,表面润湿性良好,具有耐酸性和抗致龋菌生物膜性能,可介导生物矿化,在牙体组织及充填修复材料表面形成无差别新生羟基磷灰石保护层,其与天然釉质机械性能相近,显著降低充填修复术后微渗漏的发生,实现预防和阻断继发龋发生的目的。
5.为达到上述目的,本发明用于预防和阻断继发龋的抗生物膜-再矿化材料是将牛血清白蛋白、奥替尼啶和三(2-羰基乙基)膦盐酸盐(记为tcep
·
hcl)溶于羟乙基哌嗪乙硫磺酸缓冲液(记为hepes缓冲液),得到的相转变牛血清白蛋白-奥替尼啶溶液(记为ptb-oct溶液)。
6.上述抗生物膜-再矿化材料,优选每100ml hepes缓冲液中溶解0.01~1g牛血清白蛋白、0.001~0.8g奥替尼啶、0.1~3g tcep
·
hcl。
7.进一步的,上述抗生物膜-再矿化材料,更优选每100ml hepes缓冲液中溶解0.2~0.8g牛血清白蛋白、0.003~0.4g奥替尼啶、0.4~1.5g tcep
·
hcl。
8.上述羟乙基哌嗪乙硫磺酸缓冲液的浓度为5~30mm,ph为7.0~7.4。
9.上述ptb-oct溶液的zeta电位为15~20mv。
10.本发明用于预防和阻断继发龋的抗生物膜-再矿化材料的制备方法包括如下步骤:
11.1)将牛血清白蛋白充分溶解于羟乙基哌嗪乙硫磺酸缓冲液中,得到a溶液;
12.2)将奥替尼啶充分溶解于羟乙基哌嗪乙硫磺酸缓冲液中,得到b溶液;
13.3)将a溶液与b溶液混合,静置5~50分钟,得到c溶液;
14.4)将三(2-羰基乙基)膦盐酸盐溶解于羟乙基哌嗪乙硫磺酸缓冲液中,得到d溶液;
15.5)将c溶液与d溶液混合,静置3~90分钟,得到相转变牛血清白蛋白-奥替尼啶溶液,即用于预防和阻断继发龋的抗生物膜-再矿化材料。
16.上述步骤3)中,优选将a溶液与b溶液混合,静置20~40分钟。
17.上述步骤5)中,优选将c溶液与d溶液混合,静置40~80分钟。
18.本发明还提供如上所述的用于预防和阻断继发龋的抗生物膜-再矿化材料在脱矿牙体硬组织仿生再矿化和预防继发龋的药物及护理产品中的应用。
19.本发明用于预防和阻断继发龋的抗生物膜-再矿化材料,其原理在于模拟人体内釉原蛋白介导釉质矿化的结构特征及自组装行为,不仅在牙体硬组织表面实现原位仿生再矿化,同时在充填修复材料表面及粘接界面形成无差别羟基磷灰石保护性涂层,填补目前临床常用防龋产品无法对修复充填材料及粘接界面发挥作用的空白;同时这一抗生物膜-再矿化材料负载抗菌剂,对致龋菌具有良好的抗菌性,在源头做到预防和阻断龋病的发生及进展。
20.相对于现有技术,本发明用于预防和阻断继发龋的抗生物膜-再矿化材料具有以下有益效果:
21.本发明所述材料制备过程简便快捷、条件温和、绿色环保,ptb-oct溶液在牙齿表面形成涂层(简称ptb-oct涂层),粘附稳定,表面润湿性良好,可显著减少致龋菌及其代谢产物在牙体硬组织及充填修复材料表面粘附,具有良好的抗生物膜性能;同时,ptb-oct涂层耐酸性能良好,可抵抗细菌代谢产酸对牙体组织及牙-修复体粘接界面的破坏,减少微渗漏的发生;此外,ptb-oct涂层可在牙体组织及充填修复材料表面介导无差别羟基磷灰石保护性涂层形成,再矿化脱矿牙体硬组织,同时对牙-修复体粘接界面及充填修复体表面起到保护作用,预防和阻断继发龋的发生。本材料生物安全性良好,成本低廉,操作简单,具有理想的应用效果和潜在的临床转化价值。
附图说明
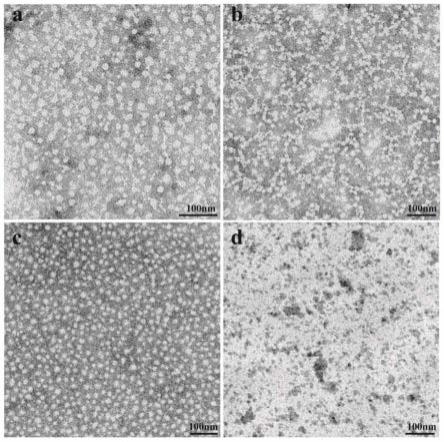
22.图1是实验1中ptb溶液和ptb-oct溶液制备过程中的透射电镜图。
23.图2是实验2中牛血清白蛋白溶液、oct溶液、ptb溶液和ptb-oct溶液的zeta电位值。
24.图3是实验3中形成的ptb-oct涂层的耐酸性表征结果。
25.图4是实验4中ptb-oct溶液、oct溶液和ptb溶液分别诱导牙釉质表面再矿化形成的涂层的扫描电镜图。
26.图5是实验5中ptb-oct溶液、oct溶液和ptb溶液抗变形链球菌生物膜的激光共聚焦显微镜图。
27.图6是实验6中树脂充填冷热循环后微渗漏染色的体式显微镜图。
具体实施方式
28.下面结合附图和实施例对本发明进一步详细说明,但本发明的保护范围不仅限于这些实施例。
29.实施例1
30.1)在常温下,将66mg牛血清白蛋白充分溶解于10ml hepes缓冲液中,得到a溶液;
31.2)将1mg奥替尼啶充分溶解于10ml hepes缓冲液中,得到b溶液;
32.3)将a溶液与b溶液混合,静置30分钟,得到c溶液;
33.4)将143mg tcep
·
hcl溶解于10ml hepes缓冲液中,得到d溶液;
34.5)将c溶液与d溶液混合,静置1小时,得到ptb-oct溶液,即用于预防和阻断继发龋的抗生物膜-再矿化材料。
35.对比例1
36.在实施例1中,将b溶液用等体积的超纯水替换,其他步骤与实施例1相同,得到相转变牛血清白蛋白溶液。
37.对比例2
38.在实施例1中,将a溶液用等体积的超纯水替换,其他步骤与实施例1相同,得到奥替尼啶溶液。
39.实施例2
40.1)在常温下,将66mg牛血清白蛋白充分溶解于10ml hepes缓冲液中,得到a溶液;
41.2)将10mg奥替尼啶充分溶解于10ml hepes缓冲液中,得到b溶液;
42.3)将a溶液与b溶液混合,静置30分钟,得到c溶液;
43.4)将71mg tcep
·
hcl溶解于10ml hepes缓冲液中,得到d溶液;
44.5)将c溶液与d溶液混合,静置1小时,得到ptb-oct溶液,即用于预防和阻断继发龋的抗生物膜-再矿化材料。
45.实施例3
46.1)在常温下,将100mg牛血清白蛋白充分溶解于10ml hepes缓冲液中,得到a溶液;
47.2)将60mg奥替尼啶充分溶解于10ml hepes缓冲液中,得到b溶液;
48.3)将a溶液与b溶液混合,静置30分钟,得到c溶液;
49.4)将143mg tcep
·
hcl溶解于10ml hepes缓冲液中,得到d溶液;
50.5)将c溶液与d溶液混合,静置1小时,得到ptb-oct溶液,即用于预防和阻断继发龋的抗生物膜-再矿化材料。
51.实施例4
52.1)在常温下,将20mg牛血清白蛋白充分溶解于10ml hepes缓冲液中,得到a溶液;
53.2)将10mg奥替尼啶充分溶解于10ml hepes缓冲液中,得到b溶液;
54.3)将a溶液与b溶液混合,静置30分钟,得到c溶液;
55.4)将286mg tcep
·
hcl溶解于10ml hepes缓冲液中,得到d溶液;
56.5)将c溶液与d溶液混合,静置1小时,得到ptb-oct溶液,即用于预防和阻断继发龋的抗生物膜-再矿化材料。
57.实施例5
58.1)在常温下,将200mg牛血清白蛋白充分溶解于10ml hepes缓冲液中,得到a溶液;
59.2)将100mg奥替尼啶充分溶解于10ml hepes缓冲液中,得到b溶液;
60.3)将a溶液与b溶液混合,静置30分钟,得到c溶液;
61.4)将71mg tcep
·
hcl溶解于10ml hepes缓冲液中,得到d溶液;
62.5)将c溶液与d溶液混合,静置1小时,得到ptb-oct溶液,即用于预防和阻断继发龋的抗生物膜-再矿化材料。
63.实施例6
64.1)在常温下,将100mg牛血清白蛋白充分溶解于10ml hepes缓冲液中,得到a溶液;
65.2)将60mg奥替尼啶充分溶解于10ml hepes缓冲液中,得到b溶液;
66.3)将a溶液与b溶液混合,静置30分钟,得到c溶液;
67.4)将430mg tcep
·
hcl溶解于10ml hepes缓冲液中,得到d溶液;
68.5)将c溶液与d溶液混合,静置1小时,得到ptb-oct溶液,即用于预防和阻断继发龋的抗生物膜-再矿化材料。
69.为了证明本发明的有益效果,发明人进行了大量的实验室研究实验,具体实验如下:
70.实验1:在对比例1中,将c溶液与d溶液混合,分别在静置5分钟和30分钟时取样,所取样品滴于铜网,磷钨酸负染后进行透射电镜检测,结果显示静置5分钟时形成直径约10~100nm的纳米颗粒,形状、大小不一,散在分布(图1a);静置30分钟后寡聚体部分聚集,相连成链状(图1b)。在实施例1中,将c溶液与d溶液混合,分别在静置3分钟和20分钟时取样,所取样品滴于铜网,磷钨酸负染后进行透射电镜检测,结果显示,静置3分钟时形成直径约20~100nm的纳米颗粒,大小不一,散在分布(图1c);静置20分钟后寡聚体部分聚集,相连成链状、片状(图1d)。说明加入oct后,纳米颗粒的大小稍有增大,并且加入oct后加速了寡聚体的聚集进而加速成膜。
71.实验2:取牛血清白蛋白溶液(a溶液)、对比例2所得奥替尼啶溶液(oct溶液)、对比例1得到的相转变牛血清白蛋白溶液(ptb溶液)和实施例1得到的ptb-oct溶液各1ml,使用粒径电位仪检测各溶液的zeta电位,结果如图2所示。由图可见,实施例1的ptb-oct溶液带正电,zeta电位为17.9
±
2.1mv。
72.实验3:将硅片置于实施例1得到的ptb-oct溶液中,静置1小时,分别使用ph=2的盐酸溶液、ph=11的氢氧化钠水溶液、ph=4的乳酸水溶液及临床用35%磷酸凝胶处理30秒,去离子水彻底冲洗干净,干燥。将所有硅片浸泡在0.1mg/ml硫黄素t(tht)溶液中染色1分钟,去离子水冲洗,激光共聚焦显微镜观察硅片表面形成的ptb-oct涂层脱落情况,结果如图3所示。由图可见,盐酸及氢氧化钠破坏大部分ptb-oct涂层,而乳酸及磷酸仅造成少量ptb-oct涂层剥脱。
73.实验4:收集因治疗需要拔除的完整无龋坏无明显磨耗阻生齿20个,用3%次氯酸钠和生理盐水冲洗,去除软组织及污物。使用低速磨牙机在流动水冷却下切割恒牙近中、远中、颊侧及舌侧釉质片,制备约4mm
×
4mm
×
2mm(长
×
宽
×
厚)的牙釉质样品。所有样品使用35%磷酸酸蚀剂处理30秒,去离子水彻底冲洗后,置于实施例1得到的ptb-oct溶液中,静置1小时。用牙科专用涂药棒先后蘸取50mm的cacl2水溶液和30mm的kh2po4水溶液涂抹10秒,彻
底干燥,重复三次。梯度脱水并干燥后进行sem检测,表征结果如图4所示。由图可见,正常恒牙釉质形貌,表面为一层致密的无釉柱釉质(图4a),经35%磷酸酸蚀剂处理后,表面呈现鱼鳞状,无釉柱釉质消失,可见釉柱及釉柱间质(图4b),经表面形成的ptb-oct涂层诱导矿化后,釉质表面鱼鳞状结构完全被晶体覆盖,新生晶体呈片状,大小相近,彼此聚集融合,形成较厚的矿物层(图4c,d)。说明本发明的ptb-oct溶液能够在牙釉质表面形成ptb-oct涂层,经简单快速涂抹钙磷溶液后可诱导新生羟基磷灰石层形成,促进脱矿釉质原位再矿化,修复牙齿病损。而经对比例1中ptb溶液处理酸蚀后釉质(图4e)和对比例2中oct溶液处理酸蚀后釉质(图4f)均呈现鱼鳞状,无法修复脱矿釉质。
74.实验5:将牙釉质片置于实施例1得到的ptb-oct溶液、对比例1所得ptb溶液和对比例2所得oct溶液中,静置1小时。将变形链球菌菌液5000rpm下离心5分钟,重悬,使用分光光度计调节菌液od
600
至0.8(约1
×
108cfu/ml)。取1ml重悬后的菌液加入牙釉质片的孔板中,厌氧条件下,于37℃培养24小时和48小时。培养结束后,无菌去离子水冲洗。吖啶橙溶液和溴化己啶溶液按体积比1:1混合成工作液,将牙釉质片转移至新孔板,每孔内加入1ml无菌pbs和20μl所述工作液,室温避光放置5分钟,用无菌pbs轻轻冲洗牙釉质片表面,去除多余的染色剂,使用激光共聚焦显微镜观察牙釉质片表面细菌粘附情况及活死细菌分布情况,表征结果如图5所示。由图可见,在24小时及48小时细菌培养后,牙釉质片表面形成变形链球菌生物膜(如图5a,b),ptb溶液处理后的釉质表面细菌粘附明显减少,但多为活菌(如图5c,d),oct溶液处理后的釉质表面多为死菌(如图5e,f),ptb-oct涂层展现良好的抗污和抗菌性能,细菌粘附明显减少,且多为死菌(如图5g,h)。
75.实验6:在离体牙颊、舌侧预备v类洞,要求长3mm、高2mm、深2mm,冲洗吹干窝洞,涂布3m粘接剂,光照20秒固化,使用3m z350膏体树脂充填窝洞,光照20秒固化。其中,在充填后离体牙随机选择一侧于牙面及树脂表面采用实施例1的ptb-oct溶液构建ptb-oct涂层,涂布氯化钙溶液和磷酸氢二钾溶液各10秒,重复3次。离体牙置于去离子水中37℃恒温24小时。随后将其放入55℃和4℃水浴中各30秒,1分钟为一个循环,重复500次。在牙体表面距离树脂边缘1mm以外均匀涂抹2层防水指甲油,待其完全干燥后,用蜡封闭牙根部分。将离体牙完全置于1%亚甲基蓝溶液中24小时,流动水充分冲洗掉多余染液。使用低速磨牙机沿釉牙骨质界下方1mm去掉牙根,沿牙体长轴将样本切成约1mm厚的牙片,使用体式显微镜观察染液渗入情况,表征结果如图6所示。由图可见,牙-树脂界面存在不同程度的亚甲基蓝染液渗入(图6a),构建ptb-oct涂层后能够显著减少微渗漏的发生(图6b)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1