利培酮血药浓度预测方法及装置与流程
1.本发明涉及大数据处理技术领域,尤其涉及一种利培酮血药浓度预测方法及装置。
背景技术:
2.精神分裂症是一种病因复杂较严重的精神疾病,病因包含遗传因素和非遗传因素,大部分精神分裂症是多种基因遗传导致的。在精神分裂症的药物治疗中,由于患者个体化基因差别和药物机制的不同,疗效和不良反应存在较大的个体差异。
3.利培酮作为临床常用的非典型抗精神病药物,在精神分裂症的治疗中发挥着重要作用。然而利培酮治疗窗窄,个体差异大,虽不易引起锥体外系反应,但在糖脂代谢异常、体重增加、肝功能异常、嗜睡等方面的药品不良反应影响患者的依从性,降低患者的生活质量,甚至危及生命。利培酮是多种代谢酶、转运体的底物,利培酮及其活性代谢物脱烷基喹硫平在个体间的药动学过程差异较大,临床使用过程中易发生基于代谢酶、转运体的药物间相互作用,造成利培酮血药浓度无法落在正常治疗窗内,难以达到理想治疗效果或药物不良反应发生率增加。因此,基于人工智能和真实世界数据构建精神分裂症患者的利培酮血药浓度个体化预测模型,对于制定药物给药方案,预测药物临床疗效及规避药物不良反应,促进利培酮的临床合理应用具有重要的理论和临床应用价值。
4.在临床预测精神分裂症患者利培酮血药浓度的研究中,通常使用poppk(群体药代动力学)模型,而目前建立或使用poppk模型的过程中需要专业的软件和技术人员,而且在适应性、功能性、易用性等方面存在一些局限性。
技术实现要素:
5.本发明提供一种利培酮血药浓度预测方法及装置,用以解决现有技术中使用poppk模型预测利培酮血药浓度要求高,在适应性、功能性和易用性方面存在局限性的缺陷,实现基于深度学习对利培酮血药浓度进行快速准确预测。
6.本发明提供一种利培酮血药浓度预测方法,包括:
7.采集待预测精神分裂症患者的临床数据;
8.将所述临床数据输入利培酮血药浓度预测模型中,获取所述利培酮血药浓度预测模型输出的所述待预测精神分裂症患者的利培酮血药浓度预测值;
9.其中,所述利培酮血药浓度预测模型是以样本精神分裂症患者的临床数据为样本,以所述样本精神分裂症患者的利培酮血药浓度实际值为标签获得。
10.根据本发明提供的一种利培酮血药浓度预测方法,所述临床数据包括人口统计学信息、用药信息、检验信息、诊断信息、手术信息、治理方案和不良反应。
11.根据本发明提供的一种利培酮血药浓度预测方法,所述将所述临床数据输入利培酮血药浓度预测模型中,获取所述利培酮血药浓度预测模型输出的所述待预测精神分裂症患者的利培酮血药浓度预测值的步骤之前,还包括:
12.获取所述样本精神分裂症患者的临床数据中每个特征变量的缺失率,删除缺失率大于第一预设阈值的特征变量;
13.基于统计方法对删除后的特征变量进行初次筛选;
14.基于特征工程对初次筛选的特征变量进行再次筛选;
15.将所述样本精神分裂症患者的利培酮血药浓度实际值作为目标变量,将再次筛选出的特征变量作为自变量,基于node模型构建所述利培酮血药浓度预测模型。
16.根据本发明提供的一种利培酮血药浓度预测方法,所述基于统计方法对删除后的特征变量进行初次筛选的步骤包括:
17.在所述删除后的特征变量为连续型变量的情况下,基于pearson检验方法判断所述目标变量与所述连续型变量之间的关系是否显著;
18.在所述关系显著的情况下,保留所述连续型变量,否则将所述连续型变量删除;
19.获取删除后的每个特征变量的离散性,将所述离散性大于第二预设阈值的特征变量取对数;
20.在所述删除后的特征变量为分类变量的情况下,基于mann-whitney u检验方法判断所述目标变量与所述分类变量之间的关系是否显著;
21.在所述关系显著的情况下,保留所述分类变量,否则将所述分类变量删除。
22.根据本发明提供的一种利培酮血药浓度预测方法,所述基于特征工程对初次筛选的特征变量进行再次筛选的步骤包括:
23.将所述样本精神分裂症患者的利培酮血药浓度实际值作为目标变量,将初次筛选出的特征变量作为协变量,基于lightgbm算法构建特征重要性预测模型;
24.基于六折交叉验证对所述特征重要性预测模型调节参数,使得所述特征重要性预测模型达到最优;
25.基于最优的所述特征重要性预测模型,获取每个初次筛选出的特征变量的重要性,筛选所述重要性最大的预设个数的特征变量;
26.基于catbost的特征序列前向选择算法从筛选的特征变量中再次筛选出最优特征变量;
27.基于随机森林模型对所述最优特征变量中的缺失值进行插补。
28.根据本发明提供的一种利培酮血药浓度预测方法,所述基于node模型构建所述利培酮血药浓度预测模型的步骤之后,还包括:
29.获取所述利培酮血药浓度预测模型的评估指标r2、rmse和mae;
30.根据所述评估指标r2、rmse和mae,对所述利培酮血药浓度预测模型调节参数,使得所述利培酮血药浓度预测模型达到最优。
31.本发明还提供一种利培酮血药浓度预测装置,包括:
32.采集模块,用于采集待预测精神分裂症患者的临床数据;
33.预测模块,用于将所述临床数据输入利培酮血药浓度预测模型中,获取所述利培酮血药浓度预测模型输出的所述待预测精神分裂症患者的利培酮血药浓度预测值;
34.其中,所述利培酮血药浓度预测模型是以样本精神分裂症患者的临床数据为样本,以所述样本精神分裂症患者的利培酮血药浓度实际值为标签获得。
35.本发明还提供一种电子设备,包括存储器、处理器及存储在存储器上并可在处理
器上运行的计算机程序,所述处理器执行所述程序时实现如上述任一种所述利培酮血药浓度预测方法。
36.本发明还提供一种非暂态计算机可读存储介质,其上存储有计算机程序,该计算机程序被处理器执行时实现如上述任一种所述利培酮血药浓度预测方法。
37.本发明还提供一种计算机程序产品,包括计算机程序,所述计算机程序被处理器执行时实现如上述任一种所述利培酮血药浓度预测方法。
38.本发明提供的利培酮血药浓度预测方法及装置,通过使用精神分裂症患者的真实世界临床数据建立利培酮血药浓度预测的专属模型,使用训练好的模型输入患者的临床数据即可自动预测出患者的利培酮血药浓度预测值,预测效率高,准确性高,覆盖人群广,从而预知利培酮血药浓度是否正常,参考利培酮血药浓度进行用药调整,降低患者发生不良反应的风险。
附图说明
39.为了更清楚地说明本发明或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
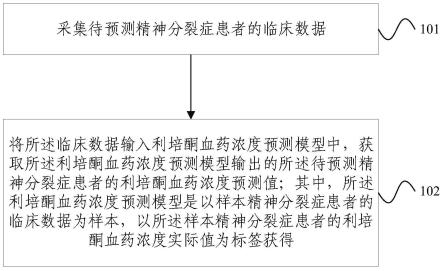
40.图1是本发明提供的利培酮血药浓度预测方法的流程示意图之一;
41.图2是本发明提供的利培酮血药浓度预测方法的流程示意图之二;
42.图3是本发明提供的利培酮血药浓度预测方法的流程示意图之三;
43.图4是本发明提供的利培酮血药浓度预测方法中odt的树形图示意图;
44.图5是本发明提供的利培酮血药浓度预测装置的结构示意图;
45.图6是本发明提供的电子设备的结构示意图。
具体实施方式
46.为使本发明的目的、技术方案和优点更加清楚,下面将结合本发明中的附图,对本发明中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
47.下面结合图1描述本发明的利培酮血药浓度预测方法,包括:
48.步骤101,采集待预测精神分裂症患者的临床数据;
49.其中,待预测精神分裂症患者为需要进行利培酮血药浓度预测的精神分裂症患者患者。
50.按照ccmd-3的诊断标准,只要满足下面症状中的至少两项,就达到精神分裂症的症状标准。
51.1、反复出现言语性幻听;
52.2、明显的思维松弛、思维破裂、言语不连贯或者思维贫乏、思维内容贫乏;
53.3、思维被插入,感觉有一种思维突然在自己的思维里出现;
54.4、思维被洞悉、被控制;
55.5、原发性妄想,包括被害妄想或者是一些被盗或者被洞悉这样的情况;
56.6、思维逻辑倒错、病理性象征性思维或者语词新作,把一些很普通的言语赋予特别的含义、情感倒错、紧张、愚蠢行为、明显的意志减退和缺乏。
57.精神分裂症的排除标准包括:
58.1、器质性精神障碍;
59.2、精神活性物质;
60.3、非成瘾物质所致精神障。
61.采集待预测精神分裂症患者在真实世界的临床数据,例如人口统计学信息、用药信息、诊断信息、血常规和尿常规等患者临床数据。
62.步骤102,将所述临床数据输入利培酮血药浓度预测模型中,获取所述利培酮血药浓度预测模型输出的所述待预测精神分裂症患者的利培酮血药浓度预测值;
63.其中,所述利培酮血药浓度预测模型是以样本精神分裂症患者的临床数据为样本,以所述样本精神分裂症患者的利培酮血药浓度实际值为标签获得。
64.样本精神分裂症患者的临床数据用于构建利培酮血药浓度预测模型,本实施例不限于利培酮血药浓度预测模型的类型。
65.采集样本精神分裂症患者的临床数据,例如利培酮血药浓度实际值、人口统计学信息、用药信息、诊断信息、血常规和尿常规等患者临床数据。根据患者不同治疗时期的需要,以患者的利培酮血药浓度监测为基准,对患者的临床数据进行拼接,建立精神分裂症患者的真实世界数据库。
66.可选地,对精神分裂症患者的真实世界数据库中的原始数据进行数据清洗后,构建利培酮血药浓度预测模型。
67.如图2所示,将待预测精神分裂症患者的临床数据输入利培酮血药浓度预测模型中,该模型即可输出利培酮血药浓度预测值,从而提高利培酮用药效果的预见性和可控性,降低药物不良反应。
68.本实施例通过使用精神分裂症患者的真实世界临床数据建立利培酮血药浓度预测的专属模型,使用训练好的模型输入患者的临床数据即可自动预测出患者的利培酮血药浓度预测值,预测效率高,准确性高,覆盖人群广,从而预知利培酮血药浓度是否正常,参考利培酮血药浓度进行用药调整,降低患者发生不良反应的风险。
69.在上述实施例的基础上,本实施例中所述临床数据包括人口统计学信息、用药信息、检验信息、诊断信息、手术信息、治理方案和不良反应。
70.其中,人口统计学信息包括患者姓名、身份证号和年龄。用药信息包括用药名称和用药量。检验信息包括检验项和检验结果。诊断信息包括诊断结果。
71.在上述各实施例的基础上,如图3所示,本实施例中所述将所述临床数据输入利培酮血药浓度预测模型中,获取所述利培酮血药浓度预测模型输出的所述待预测精神分裂症患者的利培酮血药浓度预测值的步骤之前,还包括:
72.获取所述样本精神分裂症患者的临床数据中每个特征变量的缺失率,删除缺失率大于第一预设阈值的特征变量;
73.由于样本精神分裂症患者的临床数据的特点是数据维度高且缺失严重。因此本实施例不仅处理数据缺失问题,还从高维数据中快速有效筛选出特征变量,从而使用最少的
特征变量达到最优的模型预测效果。
74.例如,设置第一预设阈值为50%,则将缺失率大于50%的特征变量删除。
75.基于统计方法对删除后的特征变量进行初次筛选;基于特征工程对初次筛选的特征变量进行再次筛选;
76.结合统计学方法和特征工程,对特征变量进行多次筛选,获取患者的重要特征和检验检测结果。将最终筛选出的特征变量作为最终的建模变量,构建新的建模数据集。
77.将所述样本精神分裂症患者的利培酮血药浓度实际值作为目标变量,将再次筛选出的特征变量作为自变量,基于node(neural oblivious decision ensembles,神经不经意决策集成)模型构建所述利培酮血药浓度预测模型。
78.其中,node模型是针对表格数据而设计的,而且在dnn(deep neural networks,深度神经网络)架构中融入了决策树的原理。因此,node算法不仅具备dnn的表征学习和end2end的优点,又继承了决策树的不受数据缩放的影响,且很容易可视化,解释性强。
79.node模型的基础模型是odt(oblivious decision tree,不经意决策树)。odt是一个决策树,但是odt在划分特征的内部节点有一定的限制,在具有相同深度的内部节点,其选择的特征和阈值也要相同。假设树的深度为d,则odt的特征划分最多也为d种。因此,odt其实就是一张具有2d个条目的表,并对应d种特征划分的所有特征组合。
80.例子,如果odt有两层,d=2。两层的特征划分分别为fc>c,fd>d,因此odt的树形图为fc》c,fd》d,如图4所示。odt是弱化版的常规决策树,相对于普通的决策树,其推断过程比较快。给定一个odt,就可以并行对d个划分阈值进行比较,然后直接通过查表方式得到预测值。
81.假设一个样本向量为x∈rn,其中n是特征总数,假设第i层用的特征是fi(x),阈值为bi,层数为d。otd的公式如下:
82.h(x)=r[1(f1(x)-b1),...,1(fd(x)-bd)]
[0083]
其中,r是一个具有d个维度的response张量,1(.)代表heaviside函数
[0084]
为了把odt用在dnn中,需要对odt进行可微处理,因此需要修改fi(x)和比较函数1(f1(x)-b1)。利用softmax、α-entmax等函数,将fi(x)转换为n个特征权重加和的形式,通过entmax将特征选择函数改为其中f∈rd×n为可训练的参数矩阵,对n个特征进行权重加和,entmax为权重。
[0085]
比较函数1(f1(x)-b1)的输出只是0和1,需要改成二分类的方式即输出[0,1]和[1,0]。因此,可以写成σ
α
=entmax
α
([x,0]),其输出一个加和为1的二维向量,由于特征的量级可能不同,将比较函数再次改写为其中,阈值bi和缩放参数τi都是可训练的参数。从而构建一个与response张量形状相同的choice张量,其中为向量外积。因此,可
微的odt的最终输出为其中r是可训练的response张量。
[0086]
node的每一层都是由多个独立的otd构成。假设一层有m棵树,则该层的输出就是把每棵树的输出串联起来,形成的形式,其维度为r
ml
,层与层之间选择类使用densenet的连接方式,即把该层前面所有层的输出都串联起来作为该层的输入。其实,在node中层与层之间的连接方式可以看作ensemble,将之前的层的输出认为新的特征,再输入到后面的层中,这样模型不但能学习到浅层的决策规则,还能学习到深层的决策规则,有效提高了模型的性能。
[0087]
本实施例通过将真实世界的临床数据建立的表格数据转换为回归任务学习,结合统计分析、机器学习和深度学习算法,构建个性化利培酮血药浓度智能监测模型,从而可以快速准确实现对精神分裂症患者利培酮血药浓度进行预测;有效筛选特征变量并处理缺失数据使得模型可以对特征数据利用最大化,即用少量的特征得到最优的预测效果。
[0088]
在上述实施例的基础上,本实施例中所述基于统计方法对删除后的特征变量进行初次筛选的步骤包括:
[0089]
在所述删除后的特征变量为连续型变量的情况下,基于pearson检验方法判断所述目标变量与所述连续型变量之间的关系是否显著;
[0090]
在所述关系显著的情况下,保留所述连续型变量,否则将所述连续型变量删除;
[0091]
例如,血压为连续型变量。通过与目标变量进行pearson检验,判断目标变量与连续型变量之间的关系是否显著。如果显著则保留,否则删除。
[0092]
获取删除后的每个特征变量的离散性,将所述离散性大于第二预设阈值的特征变量取对数;
[0093]
例如,用每个特征变量的最大值减去最小值作为每个特征变量的离散性,本实施例不限于离散型的计算方法。
[0094]
在所述删除后的特征变量为分类变量的情况下,基于mann-whitney u检验方法判断所述目标变量与所述分类变量之间的关系是否显著;
[0095]
在所述关系显著的情况下,保留所述分类变量,否则将所述分类变量删除。
[0096]
例如,诊断结果的分类包括轻度、中度和重度精神分裂症。通过与目标变量进行mann-whitney u检验,判断目标变量与分类变量的关系是否显著,如果显著则保留,否则删除。
[0097]
在上述实施例的基础上,本实施例中所述基于特征工程对初次筛选的特征变量进行再次筛选的步骤包括:
[0098]
将所述样本精神分裂症患者的利培酮血药浓度实际值作为目标变量,将初次筛选出的特征变量作为协变量,基于lightgbm算法构建特征重要性预测模型;
[0099]
基于六折交叉验证对所述特征重要性预测模型调节参数,使得所述特征重要性预测模型达到最优;
[0100]
由于患者数据维度高,经变量初筛后,得到的维度依然很高,且存在很多无用的变量和缺失值。为了降低数据的维度,保留数据的原始性,lightgbm算法具有的树功能可以有
效建模并处理数据中存在的缺失值。因此,选择lightgbm算法对精神分裂症患者数据进行建模分析,具体包括如下步骤:
[0101]
1、以利培酮血药浓度为目标变量,以初筛得到的特征变量作为协变量,基于lightgbm算法构建特征重要性预测模型。
[0102]
2、对模型进行6折交叉验证并进行调参,使得r2(r方指标)、rmse(root mean squared error,均方根误差)和mae(mean squared error,均方误差)达到最优。
[0103]
3、计算各个特征变量的重要性得分并降序排序,重要性得分越高说明该特征对模型影响越大。
[0104]
基于最优的所述特征重要性预测模型,获取每个初次筛选出的特征变量的重要性,筛选所述重要性最大的预设个数的特征变量;
[0105]
从根据重要性得分排序的特征变量中选择重要性得分排名前预设个数,如30的特征变量,实现对特征变量的第二次筛选。
[0106]
基于catbost的特征序列前向选择算法从筛选的特征变量中再次筛选出最优特征变量;
[0107]
使用catbost的特征序列前向选择算法进行第三次特征变量筛选。该算法从空集开始搜索特征,每次把一个特征变量添加到特征子集中,并进行建模,使得评价指标,如r2达到最优,最终筛选出最佳的特征组合。如果候选的特征子集对应的评价指标不如上一轮的特征子集,那么停止迭代,将上一轮的特征子集作为最优的特征选择结果。
[0108]
基于随机森林模型对所述最优特征变量中的缺失值进行插补。
[0109]
为了保证数据的完整性,尽可能多地利用现有的精神分裂症患者数据,需要对建模特征变量进行缺失值插补。
[0110]
由于随机森林模型准确度高,不容易陷入过拟合,具有一定的抗噪能力,并且对离散数据和连续数据的适应能力强。所以,选择随机森林算法对缺失值进行插补。
[0111]
在上述实施例的基础上,本实施例中所述基于node模型构建所述利培酮血药浓度预测模型的步骤之后,还包括:
[0112]
获取所述利培酮血药浓度预测模型的评估指标r2、rmse和mae;
[0113]
其中,r2的公式如下:
[0114][0115]
rmse的公式如下:
[0116][0117]
mse的公式如下:
[0118][0119]
其中,n表示样本的数量,yi表示第i个样本的真实值,表示第i个样本的预测值。r2越大越好,rmse和mae越小越好。
[0120]
根据所述评估指标r2、rmse和mae,对所述利培酮血药浓度预测模型调节参数,使得所述利培酮血药浓度预测模型达到最优。
[0121]
为了避免由于无效的自变量而高估了拟合度,将r2的公式修正为:
[0122][0123]
其中,β为预设调节系数,k为自变量的个数,n为所述样本精神分裂症患者的个数。在其他值不变的情况下,上述公式中k越大,则修正后的r2越小,k类似于一个惩罚项。
[0124]
根据rmse、mae和修正后的r2对利培酮血药浓度预测模型进行参数优化,使得修正后的r2减去rmse和mae后的差值最小,从而得到优化的利培酮血药浓度预测模型,提高预测精度和效率,而且可以通过在线学习的方式进行模型更新。
[0125]
node算法具有如下优势:
[0126]
1、能够处理大规模医学数据,低内存使用,具备更快的训练速度;
[0127]
2、特征选择方式直接,浅层的输出会直接作为后面层的输入特征;
[0128]
3、node的每一层都会产生新的特征,特征数则会随着层数的加深而不断变多,可以更好的提高模型的准确率和鲁棒性;
[0129]
4、兼具自主学习和增量学习的能力,具有更高的模型准确率;
[0130]
5、基学习器是odt,其更简单,更符合决策树,继承了决策树的优点;
[0131]
6、响应速度快,多线程并行来优化服务性能。
[0132]
本实施例组织临床多中心验证,对模型进行全面评价,根据临床实际反馈情况进行改进和优化,调整模型精度。
[0133]
下面对本发明提供的利培酮血药浓度预测装置进行描述,下文描述的利培酮血药浓度预测装置与上文描述的利培酮血药浓度预测方法可相互对应参照。
[0134]
如图5所示,该装置包括采集模块501和预测模块502,其中:
[0135]
采集模块501用于采集待预测精神分裂症患者的临床数据;
[0136]
预测模块502用于将所述临床数据输入利培酮血药浓度预测模型中,获取所述利培酮血药浓度预测模型输出的所述待预测精神分裂症患者的利培酮血药浓度预测值;
[0137]
其中,所述利培酮血药浓度预测模型是以样本精神分裂症患者的临床数据为样本,以所述样本精神分裂症患者的利培酮血药浓度实际值为标签获得。
[0138]
本发明通过使用精神分裂症患者的真实世界临床数据建立利培酮血药浓度预测的专属模型,使用训练好的模型输入患者的临床数据即可自动预测出患者的利培酮血药浓度预测值,预测效率高,准确性高,覆盖人群广,从而预知利培酮血药浓度是否正常,参考利培酮血药浓度进行用药调整,降低患者发生不良反应的风险。
[0139]
图6示例了一种电子设备的实体结构示意图,如图6所示,该电子设备可以包括:处理器(processor)610、通信接口(communications interface)620、存储器(memory)630和通信总线640,其中,处理器610,通信接口620,存储器630通过通信总线640完成相互间的通信。处理器610可以调用存储器630中的逻辑指令,以执行利培酮血药浓度预测方法,该方法包括:采集待预测精神分裂症患者的临床数据;将所述临床数据输入利培酮血药浓度预测模型中,获取所述利培酮血药浓度预测模型输出的所述待预测精神分裂症患者的利培酮血药浓度预测值;其中,所述利培酮血药浓度预测模型是以样本精神分裂症患者的临床数据为样本,以所述样本精神分裂症患者的利培酮血药浓度实际值为标签获得。
[0140]
此外,上述的存储器630中的逻辑指令可以通过软件功能单元的形式实现并作为
独立的产品销售或使用时,可以存储在一个计算机可读取存储介质中。基于这样的理解,本发明的技术方案本质上或者说对现有技术做出贡献的部分或者该技术方案的部分可以以软件产品的形式体现出来,该计算机软件产品存储在一个存储介质中,包括若干指令用以使得一台计算机设备(可以是个人计算机,服务器,或者网络设备等)执行本发明各个实施例所述方法的全部或部分步骤。而前述的存储介质包括:u盘、移动硬盘、只读存储器(rom,read-only memory)、随机存取存储器(ram,random access memory)、磁碟或者光盘等各种可以存储程序代码的介质。
[0141]
另一方面,本发明还提供一种计算机程序产品,所述计算机程序产品包括计算机程序,计算机程序可存储在非暂态计算机可读存储介质上,所述计算机程序被处理器执行时,计算机能够执行上述各方法所提供的利培酮血药浓度预测方法,该方法包括:采集待预测精神分裂症患者的临床数据;将所述临床数据输入利培酮血药浓度预测模型中,获取所述利培酮血药浓度预测模型输出的所述待预测精神分裂症患者的利培酮血药浓度预测值;其中,所述利培酮血药浓度预测模型是以样本精神分裂症患者的临床数据为样本,以所述样本精神分裂症患者的利培酮血药浓度实际值为标签获得。
[0142]
又一方面,本发明还提供一种非暂态计算机可读存储介质,其上存储有计算机程序,该计算机程序被处理器执行时实现以执行上述各方法提供的利培酮血药浓度预测方法,该方法包括:采集待预测精神分裂症患者的临床数据;将所述临床数据输入利培酮血药浓度预测模型中,获取所述利培酮血药浓度预测模型输出的所述待预测精神分裂症患者的利培酮血药浓度预测值;其中,所述利培酮血药浓度预测模型是以样本精神分裂症患者的临床数据为样本,以所述样本精神分裂症患者的利培酮血药浓度实际值为标签获得。
[0143]
以上所描述的装置实施例仅仅是示意性的,其中所述作为分离部件说明的单元可以是或者也可以不是物理上分开的,作为单元显示的部件可以是或者也可以不是物理单元,即可以位于一个地方,或者也可以分布到多个网络单元上。可以根据实际的需要选择其中的部分或者全部模块来实现本实施例方案的目的。本领域普通技术人员在不付出创造性的劳动的情况下,即可以理解并实施。
[0144]
通过以上的实施方式的描述,本领域的技术人员可以清楚地了解到各实施方式可借助软件加必需的通用硬件平台的方式来实现,当然也可以通过硬件。基于这样的理解,上述技术方案本质上或者说对现有技术做出贡献的部分可以以软件产品的形式体现出来,该计算机软件产品可以存储在计算机可读存储介质中,如rom/ram、磁碟、光盘等,包括若干指令用以使得一台计算机设备(可以是个人计算机,服务器,或者网络设备等)执行各个实施例或者实施例的某些部分所述的方法。
[0145]
最后应说明的是:以上实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的精神和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1