提高生物组织抗钙化性能的处理方法及生物组织材料与流程
1.本公开涉及一种处理生物组织的方法和通过该处理方法获得的生物组织材料,具体涉及一种处理生物组织的方法,以通过处理抑制该组织的钙化、降低心包上附着生物膜的风险和减少强度下降。
背景技术:
2.生物组织被广泛用于制造外科植入的心脏瓣膜和血管的置换假体以及经导管心脏瓣膜的置换假体。牛心包、猪心包等生物心包组织的化学组分主要包含胶原蛋白、弹性蛋白以及糖胺多糖结缔组织,其表面化学基团主要包含氨基、羧基及少量的羟基,其中羧基含量为氨基含量的2.5倍左右。从屠宰场获得的生物组织,特别是猪和牛心包组织,若不进行即时改性处理,会有脱水、降解、纤维断裂等变质风险。因此,为了能够利用生物组织作为临床材料,必须停止这种变质以延长材料的原始结构和机械完整性,并消除或至少中和归因于这些材料的抗原特性。
3.大多数临床上可用的生物假体心脏瓣膜包含了由戊二醛固定的牛心包组织。戊二醛固定可有效地交联该组织中的胶原,并大大消除生物假体的免疫原性和血栓形成性。然而,戊二醛交联法主要是对其组织中的胶原蛋白进行交联以消耗其表面残留氨基基团(-nh2),不能对弹性蛋白起到保护作用,容易引起心脏瓣膜的力学性能下降;且组织表面的羧基(-cooh)以及残留的醛基充当潜在的钙位结合点,随着时间的推移最终损害材料的生物机械性能而使组织不稳定。
4.在本领域中仍需要开发新的和改进的方法,用于限制诸如牛心包、猪心包等生物组织的钙化,从而增强组织的耐用性和稳定性。
技术实现要素:
5.本公开的目的是为了解决上述现有技术的不足而提供一种提高生物材料抗钙化性能的处理方法,能有效提升生物心脏瓣膜等生物材料的弹性性能以及抗钙化性能,潜在地延长其使用寿命。
6.本公开提供一种提高生物组织抗钙化性能的处理方法,先后包括如下步骤:
7.s1、保护氨基:利用封端剂对生物组织的氨基进行保护;
8.s2、交联羧基:利用交联剂对生物组织中的羧基进行化学交联。
9.进一步的,所述封端剂选自叔丁氧羰基(boc)、芴甲基氧羰基(fmoc)、苄氧羰基(cbz)、烯丙氧羰基(alloc)或三甲基硅乙氧羰基(teoc);所述交联剂选自二元胺类小分子、低聚物、异氰酸酯类单体、金属离子类、碳化二亚胺类或环氧硅烷类。
10.进一步的,在步骤s1之前包括步骤:
11.s11、氨基暴露:调节用于浸泡新鲜生物组织的溶液的ph值为8~10,以提高组织中的游离氨基的暴露程度。
12.进一步的,所述步骤s11选择碳酸氢钠调节ph值;所述步骤s1选择叔丁氧羰基
(boc)作为封端剂,封端剂的浓度为0.2~4.0g/l,封端保护氨基反应6~48小时,优选的,封端剂的浓度为3.0~4.0g/l。
13.进一步的,在步骤s2之前包括步骤:
14.s21、羧基暴露:通过ph值为6~6.5的弱酸性缓冲液浸泡经过步骤s1保护氨基处理后的生物组织,以提高羧基的暴露程度。
15.进一步的,在步骤s21之后和步骤s2之前包括步骤:
16.s22、羧基活化:向缓冲液中加入催化剂对经过步骤s21处理后的生物组织中暴露的羧基进行活化处理。
17.进一步的,所述步骤s22包括:
18.将经过步骤s21处理后的生物组织浸泡在mes缓冲液中,加入edc溶液搅拌并震动15分钟,再加入nhs反应,其中nhs与edc的摩尔比为1:1.5~1:4。
19.进一步的,所述步骤s2包括:
20.选择胱胺二盐酸盐作为交联剂,将交联剂溶于mes缓冲液中,使交联剂缓冲液的浓度为1~20g/l;
21.将含有交联剂的mes缓冲液滴加入步骤s22完成后的反应液中,反应6~72小时。
22.进一步的,所述生物组织是牛心包或猪心包。
23.本公开还提供一种生物组织材料,该生物组织材料采用上述方法制得,该生物组织材料不含有醛基。
24.本公开的处理方法制备得到的生物组织材料,由于其制备过程的全程中未引入醛类交联剂,避免了由于醛基残留引起的钙化风险,极大地提高了生物组织材料的抗钙化性能;由于制备过程中,对弹性蛋白中的羧基进行交联处理,避免弹性蛋白降解,从而保留弹性蛋白结构,即对弹性蛋白起到保护作用,制得的生物组织材料具有较好的弹性性能。因此,潜在地延长其使用寿命。
附图说明
25.图1为本公开的反应过程原理示意图;
26.图2为两种改性处理方法获得的组织的应力应变性能测试曲线图;
27.图3a-图3d为本公开的方法与戊二醛交联法对比反应交联程度的组织表面形貌图片;
28.图4a和图4b为本公开的方法获得的改性后的组织应用于动物体内一段时间后的钙化斑点形貌图片。
具体实施方式
29.下面将结合本公开实施例中的附图,对本公开实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本公开一部分实施例,而不是全部的实施例。基于本公开中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本公开保护的范围。
30.本公开提供的一种提高生物组织抗钙化性能的方法主要包括两大步骤,其中生物组织以心包组织为例,首先在溶剂体系中通过封端保护剂对心包组织中的氨基进行封端保
护处理,然后进一步通过在缓冲液体系中使用外加的交联剂和催化剂对心包组织中的羧基进行交联处理,最后得到具有仿生结构的交联反应产物。这种处理组织的方式反应条件温和,由于其制备过程的全程中未引入醛类交联剂,避免了醛基残留在组织表面引起的钙化风险;另外,相比于生物组织自身所带的反应基团(例如氨基基团),外加的交联基团的反应活性大大提高,因此,能够最大程度地消耗生物组织上面的羧基基团,最大程度地降低钙化风险;因此,能够有效提高生物组织的抗钙化性能,从而提高生物组织的使用寿命。再有,这种处理组织的方式整体只需一次交联反应,整体改性时间缩短。
31.生物组织:可以为哺乳动物组织,包括动物心包(例如牛心包、猪心包)、瓣膜或跟腱等组织的任意一种。
32.氨基封端/保护:可以采用叔丁氧羰基(boc)、芴甲基氧羰基(fmoc)、苄氧羰基(cbz)、烯丙氧羰基(alloc)或三甲基硅乙氧羰基(teoc)中的任意一种作为封端保护剂对生物组织的游离氨基进行保护。
33.羧基交联:可以采用二元胺类小分子或者低聚物、异氰酸酯类单体、金属离子类、碳化二亚胺类、环氧硅烷类等中的任意一种作为交联剂对生物组织的游离羧基进行交联。
34.溶剂体系:包含乙醇、乙腈、二氧六环、二甲基甲酰胺、二甲基亚砜、乙酸乙酯、水、生理盐水以及缓冲液中的一种或多种。
35.缓冲液:包含2-(n-吗啉)乙磺酸(mes)、磷酸盐缓冲液(pbs)、醋酸/醋酸钠缓冲液等任意一种。
36.催化剂:可采用碳二亚胺类缩合剂、鎓盐类缩合剂或有机磷类缩合剂,例如:1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc)、1-羟基苯并三唑(hobt)、n-羟基琥珀酰亚胺(nhs)、2-(7-氮杂苯并三氮唑)-n,n,n',n'-四甲基脲六氟磷酸酯(hatu)、o-苯并三氮唑-四甲基脲六氟磷酸盐(hbtu)、苯并三氮唑-1-基氧基三(二甲基氨基)磷鎓六氟磷酸盐(bop)或者六氟磷酸苯并三唑-1-基-氧基三吡咯烷基磷(pybop)中的任意一种。
37.实施例一:先对氨基进行保护,再利用二元胺类小分子(例如胱胺二盐酸盐)对羧基进行交联
38.保护氨基
39.对心包生物组织中的氨基保护过程包括如下步骤:
40.1.1)向乙腈、二氧六环和磷酸盐缓冲液的混合溶剂中添加碳酸氢钠或氢氧化钠等碱性物质,调节反应体系至弱碱性ph8~10,有利于氨基基团的暴露,以提高氨基基团的活性,进而实现下一步反应;将新鲜牛心包生物组织铺展固定在固定架上,并置于前述具有碳酸氢钠的溶液中,在0℃环境中使其完全浸泡30分钟。
41.1.2)配制封端保护剂溶液:配制二碳酸二叔丁酯/二氧六环溶液,二碳酸二叔丁酯与前一步骤中的碳酸氢钠投料质量比例为1:0.2~1:4,例如:1:0.2,1:0.4,1:0.6,1:0.8,1:1,1:1.2,1:1.4,1:1.6,1:1.8,1:2,1:3或1:4以及1:0.2~1:4之间的其它具体点值;二碳酸二叔丁酯浓度为0.2~4.0g/l,例如:0.2g/l,0.4g/l,0.6g/l,0.8g/l,1.0g/l,1.2g/l,1.4g/l,1.6g/l,1.8g/l,2.0g/l,3.0g/l或4.0g/l以及0.2~4.0g/l之间的其它具体点值。
42.1.4)将步骤1.2)的溶液与步骤1.1)的溶液混合,在室温环境下反应6-48小时。可选的,在反应过程中可进行氮气保护。
43.1.5)步骤1.4)中每升混合溶液浸泡360cm2,例如每升混合溶液浸泡2片10*18cm的
心包组织。
44.1.6)反应完毕后取出心包组织,并用生理盐水冲洗数次。
45.交联羧基
46.保护氨基步骤完成后,交联羧基通过包括如下步骤的方法进行:
47.2.1)羧基暴露:将经氨基保护的心包组织浸泡在mes缓冲液中,调节缓冲液至弱酸性,ph值为6~6.5提高生物新组织中羧基的暴露程度。
48.2.2)向缓冲液中加入催化剂对生物组织中的羧基进行活化处理:加入过量的1-(3-二甲基氨基丙基)-3-乙基碳化二亚胺盐酸盐(edc),搅拌/振动15分钟;加入n-羟基琥珀酰亚胺(nhs),edc与nhs投料摩尔比例为1.5:1~4:1,例如:1.5:1,2:1,2.5:1,3:1,3.5:1或4:1以及上述1.5:1~4:1之间的其他具体点值,对羧基进行活化处理。
49.2.3)向缓冲液中加入交联剂:将一定量的胱胺二盐酸盐(浓度为1g/l~20g/l,例如:1g/l,2g/l,3g/l,4g/l,5g/l,10g/l,15g/l或20g/l以及1g/l~20g/l之间的其它具体点值)溶于mes缓冲液中。
50.2.4)将步骤2.3的溶液与步骤2.2完成后的反应液混合,反应时间为6~72小时。该步骤中的反应可在室温下进行,并且反应过程中可进行氮气保护。
51.2.5)反应完毕后使用生理盐水冲洗数次。
52.可选的,在步骤2.4与步骤2.5之间,可向反应液中通10~60分钟的氧气,促进交联反应。
53.对比例二:对照样品处理方法
54.将新鲜牛心包铺展并固定在固定架上,置于浓度为0.625%戊二醛溶液中进行交联24小时。取出使用生理盐水清洗三次进行试验检测。
55.改性结果检测及对比
56.a1.热皱缩温度(ts)测试验证
57.热皱缩温度反映心包材料交联程度的一个指标,热皱缩温度越高,间接的说明交联度越高,热稳定性越好,新鲜牛心包的热皱缩温度在68℃左右,目前国内外报道的临床使用的生物瓣膜的热收缩温度在83-87℃左右。
58.通过改性牛心包得到的热皱缩温度在84℃左右,与主流产品ts接近。
59.表1热皱缩温度对比
60.改性方法ts/℃实施例一84.2
±
0.7对比例二83.8
±
0.8
61.a2.拉伸性能测试验证
62.参考图2所示的应力应变曲线图,计算实施例一和对比例二对应的弹性模量如表2所示,其中,图2中的曲线的线性段的斜率表示对应的弹性模量。可以看出经过实施例一改性后的牛心包的弹性模量相比对比例二改性后的牛心包的弹性模量要小,断裂伸长率增加,因此,实施例一改性牛心包具有较好的弹性性能。
63.表2弹性模量对比
64.样品实施例一对比例二弹性模量3.17mpa6.55mpa
65.a3.通过氨基的保护效率间接对比交联反应活性
66.根据茚三酮显色法对氨基含量进行定量表征,并通过紫外可见吸收光谱对氨基接枝率进行了计算(通过使用甘氨酸建立标准曲线,样品与茚三酮进行反应后读取570nm的吸光度)。
67.c0:新鲜心包单位质量的游离氨基浓度
68.c1:保护后单位质量的游离氨基浓度
69.表3不同二碳酸二叔丁酯浓度氨基保护率汇总
70.二碳酸二叔丁酯浓度0.2g/l0.6g/l1.8g/l3g/l4g/l氨基保护率11.2%25.3%50.6%91.6%91.7%
71.由表3可知,二碳酸二叔丁酯的浓度为3.0~4.0g/l时,氨基保护率可达91.5%以上。
72.表4保护氨基前与保护氨基后心包组织中的氨基数量对比
[0073] 吸光度570质量/g转换率游离氨基残留量新鲜心包0.2490.0115//实施例一保护后心包0.0030.005191.58%8.42%实施例一改性后样品0.0060.006692.68%7.32%对比例二对照样品0.0090.014593.05%6.95%
[0074]
保护后心包组织的氨基转换率可达到91.58%,完成最终改性后心包样品的氨基转换率为92.68%,氨基保护反应阶段结束后的氨基残留量与最终的样品的氨基残留量相当,表明在氨基保护反应阶段中氨基的反应足够充分,并且本公开的改性方法对保护后心包的游离氨基没有进一步反应。在下一阶段的羧基交联反应中,羧基主要是与加入的交联剂中的氨基基团发生交联反应,相比心包组织自身的反应基团,加入的交联剂中的氨基基团反应活性大大提高。
[0075]
a4.交联后的组织形态对比
[0076]
图3a与图3b分别为本公开改性心包以及戊二醛交联心包的天狼猩红染色图片,可以看出改性方法和戊二醛交联法得到的心包组织胶原纤维排列都比较紧致,两者没有形态上的显著差异。图3c与图3d分别为本公开改性心包以及戊二醛交联心包的维多利亚蓝染色图片,可以看出经过两种改性方法处理,心包内弹性蛋白纤维在心包内分布及排列在形态上没有显著差异。
[0077]
a5.抗钙化研究:皮下植入动物研究对比
[0078]
动物品系:3周龄刚断乳体重50g左右的wistar雄性大鼠
[0079]
数量:12只
[0080]
瓣叶:实施例一及对比例二制备得到的1cm
×
1cm瓣叶各12片
[0081]
背部皮下植入,每只大鼠分别植入实施例一及对比例二制备得到的瓣叶各1片,间隔至少1cm,植入后缝合组织,关闭皮肤。
[0082]
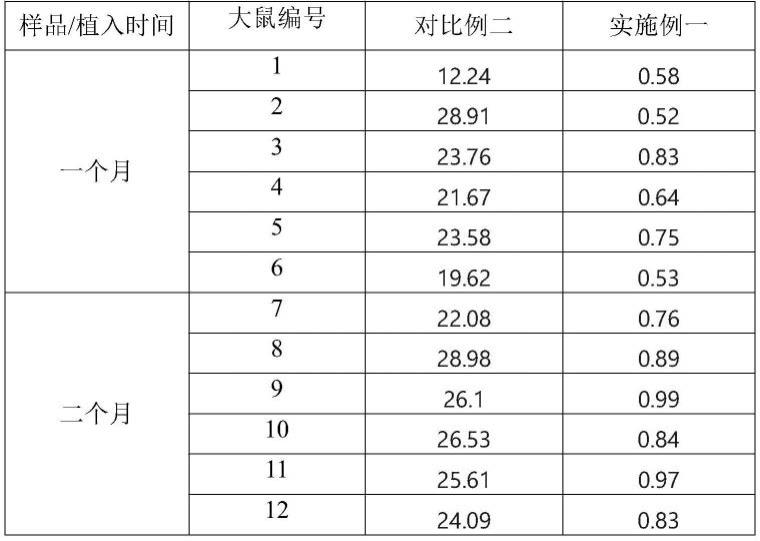
在植入一个月(四周)后以及植入二个月(八周)后各取6只大鼠,取出组织,分离表面结缔组织,使用纯净水轻微振荡洗去表面血污,进行后续使用电感耦合等离子光谱发生仪(icp)进行钙含量测试及染色样品制备。从表5可以看出本公开改性处理的心包组织相比
戊二醛改性交联的心包组织经过两个月皮下植入试验后,钙含量显著下降。
[0083]
从图4a植入一个月(四周)后与图4b植入二个月(八周)后的组织茜素红染色结果,可以看出切片没有明显的钙化点。
[0084]
表5钙含量:μg/mg
[0085][0086]
通过本公开的改性方法制备得到的生物组织材料,由于其制备过程的全程中未引入醛类交联剂,避免了由于醛基残留引起的钙化风险;由于制备过程中,对弹性蛋白中的羧基进行交联处理,避免弹性蛋白降解,从而保留弹性蛋白结构,即对弹性蛋白起到保护作用,因此,制得的生物组织材料具有较好的弹性性能。通过本公开的一些实施方式的改性方法制备得到的生物组织材料中含有二硫键桥接仿生结构,蛋白质空间结构稳定。通过本公开的改性方法制备得到的生物组织材料,应用于外科植入的人工心脏瓣膜或经导管植入的人工心脏瓣膜,可以延长人工心脏瓣膜植入人体后的有效工作年限。
[0087]
以上所述仅为本公开的几个实施例,本领域的技术人员依据申请文件公开的内容可以对本公开实施例进行各种改动或变型而不脱离本公开的精神和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1