一种薄膜的制备方法及其应用与流程
1.本发明属于医用材料领域,具体设计一种薄膜的制备方法和应用。
背景技术:
2.放射治疗是利用放射线,如α射线、β射线、x射线、γ射线、质子线、重离子线等治疗肿瘤的一种局部治疗方法。放射治疗按照射方法分为两类,即远距离治疗和近距离治疗。其中,远距离治疗又称外照射,通过身体皮肤照射肿瘤。近距离治疗又称体内照射,可将放射源直接植入在肿瘤内或靶区边缘,从而可以使辐射剂量精准覆盖病灶区域,同时最大限度的避免周边重要组织器官受到辐射。近距离放疗将放射性核素外面包裹上一层金属,制成针状、管状或粒子状,置于组织、器官或腔道内进行近距离放疗,如腔内照射通过体腔照肿瘤,如通过阴道照射子宫颈癌;管内照射通过食管、气管、胆管照射该处癌症;组织间照射将放射源陷植到肿瘤组织进行照射,如舌癌以及术中插植照射。现有技术中,近距离放疗中的操作并不精确,如放射粒子的位置、剂量和放射源种类是根据医生的经验粗略地估计、选择并固定的,而不是由具体病灶的范围、方位、大小、肿瘤细胞活性、类型等决定的。因此,放疗过程中患者面临的放疗剂量出错风险也在加大,剂量验证作为放疗质量保证的重要组成部分变得越来越重要。
3.目前剂量验证方法是将静态体模按照与患者定位时相同条件进行ct扫描,再将患者的治疗计划导入到模体ct图像序列进行计算,得到理论剂量分布,然后以模体代替患者将放疗计划在加速器上执行,将实测的剂量分布(gafchromic ebt3+胶片)与计划系统计算的剂量分布进行比较。然而,在上述剂量验证方法中ebt胶片测得的是光密度值(od),存在线性范围窄的缺点,导致对比结果不准确。而且,当前放疗验证普遍的模式是建立在目标位置和形状是己知而且是保持静止的基础上,这样的刚性关系在某些情况下是不成立的,例如胸腔会受到呼吸和心跳等运动的影响,在放射治疗过程中目标区域随着运动器官一起运动造成了治疗计划中的剂量分布和目标实际接受的剂量分布存在较大差异。
4.为了解决由于所采用的验证材料和验证模式造成的治疗计划中的剂量分布和目标实际接受的剂量分布存在的较大差异的问题,保证治疗计划中的剂量分布和目标实际接受的剂量分布对比的准确性,本技术提供了一种薄膜的制备方法及其应用。
技术实现要素:
5.本发明的一个目的是提供一种薄膜的制备方法,通过该方法制备的薄膜可以解决现有技术中由于所采用的验证材料和验证模式造成的治疗计划中的剂量分布和目标实际接受的剂量分布存在的较大差异的问题。
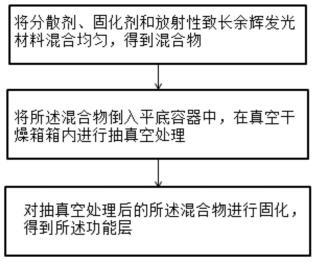
6.该薄膜的制备方法包括功能层的制备步骤:
7.将质量比为200-2000:6-240:1的分散剂、固化剂和放射性致长余辉发光材料混合均匀,得到混合物;
8.将所述混合物倒入平底容器中,在真空干燥箱箱内进行抽真空处理;
9.对抽真空处理后的所述混合物进行固化,得到所述功能层。
10.可选地,所述分散剂、所述固化剂和放射性致长余辉发光材料的质量比为1000:10:1。
11.可选地,所述分散剂为疏水性高分子聚合物材料,所述固化剂为道康宁184。
12.可选地,抽真空的条件为10-4000pa,固化条件为干燥箱参数设定温度为20-100℃,固化时间为10-300分钟。
13.可选地,该薄膜的制备方法还包括粘结层的制备步骤:
14.将聚乙烯醇凝胶以1.2g/m
2-2g/m2的涂布量涂布在所述功能层上,得到所述粘结层。
15.可选地,所述聚乙烯醇凝胶的制备方法如下:
16.将聚乙烯醇加入去离子水中,使得聚乙烯醇的浓度达到7%,煮沸溶解后于-20℃下冷冻12小时,室温解冻4小时,重复冷冻和解冻操作5次,得到所述聚乙烯醇水凝胶。
17.可选地,该薄膜的制备方法还包括基层的复合步骤:
18.将聚乙烯树脂在压力为1.8mpa-4.5mpa、温度为50℃-65℃的条件下与所述粘结层复合,得到薄膜半成品;
19.将所述薄膜半成品在50℃-55℃的温度下进行熟化处理5h-8h,得到所述薄膜。
20.可选地,所述聚乙烯树脂通过流延工艺制得。
21.本发明的一个目的是提供如上任一项所述的薄膜的制备方法制备的薄膜在临床放疗剂量定量成像中的应用。
22.本发明所提供的薄膜的制备方法制备的功能层中包含放射性致长余辉发光材料,可以代替ebt胶片进行获得放射治疗计划的二维剂量分布,获得较宽的线性范围,提高治疗计划中的剂量分布和目标实际接受的剂量分布对比的准确性;同时,该薄膜可以穿戴在人体上,排除放射治疗过程中目标区随着运动器官一起运动造成了治疗计划中的剂量分布和目标实际接受的剂量分布存在较大差异,进一步提高了治疗计划中的剂量分布和目标实际接受的剂量分布对比的准确性。
附图说明
23.图1为本发明提供的一个薄膜的制备方法的流程图;
24.图2为本发明提供的ebt的线性范围和灵敏度值;
25.图3为本发明提供的薄膜的线性范围和灵敏度值。
具体实施方式
26.为了使本发明的上述目的、特征和优点能够更加明显易懂,下面结合附图对本发明的具体实施方式做详细的说明,但不能理解为对本发明的可实施范围的限定。
27.鉴于现有技术中,ebt胶片的线性范围窄和目标区域随运动器官一起运动导致的计划中的剂量分布和目标实际接受的剂量分布存在较大差异的问题,本发明提供一种薄膜的制备方法,通过该薄膜的制备方法制备的薄膜可以提高了治疗计划中的剂量分布和目标实际接受的剂量分布对比的准确性。
28.该薄膜的制备方法包括功能层的制备步骤:
29.将质量比为200-2000:6-240:1的分散剂、固化剂和放射性致长余辉发光材料混合均匀,得到混合物。
30.放射性致长余辉发光材料在放射线中被激发,使放射性致长余辉发光材料发出余辉,该余辉可以被肉眼或仪器识别。分散剂使放射性致长余辉发光材料均匀地分散在功能层中,固化剂用于使分散剂和放射性致长余辉发光材料固化成膜,可以覆盖在病灶区域。在分散剂、固化剂和放射性致长余辉发光材料的质量比为200-2000:6-240:1的情况下,放射性致长余辉发光材料在功能层的分布均匀,使功能层的各部位在放射线的照射后都可以受到激发发出余晖,各部位余晖的光强和受到照射的强度成正比,功能层能够固化成膜,同时使得放射性致长余辉发光材料在功能层中质量分数占有较大的比例,使功能层发出的足够强度的余晖被肉眼或机器识别。
31.将混合物倒入平底容器中,在真空干燥箱箱内进行抽真空处理。
32.上述操作去除混合物中的水分利于进行固化操作,同时真空处理能够去除混合物中的气泡,避免制备的薄膜中存在气泡使得放射性致长余辉发光材料不均匀对薄膜成像的影响。
33.将抽真空处理后的混合物进行固化,得到功能层。
34.混合物固化成膜得到功能层,该功能层可单独用于临床放疗剂量定量成像,附着在病灶区域,也可和其他膜层复合,形成具备多功能的薄膜。
35.该薄膜可以代替ebt胶片进行获得放射治疗计划的二维剂量分布,获得较宽的线性范围,提高治疗计划中的剂量分布和目标实际接受的剂量分布对比的准确性;同时,该可以穿戴在人体上,排除放射治疗过程中目标区随着运动器官一起运动造成了治疗计划中的剂量分布和目标实际接受的剂量分布存在较大差异,进一步提高了治疗计划中的剂量分布和目标实际接受的剂量分布对比的准确性。
36.在一个实施例中,分散剂、固化剂和放射性致长余辉发光材料的质量比为1000:10:1。
37.进一步地,分散剂为疏水性高分子聚合物材料,固化剂为道康宁184。
38.少量的道康宁184即可实现固化,避免放射性致长余辉发光材料的浓度被稀释。
39.可选地,道康宁184可用乙烯基三胺deta、氨乙基哌嗪ae、二氨基环己烷dach、异佛尔酮二胺ipda、亚甲基双环己烷胺4,4'-pacm、乙二胺eda、二乙烯三胺deta和二已基三胺代替。
40.可选地,疏水性高分子聚合物选自聚二甲基硅氧烷、环甲基硅氧烷、氨基硅氧烷、聚甲基苯基硅氧烷、聚醚聚硅氧烷共聚物、聚烯烃、聚碳酸酯、聚酰胺、聚丙烯腈和聚酯中的一种或多种。优选,聚二甲基硅氧烷。
41.在一个实施例中,抽真空的条件为10-4000pa,固化条件为干燥箱参数设定温度为20-100℃;固化时间为10-300分钟。
42.在一个实施例中,该薄膜的制备方法还包括粘结层的制备步骤:
43.将聚乙烯醇凝胶以1.2g/m
2-2g/m2的涂布量涂布在所述功能层上,得到粘结层。
44.进一步地,聚乙烯醇凝胶的制备方法如下:
45.将聚乙烯醇加入去离子水中,使得聚乙烯醇的浓度达到7%,煮沸溶解后于-20℃下冷冻12小时,室温解冻4小时,重复冷冻和解冻操作5次,得到所述聚乙烯醇水凝胶。
46.在一个实施例中,该薄膜的制备方法还包括基层的复合步骤:
47.将聚乙烯树脂在压力为1.8mpa-4.5mpa、温度为50℃-65℃的条件下与粘结层复合,得到薄膜半成品;
48.将薄膜半成品在50℃-55℃的温度下进行熟化处理5h-8h,得到薄膜。
49.进一步地,聚乙烯树脂通过流延工艺制得。
50.本发明的制备步骤简洁,制备过程精确可控,所制备薄膜表面耐用性强,具备良好的韧性,可贴合身体各部位来使用,并能进行多次贴合、剥离的循环重复使用,可适用基体范围广,该薄膜可以应用于研究在呼吸运动状态下的剂量空间分布,让感兴趣点和空间分析变成可能,以指导放疗医生靶区勾画。
51.本发明的一个目的是提供如上任一项所述的薄膜的制备方法制备的薄膜在临床放疗剂量定量成像中的应用。
52.参阅说明书图2和图3,本发明所提供的薄膜具有较ebt胶片更宽的线性范围和更高的灵敏值。该薄膜穿戴在人体上,可以提高治疗计划中的剂量分布和目标实际接受的剂量分布的准确性。
53.实施例1
54.取质量比为1000:10:1的疏水性高分子聚合物材料、固化剂、放射性致长余辉发光材料,然后由搅拌机搅拌混合均匀,得到混合物;将混合均匀后的混合物倒入平底容器中,然后放置在真空干燥箱中进行抽真空处理,去除混合物中的气泡;将真空处理后的混合物进行固化,获得表面平整的外层薄膜。
55.实施例2
56.1、取质量比为1000:10:1的疏水性高分子聚合物材料、固化剂、放射性致长余辉发光材料,然后由搅拌机搅拌混合均匀,得到混合物;将混合均匀后的混合物倒入平底容器中,然后放置在真空干燥箱中进行抽真空处理,去除混合物中的气泡;将真空处理后的混合物进行固化,获得表面平整的外层薄膜;
57.2、将聚乙烯醇水凝胶以1.5g/m2的涂布量涂布在步骤1制得的基层薄膜上,得到粘结层,然后将基层薄膜在压力为2mpa、温度为60℃的条件下与粘结层复合而成,得到复合薄膜半成品;
58.3、将步骤2的复合薄膜半成品在50℃的温度下进行熟化处理5h,即得所述可穿戴薄膜。
59.实施例3
60.1、将聚乙烯醇(pva-1779)加入去离子水中,使得pva的浓度达到7%,煮沸溶解后于-20℃下冷冻12小时,室温解冻4小时,重复冷冻和解冻操作5次,得到聚乙烯醇水凝胶;
61.2、将pe树脂经流延工艺制得基层薄膜;
62.3、取质量比为1000:10:1的疏水性高分子聚合物材料、固化剂、放射性致长余辉发光材料,然后由搅拌机搅拌混合均匀,得到混合物;将混合均匀后的混合物倒入平底容器中,然后放置在真空干燥箱中进行抽真空处理,去除混合物中的气泡;将真空处理后的混合物进行固化,获得表面平整的外层薄膜;
63.4、将步骤1得到的聚乙烯醇水凝胶以1.5g/m2的涂布量涂布在步骤2制得的基层薄膜上,得到粘结层,然后将步骤3制得的外层薄膜在压力为2mpa、温度为60℃的条件下与粘
结层复合而成,得到复合薄膜半成品;
64.5、将步骤4的复合薄膜半成品在50℃的温度下进行熟化处理5h,即得所述可穿戴薄膜。
65.实施例4
66.1、将聚乙烯醇(pva-1779)加入去离子水中,使得pva的浓度达到7%,煮沸溶解后于-20℃下冷冻12小时,室温解冻4小时,重复冷冻和解冻操作5次,得到聚乙烯醇水凝胶;
67.2、将pe树脂经流延工艺制得基层薄膜;
68.3、取质量比为1000:10:1的疏水性高分子聚合物材料、固化剂、放射性致长余辉发光材料,然后由搅拌机搅拌混合均匀,得到混合物;将混合均匀后的混合物倒入平底容器中,然后放置在真空干燥箱中进行抽真空处理,去除混合物中的气泡;将真空处理后的混合物进行固化,获得表面平整的外层薄膜;
69.4、将步骤1得到的聚乙烯醇水凝胶以1.5g/m2的涂布量涂布在步骤2制得的基层薄膜上,得到粘结层,然后将步骤3制得的外层薄膜在压力为2mpa、温度为60℃的条件下与粘结层复合而成,得到复合薄膜半成品;
70.5、将步骤4的复合薄膜半成品在50℃的温度下进行熟化处理5h,即得所述可穿戴薄膜。
71.实施例5
72.1、将聚乙烯醇(pva-1779)加入去离子水中,使得pva的浓度达到7%,煮沸溶解后于-20℃下冷冻12小时,室温解冻4小时,重复冷冻和解冻操作5次,得到聚乙烯醇水凝胶;
73.2、将pe树脂经流延工艺制得基层薄膜;
74.3、取质量比为1000:10:1的疏水性高分子聚合物材料、固化剂、放射性致长余辉发光材料,然后放置在真空干燥箱中进行抽真空处理,去除混合物中的气泡;将真空处理后的混合物进行固化,获得表面平整的外层薄膜;
75.4、将步骤1得到的聚乙烯醇水凝胶以1.5g/m2的涂布量涂布在步骤2制得的基层薄膜上,得到粘结层,然后将步骤3制得的外层薄膜在压力为2mpa、温度为60℃的条件下与粘结层复合而成,得到复合薄膜半成品;
76.5、将步骤4的复合薄膜半成品在50℃的温度下进行熟化处理5h,即得所述可穿戴薄膜。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1