一种多功能可注射组织粘合剂及其制备方法与流程
本发明属于临床应用材料领域,具体涉及一种多功能可注射组织粘合剂及其制备方式。
背景技术:
1、组织粘合剂作为新一代临床应用材料,可快速闭合伤口,有效防止液体渗透,并最大限度地降低附加创伤。临床常用的粘合剂主要分为三大类,生物提取类,合成类及半合成类。然而,目前商用的粘合剂已逐步显示出以下两大不足:(1)优异的生物安全性和良好的组织粘合强度难以兼顾;(2)所需生物功能缺乏,易出现伤口感染、愈合缓慢等问题。
2、生物提取类粘合剂,如纤维蛋白胶(crossealtm、cryosealtm、)、胶原基蛋白粘合剂等,虽然具有优异的生物相容性,且反应过程模拟自身交联固化机制,温和安全,并且可伴随伤口的愈合而发生相应降解,具有一定的促组织愈合活性。然而,此类材料内聚力低,且与组织界面之间无稳定连接,因此粘合强度普遍不足,且凝血效果受限于伤口环境,导致其应用范围十分有限。
3、合成类组织粘合剂,如α-氰基丙烯酸酯胶聚乙二醇胶(cosealtm、)等,虽然能在材料内部及组织界面间建立稳定的共价连接,具有较高的粘合强度,但是反应过程常伴随放热、毒副产物的溶出以及有毒催化剂的使用等,导致其生物安全性较差,同时降解速率受限于反应类型,通常不能随伤口的愈合而按需降解,可能会长期占位而影响愈合。
4、在生物提取及合成类组织粘合剂的基础上,为了获得更高的粘合强度和生物安全性,基于合成与天然分子相结合的半合成类粘合剂应运而生。然而,目前的半合成类组织粘合剂,如明胶基粘合剂牛血清白蛋白基粘合剂为追求高的交联效率和强度,通常会用到活性较高但毒性较大的交联剂,如甲醛、戊二醛等,依然无法根本解决生物安全性与粘合强度相矛盾的问题。
5、申请号为cn202011631269.1的中国专利公开了一种复合组织粘合剂及其制备方法和应用。该复合组织粘合剂包括三维多孔基质以及吸附在基质表面的增强粘附因子,所述三维多孔基质由甲基丙烯酸酐化明胶和接枝n-羟基琥珀酰亚胺的聚丙烯酸的复合水凝胶冻干得到,所述增强粘附因子为聚多巴胺。该发明具有两种组分可与创面组织上的氨基进行键合,虽然与湿润创面的组织粘附强度可以达到180kpa以上,但并未表现出良好的抗菌性能,以及针对伤口愈合的生物学活性。此外,因其可注射性的缺乏而无法应用于复杂伤口的密封,局限性较大。
6、因此,设计一款制备简单,同时具有优异的生物安全性和高粘合强度、抗溶胀、抗菌、促进组织愈合的多功能可注射组织粘合剂,从而进一步扩大其临床应用范围,并同时提升伤口愈合质量及缩短住院周期,具有重要研究及实用意义。
技术实现思路
1、为了解决上述问题,本发明提供了一种多功能可注射组织粘合剂及其制备方法。模拟天然细胞外基质成分的仿生设计:以透明质酸(ha)和iii型重组胶原(col)为主要成分,可充分发挥天然分子高生物安全性、抗炎、促血管生成和高细胞亲和性等优势。
2、对天然大分子的功能化基团修饰:对ha和col分别进行活性酯(nhs)和还原态多酚功能基团(dopared)的修饰,利用ha上的nhs基团与col及组织表面上的氨基或巯基进行亲核加成反应,可实现组织伤口原位密封,并通过改变缓冲液中无机盐的类型及浓度,对凝胶化时间实现可控调节。随后,网络中的还原态多酚基团可发生缓慢氧化而自聚,并能与周围剩余氨基或巯基发生席夫碱反应或迈克尔加成,以增强材料的内聚力和粘合力,并起到自增强及抗溶胀效果。同时,原位生成适量h2o2,赋予粘合剂长效抗菌活性。
3、一方面,本发明提供了一种多功能组织粘合剂。
4、所述的多功能组织粘合剂中包括:
5、(1)组分a:化学修饰还原型多酚基团且表面含rgd序列、赖氨酸、天冬氨酸和/或谷氨酸的活性蛋白;
6、(2)组分b:化学修饰活性酯基团的天然多糖;
7、(3)成胶缓冲液:碱性缓冲溶液及酸性溶液。
8、具体地,所述的组分a中的活性蛋白表面包含:rgd序列以提供细胞可黏附的活性位点;赖氨酸链段以提供可反应的活性氨基;天冬氨酸和/或谷氨酸链段以提供可反应的活性羧基。
9、优选地,所述活性蛋白选自:重组i型胶原、重组iii型胶原、明胶、溶菌酶中的一种或多种。
10、具体地,所述的组分a中的多酚基团选自:邻苯二酚、邻苯三酚或其组合。
11、所述的多酚基团的还原程度利用还原剂进行可控调节,其酚醌比例在2:8到8:2之间。
12、优选地,所述的组分a为还原型多巴胺功能化重组ⅲ型胶原(col-dopared)。
13、所述的组分b中的天然多糖的活性酯基团选自:琥珀酰亚胺碳酸酯、琥珀酰亚胺乙酸酯、琥珀酰亚胺丙酸酯、琥珀酰亚胺琥珀酸酯、琥珀酰亚胺戊二酸酯中的一种或多种。
14、所述的活性酯基团修饰率为10-50%。
15、优选地,所述的组分b中的天然多糖侧链含有羧基基团。
16、优选地,所述的组分b中的天然多糖分子量为10-500kda。
17、优选地,所述的组分b为活性酯功能化透明质酸(ha-nhs)。
18、所述的成胶缓冲液中:
19、碱性缓冲液中的无机盐选自:四硼酸钠、碳酸钠、磷酸氢二钠或其组合;
20、酸性溶液中的酸性物质选自:盐酸、乙酸、磷酸二氢钠或其组合。
21、本发明方案的反应原理:
22、成胶及粘合原理:透明质酸侧链上修饰的活性酯基团可与重组ⅲ型胶原及组织表面蛋白中赖氨酸上的氨基进行自发的亲核加成反应,形成稳定的酰胺键,实现前驱液的固化和伤口密封。
23、成胶时间可控原理:活性酯与氨基之间的酰胺化反应为亲核加成过程,其反应速率与氨基组分的脱质子化程度密切相关,氨基的脱质子化程度越高,亲核性越强,反应速率越快。而氨基组分的脱质子化程度又与体系环境的ph值呈正相关,因此通过调整缓冲液中强碱弱酸盐的类型及浓度,即可实现对凝胶化时间的精准控制。
24、自增强原理:重组ⅲ型胶原上修饰的还原型多巴胺基团具有自氧化特性,通过缓慢的自聚反应形成凝胶内部的二重交联,氧化后的苯醌基团可与周围的氨基、巯基发生迈克尔加成或席夫碱反应,进一步提升粘合强度及胶体的稳定性。
25、抗菌原理:重组ⅲ型胶原上修饰的还原型多巴胺基团在自氧化过程中,可将酚羟基中储存的电子传递给周围的氧气,从而原位生成过氧化氢,一种高效、清洁的抗菌剂,赋予材料良好的抗菌活性。
26、促进组织愈合原理:活性蛋白本身的rgd序列及所修饰的还原态多酚基团均可促进细胞黏附,同时伴随材料的降解也为新生组织的生长提供了空间,从而加速组织愈合。
27、另一方面,本发明提供了一种粘合剂医疗器械包。
28、所述的粘合剂医疗器械包包括前述的一种多功能可注射组织粘合剂。
29、所述的组织粘合剂的成分分别包装,其中组分a和组分b为粉末;所述的碱性缓冲液和酸性溶液为液体。
30、所述的粘合剂医疗器械包包括一种双筒注射器或涂抹棒。
31、优选地,所述的多功能组织粘合剂包括活性酯功能化透明质酸(ha-nhs)、还原型多巴胺功能化重组ⅲ型胶原(col-dopared)、酸性溶液、碱性缓冲液;进一步优选地,所述的酸性溶液为盐酸稀释液,所述的碱性缓冲液为na2b4o7溶液;更进一步地,所述的盐酸稀释倍数为105,所述的na2b4o7溶液浓度为0.1m。
32、在一些实施例中,所述的ha-nhs以60mg/ml的浓度溶于盐酸稀释液(105倍);所述的col-dopared以120mg/ml的浓度溶于0.1m的na2b4o7溶液。
33、再一方面,本发明提供了一种制备前述的组织粘合剂的方法。
34、步骤包括:
35、(1)将组分a、b的粉末分别溶于碱性缓冲液和酸性溶液中,得成胶前驱液a和成胶前驱液b。
36、(2)利用双筒注射器或涂抹棒,将胶前驱液a和成胶前驱液b混合均匀,形成所述的多功能组织粘合剂。
37、优选地,所述的方法如下:将还原型多巴胺功能化重组ⅲ型胶原(col-dopared)溶解于碱性缓冲液中作为成胶前驱体a,将活性酯功能化透明质酸(ha-nhs)溶于弱酸性溶液中作为成胶前驱体b。将两种溶液混合后交付,原位形成该凝胶粘合剂(ha-col)。
38、再一方面,本发明提供了前述的多功能可注射组织粘合剂的应用。
39、所述的应用为术后血管、心脏、硬脑膜等软/硬组织密封。
40、本发明的有益效果:
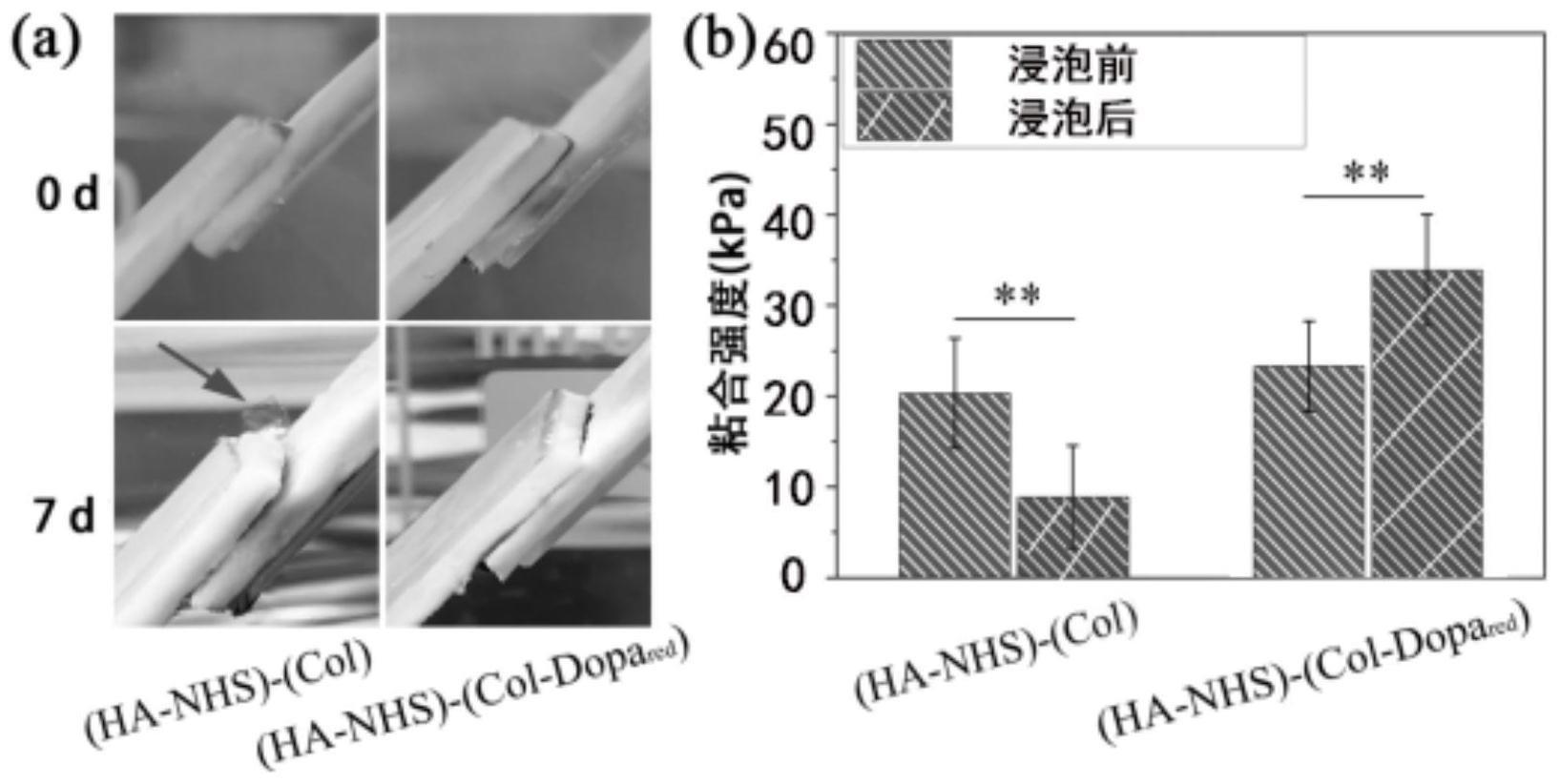
41、1.解决了目前粘合剂存在优异的生物安全性和良好的组织粘合强度难以兼顾,易吸收体液而溶胀过大的问题,该粘合剂可与组织间建立稳固连接,并可通过后续凝胶网络内部的自交联而有效抵御因体液浸润而发生的过度溶胀,降低了压迫周围组织、神经以及粘合力减弱甚至粘合剂脱落的风险,保证了其在应用过程中的安全性和稳定性。
42、2.解决了目前粘合剂缺乏抗菌活性,无法避免伤口感染的不足,该粘合剂模拟了生物体抗菌机制,通过原位释放清洁、高效、安全的抗菌剂杀灭细菌。
43、3.解决了目前粘合剂缺乏生物活性,无法促进组织愈合的不足,模拟了天然细胞外基质的成分与结构,为组织再生提供了良好的微环境。
- 还没有人留言评论。精彩留言会获得点赞!