一种伊班膦酸钠注射液及其制备方法与流程
1.本发明属于医药技术领域,具体涉及一种油包水型的伊班膦酸钠注射液及其制备方法。
背景技术:
2.伊班膦酸钠注射液系第三代双膦酸盐类药物,主要治疗绝经后骨质疏松症、预防乳腺癌骨转移患者骨相关事件的发生、治疗伴有或不伴有骨转移的恶性肿瘤引起的高钙血症。然而目前上市的伊班膦酸钠注射液在注射时有较强的刺激性,因此需要慢滴输液,一次给时间长达2小时。不但给药时间长,而且仍然存疼痛等刺激性副作用。给患者带来严重不适和顺应差的感受。
3.为了解决现有伊班膦酸钠注射液的不足,提供了一种新型的油包水型伊班膦酸钠注射液。
技术实现要素:
4.本发明的目的在于提供一种伊班膦酸钠注射液及其制备方法,该注射液为油包水型注射液,可显著降低伊班膦酸钠的刺激性,特别是皮下注射时的刺激性。
5.为实现本发明的目的,提供如下实施方案:
6.本发明的一种伊班膦酸钠注射液,由伊班膦酸钠、水、大豆油、司盘80、吐温80组成的油包水型注射液,其特征在于:大豆油与注射用水的比为3.0:1-4.0:1,司盘80的含量为4.0-6.0%,吐温80的含量为0.7-1.0%。
7.优选的,上述本发明的注射液,所述大豆油与注射用水的比为3.4:1,所述司盘80的含量为5.5%,所述吐温80的含量为0.9%。
8.优选的,上述本发明的注射液,所述伊班膦酸钠与大豆油的重量比为1:164-1:188,优选为1:170。
9.本发明还提供了一种上述本发明的注射液的制备方法,包含以下步骤:
10.1)称取处方量的注射用水,置于配液容器1中,加入处方量的伊班膦酸钠,搅拌溶解完全,得a相;
11.2)称取处方量的大豆油,置于配液容器2中,加入处方量的司盘80、吐温80,搅拌溶解完全,得b相;
12.3)将a相和b相加热到70
±
3℃,在搅拌速度为300-500r/min、加热保持温度为70
±
3℃的条件下将水相加至油相,搅拌0.5小时,关闭加热继续在搅拌速度为100-200r/min条件下搅拌1小时,过滤;
13.4)将步骤3)的滤液灌封于安瓿瓶中,灭菌即得。
14.本发明的伊班膦酸钠注射液可用于静脉给药和皮下给药,优选为皮下给药。
15.本发明的伊班膦酸钠注射液,将伊班膦酸钠用注射用水溶解得含伊班膦酸钠的水相、将司盘80、吐温80溶于大豆油中得含大豆油的油相,再在搅拌下将含伊班膦酸钠的水相
加入到含大豆油的油相中乳化,制备成含伊班膦酸的油包水型注射剂。与现有技术相比,该方法显著降低了伊班膦酸钠皮下注射的刺激性。可提高注射液的安全性和患者的顺应性。
具体实施方式
16.通过以下实施例可以更好地理解本发明的实质。以下实施例是用于说明和理解本发明的精神实质,但不应被理解为限制本发明的范围。
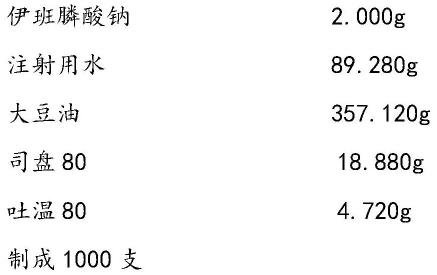
17.实施例1
18.处方:
19.制备工艺:
20.1)称取处方量的注射用水,置于配液容器1中,加入处方量的伊班膦酸钠,搅拌溶解完全,得a相;
21.2)称取处方量的大豆油,置于配液容器2中,加入处方量的司盘80、吐温80,搅拌溶解完全,得b相;
22.3)将a相和b相加热到70
±
3℃,在搅拌速度为300-500r/min、加热保持温度为70
±
3℃的条件下将水相加至油相,搅拌0.5小时,关闭加热继续在搅拌速度为100-200r/min条件下搅拌1小时,过滤;
23.4)将步骤3)的滤液灌封于安瓿瓶中,灭菌即得。
24.实施例2
25.处方:
26.制备工艺:
27.1)称取处方量的注射用水,置于配液容器1中,加入处方量的伊班膦酸钠,搅拌溶解完全,得a相;
28.2)称取处方量的大豆油,置于配液容器2中,加入处方量的司盘80、吐温80,搅拌溶解完全,得b相;
29.3)将a相和b相加热到70
±
3℃,在搅拌速度为300-500r/min、加热保持温度为70
±
3℃的条件下将水相加至油相,搅拌0.5小时,关闭加热继续在搅拌速度为100-200r/min条
件下搅拌1小时,过滤;
30.4)将步骤3)的滤液灌封于安瓿瓶中,灭菌即得。
31.实施例3
32.处方:
33.制备工艺:
34.1)称取处方量的注射用水,置于配液容器1中,加入处方量的伊班膦酸钠,搅拌溶解完全,得a相;
35.2)称取处方量的大豆油,置于配液容器2中,加入处方量的司盘80、吐温80,搅拌溶解完全,得b相;
36.3)将a相和b相加热到70
±
3℃,在搅拌速度为300-500r/min、加热保持温度为70
±
3℃的条件下将水相加至油相,搅拌0.5小时,关闭加热继续在搅拌速度为100-200r/min条件下搅拌1小时,过滤;
37.4)将步骤3)的滤液灌封于安瓿瓶中,灭菌即得。
38.实施例4动物刺激性实验
39.参照中国药物刺激性、过敏性和溶血性研究技术指导原则,对本发明的伊班膦酸钠注射液进行刺激性试验,实验动物为家兔,设置试验组(本发明的伊班膦酸钠注射液,实施例1-3,以实施例3的注射液为代表),阳性对照组(选取参比制剂邦罗力(bondronat)2ml:2mg),原料组、空白组(生理盐水)。本品拟用于临床的用法用量为一次4mg,皮下注射,单次使用最高剂量为0.067mg/kg(按成人均重60kg计算)。本试验的参比制剂、原料组和实施例3组均按1.2mg/kg的给药体积背部皮下注射给药,剂量为1.2mg/kg。
40.分组与给药
41.9只兔子分为3组,采用同体左右侧自身对比法。各组动物数量及给药方案如下表:
42.43.原料组样品制备:
44.处方:伊班膦酸钠2.000g
45.生理盐水498.000g
46.制成1000支
47.制备工艺:
48.称取处方量的生理盐水,加入处方量的伊班膦酸钠,搅拌溶解完全,过滤,滤液灌封于安瓿瓶中,灭菌即得。
49.实验观察
50.(1)家兔一般情况观察
51.给药前及给药后6h、24h、48h和72h,对家兔一般症状进行观察。内容包括中枢和运动神经系统、植物神经系统、呼吸系统、心血管系统、消化系统、泌尿生殖系统、皮肤和皮毛、眼等。
52.(2)皮下刺激性症状观察
53.观察动物在皮下注射过程中及注射结束后是否有嘶叫、躲避等疼痛反应,以及注射部位是否出现增厚现象。
54.给药前及给药后24h、48h和72h肉眼观察注射部位,参照皮肤刺激反应评价标准对皮下注射部位的反应进行评分,参照皮肤刺激强度分级标准评价皮下注射的刺激性强度。皮肤反应评分标准见表1,皮下注射刺激性刺激强度分级标准见表2,实验结果见表3。
55.表1皮肤反应的评分标准
[0056][0057]
表2皮下注射刺激性刺激强度分级标准
[0058][0059]
表3伊班膦酸钠注射液给药的皮下刺激性试验结果
[0060][0061]
表3的结果表明,本发明的伊班膦酸钠注射液,采用油包水型,相比现有上市的注射液安全性非常好,可以实现皮下注射,缩短注射时间,可以提高患者的顺应性。
[0062]
任何在本发明的精神实质上进行简单的修饰和变通,也属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1