一种芦可替尼组合物及其制备方法与流程
1.本发明属于药物制剂领域,具体涉及一种芦可替尼或其药学上可接受的盐的组合物及其制备方法。
背景技术:
2.芦可替尼(又称鲁索替尼,鲁索利替尼,ruxolitinib)其化学名为(r)-3-环戊基-3-[4-(7h-吡咯并[2,3-d]嘧啶-4-基)-1h-吡唑-1-基]丙腈,是一种jak1和jak2酪氨酸激酶抑制剂,用于中危或高危的原发性骨髓纤维化(primary myelofibrosis,pmf)(亦称为慢性特发性骨髓纤维化)、真性红细胞增多症继发的骨髓纤维化(myelofibrosis secondary to polycythemia vera,ppv-mf)或原发性血小板增多症继发的骨髓纤维化(myelofibrosis secondary to primary thrombocytosis,pet-mf)的成年患者,可以治疗与上述疾病相关的脾肿大或其他症状。
[0003][0004]
公开号为cn103002875b的中国发明专利申请公开了一种用于局部皮肤施用的水包油乳液形成的霜剂,该霜剂所用的治疗剂(r)-3-环戊基-3-[4-(7h-吡咯并[2,3-d]嘧啶-4-基)-1h-吡唑-1-基]丙腈(即芦可替尼)或其药学上可接受的盐,油相选自凡士林、脂肪醇、矿物油、甘油三酯和二甲基硅氧烷的一种或多种物质、乳化剂组分包含独立地选自甘油脂肪酯和山梨醇酐脂肪酯的一种或多种物质、溶剂组分包含独立地选自亚烷基二醇和聚亚烷基二醇的一种或多种物质、稳定剂组分包含独立地选自多糖的一种或多种物质,一般外用制剂ph值要求在4.5-7之间,而该专利中的制剂样品ph值在3.1-3.6左右,使用时对患者具有一定的皮肤刺激性,且不适用于皮肤有一定破损的部位。
[0005]
公开号us20200405627a1的美国发明专利公开了使用1.5%w/w芦可替尼水包油乳液治疗白癜风的方法,所述芦可替尼水包油乳液油组分选自凡士林,脂肪醇,矿物油,甘油三酸酯和聚二甲基硅氧烷的物质,乳化剂组分甘油脂肪酸酯和脱水山梨糖醇脂肪酸酯的物质,溶剂组分亚烷基二醇和聚亚烷基二醇的物质,稳定剂组分选自多糖的物质如黄原胶。
[0006]
体外释放试验是目前评价半固体制剂(如乳膏剂、软膏剂、凝胶剂等)的公认的有
效方法,是制剂体内药效的体外体现。体外释放具有可操作性强、重现性好、灵敏度高的特点。因此,合适的体外释放试验方法将有助于透皮吸收制剂的开发。公开号cn111337640a的中国发明专利公开了一种快速评价外用制剂体外释放的方法。目前主要使用franz扩散池法评价外用制剂体外释放和渗透,体外释放则使用人工膜,渗透则使用离体大鼠腹部皮肤或离体巴拿马香猪的皮肤或人工仿生膜(membrane)考察药物的皮肤透过率。
技术实现要素:
[0007]
本发明的一方面是提供一种芦可替尼组合物,所述组合物含有治疗剂和乳化剂。
[0008]
根据本发明的一些实施例,所述治疗剂为芦可替尼和/或其药学上可接受的盐,其含量以基于游离碱按所述组合物重量计的0.5%~2.0%。
[0009]
根据本发明的一些实施例,所述乳化剂为聚氧乙烯烷基芳基醚、聚氧乙烯单月桂酸酯、聚氧乙烯单月桂酸酯、聚氧乙烯月桂醚、聚氧乙烯氢化蓖麻油、聚氧乙烯蓖麻油、聚氧乙烯植物油、聚氧乙烯单油酸酯、聚氧乙烯单月桂酸酯、维生素e琥珀酸的一种或多种,优选聚氧乙烯氢化蓖麻油、聚氧乙烯蓖麻油、聚氧乙烯单油酸酯、聚氧乙烯单月桂酸酯、维生素e琥珀酸的一种或多种,进一步优选聚氧乙烯氢化蓖麻油、聚氧乙烯蓖麻油、维生素e琥珀酸一种或多种。
[0010]
根据本发明的一些实施例,所述乳化剂为聚氧乙烯氢化蓖麻油、聚氧乙烯蓖麻油、维生素e琥珀酸一种或多种,所述的聚氧乙烯氢化蓖麻油选自rh20、rh30、rh40、rh50、rh60的一种或多种,优选rh40和rh60的一种,更优选rh40;聚氧乙烯蓖麻油选自el20、el25、el30、el35、el40、el60的一种或多种,优选el30、el35、el40的一种或多种,更优选el35;所述的维生素e琥珀酸选自ve-tpgs 400、ve-tpgs 1000、ve-tpgs1500的一种或多种,优选ve-tpgs 1000;乳化剂含量按所述组合物重量计的2%-30%,进一步的优选3%-12%。
[0011]
根据本发明的一些实施例,所述的芦可替尼组合物包含治疗剂、乳化剂、助乳化剂。
[0012]
根据本发明的一些实施例,所述助乳化剂包含丙二醇单辛酸酯(capryol-90),其含量按所述组合物重量计0~10%,优选0~7%;
[0013]
根据本发明的一些实施例,所述的芦可替尼组合物包含治疗剂、乳化剂、助乳化剂、溶剂。
[0014]
根据本发明的一些实施例,所述溶剂为丙二醇,二乙二醇单乙醚(hp),乙醇的一种或多种,其含量按所述组合物重量计0~60%,优选0~50%;
[0015]
根据本发明的一些实施例,所述的芦可替尼组合物包含治疗剂、乳化剂、助乳化剂、溶剂、水相。
[0016]
根据本发明的一些实施例,所述水相包括水和任选的辅料。可以在水中添加ph调节剂、渗透压调节剂、防腐剂、抗氧剂及遮光剂等,进一步提高所述芦可替尼组合物制剂满足临床不同给药途径的需求,其含量以重量百分比计为与治疗剂、乳化剂、助乳化剂、溶剂之和为100%。
[0017]
在一些实施例中,所述芦可替尼组合物包含:
[0018]
治疗剂:芦可替尼或其药学上可接受的盐;
[0019]
乳化剂:聚氧乙烯氢化蓖麻油、聚氧乙烯蓖麻油、维生素e琥珀酸一种或多种;
[0020]
助乳化剂:丙二醇单辛酸酯;
[0021]
溶剂:丙二醇、二乙二醇单乙醚、乙醇一种或多种;
[0022]
以及至100wt%的水;
[0023]
在一些实施例中,以所述组合物的总重量计,所述芦可替尼组合物包含:
[0024]
治疗剂:芦可替尼或其药学上可接受的盐0.5%~2.0%(以游离碱计);
[0025]
乳化剂:聚氧乙烯氢化蓖麻油、聚氧乙烯蓖麻油、维生素e琥珀酸一种或多种,2%-30%,进一步的优选3%-12%;
[0026]
助乳化剂:丙二醇单辛酸酯0~10%,优选0~7%;
[0027]
溶剂:丙二醇、二乙二醇单乙醚、乙醇一种或多种,0~60%,优选0~50%;
[0028]
以及至100wt%的水;
[0029]
根据本发明的实施例,所述芦可替尼组合物的制备方法为:1)将治疗剂、乳化剂、助乳化剂加热至30-70℃,优选35-60℃,搅拌后加水相即得;或2)治疗剂、助乳化剂、混合加热至30-70℃搅拌溶解,再加入乳化剂,优选35-60℃,搅拌后加水相即得。
[0030]
根据本发明的实施例,所述芦可替尼组合物的制备方法为:1)将治疗剂、乳化剂、溶剂、助乳化剂加热至30-70℃,优选35-60℃,搅拌后加水相即得;或2)治疗剂、助乳化剂、溶剂混合加热至30-70℃搅拌溶解,再加入乳化剂,优选35-60℃,搅拌后加水相即得。
[0031]
在本发明的又一方面,本发明提供了一种前面所述芦可替尼组合物的用途,所述组合物可用于制备药物制剂,所述制剂包括但不限于片剂、颗粒剂、微丸剂、软膏剂、乳膏剂、凝胶剂。
[0032]
在本发明的又一方面,本发明提供了一种前面所述芦可替尼组合物的用途,具体的为芦可替尼凝胶,所述凝胶除含有前面所述芦可替尼组合物外,还含有凝胶材料。所述凝胶材料选自卡波姆、甲基纤维素、羧甲基纤维素钠、壳聚糖、结冷胶、瓜尔胶、羧甲基纤维素钠、羟丙基纤维素中的一种或多种,优选卡波姆,其含量以重量百分比计为0.10%~2.0%,进一步的优选0.25%~1.0%。
[0033]
在一些实施例中,所述芦可替尼凝胶包含:
[0034]
治疗剂:芦可替尼,或其药学上可接受的盐;
[0035]
乳化剂:聚氧乙烯氢化蓖麻油、聚氧乙烯蓖麻油、维生素e琥珀酸一种或多种;
[0036]
助乳化剂:丙二醇单辛酸酯;
[0037]
溶剂:丙二醇、二乙二醇单乙醚、乙醇一种或多种;
[0038]
凝胶材料:卡波姆、甲基纤维素、羧甲基纤维素钠、壳聚糖、结冷胶、瓜尔胶、羧甲基纤维素钠、羟丙基纤维素中的一种或多种;
[0039]
以及至100wt%的水;
[0040]
在一些实施例中,以所述凝胶的总重量计,所述芦可替尼凝胶包含:
[0041]
治疗剂:芦可替尼或其药学上可接受的盐0.5%~2.0%(以游离碱计);
[0042]
乳化剂:聚氧乙烯氢化蓖麻油、聚氧乙烯蓖麻油、维生素e琥珀酸一种或多种,2%-30%、优选3%-12%;
[0043]
助乳化剂:丙二醇单辛酸酯0~10%、优选0~7%;
[0044]
溶剂:丙二醇、二乙二醇单乙醚、乙醇一种或多种0~60%,优选0~50%、更优选2~50%;
[0045]
凝胶材料:卡波姆、甲基纤维素、羧甲基纤维素钠、壳聚糖、结冷胶、瓜尔胶、羧甲基纤维素钠、羟丙基纤维素中的一种或多种0.10%~2.0%,优选0.25%~1.0%;
[0046]
以及至100wt%的水;
[0047]
在一些实施例中,以所述凝胶的总重量计,所述芦可替尼凝胶包含:
[0048]
治疗剂:芦可替尼或其药学上可接受的盐0.5%~2.0%(以游离碱计);
[0049]
乳化剂:聚氧乙烯氢化蓖麻油1~10%、聚氧乙烯蓖麻油1~20%、维生素e琥珀酸0~20%;
[0050]
助乳化剂:丙二醇单辛酸酯0~20%;
[0051]
溶剂:丙二醇1~50%、二乙二醇单乙醚1~10%、乙醇0~50%;
[0052]
凝胶材料:卡波姆0.10%~10.0%;
[0053]
以及至100wt%的水;
[0054]
在一些实施例中,以所述凝胶的总重量计,所述芦可替尼凝胶包含:
[0055]
治疗剂:芦可替尼或其药学上可接受的盐0.5%~2.0%(以游离碱计);
[0056]
乳化剂:聚氧乙烯氢化蓖麻油1.0~5.0%、聚氧乙烯蓖麻油1~10%、维生素e琥珀酸0~10%;
[0057]
助乳化剂:丙二醇单辛酸酯0~10%;
[0058]
溶剂:丙二醇1~45%、二乙二醇单乙醚1~5.0%、乙醇0~40%;
[0059]
凝胶材料:卡波姆0.10%~5.0%;
[0060]
以及至100wt%的水;
[0061]
在一些实施例中,以所述凝胶的总重量计,所述芦可替尼凝胶包含:
[0062]
治疗剂:芦可替尼或其药学上可接受的盐0.5%~2.0%(以游离碱计);
[0063]
乳化剂:聚氧乙烯氢化蓖麻油1~2%、聚氧乙烯蓖麻油4~10%、维生素e琥珀酸0~5%;
[0064]
助乳化剂:丙二醇单辛酸酯0~7%;
[0065]
溶剂:丙二醇5~45%、二乙二醇单乙醚2~5%、乙醇0~15%;
[0066]
凝胶材料:卡波姆0.25%~1.0%;
[0067]
以及至100wt%的水;
[0068]
根据本发明的实施例,所述芦可替尼组合物凝胶的制备方法包括如下步骤:将上述芦可替尼组合物除水相外混合加热至30-70℃,优选35-60℃,搅拌使辅料完全融化及治疗剂溶解后,再与溶胀好的卡波姆搅拌均匀后加入水相,即得芦可替尼凝胶。
[0069]
本发明的又一方面是提供一种如前所述芦可替尼组合物和芦可替尼凝胶用于治疗疾病的用途,所述的疾病为皮炎、银屑病、白癜风、汗腺炎、荨麻疹、斑秃的一种或多种。
[0070]
本发明的有益效果为:本发明提供的芦可替尼组合物的平均粒径范围为10~200nm,pdi值0.05~0.40,进一步的可以达到平均粒径范围为10-100nm,pdi值0.05-0.20,且稳定性好、不易产生聚集、絮凝等。更进一步的,以本发明组合物制成的凝胶相比于芦可替尼乳膏,提高了透膜效率、可满足外用皮肤在ph值5-7条件下给药的稳定性。更进一步的,以本发明组合物制成的凝胶相比于芦可替尼乳膏、以及市售的卡泊三醇和苯维莫德,在银屑病治疗方面具有更好的药效。
[0071]
下面将结合实施例对本发明的方案进行解释。本领域技术人员将会理解,下面的
实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体技术或条件的,按照本领域内的文献所描述的技术或条件或按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规产品。
附图说明
[0072]
图1:实施例6中给药后7天pasi评分
[0073]
图2:实施例6中pasi外观评分曲线图
具体实施方式
[0074]
以下实施例中所用试剂和原料均可通过商购获得。
[0075]“二乙二醇单烷基醚”应该被理解为一种以上被c1至c6烷基醚取代的二乙二醇。二乙二醇单烷基醚是二乙二醇单乙醚(dgme)和二乙二醇单甲醚(dgmm)中的一种或两种。
[0076]
本发明实施例中的hp代指二乙二醇单烷基醚,进一步的是二乙二醇单乙醚。
[0077]
本发明中“pdi”是多分散性指数(polydispersity index)的简称,其物理含义是粒径分布的均匀性,其值分布范围越小则粒径分散越均匀。
[0078]
芦可替尼组合物的平均粒径和pdi值的检测仪器为:马尔文nano s90。
[0079]
实施例1:芦可替尼组合物及其制备方法
[0080]
一、处方组成
[0081]
本发明的芦可替尼组合物含有以下成分:
[0082]
治疗剂:芦可替尼(含量以游离碱计)
[0083]
乳化剂:聚氧乙烯氢化蓖麻油、聚氧乙烯蓖麻油、维生素e琥珀酸一种或多种
[0084]
助乳化剂:丙二醇单辛酸酯(capryol-90)
[0085]
溶剂:丙二醇、二乙二醇单乙醚(hp)、乙醇一种或多种
[0086]
水相:包含水和药学上可接受的辅料,所述辅料包括但不限于ph调节剂、渗透压调节剂、防腐剂、抗氧剂、遮光剂。
[0087]
二、芦可替尼组合物的制备
[0088]
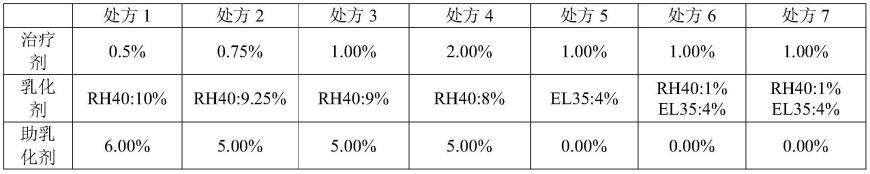
处方1-处方7以方法1制备:将治疗剂、乳化剂、助乳化剂、溶剂混合加热至50℃,搅拌使辅料完全融化及治疗剂溶解后,加入水相,即得。
[0089]
处方8-处方14以方法2制备:将治疗剂、助乳化剂、溶剂混合加热至50℃,搅拌使辅料完全融化及治疗剂溶解后,再加入乳化剂,搅拌后加水相即得。
[0090]
表1:组分比例考察
[0091]
[0092][0093]
表2:组分比例考察
[0094][0095]
由表1、表2可知,当治疗剂含量为0.5%~2.0%时,乳化剂可以为聚氧乙烯氢化蓖麻油、聚氧乙烯蓖麻油、维生素e琥珀酸一种或多种,其含量为3~12%w/w;助乳化剂含量则为0~7%w/w;溶剂含量则为2~50%w/w;水相含量与治疗剂、乳化剂、助乳化剂、溶剂含量之和为100%,所得的芦可替尼组合物具有平均粒径均在100nm以下、pdi值均在0.2以下。
[0096]
实施例2:不同乳化剂考察
[0097]
实施例2与实施例1的制备方法相同,不同之处仅在于所使用乳化剂种类、用量,具体如下表所示:
[0098]
表3:对比例考察
[0099][0100][0101]
由表3可知,乳化剂选择kolliphor hs15、甘油脂肪酯、泊洛沙姆407、吐温80、聚氧乙烯十六烷基醚、聚氧乙烯失水山梨醇单月桂酸酯,均不能形成理想粒径和pdi的芦可替尼组合物。
[0102]
实施例3:芦可替尼组合物处方的稳定性考察
[0103]
选取实施例1中芦可替尼组合物处方2、处方8、处方9、处方12,根据本发明芦可替尼组合物处方在25℃和40℃下,一个月和两个月平均粒径和pdi的变化,以考察本发明芦可替尼组合物处方的稳定性,具体结果如表4所示。
[0104]
表4:芦可替尼组合物的稳定性
[0105][0106]
结果可知,本发明提供的芦可替尼组合物平均粒径和pdi在室温和40℃下均没有发生显著性的变化,稳定性良好。
[0107]
另外选取实施例1中芦可替尼组合物处方12,考察本发明芦可替尼组合物处方的ph稳定性。将处方12使用三乙醇胺调节至不同的ph值,进行室温和加速实验考察处方中芦可替尼的含量,具体结果如表5所示。
[0108]
表5:芦可替尼组合物处方的ph稳定性
[0109][0110]
结果表明,本发明芦可替尼组合物处方在不同ph值3-7条件下芦可替尼的含量均未发生明显变化,稳定性良好。
[0111]
实施例4:芦可替尼凝胶及其稳定性
[0112]
选取实施例2中的处方9、处方10、处方12分别制成凝胶处方1、凝胶处方2、凝胶处方3,凝胶总重为100g。
[0113]
制备方法为:将上述芦可替尼组合物除水相外混合加热至45℃,搅拌使辅料完全融化及治疗剂溶解后,与溶胀好的卡波姆搅拌均匀后再加入水相,即得芦可替尼组合物凝胶。
[0114]
根据凝胶处方1、凝胶处方2、凝胶处方3芦可替尼的含量考察本发明提供的凝胶处方的稳定性,具体结果如表6所示。
[0115]
表6:芦可替尼凝胶处方稳定性
[0116][0117]
结果表明,凝胶处方1、凝胶处方2、凝胶处方3的ph值均在5-7之间,且含量在25℃及40℃条件下没有发生显著性的变化,温度稳定性良好。
[0118]
实施例5:芦可替尼凝胶的体外渗透释放研究
[0119]
实验方法:采用franz扩散池(天津博宇伟业科技有限公司,型号tp-6),将人工透皮膜(membrane)固定于扩散池与接收池之间,扩散池直径为1.5cm,接收池体积为15ml,扩散池装入约300mg芦可替尼凝胶样品,接收池注入接收液(0.05m的ph 7.2-7.4的磷酸盐缓冲液)。水浴温度为32
±
1℃,恒温磁力搅拌转速为300rpm/min。分别于1h、2h、4h、6h、8h从接收池中取出1.5ml,同时及时补加相同量同温度的接收液至接收池,将取出的接收液样品经高速离心(18000rpm/min,离心10min),取上清液hplc法测定不同时间点溶液的浓度(cn)。
[0120]
单位面积累积药物渗透量,计算公式如下:
[0121][0122]
其中,
[0123]
qn:为第n个时间点单位面积的累积药物渗透量(单位:mg/cm2);
[0124]
cn:为第n个时间点的药物浓度(单位:mg/ml);
[0125]ci-1
:为第i-1个时间点的药物浓度(单位:mg/ml);
[0126]
v:为接收池体积(单位:ml);
[0127]
s:为有效渗透面积,本试验中为1.76625cm2;
[0128]
对比例参照因塞特控股公司中国发明专利cn103002875b说明书实施例3中表4所示的处方(芦可替尼游离碱浓度1.0%)制备而成。。
[0129]
表7:本发明处方体外累积释放量(单位:mg/cm2)
[0130] 凝胶处方1凝胶处方2凝胶处方3对比乳膏处方30min0.00100.00050.00810.00001h0.00440.00160.02560.00032h0.01810.01040.06520.00684h0.06620.03540.14300.02946h0.11190.06890.21010.05088h0.15210.10860.27670.0694
[0131]
根据表8:凝胶处方1、凝胶处方2、凝胶处方3相比对比乳膏均具有更快的释放结果,体外释放量显著高于对比乳膏。
[0132]
实施例6:芦可替尼凝胶银屑病药效研究
[0133]
本发明药物能有效改善银屑病症状,本发明药物对银屑病的治疗效果,可通过下
述实验研究得到进一步证实。
[0134]
动物实验:寻常型银屑病(pso)小鼠模型的建立和药物处理
[0135]
1药物与试剂
[0136]
实验材料:健康spf级c57bl/6j小鼠(雌雄各半,8-9周龄,体重20-25g)48只,造模药物(5%咪喹莫特乳膏,四川明欣药业);阳性对照药物(市售卡泊三醇软膏、市售本维莫德乳膏);空白凝胶制剂;市售芦可替尼磷酸盐乳膏(简称原研乳膏,芦可替尼游离碱1.5%);凝胶1;凝胶2;其中凝胶1和凝胶2的处方组成见表8。
[0137]
表8:凝胶1和凝胶2的处方组成(以总重量100g计)
[0138][0139][0140]
2实验方法
[0141]
2.1实验分组
[0142]
实验分组:实验分8组,每组6只,实验共用48只。
[0143]
1)空白对照组(除剃毛外不做任何处理)(n=6只);
[0144]
2)pso模型组(除涂抹咪喹莫特造模外不做任何处理)(n=6只);
[0145]
3)pso模型+空白凝胶制剂组(外用涂抹,频率2次/日,15mg/cm2,连续治疗7天)(n=6只);
[0146]
4)pso模型+阳性药物a组(0.005%卡泊三醇软膏处理,外用涂抹,频率2次/日,15mg/cm2,连续治疗7天)(n=6只);
[0147]
5)pso模型+阳性药物b组(1%本维莫德乳膏处理,外用涂抹,频率2次/日,15mg/cm2,暂定连续治疗7天)(n=6只);
[0148]
6)pso模型+凝胶样品1(外用涂抹,频率2次/日,15mg/cm2,连续治疗7天)(n=6只);
[0149]
7)pso模型+市售芦可替尼乳膏(外用涂抹,频率2次/日,15mg/cm2,连续治疗7天)(n=6只);
[0150]
8)pso模型+凝胶样品2(外用涂抹,频率2次/日,15mg/cm2,连续治疗7天)(n=6只)。实验步骤:
[0151]
造模:小鼠适应性饲养7天,制作寻常型银屑病(pso)小鼠模型。造模方式如下:清理小鼠背部皮肤面积约2cm*3cm,暴露皮肤处每天上午局部外用5%咪喹莫特乳膏50mg,连续使用3天,用于模型制备,后期继续给予造模药物。
[0152]
模型验证:此模型已具备成熟的sop标准,不再另设老鼠进行模型验证。
[0153]
治疗:(造模3天后),于第4天进行相应药物治疗,在给药治疗期间继续给予5%imq维持造模,根据给药天数情况维持给予造模药物。
[0154]
第1)组:空白对照组(不治疗)不做任何处理;
[0155]
第2)组:模型组涂抹5%咪喹莫特软膏62.5mg/只维持造模,不做任何治疗处理;
[0156]
第3)组:模型组涂抹5%咪喹莫特软膏62.5mg/只维持造模,另外每日涂抹空白凝胶,频率2次/日,连续治疗7天;
[0157]
第4)组:模型组涂抹5%咪喹莫特软膏62.5mg/只维持造模,另外每日涂抹阳性药物a(卡泊三醇软膏),频率2次/日,连续治疗7天;
[0158]
第5)组:模型组涂抹5%咪喹莫特软膏62.5mg/只维持造模,另外每日涂抹阳性药物b(本维莫德乳膏),频率2次/日,连续治疗7天;
[0159]
第6)组:模型组涂抹5%咪喹莫特软膏62.5mg/只维持造模,另外每日涂抹供试药物(本实施例凝胶1),频率2次/日,连续治疗7天;
[0160]
第7)组:模型组涂抹5%咪喹莫特软膏62.5mg/只维持造模,另外每日涂抹供试药物(市售芦可替尼磷酸盐乳膏),频率2次/日,连续治疗7天给药顺序:早上给予1次治疗药物、中午给予1次造模药物、晚上给予1次治疗药物。
[0161]
第8)组:模型组涂抹5%咪喹莫特软膏62.5mg/只维持造模,另外每日涂抹供试药物(本实施例凝胶2),频率2次/日,连续治疗7天
[0162]
注:为了防止动物之间有舔舐药物的现象。动物背部涂完凝胶后,单独放置在无垫料的独立笼内活动一段时间,让凝胶自然风干(预计1小时内),然后再放入饲养笼正常喂养。禁单独喂养,容易出现抑郁;禁用纱布包裹涂抹部位,会吸附走药剂。
[0163]
2.2实验结果:pso动物模型药物处理后的病理检测
[0164]
实验步骤:
[0165]
各组小鼠银屑病样皮损面积和疾病严重程度(pasi)评分:每天观察各组小鼠的体重和皮损变化情况(体重测定:从适应性饲养至给药结束,每只每天1次,共计17次;皮损评分:造模期间至给药期间每天进行评分,每只每天1次,共计10次),采用数码照相的方法每日记录,并依据pasi评分标准,给予小鼠皮损处红斑、鳞屑及浸润增厚程度0~4的积分,将三者评分相加得到总的皮损严重程度评分,对各组小鼠积分取平均值后绘制皮损积分趋势线,观察各组小鼠皮损的变化情况。
[0166]
2.3统计方法:
[0167]
结果以均数
±
标准误(mean
±
s.e.m.)表示,并采用spss 17.0统计软件进行分析,各组间差异比较用单因素方差分析(one-way anova)(不假定方差齐性dunnett's t3)。p《0.05表示差异具有统计学意义。
[0168]
3结果:
[0169]
本发明凝胶和阳性药物以及市售芦可替尼磷酸盐乳膏对咪喹莫特诱导小鼠银屑病模型皮损外观(pasi)情况的影响
[0170]
根据小鼠皮损处红斑、鳞屑及浸润增厚程度进行pasi评分,从给药7天评分趋势图观察,在给予药物4天后,药物与模型组比较,pasi评分下降趋势明显。在第4天,与模型组比较,苯维莫德,本发明凝胶组均有显著性下降,与空白凝胶组比较,也显著性下降(p《0.05或p《0.01)。在给药第5天,与模型组比较,本发明凝胶组的pasi评分显著下降,与空白凝胶比较,凝胶组显著下降。给药第6天和给药第7天,与模型组和空白凝胶组比较,本发明凝胶组评分显著性下降(p《0.01),具体详见图1和图2。
[0171]
4结论
[0172]
本研究采用咪喹莫特诱导银屑病小鼠模型评价专利方和阳性药物及市售对比方芦克替尼乳膏的保护作用,结果显示,本发明凝胶和阳性药物及市售芦克替尼乳膏均能够显著性降低小鼠pasi评分,本发明凝胶与阳性药物及市售芦克替尼乳膏相比,本发明凝胶效果更优,说明本发明凝胶和阳性药物及市售芦克替尼乳膏均有治疗银屑病作用,而在同浓度下本发明凝胶外用治疗银屑病疗效优于阳性药物及市售芦克替尼乳膏。
[0173]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含本发明的至少一个实施例或示例中。在本发明说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外在不互相矛盾的情况下,本领域技术人员可以将本说明书中描述的不同实施例或示例的特征进行结合或组合。
[0174]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1