一种趋化素样因子1衍生肽在制备镇痛制剂中的应用
1.本发明涉及医学技术领域,尤其涉及一种趋化素样因子1衍生肽在制备镇痛制剂中的应用。
背景技术:
2.随着急性和慢性疾病的病发几率的升高,伴随疾病而来的疼痛也严重危害人类身心健康,同时,疼痛还具有很大的致残几率。
3.慢性疼痛分为慢性原发性疼痛、慢性癌症相关性疼痛、慢性术后或创伤后疼痛、慢性继发性肌肉骨骼疼痛、慢性继发性内脏痛和慢性神经病理性疼痛,其中,慢性神经病理性疼痛的诊治手段缺失,现有药物缓解效果一般,且不良反应严重。神经病理性疼痛(neuropathic pain,np)是指由躯体感觉神经系统的损伤或者疾病所导致的疼痛。np的主要影响因素包含由外伤、感染、放化疗及代谢疾病等导致的外周或中枢神经系统损伤。np临床表现包括痛觉过敏、痛觉超敏和自发痛。np是一类十分普遍的慢性疼痛。np不仅会引起痛觉感受、传递系统等结构和功能的改变,同时也会导致其它神经系统功能紊乱,例如睡眠障碍、抑郁行为以及认知功能下降,np会使患者的身心健康及生活质量受到极大影响。
4.与神经病理性疼痛具有共同的致病机制的疼痛性病症还有纤维肌痛(fibromyalgia,fm)和带状疱疹痛。纤维肌痛是一种病因不明的复杂综合征,以慢性全身疼痛为特征。因此,纤维肌痛的诊断标准、病理生理机制和治疗方法仍存在争论。根据国际疾病分类,纤维肌痛被归类为慢性广泛性疼痛细分中的慢性原发性疼痛。就患病率而言,纤维肌痛是第三大最常见的肌肉骨骼疾病,影响世界人口的2
–
3%,男女比例为3:1。fda批准用于治疗纤维肌痛的一线药物有加巴喷丁类药物(加巴喷丁,gabapentin、普瑞巴林,pregabalin)、5羟色胺和去甲肾上腺素再摄取抑制剂(度洛西汀,duloxetine、米那普仑,minapulen)。针对躯体感觉神经系统的损伤或疾病而直接造成的疼痛,现有技术中涉及有用于抑制该类疼痛的化合物,例如专利公开号为cn1918156b的中国专利公开了一种新的化合物及其药学上可接受的盐与溶剂合物。该化合物的d与e为不同基团,两个基团分别为n和cr50。该化合物包含取代基a的基团实施例,例如杂芳基、芳基、杂环烷基、环烷基、芳基、炔基、烯基、氨基烷基、烷基或氨基。包含取代基b的基团实施例,例如芳基和杂芳基。该化合物能够介导肺病、多发性硬化、类风湿性关节炎、骨关节炎、中风、心脏再灌注损伤、疼痛(例如急性疼痛、急性与慢性炎性疼痛及神经病性疼痛)等疾病。
5.由于目前纤维肌痛药物依然存在令人不满意的疗效或副作用的问题,这些药物的使用仍然存在局限性。因此,对疗效确定且副作用小的新药仍有广泛的需求。
6.本发明提供一种趋化素样因子1衍生肽,其在抑制神经病理性疼痛、纤维肌痛及带状疱疹痛方向具有明显效果。
7.此外,一方面由于对本领域技术人员的理解存在差异;另一方面由于申请人做出本发明时研究了大量文献和专利,但篇幅所限并未详细罗列所有的细节与内容,然而这绝非本发明不具备这些现有技术的特征,相反本发明已经具备现有技术的所有特征,而且申
请人保留在背景技术中增加相关现有技术之权利。
技术实现要素:
8.针对现有技术之不足,本发明提供了一种趋化素样因子1衍生肽在制备镇痛制剂中的应用。趋化素样因子1衍生肽抑制神经病理性疼痛、纤维肌痛及带状疱疹痛。所述趋化素样因子1衍生肽(c19)包含:由seq id no:1所示的氨基酸序列构成的多肽;或于seq id no:1所示的氨基酸序列上缺失、插入或者置换一个或多个氨基酸且与seq id no:1所示的氨基酸序列具有相同的生物学功能的多肽,其中,seq id no:1为:phe asn pro ser gly pro tyr gln lys lys pro val his glu lys lys glu val leu。
9.seq id no:1所示的氨基酸序列还能够表示为:fnpsgpyqkkpvhekkevl。
10.根据一种优选实施方式,本发明提供的修饰的趋化素样因子1衍生肽可以是基本上纯化的或分离的。趋化素样因子1衍生肽可以在从细胞中表达时被分泌至可溶解的上清中。趋化素样因子1衍生肽能够进行氨基酸替代,环化。趋化素样因子1衍生肽能够包含修饰的氨基酸,如选自如下的修饰:糖基化,唾液酸化,法尼基化,羧化,羟化,与聚合物缀合(如peg化或者与葡聚糖缀合),与多聚化结构域、毒素、可检测标记或药物缀合,磷酸化。例如,修饰的趋化素样因子1衍生肽能够糖基化。多聚化结构域包括fc结构域。
11.根据一种优选实施方式,所述趋化素样因子1衍生肽能够治疗由神经病理性疼痛、纤维肌痛、带状疱疹神经痛。
12.根据一种优选实施方式,所述趋化素样因子1衍生肽能够治疗坐骨神经分支选择性损伤导致的神经病理性疼痛。
13.根据一种优选实施方式,所述趋化素样因子1衍生多肽为:与由seq id no:1构成的所述多肽具有至少90%同源性且与由seq id no:1构成的所述多肽的生物学功能相同的多肽。
14.根据一种优选实施方式,所述制剂的给药量为100~5000μg/kg 体重。所述给药量指单次给药量。
15.本发明提供一种抗神经病理性疼痛及纤维肌痛的趋化素样因子1衍生肽的制备方法。所述制备方法包含以下步骤:于反应柱中进行多肽的合成;于切割液中进行多肽的切割;收获并纯化所得到的多肽产物。
16.本发明提供一种药物组合物。药物组合物包含:治疗量的趋化素样因子1衍生肽或所述趋化素样因子1衍生肽的功能等效物、所述趋化素样因子1衍生肽或所述趋化素样因子1衍生肽的功能等效物的药学上可接受的载体,所述趋化素样因子1衍生肽包含:由seq id no:1所示的氨基酸序列构成的多肽;或于seq id no:1所示的氨基酸序列上缺失、插入或者置换一个或多个氨基酸且与seq id no:1所示的氨基酸序列具有相同的生物学功能的多肽,其中,seq id no:1为:phe asn pro ser gly pro tyr gln lys lys pro val his glu lys lys glu val leu;所述治疗量能够有效抑制神经病理性疼痛、纤维肌痛及带状疱疹痛。
17.本发明的治疗量的所述趋化素样因子1衍生肽基于疾病的严重程度及发展程度、患者的个人体质区别(体重、体表面积、代谢状况、年龄)变化。药物组合物能够干预或治疗由神经病理性疼痛、纤维肌痛及带状疱疹痛引发的神经炎症。
18.根据一种优选实施方式,药物组合物为适用于静脉内、肌内、皮内、皮下或鞘内给药的注射剂、口服制剂及口腔或经鼻吸入剂。
19.根据一种优选实施方式,药物组合物包含药学上可接受的赋形剂和其药学上可接受的盐。优选地,所述药物组合物药学上可接受的盐能够包括:钠、钾、钙、铵、有机氨基或镁盐或类似的盐。
20.根据一种优选实施方式,药物组合物包含注射药用的亲水性聚合物中的一种或多种。优选地,亲水性聚合物为聚乙二醇。
21.根据一种优选实施方式,所述药物组合物为适用于静脉内、肌内、皮内、皮下或鞘内给药的冻干粉针剂、水针剂及水凝胶等剂型。
22.本发明提供了所述趋化素样因子1衍生肽在镇痛中的用途。所述趋化素样因子1衍生肽能够对病因不明的原发性的纤维肌痛综合征产生抑制效果。所述趋化素样因子1衍生肽能够对继发性的纤维肌痛综合征(例如继发于类风湿关节,系统性红斑狼疮或者是系统性硬化症的疼痛感)产生抑制效果。
23.本发明提供了所述趋化素样因子1衍生肽或与所述趋化素样因子1衍生肽功能等效物用于制备药品的用途,所述药品用于抑制神经病理性疼痛或纤维肌痛。优选地,本发明的所述趋化素样因子1衍生肽、其类似物、其衍生物、其对应的cdna、其对应的基因、拮抗所述趋化素样因子1衍生肽的抗体能够被用作药品。
24.神经病理性疼痛是指神经系统的功能障碍所引起的疼痛,可以表现为躯体疼痛、内脏疼痛和神经痛。神经系统的原发疾病也会引起疼痛,而最重要的疼痛特征跟原发疾病造成的损伤有关系。疼痛往往会发生在损伤愈合以后。例如,带状疱疹后的神经痛表现为持续存在的撕裂样、灼烧样的疼痛,且伴随植物神经紊乱的症状(植物神经紊乱的患者表现为情绪烦躁不安)。 带状疱疹后的神经痛还表现为丘脑痛,其表现为剧烈的一侧肢体刀割样、电击样、灼烧样、蚂蚁爬行的感觉等。这种情况与丘脑病变和中枢的敏感化作用有关系。本发明中的趋化素样因子1衍生肽能够作用于神经系统,以缓解上述类型的疼痛。
25.本发明提供一种控释微球制剂,由所述趋化素样因子1衍生肽和兼容性载体组成,所述趋化素样因子1衍生肽包含:由seq id no:1所示的氨基酸序列构成的多肽;或于seq id no:1所示的氨基酸序列上缺失、插入或者置换一个或多个氨基酸且与seq id no:1所示的氨基酸序列具有相同的生物学功能的多肽,其中,seq id no:1为:phe asn pro ser gly pro tyr gln lys lys pro val his glu lys lys glu val leu。
26.优选地,控释微球制剂能够为采用plga材料。
27.plga微球相对于常规注射剂具有如下优点:1.释药周期长,避免频繁给药;2.使用安全;
3.药理作用增强;4.避免发生明显的不良反应;5.生物利用度显著提高。
28.根据一种优选实施方式,所述兼容性载体能够为淀粉、明胶、葡糖糖、清蛋白、聚乳酸、聚乳酸乙醇酸共聚物、聚邻酯、聚内酯或聚酐及其他高分子材料。
29.根据一种优选实施方式,所述控释微球制剂通过皮下注射或者深部肌肉注射进入人体内,经兼容性载体表面释放、药物扩散、聚合物溶蚀降解等方式,实现增加载药量、提升包封率、或者实现靶向精准用药等效果。
附图说明
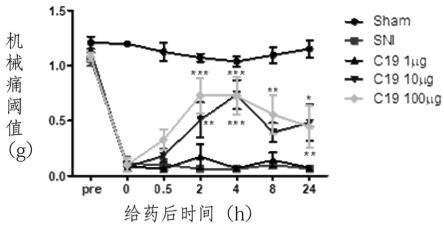
30.图1是c19对sni小鼠机械痛阈值的影响的折线图。
具体实施方式
31.下面结合附图进行详细说明。
[0032]“药学上可接受的载体”是指有助于向个体给药并被个体吸收的,包括在本发明的组合物中而不会对患者引起显著不良毒性作用的物质。药学上可接受的赋形剂的非限制性实例包括:水、nacl、生理盐水溶液、乳酸林格氏液、普通蔗糖、普通葡萄糖、粘合剂、填充剂、崩解剂、润滑剂、包衣、甜味剂、调味剂、盐溶液(如林格氏液)、醇、油、明胶、碳水化合物(如乳糖、直链淀粉或淀粉)、脂肪酸酯、羟甲基纤维素、聚乙烯吡咯烷酮和色素等。此类制剂可灭菌,并且若需要,可与不会与本发明的化合物发生有害反应的助剂(如润滑剂、防腐剂、稳定剂、润湿剂、乳化剂、用于影响渗透压的盐、缓冲剂、着色和/或芳香物质等)混合。
[0033]
实施例1本实施例通过小鼠实验验证c19于抑制神经病理性疼痛的用途。
[0034]
一、实验材料本实验使用坐骨神经分支选择性损伤(spared never injury,sni)致神经病理性疼痛小鼠模型证明c19在抑制机械痛敏中的作用。
[0035]
sni模型是一种与人类神经病理性疼痛有关的模型,该模型暴露了三叉处的坐骨神经,用5-0丝线紧紧结扎腓总神经和胫总神经,然后切断2mm远侧神经,保留腓肠神经。该模型模拟与周围神经损伤相关的人类神经病理性疼痛,具有成模快、维持时间长和手术过程操作简单等优点。
[0036]
本实验目的是评价c19对机械性损伤导致的异常疼痛的影响。对于神经病理性疼痛患者的触痛,机械痛敏数据具有代表性。本实验采用的sni模型小鼠c57购自北京维通利华实验动物科技有限公司,雄性,20-25g,spf级动物,动物合格证号:scxk(京)2016-0006。
[0037]
二、实验方法(1)小鼠饲养每只笼子放置5-6只小鼠。饲养环境保持恒温恒湿。日光灯每12h明暗交替。笼子内放置水和食物,使小鼠自由摄食饮水。
[0038]
(2)机械痛阈值的测定将小鼠置于铁丝网上,用开口向下的透明塑料筐分别将小鼠固定在框内,框的大
小要保证动物有足够的活动空间。测试前让动物在此环境中适应3-4次,每次适应15-20min;运用不同粗细的von-frey纤维丝透过铁丝网从垂直于脚掌的方向刺激小鼠左后侧足外侧跖面。每次检测要使纤维丝弯折到90度角后停留5s,观察小鼠在此时间内是否会出现缩足、舔足和抬足等疼痛反应;如果动物出现疼痛反应,则换用相邻更小折力的纤维丝;如果动物无缩足等疼痛反应,则换用相邻更大折力的纤维丝;按上述原则依次交替进行测定,待第一次出现阳、阴(或阴、阳)反应交替值之后,再连续测定4次;最后运用up-and-down方法计算出动物的机械痛阈值。
[0039]
(3)机械性异常疼痛的诱导测量大鼠左后爪机械刺激的基础痛阈值;进行sni手术,对照组仅暴露坐骨神经,不进行结扎和间断操作。
[0040]
(4)给药将c19溶解于生理盐水中;分别将混合c19的生理盐水和生理盐水以腹腔注射给药的方式给予小鼠;给药后不同时间点进行机械痛阈值的测定。
[0041]
(5)统计学graphpad prism version 5软件用于统计分析。数据均以mean
±
sem表示,采用单因素方差分析one-way anova,p《0.05为具有统计学意义。
[0042]
结果显示,c19给药后,sni模型小鼠的机械痛阈值的降低被显著抑制。实验结果说明,c19显著抑制神经病理性疼痛动物模型中的机械痛敏。图1示出小鼠术后第7天腹腔注射不同剂量c19后的机械痛阈值的结果。图1中的sham表示正常小鼠,sni为sni模型小鼠,c19 1μg表示喂食1μg 的c19的sni模型小鼠,c19 10μg表示喂食10μg 的c19的sni模型小鼠,c19 100μg表示喂食100μg 的c19的sni模型小鼠,其中,sham和sni为对照组。
[0043]
从图1中可看出,由于正常小鼠(sham)并未受到疼痛处理,正常小鼠的机械痛阈值平稳,且始终处于1.0~1.5之间。sni模型小鼠(sni)受到疼痛处理,sni模型小鼠的机械痛阈值平稳,且始终处于0~0.5之间。在腹腔注射1μg c19后24h,c19 1μg模型小鼠的机械痛阈值与sni模型小鼠大致相同,并始终处于0~0.5之间。在腹腔注射10μg c19后,c19 10μg模型小鼠的机械痛阈值在0.5h比未注射c19时明显提高,并在注射后4h内逐步提高,至给药后4h时达到最高点。随着给药后时间的增长,c19 10μg模型小鼠的机械痛阈值在4h的高峰处逐渐降低,但在给药后24h内,c19 10μg模型小鼠的机械痛阈值始终高于同时间的sni模型小鼠和c19 1μg模型小鼠。c19 100μg模型小鼠在给药后,机械痛阈值在2h时即达到高峰,且在高峰处保持至给药后4h。在给药后4h,c19 100μg模型小鼠的机械痛阈值相较c19 10μg模型小鼠缓慢下降。至给药后24h,c19 10μg模型小鼠和c19 100μg模型小鼠的机械痛阈值高于c19 1μg模型小鼠和sni模型小鼠,c19 10μg模型小鼠和c19 100μg模型小鼠的机械痛阈值大致相同。根据图1所示的结果,c19 100μg模型小鼠的给药量能够在短时间内(2h)迅速达到抑制疼痛的高峰,并使得抑制疼痛的最佳效果持续至少2h。c19 10μg模型小鼠的给药量同样能够在一个时间段(4h)对小鼠的疼痛达到与c19 100μg模型小鼠相同的抑制疼痛的最佳效果,但其持续时间不如c19 100μg模型小鼠的给药量所达到的持续时间。
[0044]
图片中的“*”表示该时间节点的实验数据的显著性,其中,*p 《 0.05,**p 《 0.01,***p 《 0.001。
[0045]
根据一种优选实施方式,以小鼠重量作为给药标准,100μg的c19给药量能够显著抑制20g的小鼠机械痛敏。小鼠重量平均值20g。
[0046]
抗神经病理性疼痛及纤维肌痛的趋化素样因子1衍生肽的制备方法,包含以下步骤:将趋化素样因子1衍生肽的编码dna重组至表达载体;将所述重组表达载体转化至宿主细胞内;在适合的诱导表达条件下,培养被转化的所述宿主细胞;收获并纯化所得到的表达产物。优选地,宿主细胞能够为大肠杆菌。重组的方法为同源重组法。诱导表达条件能够为在ms培养基上培育。
[0047]
神经病理性疼痛和纤维肌痛共同的致病机制涉及神经炎症的发生,因而针对神经炎症缓解来开发新药是重要的治疗策略。异常的神经炎症是神经病理性疼痛、纤维肌痛发病过程中的重要事件。趋化素样因子1(chemokine like factor 1,cklf1)具有类似cc类趋化因子的结构特征和趋化功能。研究显示,cklf1可通过参与炎症反应参与多种外周及神经系统疾病的发生与发展。因此,干预cklf1介导的炎性损伤、寻找新的相关治疗靶点将具有重要的临床意义。cklf1衍生肽c19可抑制多种趋化因子受体及配体相互作用,在自身免疫性疾病、过敏性疾病(过敏性哮喘、过敏性鼻炎)以及神经系统疾病中发挥疗效。专利号为cn100467487c的中国专利公开了一种具有多种功能的多肽(c19)。c19对ifn-γ刺激的u937细胞具有趋化作用。本实施例提供了c19肽在制备预防和/或治疗人免疫缺陷病毒感染、过敏性疾病、抑制排斥、脑部疾病或自身免疫疾病的药物中的应用。本实施例涉及的cklf1-c19在抗神经病理性疼痛、纤维肌痛及带状疱疹痛等方面具有疗效。
[0048]
神经炎症能够由以下病症诱发:中毒以及感染因素,除了重金属中毒以及药物中毒、农药中毒之外,还包括病毒感染、患有慢性感染性疾病等;肿瘤性疾病;神经性的创伤,包括重物撞击、刀伤、烧伤等等;血管炎性疾病,包括红斑狼疮、关节炎等等;代谢障碍疾病,较为常见的有糖尿病、尿毒症等;缺乏维生素b和维生素e,以及酒精中毒等因素所导致的身体代谢功能障碍;遗传性的疾病,如先天性神经炎疾病;局部神经受伤。
[0049]
本发明提供的c19或包含c19的药物组合物能够用于抑制因上述疾病引起疼痛。
[0050]
实施例2神经病理性疼痛指由躯体感觉系统的损害或疾病导致的疼痛,分为周围性和中枢性神经病理性疼痛。神经病理性疼痛发病的诱因众多,目前尚未完全探明。现有技术中,多采用能够缓解疼痛的镇痛药减轻神经病理性疼痛的症状。由于患者往往会选择出院回家,而神经病理性疼痛会于患者的日常生活中突发,患者在遭遇疼痛时仅能够自行注射或服用镇痛药物以缓解疼痛。
[0051]
目前留存于市面的镇痛药物大多具有成瘾性,患者需要受监控的使用,一方面,患者无可避免的在大量服用该类镇痛药物时会产生成瘾症状;另一方面,在疼痛已经发作时
服用药物会产生药效滞后性,进而影响患者的日常生活。
[0052]
本发明基于不具备成瘾性和耐药性且具有镇痛作用的c19而提供一种能够使患者用于日常生活的镇痛泵。
[0053]
由于c19不具有成瘾性且为人体更容易发挥镇痛作用的成分,因此,采用能够保持c19蛋白质特性的镇痛泵为患者给药能够使药物对患者发挥最大作用。
[0054]
需要注射镇痛药物以缓解疼痛的患者一般都具有持久性且疼痛度较高的痛感。现有技术中的镇痛药物注射一般是间歇性注射药物,以间歇性为患者提供无痛的时间段。然而,相较于间歇性感知疼痛,患者更需要持续性降低疼痛,即忍耐低痛感以维持正常的生活和情绪。由于仅需要考虑药品的毒副作用(体内累积量),而不需要考虑连续供药产生的成瘾性,镇痛泵能够为患者持续性提供低剂量药物,使得药物能够持久降低患者的尖锐疼痛,而避免患者间歇性疼痛的痛苦。本发明中的c19能够基于镇痛泵的智能化设置持续性降低非清醒状态下的患者的痛感,以使得患者能够维持长久健康的睡眠或休息。
[0055]
镇痛泵设置有手动模式和自动模式。当患者处于清醒状态时,镇痛泵切换为手动模式。当患者感知疼痛时,患者可摁压开关,镇痛泵即向患者提供单次安全量的c19。
[0056]
当患者处于睡眠或非清醒状态时,镇痛泵切换为停止或自动给药模式。当患者处于非清醒状态时,疼痛的发作会影响睡眠,导致患者形成精神上的恶性循环,即长期缺乏休息会加重病症,病症的加重也同时影响患者睡眠。由于疼痛而减少睡眠时间的患者会长期处于抑郁、暴躁等情绪,因此,严重的患者会产生轻生的念头。
[0057]
镇痛泵包含用于监测脑神经细胞的电生理活动的脑电图监测单元,中心处理器和给药单元。当患者需要进入睡眠状态时,其佩戴脑电图监测单元。中心处理器基于所述脑电图监测单元提供的脑部电信号进行特征提取。中心处理器响应于脑部电信号出现于疼痛相关的电信号,进而触发给药单元为患者提供至少单次安全量的c19。
[0058]
镇痛泵还包含肌电信号检测单元。该肌电信号检测单元基于神经病理性疼痛的发病区域,进而针对至少两个肌肉群进行监测。优选地,两个肌肉群至少包含针对神经末梢的肢端肌肉群和针对中枢神经的脸部肌肉群。中心处理器响应于患者出现疼痛症状,进而控制肌电信号检测单元开启。肌电信号检测单元至少针对两个肌肉群进行检测,并将检测信号发送给中心处理器以使中心处理器确认疼痛发生区域。
[0059]
根据疼痛发生的区域和疼痛的等级,给药单元至少提供三种给药模式。当疼痛处于五级以内且发生在神经末梢位置时,给药单元提供第一种给药模式。第一种给药模式为患者提供流速为第一流速且总给药量为第一剂量的c19。
[0060]
当疼痛处于五级以上且发生在神经末梢位置或当疼痛处于五级以下且发生在中枢神经位置时,给药单元提供第二种给药模式。第二种给药模式为患者提供流速为第二流速且总给药量为第二剂量的c19。
[0061]
当疼痛处于五级以上且发生在中枢神经位置时,给药单元提供第三种给药模式。第三种给药模式为患者提供流速为第三流速且总给药量为第三剂量的c19。
[0062]
根据一种优选实施方式,第一流速小于第二流速。第二流速小于第三流速。第一剂量小于第二剂量。第二剂量小于第三剂量。优选地,第一剂量为0.5μg/kg。第二剂量为0.75μg/kg。第三剂量为1μg/kg。第一流速为0.5ml/h。第二流速为1ml/h。第一流速为2ml/h。
[0063]
通过实验证明,本实施例提供的镇痛泵能够根据患者的神经性疼痛的病发等级和病发区域进行c19药剂的注射速度和注射药量的调整,使得药物在进入人体时能够降低人体由炎症反应引起的神经或组织损伤的程度。通过使用该镇痛泵对患者进行c19的施用能够使c19更加适用于因不同区域神经病变引起患者的疼痛的情况。本实施例提供了镇痛泵配合患者的不同生理情况向患者施用c19的施用方法,使用该施用方法的患者的使用反馈相较于基于主观判断进行c19施用的患者的使用反馈更好。
[0064]
根据一种优选实施方式,中心处理器基于离散小波变换的特征组合方法,利用小波分解系数提取小波能量占比、系数统计特征、样本熵和锁相值四种组合特征。为了识别疼痛水平,采用anova进行粗特征选择,选出在不同疼痛水平下具有显著性差异的特征,然后用支持向量机进行疼痛等级识别。世界卫生组织(wto)将疼痛程度划分为十级。
[0065]
中心处理器能够基于电信号的特征将于疼痛相关的特征分为十级,并能够在患者处于不同等级的情况下,调整给药单元为患者提供的c19的用量。
[0066]
例如,当患者希望进入睡眠时间时,患者佩戴脑电图监测单元。中心处理器以30s/次的周期接收患者的脑部电信号。当中心处理器判断患者进入二级疼痛时,中心处理器触发给药单元为患者提供两个单元的c19。当上述特征的脑部电信号在给药后1h未回复平稳时,给药单元补注一次c19。在剩余监测时间,当患者出现更高的疼痛等级时,中心处理器才能够提供c19。优选地,c19为冻干粉针剂,一个单元的c19能够为50μg。c19的用量为1μg/kg。
[0067]
本实施例提供的镇痛泵能够使患者处于睡眠阶段时被自动注射镇痛药物而无需在疼痛清醒后注射镇痛药物的情况。本实施例提供的镇痛药物和镇痛泵能够为患者提供安稳的睡眠时期,使得患者通过有效的睡眠和休息提高身体素质,以对抗神经病理性疼痛,并使得患者在清醒状态下保持一定的稳定情绪,进而保证患者维持正常的日常生活。
[0068]
本实施例提供的镇痛泵仅适用于本发明提供的镇痛肽,而非其他可能具备成瘾性或耐药性的药物。由于镇痛肽的特性,其能够被少量多次的使用于日常生活中,在不影响患者身体的情况下可以长时间使用。
[0069]
实施例3本实施例提供一种制备本发明提供的多肽的方法。本实施例提供一种自c端合成多肽的方法。
[0070]
一、实验材料保护氨基酸:fmoc-asp(otbu)-oh,fmoc-gln(trt)-oh,fmoc-gly-oh,fmoc-asn(trt)-oh,fmoc-pro-oh,fmoc-glu(otbu)-oh,fmoc-his(trt)-oh,fmoc-leu-oh,fmoc-phe-oh,fmoc-lys(boc)-oh,fmoc-val-oh,fmoc-ser(tbu)-oh,fmoc-tyr(tbu)-oh;起始树脂;缩合剂及有机碱;dmf;dcm;甲醇;六氢吡啶。
[0071]
二、实验步骤9种氨基酸混合溶液的配制:称取以上9种保护氨基酸各1mmol溶于63.4ml dmf溶液中,配制成0.3mmol/ml的氨基酸混合溶液,备用。
[0072]
kaiser test试剂的配制:
a液:80%的苯酚+20%的无水乙醇;b液:重蒸吡啶;c液:5克茚三酮+100ml无水乙醇。
[0073]
脱保护溶液的配制:20%的六氢吡啶和80%的dmf混合。
[0074]
多肽切割液的配制:87.5%tfa、5%苯甲硫醚、2.5%苯酚、2.5%edt和2.5%h2o混合。
[0075]
多肽的合成:a.树脂溶胀:称fmoc-leu-wang-resin树脂倒入反应柱中,加入dcm浸泡30min,抽干;b.脱保护:向反应柱中加入适量脱保护溶液,通氮气搅拌鼓动30min,抽干;c.称料:量取树脂3倍摩尔量fmoc-val-oh的氨基酸混合溶液或称取同样量的保护氨基酸,再称取2.85倍摩尔量的hbtu,备用;d.脱保护洗涤:向反应柱中加入适量dmf,氮气鼓动2min,抽干,重复操作6次;e投料:将已备好的氨基酸混合溶液或保护氨基酸和hbtu加入反应柱中,再加入树脂6倍摩尔量的nmm,氮气搅拌鼓动30min;f.反应后洗涤:将反应柱中的溶液抽干,加入适量dmf洗涤,氮气鼓动2min,抽干,重复操作3次;g.检测:取适量(10~20颗)树脂于小试管中,加入a,b,c液各两滴。放入干式加热器中加热3min(110℃),取出后若溶液显蓝色,树脂有杂色不透明,则反应没有完全,需要重新再反应一次;若溶液颜色微黄,树脂无色透明则为反应完全,可以连接下一个氨基酸,具体步骤重复以上b-f这五个步骤,直到连完最后一个氨基酸fmoc-phe-oh,并脱除其最后fmoc;h.合成完毕后的洗涤和干燥:在连完最后一个氨基酸并已脱保护洗涤之后,抽干,向反应柱中加入适量甲醇,氮气鼓动2min,抽干,再加入适量dcm,氮气鼓动2min,抽干重复操作3次,最后反应釜中加入适量甲醇,氮气鼓动2min,抽干,重复操作2次,将树脂装入合适器皿中置于真空干燥器内真空干燥12h待切割。
[0076]
多肽的切割a.切割:将干燥后的树脂装入合适的圆底烧瓶中,加入适量配好的切割液(1g/10ml),放置于恒温摇床中25℃恒温振荡2h;b.过滤:用50ml的砂芯漏斗过滤掉树脂颗粒,然后将滤液倒入100ml的离心管内,加入6~8倍体积量的无水乙醚,边加边搅拌,析出的白色固体为即所需多肽粗品;c.洗涤:将离心管密封后放入离心机中以4000r/min的转速离心3min,取出,将上层清液倒掉,再加入乙醚,用玻璃棒搅拌均匀,再次离心,如此重复操作洗涤5次;d.干燥:将以洗涤5次的后的多肽放入真空干燥器中真空干燥24h,最后的所得白色粉末即为所需多肽的粗品,称量,待纯化。
[0077]
需要注意的是,上述具体实施例是示例性的,本领域技术人员可以在本发明公开内容的启发下想出各种解决方案,而这些解决方案也都属于本发明的公开范围并落入本发明的保护范围之内。本领域技术人员应该明白,本发明说明书及其附图均为说明性而并非构成对权利要求的限制。本发明的保护范围由权利要求及其等同物限定。本发明说明书包含多项发明构思,诸如“优选地”、“根据一个优选实施方式”或“可选地”均表示相应段落公
开了一个独立的构思,申请人保留根据每项发明构思提出分案申请的权利。在全文中,“优选地”所引导的特征仅为一种可选方式,不应理解为必须设置,故此申请人保留随时放弃或删除相关优选特征之权利。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1