一种平衡妇科微生态菌群结构的生物抑菌凝胶的制作方法
1.本发明涉及生物化学技术领域,具体涉及一种平衡妇科微生态菌群结构的生物抑菌凝胶。
背景技术:
2.需氧菌性阴道炎(aerobic vaginitis,av)、细菌性阴道病(bacterial vaginosis,bv)和外阴阴道假丝酵母菌病(vulvovaginal candidiasis,vvc)是由于阴道菌群失衡或外源致病菌侵入引起的三类高发病率和高复发率的妇科下生殖道疾病。这三类妇科感染及其引发的混合感染不仅可导致患者外阴阴道瘙痒、红肿、疼痛、分泌物有异味等不适,还与盆腔炎症性疾病、不孕症以及流产、早产、胎膜早破、绒毛膜羊膜炎、新生儿感染、产褥感染等不良妊娠结局有关,同时也会增加性传播病原体(如hpv、hiv、阴道毛滴虫、沙眼衣原体等)的感染风险。在最新《需氧菌性阴道炎诊治专家共识(2021修订版)》和《细菌性阴道病诊治指南(2021修订版)》中明确指出微生态制剂如阴道局部乳杆菌制剂、中医药凝胶对于辅助患者恢复阴道微生态平衡、巩固疗效及预防复发具有一定的作用。
3.凝胶具有良好的生物黏附性和生物相容性,有效成分可黏附在阴道粘膜上,从凝胶缓慢地扩散到粘膜,停留时间较长,有利于彻底杀灭病原菌,并且凝胶剂以其独特的润滑性、清凉感及使用方便等优点而受到患者的青睐。然而,目前市场上的妇科凝胶或妇科凝胶相关专利所体现的凝胶功能主要是不同的抗菌成分配方组成及以此为基础发挥有效杀菌或粘附修复等作用,不能达到在杀死阴道中病原菌的同时维持乳杆菌的活性。同时由于阴道内部为一种含盐离子的弱酸性环境,低ph和较高的盐离子都会降低常规凝胶类制剂的交联,易使赋形剂水化,丧失其缓释能力。
技术实现要素:
4.本发明要解决的技术问题是针对现有凝胶产品对乳杆菌的保护性能不足的问题提供一种平衡妇科微生态菌群结构的凝胶,该凝胶能够抑制常见阴道有害菌的同时有效维持乳杆菌的活性。
5.基于上述问题,本发明提出的技术方案是一种平衡妇科微生态菌群结构的生物抑菌凝胶,包含的特征物质有包含溶菌酶和咖啡酸的生物抑菌液,还包括由赋形剂、金属盐及螯合剂组成的组合物,其中,赋形剂为avc,金属盐中阳离子为ca
2+
或mg
2+
,离子螯合剂为egta或edta。
6.赋形剂增强了凝胶的粘度和交联度,进而影响抗菌物质与病原菌的直接接触,由黄原胶、avc、卡波姆、sepimax zen等几个不同赋性剂配置生物抑菌液凝胶,由实验得出赋形剂avc对凝胶的抗菌作用影响最小,同时由于离子会破坏赋形剂的交联从而增强抗菌物质与病原菌的作用,而螯合剂不仅会调节盐离子对赋形剂的影响,本身也可能会影响病原菌的活性,同时螯合剂对离子的螯合作用也受到ph的影响,进而通过加入金属盐及螯合剂可调节赋形剂且影响微生物的活性,对由赋形剂配制的生物抑菌凝胶进行抗活性验证发
现,avc赋形的凝胶对于大肠埃希氏菌的杀菌率为100%,对于白假丝酵母的杀菌率均为0,对于金黄色葡萄球菌和卷曲乳杆菌的杀菌率最高在60%-70%之间且随着avc含量的升高而降低,详见表1和图1,加入盐离子后,随着盐离子添加量的升高,生物抑菌液凝胶对大肠埃希氏菌、白假丝酵母的抗菌活性呈现增强趋势,卷曲乳杆菌的抗菌性能都呈现增强趋势,但对于金黄色葡萄球菌和卷曲乳杆菌的抗菌活性呈现出先增强后降低的趋势,而金属盐添加量在0.3%及以上时,生物抑菌液凝胶表现出对卷曲乳杆菌更友好的作用,详见表2和图2。
7.表1赋形剂与抗菌液配置的生物抑菌凝胶中赋形剂添加量
[0008][0009]
表2赋形剂、金属盐与抗菌液配置的生物抑菌凝胶中氯化钙添加量
[0010][0011]
再次加入离子螯合剂后,生物抑菌液凝胶对大肠埃希氏菌、金黄色葡萄球菌、白假丝酵母的杀菌率可以提升到90%,而对卷曲乳杆菌的杀菌率为0,详见表3和图3。
[0012]
表3赋形剂、金属盐、螯合剂与抗菌液配置的生物抑菌凝胶中egta的添加量
[0013][0014]
离子及离子螯合剂的相互作用也会受到不同ph的影响,乳杆菌会降低环境ph的特征,影响离子螯合剂的螯合作用,本技术通过通过在具有广谱抑抗菌作用的生物抑菌液基础上,为得到妇科凝胶在保持对常见病原菌如大肠埃希氏菌、金黄色葡萄球菌、白假丝酵母具有很好的抗菌作用的同时,对乳杆菌的活性具有较小的影响,提出优化的赋形剂、离子及离子螯合剂的组成比例,其中,赋形剂的含量为0.5%,金属盐的含量为0.3%~0.4%,螯合剂的含量为0.2%~0.3%。
[0015]
其中,金属盐中阳离子选用正二价金属阳离子,可选用氯化钙和氯化镁,实验发现,虽然正一价金属阳离子对大肠埃希氏菌、金黄色葡萄球菌、白假丝酵母都呈现增强趋
势,如na
+
、k
+
,但是对卷曲乳杆菌的杀菌率也较大,杀菌率最高达99%。金属盐中阳离子选用正二价金属阳离子,生物抑菌液凝胶表现出对卷曲乳杆菌更友好;金属盐选用氯化钙时凝胶对卷曲乳杆菌的保护作用最强。
[0016]
其中,螯合剂选用egta时,生物抑菌液凝胶对卷曲乳杆菌的保护作用优于螯合剂选用edta。
[0017]
制备平衡妇科微生态菌群结构的凝胶的方法,包括以下步骤:1)将生物抑菌液加入烧杯中,混合均匀;2)在步骤1)的溶液中加入赋形剂,按照1000rpm/min的搅拌速度搅拌15分钟,充分混匀;3)在步骤2)得到的溶液中再加入金属盐溶液,1000rpm/min的搅拌速度搅拌5分钟,充分混匀;4)在步骤3)得到的溶液中再加入金属盐溶液,1000rpm/min的搅拌速度搅拌5分钟,充分混匀。
[0018]
本发明的优点和有益效果:通过对生物抑菌液凝胶中赋形剂、金属离子及螯合剂进行不同组分比例组成对常见病原菌及对阴道有益的乳杆菌生物活性的影响验证,得到可能受乳杆菌自身产酸的性能特点的影响的最佳组合。
[0019]
本发明通过在生物抑菌液中添加由赋形剂、金属盐和螯合剂形成的组合物,能够保持生物抑菌凝胶的缓释能力,制得的生物抑菌凝胶实现了对致病菌的抗菌的同时,有效维持了卷曲乳杆菌的活性。
附图说明
[0020]
图1是本发明中avc与生物抑菌液配置的生物抑菌液凝胶作用于不同菌落后的菌落数量的线形图。
[0021]
图2是本发明中avc、金属盐与生物抑菌液配置的生物抑菌液凝胶作用于不同菌落后的菌落数量的线形图。
[0022]
图3是本发明中avc、金属盐、螯合剂与生物抑菌液配置的生物抑菌液凝胶作用于不同菌落后的菌落数量的线形图。
[0023]
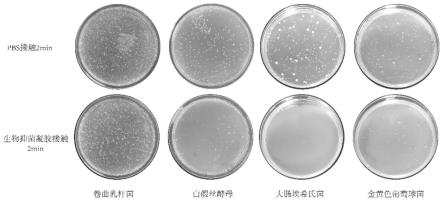
图4是本发明中实施例1得到的生物抑菌液凝胶接触菌落2min后菌落数量与pbs接触菌落2min后菌落数量的对比图。
具体实施方式
[0024]
下面结合具体实施例对本发明的具体实施方式作详细说明。
[0025]
实施例1
[0026]
1)按照表4的配方配置生物抑菌凝胶产品。
[0027]
表4凝胶产品配方表
[0028]
原料序号原料名称原料含量(%)1生物抑菌液702avc0.53氯化钙0.44egta0.25水29
[0029]
2)菌株培养、菌悬液制备:利用tsa琼脂培养基于37℃需氧条件培养大肠埃希氏
菌、金黄色葡萄球菌;利用沙氏琼脂培养基于37℃培养白假丝酵母;利用mrs琼脂培养基于37℃培养卷曲乳杆菌,挑取菌落于无菌1
×
pbs溶液中,调节菌悬液度为108cfu/ml。
[0030]
3)抑菌实验:实验操作主要参考《gb 15979-2002一次性使用卫生用品卫生标准》方法,具体如下:分别吸取100μl菌悬液置于5ml待测样本中,充分混匀,设置接触时间2min,待时间结束后,分别吸取0.5ml加入到4.5ml 1
×
pbs溶液进行梯度稀释,取合适的梯度分别吸取1ml置于两个平皿,用凉至40~45℃的培养基15ml作倾注,转动平皿,使其充分均匀,琼脂凝固后翻转平板于37℃培养18-48h,观察记录菌落生成情况,结果详见图4,可见,添加由赋形剂、金属盐及螯合剂组成的组合物于抗菌液中,对大肠埃希氏菌、金黄色葡萄球菌、白假丝酵母这几个致病菌的抗菌效果更优,同时,还有效维持了卷曲乳杆菌的活性。
[0031]
实施例2
[0032]
1)按照表5的配方配置生物抑菌凝胶产品。
[0033]
表5凝胶产品配方表
[0034]
原料序号原料名称原料含量(%)1生物抑菌液702avc0.53氯化镁0.44egta0.25水29
[0035]
2)菌株培养、菌悬液制备:利用tsa琼脂培养基于37℃需氧条件培养大肠埃希氏菌、金黄色葡萄球菌;利用沙氏琼脂培养基于37℃培养白假丝酵母;利用mrs琼脂培养基于37℃培养卷曲乳杆菌,挑取菌落于无菌1
×
pbs溶液中,调节菌悬液度为108cfu/ml。
[0036]
3)抑菌实验:实验操作主要参考《gb 15979-2002一次性使用卫生用品卫生标准》方法,具体如下:分别吸取100μl菌悬液置于5ml待测样本中,充分混匀,设置接触时间2min,待时间结束后,分别吸取0.5ml加入到4.5ml 1
×
pbs溶液进行梯度稀释,取合适的梯度分别吸取1ml置于两个平皿,用凉至40~45℃的培养基15ml作倾注,转动平皿,使其充分均匀,琼脂凝固后翻转平板于37℃培养18-48h,观察记录菌落生成情况。
[0037]
实施例3
[0038]
1)按照表6的配方配置生物抑菌凝胶产品。
[0039]
表6凝胶产品配方表
[0040]
原料序号原料名称原料含量(%)1生物抑菌液702avc0.53氯化镁0.34egta0.25水29
[0041]
2)菌株培养、菌悬液制备:利用tsa琼脂培养基于37℃需氧条件培养大肠埃希氏菌、金黄色葡萄球菌;利用沙氏琼脂培养基于37℃培养白假丝酵母;利用mrs琼脂培养基于37℃培养卷曲乳杆菌,挑取菌落于无菌1
×
pbs溶液中,调节菌悬液度为108cfu/ml。
[0042]
3)抑菌实验:实验操作主要参考《gb 15979-2002一次性使用卫生用品卫生标准》
方法,具体如下:分别吸取100μl菌悬液置于5ml待测样本中,充分混匀,设置接触时间2min,待时间结束后,分别吸取0.5ml加入到4.5ml 1
×
pbs溶液进行梯度稀释,取合适的梯度分别吸取1ml置于两个平皿,用凉至40~45℃的培养基15ml作倾注,转动平皿,使其充分均匀,琼脂凝固后翻转平板于37℃培养18-48h,观察记录菌落生成情况。
[0043]
实施例4
[0044]
1)按照表7的配方配置生物抑菌凝胶产品。
[0045]
表7凝胶产品配方表
[0046]
原料序号原料名称原料含量(%)1生物抑菌液702avc0.53氯化镁0.44edta0.25水29
[0047]
2)菌株培养、菌悬液制备:利用tsa琼脂培养基于37℃需氧条件培养大肠埃希氏菌、金黄色葡萄球菌;利用沙氏琼脂培养基于37℃培养白假丝酵母;利用mrs琼脂培养基于37℃培养卷曲乳杆菌,挑取菌落于无菌1
×
pbs溶液中,调节菌悬液度为108cfu/ml。
[0048]
3)抑菌实验:实验操作主要参考《gb 15979-2002一次性使用卫生用品卫生标准》方法,具体如下:分别吸取100μl菌悬液置于5ml待测样本中,充分混匀,设置接触时间2min,待时间结束后,分别吸取0.5ml加入到4.5ml 1
×
pbs溶液进行梯度稀释,取合适的梯度分别吸取1ml置于两个平皿,用凉至40~45℃的培养基15ml作倾注,转动平皿,使其充分均匀,琼脂凝固后翻转平板于37℃培养18-48h,观察记录菌落生成情况。
[0049]
实施例5
[0050]
1)按照表8的配方配置生物抑菌凝胶产品。
[0051]
表8凝胶产品配方表
[0052]
原料序号原料名称原料含量(%)1生物抑菌液702avc0.53氯化钙0.44edta0.35水29
[0053]
2)菌株培养、菌悬液制备:利用tsa琼脂培养基于37℃需氧条件培养大肠埃希氏菌、金黄色葡萄球菌;利用沙氏琼脂培养基于37℃培养白假丝酵母;利用mrs琼脂培养基于37℃培养卷曲乳杆菌,挑取菌落于无菌1
×
pbs溶液中,调节菌悬液度为108cfu/ml。
[0054]
3)抑菌实验:实验操作主要参考《gb 15979-2002一次性使用卫生用品卫生标准》方法,具体如下:分别吸取100μl菌悬液置于5ml待测样本中,充分混匀,设置接触时间2min,待时间结束后,分别吸取0.5ml加入到4.5ml 1
×
pbs溶液进行梯度稀释,取合适的梯度分别吸取1ml置于两个平皿,用凉至40~45℃的培养基15ml作倾注,转动平皿,使其充分均匀,琼脂凝固后翻转平板于37℃培养18-48h,观察记录菌落生成情况。
[0055]
以上对发明的几个实施例进行了详细说明,但所述内容仅为本发明的较佳实施
例,不能被认为用于限定本发明的实施范围。凡依本发明申请范围所作的均等变化与改进等,均应仍归属于本发明的专利涵盖范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1