1.本发明涉及生物医药技术领域,特别涉及素在增强青蒿素类药物抑制破骨细胞分化的应用。
背景技术:2.青蒿素是从黄花蒿中提取的有效抗疟疾成分,为一种内含过氧化基团的倍半萜内酯化合物,青蒿素及衍生物(包括青蒿琥酯、双氢青蒿素、蒿甲醚等)已有效地用于抗疟药物并具有良好的临床疗效和耐受性。青蒿素类药物可通过降低破骨细胞分化抑制骨质疏松。青蒿素类药物(包括青蒿素、青蒿琥酯、双氢青蒿素、蒿甲醚)可有效抑制雌激素缺失、细菌脂多糖、关节炎、肠道炎症疾病等因素诱导的骨质疏松的发生。
3.近年来,其在骨质疏松中的治疗作用引起学者关注。然而大多数研究主要集中在青蒿素类药物抑制骨丢失的现象观察以及破骨细胞分化的相关通路,对其抑制的根本机理还少有研究。青蒿素类药物的内过氧化物基团已被证实有重要的抗疟活性,可被含铁血红素以及亚铁激活,释放烷基化的碳自由基和活性氧来发挥抗疟作用。破骨细胞分化中,摄取大量铁元素,提示破骨细胞更容易受到青蒿素类药物的影响。本发明以破骨细胞铁含量高这一特性为切入点,结合青蒿素类药物对铁依赖的抗疟机制,发现破骨细胞内铁元素通过激活青蒿素类药物过氧基团释放大量活性氧自由基诱导破骨细胞铁死亡从而抑制骨吸收的机制,为骨质疏松等骨骼相关疾病的治疗提供新策略。
技术实现要素:4.本发明的目的在于至少解决现有技术中存在的技术问题之一,提供素在增强青蒿素类药物抑制破骨细胞分化的应用,以解决上述背景技术中提出的问题。
5.为实现上述目的,本发明提供如下技术方案:铁元素在增强青蒿素类药物抑制破骨细胞分化作用中药物的应用,铁元素用于增强青蒿素类药物抑制破骨细胞分化作用中药物。
6.优选的,其药物可为铁元素和青蒿素类药物的复合药物。
7.优选的,铁元素类药物为含有铁元素的试剂。
8.优选的,所述青蒿素类药物为具有青蒿素母核结构的倍半萜内酯类化合物或其衍生物。
9.与现有技术相比,本发明的有益效果是:
10.该素在增强青蒿素类药物抑制破骨细胞分化的应用,破骨细胞分化中,胞内铁元素含量升高,转铁蛋白可以促进青蒿琥酯对破骨细胞活力及分化的抑制作用,抑制转铁蛋白受体介导的铁摄取可降低青蒿琥酯的抑制效应,其机制在于青蒿琥酯可诱导破骨细胞发生铁死亡。
11.下面结合附图和实施例对本发明进一步地说明:
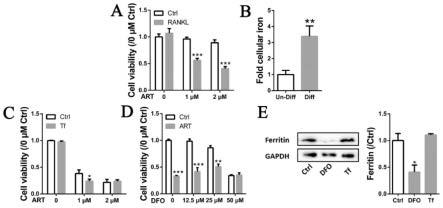
12.图1为青蒿琥酯与转铁蛋白(或去铁胺)对破骨细胞活力影响的示意图。
13.图2为青蒿琥酯与转铁蛋白复合处理对破骨细胞分化影响的示意图。
14.图3为青蒿琥酯对破骨细胞铁死亡影响的示意图。
具体实施方式
15.本部分将详细描述本发明的具体实施例,本发明之较佳实施例在附图中示出,附图的作用在于用图形补充说明书文字部分的描述,使人能够直观地、形象地理解本发明的每个技术特征和整体技术方案,但其不能理解为对本发明保护范围的限制。
16.本发明提供一种技术方案:素在增强青蒿素类药物抑制破骨细胞分化的应用,在图1中,rankl可诱导raw264.7细胞分化为成熟破骨细胞。a为青蒿琥酯对分化与未分化raw264.7细胞活力的影响;b为破骨细胞分化对细胞铁含量的影响;c为青蒿琥酯与转铁蛋白处理对分化raw264.7细胞活力的影响;d为青蒿琥酯与去铁胺处理对分化raw264.7细胞活力的影响;e为转铁蛋白和去铁胺对分化raw264.7细胞铁蛋白表达的影响。
17.在图2中,a为对破骨细胞形成的影响;b为对骨吸收能力的影响;c为对trap活性的影响;d、e、f分别为对分化标志基因car2、mmp9和v-atpase表达的影响。
18.在图3中,a为mda含量的影响;b为对4-hne含量的影响。
19.实施例1:青蒿琥酯对破骨细胞分化的抑制作用与细胞铁含量相关
20.采用小鼠raw264.7细胞为研究对象。raw264.7细胞在含有50ng/ml rankl(receptor activator for nuclear factor-κb ligand)条件下,可进行破骨细胞向分化,分化为成熟的多核细胞。采用cck8法检测细胞活力。青蒿琥酯(artesunate,art)在1μm和2μm条件下,对未诱导破骨细胞分化的raw264.7细胞没有影响,但是显著抑制正在分化的raw264.7细胞活力。破骨细胞分化种,铁摄取增强(图1a)。通过亚铁嗪比色法检测raw264.7细胞分化前后细胞总铁含量,发现raw264.7细胞分化后,细胞含量升高2倍(图1b)。为进一步探究细胞内铁元素含量对青蒿琥酯抑制效应的影响,分别采用转铁蛋白(transferrin,tf)和去铁胺(deferoxamine,dfo)进行处理。200μg/ml转铁蛋白可以加重青蒿琥酯在1μm时的抑制效应,50μm去铁胺则抑制青蒿琥酯的抑制效应(图1c和d)。50μm去铁胺可以有效抑制细胞内铁蛋白的表达,提示去铁胺起到有效的铁螯合作用,抑制细胞对铁元素的摄取(图1e)。
21.以上结果说明,青蒿素类药物对破骨细胞活力的抑制作用依赖于细胞铁含量,铁含量增加则增强青蒿素类药物的抑制效应。
22.实施例2:转铁蛋白可以加重青蒿琥酯对破骨细胞分化的抑制作用
23.成熟的破骨为多核且trap(tartrate-resistant acid phosphatase)染色阳性细胞,并且获得骨吸收的能力。由转铁蛋白受体介导的转铁蛋白吞为破骨细胞的主要铁摄取方式。为了进一步探究铁摄取对青蒿琥酯抑制破骨细胞分化的影响,采用转铁蛋白与青蒿琥酯复合处理破骨细胞向分化中raw264.7细胞。如图2a所示,酒红色细胞为trap染色阳性细胞。结果显示,200μg/ml转铁蛋白可以加重青蒿琥酯对破骨细胞形成的抑制作用(图2a)。将raw264.7细胞接种到骨基质类似物表面,通过查看骨基质类似物表面陷窝的面积,判断骨吸收能力的大小。结果显示,200μg/ml转铁蛋白可以加重青蒿琥酯对破骨细胞骨吸收能力的抑制作用(图2b)。与青蒿琥酯组相比,转铁蛋白与青蒿琥酯复合处理加重了对trap活性的抑制效应(图2c)。破骨细胞在进行骨吸收时,需要分泌多种酶类降解骨基质,如car2
(carbonic anhydrase ii)、mmp9(matrix metallopeptidase 9)、v-atpase(vacuolar-type h(+)-atpase)等。实验结果显示,转铁蛋白单独处理可促进这些酶蛋白的表达,但是会加重青蒿琥酯对这些降解酶表达的抑制作用(图2d-f)。以上结果说明,转铁蛋白可加重青蒿素类药物对破骨细胞分化的抑制作用。
24.实施例3:青蒿琥酯可诱导破骨细胞铁死亡
25.铁死亡是一种铁依赖性的以脂质过氧化为特征的死亡方式。为了检测青蒿琥酯是否会诱导破骨细胞铁死亡的发生,检测脂质过氧化相关产物丙二醛(malondialdehyde,mda)和4-羟基壬烯醛(4-hydroxynonenal,4-hne)的含量。实验结果显示,青蒿琥酯可以浓度梯度依赖性地增加mda和4-hne的水平(图3a和b)。
26.以上结果说明,青蒿素类药物对破骨细胞的毒性作用与铁死亡相关。
27.综上,破骨细胞摄取额外的铁元素可以增强青蒿素类药物对破骨细胞的毒性,包括对细胞活力和分化功能的抑制作用。其机制与诱导细胞铁死亡发生相关。
28.以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
