一种食管癌个性化治疗决策方法、系统及含其的存储介质与流程
本发明属于人类疾病的个性化治疗领域,涉及一种基于蛋白组panel分型、通过机器学习算法构建的用于食管癌个性化治疗决策的预测模型和个性化治疗决策方法、系统及含其的计算机可读存储介质和电子设备。
背景技术:
1、食管癌(esophageal cancer,ec)是一种常见得致命癌症,预后差和具有较高得致死率,是全球第八大常见的癌症,也是全球第六大癌症相关死亡原因。食管癌早期检出率低、晚期治愈率低,5年生存率低于19%。食管癌病人的首选治疗方法是外科手术。对于一些没有手术治疗机会的患者,只能靠药物提高生活质量甚至维持生存。尽管近年来一线治疗药物的迭代更新、二线治疗药物以及靶向药物帕博利珠单抗(pembrolizumab,keytruda)免疫抑制剂的深入研发取得了重大进展,但是药物耐受问题仍未得到解决,食管癌治疗的总体预后仍处于较差水平。在临床上,肿瘤的治疗效果存在较大的个体差异,但是药物个性化的选择依据过少,临床急需指导个体化精准医疗的标志物,从而缓解药物耐受问题。
2、基因组学、转录组学技术的发展,推进了肿瘤发生相关基因及重要驱动基因突变模式的研究和规模化发现,推动了精准医学的产生和发展。但是,仅仅从基因层面探讨肿瘤的精准诊疗尚不能满足临床需求。蛋白质组学研究从蛋白质层面阐释特定生物现象发展的原因,揭示发展规律,以蛋白质组为核心的多维度组学对生命科学研究及精准医学诊疗的发展具有重大意义。
3、据报道,目前的研究多是通过整合基因组数据集鉴定肿瘤的特征基因及信号网络,针对不同人类群体已提出基于基因组的分子分类系统。2017年1月,癌症基因组图谱(tcga)项目绘制了164例食管癌患者的基因组图谱,并将食管癌分为三个亚型:①escc1亚型;②escc2亚型;③escc3亚型;同年5月,中国华大基因等联合发表了关于食管癌分型的文章,基于转录组数据,将360例食管鳞状细胞癌分为四个亚型:①与癌细胞分化相关(well-differentiated)的esc1亚型;②转移相关(metastasisi-associated)escc2亚型;③适中(moderated)escc3亚型;④染色体不稳定阳性(cin+)escc4亚型,不同的分子亚型具有不同的分子特征和与不同的临床结果关联;在过去的几年中,通过大规模的癌症基因组测序进行了许多类似的研究,可以看到食管癌被划分为分子遗传学上不同的异质性亚组,而不是单一类型的癌症。因此,为了实现食管癌的个体化治疗,有必要根据分子遗传学和病理学特征来识别亚类,发现并应用相应的靶基因。此外,在食管癌研究中,已经报道了可以根据食管癌的亚型对食管癌的预后进行分类的结果。目前已涌现的多项研究性专利均是基于基因组和转录组的基因表达水平实现对食管癌的早期筛查,如食管癌预后标志物及其应用(专利号cn106701992a),食管癌的诊治标志物(专利号cn105886627b)。然而在临床中,针对食管癌患者的一线治疗方案,如铂类加紫杉醇方案、化疗联合放疗(铂类加紫杉醇联合放疗)方案;然而并不是所有患者都能够从这些治疗方案中获益,癌症的治疗耐受仍然是一个亟需解决的问题;目前仍然缺乏筛选能在不同治疗方案中获益的方法,实现癌症患者的个性化治疗。
4、作为“生命的执行者”,蛋白质决定表型,并可能弥补研究与临床实践之间的鸿沟。目前在蛋白层面上已实现基于弥漫型胃癌的分子分型、用于分型的蛋白标志物及其筛选方法和应用(专利号cn 108445097 a),提示在基于蛋白的分子与患者的生存及治疗反应具有强关联性。然而,目前仍未实现食管癌的个性化治疗方案,甄别出能够从不同治疗方案中获益的食管癌患者。
技术实现思路
1、为解决现有技术中缺乏食管癌治疗的预测模型,从而有效提供计算机辅助的个性化治疗决策方案的缺陷,本发明提供了一种食管癌个性化治疗决策方法、系统及含其的存储介质。
2、本发明利用蛋白质组学技术联合机器学习算法,根据已治疗患者的蛋白表达数据构建针对食管癌不同治疗反应的预测模型,该预测模型覆盖了目前消化道的化疗及放化疗方案,有助于临床医生根据未治疗患者的蛋白表达数据与预测模型的吻合程度制定个性化药物治疗方案,使患者获得最大收益,从而为临床用药抉择奠定基础。
3、为解决上述技术问题,本发明的技术方案之一为:提供一种食管癌治疗预测模型的构建方法,其包括以下步骤:
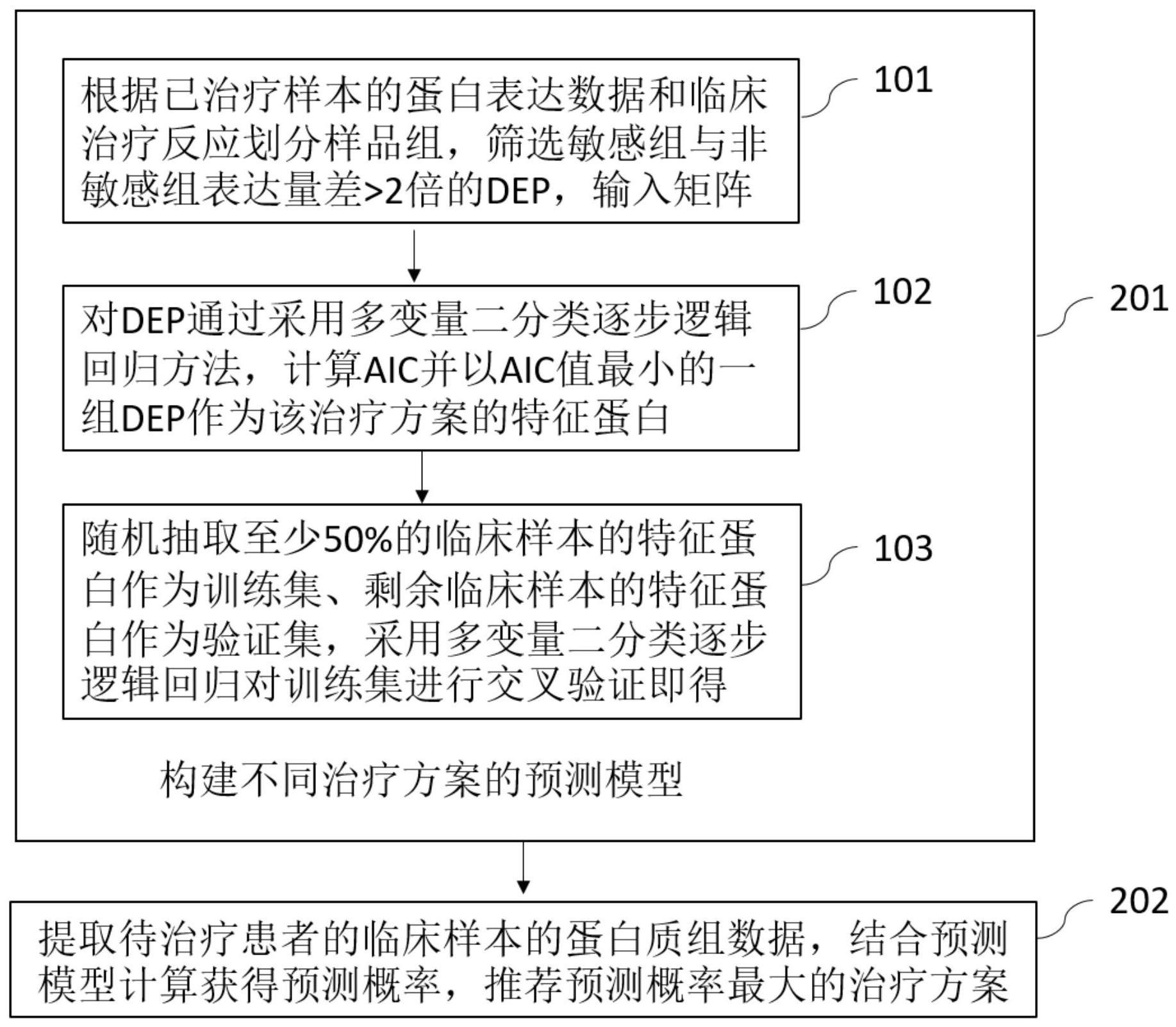
4、(1)划分样品组:获得用不同治疗方案治疗的患者治疗前样本的蛋白表达数据和临床治疗反应信息,将所述样本划分为敏感组和非敏感组;筛选所述敏感组相对非敏感组的蛋白表达量差异达到2倍以上且p<0.05的差异表达蛋白dep,并输入矩阵;
5、(2)特征蛋白选取:对步骤(1)所述的dep通过采用多变量二分类逐步逻辑回归方法,计算dep的赤池信息量准则(aic),得到aic值最小的一组dep,作为该治疗方案的特征蛋白;
6、(3)构建预测模型:在各治疗方案中随机抽取至少50%的临床样本,以其对应的特征蛋白作为训练集、剩余临床样本对应的特征蛋白作为测试集,采用多变量二分类逐步逻辑回归对训练集进行交叉验证,所述交叉验证为10倍交叉验证;即得该治疗方案的预测模型。
7、在一些优选的实施例中:
8、步骤(2)中,所述特征蛋白的选取使用r studio软件;采用proc数据包,并设置glm函数中family=binomial,step函数中direction='backward';和/或,
9、步骤(3)中,所述至少50%的样本为至少60%、至少70%或选至少80%的样本,所述10倍交叉验证重复10次;和/或,
10、所述临床治疗反应信息包括采用普通x射线、ct扫描和/或mri扫描评价的治疗效果;和/或,
11、所述患者基于recist标准进行分组,其中,所述敏感组包括完全缓解和部分缓解,所述非敏感组包括疾病稳定和疾病进展。
12、在一些更优选的实施例中:所述治疗方案选自化疗及放化疗方案;较佳地,
13、步骤(1)中,根据分别采用化疗及放化疗方案的已治疗的癌症患者治疗前样本的蛋白表达数据和临床治疗反应信息,将所述样本划分为化疗敏感组ctsg、化疗非敏感组ctnsg、放化疗敏感组crtsg、放化疗非敏感组crtnsg,筛选所述敏感组相对非敏感组的蛋白表达量差异达到2倍以上且p<0.05的差异表达蛋白dep,并输入矩阵;
14、步骤(2)中,计算不同治疗方案的dep的aic值,选择aic值最小的一组dep作为某种治疗方案的特征蛋白,应用多变量二分类逐步逻辑回归方法分别简历化疗及放化疗方案的预测模型;
15、步骤(3)中,在化疗及放化疗方案的队列中各随机抽取80%的临床样本作为训练集、剩余临床样本作为验证集,进行10倍交叉验证,并重复10次,即得化疗及放化疗方案的预测模型。
16、在一些进一步更优选的实施例中:所述蛋白表达数据的获得包括以下步骤:
17、(a)样本制备:所述样本制成福尔马林固定石蜡包埋组织切片,和/或,所述样品的食管癌细胞占总细胞数的80%以上;和/或,所述样本使用的裂解缓冲液为0.1m tris-hcl,ph 8.0,并添加0.1m dtt和1mm pmsf;和/或,所述样本的蛋白用含胰蛋白酶的50mmnh4hco3,于37℃温育18-20小时进行酶解;和/或,离心收集获得经酶解的肽段;和/或,
18、(b)质谱检测:所述肽段用q-exactive hf-x混合四极轨道阱质谱仪和高效液相色谱系统进行检测,并得到该肽段对应的质谱数据;和/或,使用xcalibur软件控制进行数据采集;和/或,
19、(c)数据处理:采集的数据使用firmiana数据库及maxquant软件处理;和/或,第一个搜索质量耐受性为20ppm,主要搜索肽耐受性为0.5da;和/或,计算方法为无标记的ibaq,并用fot来表示样本中蛋白质的标准化丰度;和/或,选择具有至少一条专属肽段,且fdr小于1%的蛋白质。
20、为解决上述技术问题,本发明的技术方案之二为:提供一种个性化食管癌治疗的决策方法,其包括以下步骤:
21、(a)获得如本发明技术方案之一所述食管癌治疗预测模型的构建方法得到的不同治疗方案的预测模型;
22、(b)提取待治疗患者的临床样本的蛋白表达数据,结合不同治疗方案的预测模型,使用r studio软件的predict函数,参数设置type="prob"来计算对各治疗方案敏感的预测概率,向患者推荐预测概率最大的治疗方案。
23、为解决上述技术问题,本发明的技术方案之三为:提供一种食管癌治疗预测模型的构建装置,其包括:
24、样品分组模块:所述样品分组模块用于获得用不同治疗方案治疗的患者治疗前样本的蛋白表达数据和临床治疗反应信息,将所述样本划分为敏感组和非敏感组;筛选所述敏感组相对非敏感组表达量达到2倍以上且p<0.05的蛋白即s蛋白、非敏感组相对敏感组表达量达到2倍以上且p<0.05的蛋白即ns蛋白,并输入矩阵;和,
25、特征蛋白选取模块:所述特征蛋白选取模块对步骤(1)所述的dep通过采用多变量二分类逐步逻辑回归方法,计算dep的赤池信息量准则(aic),得到aic值最小的一组dep,作为该治疗方案的特征蛋白;和,
26、预测模型构建模块:所述预测模型构建模块在各治疗方案中随机抽取至少50%的临床样本,以其对应的特征蛋白作为训练集、剩余临床样本对应的特征蛋白作为测试集,采用多变量二分类逐步逻辑回归对训练集进行交叉验证,所述交叉验证为10倍交叉验证,重复10次;即得该治疗方案的预测模型。
27、在一些更优选的实施例中,
28、所述预测模型建立模块中,所述auc值的计算使用r studio软件;采用proc数据包,并设置glm函数中family=binomial,step函数中direction='backward';和/或,
29、所述最佳预测模型训练模块中,所述至少50%的样本为至少60%、至少70%或至少80%的样本,所述10倍交叉验证重复10次。
30、临床治疗反应信息包括采用普通x射线、ct扫描和/或mri扫描评价的治疗效果;和/或,
31、所述患者基于recist标准进行分组,其中,所述敏感组包括完全缓解和部分缓解,所述非敏感组包括疾病稳定和疾病进展。
32、在一些优选的实施例中,所述治疗方案选自化疗及放化疗方案;较佳地,
33、所述样品分组模块中,根据分别采用化疗及放化疗方案的已治疗的癌症患者治疗前样本的蛋白表达数据和临床治疗反应信息,将所述样本划分为化疗敏感组、化疗非敏感组、放化疗敏感组、放化疗非敏感组,筛选各组的特征蛋白分别获得各组的差异倍数达到2倍以上且p<0.05即dep,并输入矩阵;
34、所述特征蛋白选取模块中,对所述样品分组模块获得的dep采用多变量二分类逐步逻辑回归方法,计算不同治疗方案的dep的aic值,选择aic值最小的一组dep作为某种治疗方案的特征蛋白,获得化疗和放化疗方案的特征蛋白;
35、所述预测模型建立模块中,在化疗和放化疗方案中各随机抽取80%的临床样本,以其对应的特征蛋白作为训练集、剩余临床样本对应的特征蛋白作为测试集,应用多变量二分类逐步逻辑回归对训练集进行10倍交叉验证,并重复10次,即得化疗及放化疗方案的预测模型。
36、在一些进一步更优选的实施例中,所述构建装置还包括:
37、样本制备模块:所述样本制备模块将样本制成福尔马林固定石蜡包埋组织切片,所述样品的食管癌细胞占总细胞数的80%以上;裂解样本使用的裂解缓冲液为0.1m tris-hcl、ph 8.0,添加0.1m dtt和1mm pmsf;使用含胰蛋白酶的50mm nh4hco3对所述样本的蛋白进行酶解,于37℃温育18-20小时,离心收集获得经酶解的肽段;和/或,
38、质谱检测模块:所述质谱检测模块所述肽段用q-exactive hf-x混合四极轨道阱质谱仪和高效液相色谱系统进行检测,并得到该肽段对应的质谱数据;使用xcalibur软件控制进行数据采集;和/或,
39、数据处理模块:所述数据处理模块采集的数据使用firmiana数据库及maxquant软件处理;第一个搜索质量耐受性为20ppm,主要搜索肽耐受性为0.5da;计算方法为无标记的ibaq,并用fot来表示样本中蛋白质的标准化丰度;选择具有至少一条专属肽段,且fdr小于1%的蛋白质。
40、为解决上述技术问题,本发明的技术方案之四为:提供一种个性化食管癌治疗决策系统,其包括:
41、如本发明的技术方案三所述的食管癌治疗预测模型的构建装置;以及
42、方案决策模块:所述方案决策模块提取待治疗患者的临床样本的蛋白表达数据(例如通过质谱检测获得),结合不同治疗方案的预测模型,使用rstudio软件的predict函数,参数设置type="prob"来计算对各治疗方案敏感的预测概率,向患者推荐预测概率最大的治疗方案。
43、为解决上述技术问题,本发明的技术方案之五为:提供了一种电子设备,其包括存储器和处理器;所述存储器包括存储在其中的可在处理器上运行的计算机程序;其中,
44、所述处理器执行所述计算机程序时实现本发明的技术方案之一所述的食管癌治疗预测模型的构建方法、本发明的技术方案之二所述的个性化食管癌治疗的决策方法,或本发明的技术方案之三所述的食管癌治疗预测模型的构建方法。
45、为解决上述技术问题,本发明的技术方案之六为:提供了一种计算机可读存储介质,其上存储有计算机程序,其中,所述计算机程序被处理器执行时可实现如本发明的技术方案之一所述的食管癌治疗预测模型的构建方法的步骤、本发明的技术方案之二所述的个性化食管癌治疗的决策方法的步骤,或本发明的技术方案之三所述的食管癌治疗预测模型的构建方法的步骤。
46、在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
47、本发明所用试剂、原料、设备和药物均市售可得。
48、本发明的积极进步效果在于:
49、本发明提供了疾病的个性化治疗决策方法及执行该决策方法的决策系统,所述决策系统包括:食管癌治疗预测模型的构建装置、模型比较模块和方案决策模块,通过结合机器算法构建治疗反应的预测模型,可向待治疗患者推荐适合其的个性化治疗方案,并在一定程度上实现个性化治疗。
- 还没有人留言评论。精彩留言会获得点赞!