用补体旁路途径抑制剂治疗镰状细胞病或β地中海贫血的方法与流程
背景技术:
1、镰状细胞病(scd)是全球最常见的单基因疾病。在一些形式下,这种疾病是由β珠蛋白基因中的突变引起的,例如,β珠蛋白基因中的导致位置6处谷氨酸被缬氨酸取代的单核苷酸突变,该基因也是导致β地中海贫血(bt)的原因。尽管广泛认识到该疾病的根本原因,但控制scd症状的可用治疗选择很少。scd的两个主要表现,贫血和血管闭塞危象(voc),影响scd患者的死亡率、发病率和生活质量。尽管scd患者有两种经批准的治疗选择,羟基脲和l-谷氨酰胺,但它们通常被认为是减弱疾病症状的次优方案。因此,在本领域中对新治疗存在需要。
技术实现思路
1、本文描述了特异性或基本上特异性结合补体途径组分(例如,补体c5)并且选择性阻断旁路补体途径激活的组合物。通过抑制补体c5的功能活性,本文所述的补体c5抑制剂(例如,抗c5单价抗体或其片段)抑制旁路补体途径诱导的攻膜复合物的组装。此外,单个补体c5分子与补体c5抑制剂的选择性结合可以减少由聚集引起的不期望的免疫复合物。因此,补体c5单体或多聚体的选择性靶向可转而改善镰状细胞病(scd)、β地中海贫血(bt)或镰状细胞bt患者的临床益处。
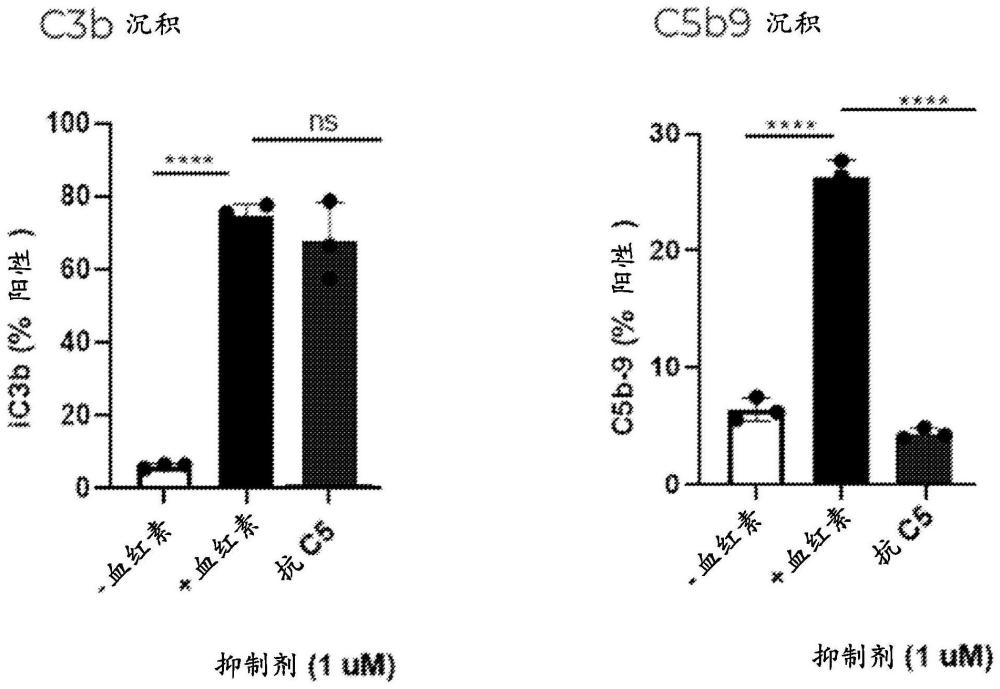
2、本披露部分地基于以下发现,旁路补体途径的抑制剂,例如像补体c5抑制剂,可以减弱甚至停止scd的症状。通过使用已建立的scd实验室模型(经受缺氧条件的townes ss小鼠),本披露首次证明,用c5抑制剂(如抗c5抗体)治疗动物抑制了scd的病理生理学,关于:(1)抑制红细胞(rbc)上的补体沉积;(2)减弱血管内溶血;和/或降低血管闭塞危象(voc)的严重程度。更特别地,使用已建立的细胞模型,本披露显示,通过用抗c5单克隆抗体(mab)预处理逆转了在缺氧条件下scd小鼠rbc中c5b9和c3的补体片段沉积增强。此外,通过用抗c5mab预处理有效减弱了在缺氧条件下血管内溶血水平的增加(通过血浆乳酸脱氢酶(ldh)活性、游离血红素和游离血红蛋白水平和/或总胆红素水平测定)。第三,通过用抗c5 mab预处理有效降低了在缺氧条件下scd小鼠的肺和肝等重要器官的血管中血管闭塞的增加,而在用缓冲液预处理的假(对照)scd小鼠中未观察到这种影响。这些数据表明,抗补体抗体(如抗c5抗体)在细胞和器官水平上均保护scd动物免受损伤。本披露提供的科学证据支持补体抑制剂(尤其是c5拮抗剂,如抗c5抗体)在治疗scd和相关病症(诸如bt和镰刀bt)中的用途。此外,比较评估指示了抗c5抗体在逆转scd小鼠模型中血管闭塞方面与使用羟基脲(hu)的标准治疗方法相比的惊人效果。这些数据表明,抗c5抗体预处理在降低肾、肝、脾和肺处缺氧诱导的血管闭塞方面比hu更有效。因为肺在scd的病理生理学的上下文中是主要的靶组织,本文的数据指向在体内设定中抗c5抗体对scd症状的显著保护效果。
3、在一个方面,本披露的特征是一种治疗受试者中scd的方法,该方法包括向该受试者施用有效量的包括补体c5抑制剂的组合物。
4、在另一方面,本披露的特征是一种治疗受试者中bt的方法,该方法包括向该受试者施用有效量的包括补体c5抑制剂的组合物。
5、在另一方面,本披露的特征是一种治疗受试者中镰状细胞bt的方法,该方法包括向该受试者施用有效量的包括补体c5抑制剂的组合物。
6、在前述方面中任一项的一些实施例中,该补体c5抑制剂选自由抗体或其抗原结合片段、肽、小分子、核酸分子和适配体组成的组。在一些实施例中,该补体c5抑制剂是抗c5抗体或其抗原结合片段。
7、在前述方面中任一项的一些实施例中,该抗c5抗体或其抗原结合片段包括:cdr-h1(seq id no:5)、cdr-h2(seq id no:6)和cdr-h3(seq id no:7);或cdr-h1(seq id no:8)、cdr-h2(seq id no:9)、cdr-h3(seq id no:10)、cdr-l1(seq id no:11)、cdr-l2(seqid no:12)和cdr-l3(seq id no:13);或cdr-h1(seq id no:14)、cdr-h2(seq id no:15)、cdr-h3(seq id no:16)、cdr-l1(seq id no:17)、cdr-l2(seq id no:18)和cdr-l3(seq idno:19);或cdr-h1(seq id no:20)、cdr-h2(seq id no:21)、cdr-h3(seq id no:22)、cdr-l1(seq id no:23)、cdr-l2(seq id no:24)和cdr-l3(seq id no:25);或cdr-h1(seq idno:26)、cdr-h2(seq id no:27)、cdr-h3(seq id no:28)、cdr-l1(seq id no:29)、cdr-l2(seq id no:30)和cdr-l3(seq id no:31)。
8、在前述方面中任一项的一些实施例中,该抗c5抗体或其抗原结合片段包括:seqid no:2的氨基酸序列;seq id no:46的氨基酸序列;seq id no:35的hcvr和seq id no:36的lcvr;seq id no:37的hcvr和seq id no:36的lcvr;seq id no:38的hcvr和seq id no:39的lcvr;seq id no:40的hcvr和seq id no:41的lcvr;seq id no:42的hcvr和seq idno:43的lcvr;或seq id no:44的hcvr和seq id no:45的lcvr。
9、在前述方面中任一项的一些实施例中,该c5抑制剂包括:依库丽单抗(eculizumab)或其生物仿制药、诺马科潘(nomacopan)、齐芦克布仑(zilucoplan)、塞迪司兰(cemdisiran)、zimura、依库珠单抗(ravulizumab)、sobi005、特度鲁单抗(tesidolumab)、帕泽利单抗(pozelimab)、或可伐利单抗(crovalimab)。
10、在前述方面中任一项的一些实施例中,该适配体是arc-1905(avacincaptadpegol;cas#1491144-00-3和fda药品#k86enl12i5)。
11、在前述方面中任一项的一些实施例中,该组合物包括补体c5抑制剂和药学上可接受的载剂。
12、在前述方面中任一项的一些实施例中,该补体c5抑制剂是抗c5抗体或其抗原结合片段(例如,包括可变重链互补决定区(vhcdr1-3)和可变轻链互补决定区(vlcdr1-3)的片段)。
13、在任何前述方面的一些实施例中,该方法降低了该受试者的血管内溶血。
14、在前述方面的一些实施例中,scd包括溶血性贫血或急性voc事件。例如,在一些实施例中,voc事件是肺voc和/或肝voc。在一些实施例中,该肺voc表现为急性胸腔综合征(acs)和/或慢性肺病;和/或该肝voc表现为严重腹痛和/或肝功能障碍。
15、在前述方面的一些实施例中,该受试者呈现腹部鼓胀、右上腹痛或急性疼痛性肝肿大。
16、在任何前述方面的一些实施例中,该受试者是被诊断为患有scd、bt或镰状细胞bt的人患者。
17、在任何前述方面的一些实施例中,该人患者未满18岁。
18、在前述方面的一些实施例中,该患有scd的受试者被诊断为具有β珠蛋白基因中的突变。例如,在一些实施例中,该β珠蛋白基因中的突变是β珠蛋白基因中的单核苷酸突变。在一些实施例中,该β珠蛋白基因中的单核苷酸突变导致相对于seq id no:1(vhltpeeksavtalwgkvnvdevggealgrllvvypwtqrffesfgdlstpdavm gnpkvkahgkkvlgafsdglahldnlkgtfatlselhcdklhvdpenfrllgnvlvc vlahhfgkeftppvqaayqkvvagvanalahkyh)在位置6处谷氨酸被缬氨酸取代。
19、在前述方面的一些实施例中,该scd包括红细胞(rbc)中的补体沉积。例如,在一些实施例中,该scd包括rbc中的c5b9沉积。
20、在前述方面的一些实施例中,该scd包括血管内溶血(ivh)。例如,在一些实施例中,ivh的特征在于包括乳酸脱氢酶(ldh)、胆红素、游离血红蛋白和游离血红素在内的至少一种标志物的增加。
21、在任何前述方面的一些实施例中,在向该受试者施用该补体c5抑制剂后,该受试者表现出scd、bt或镰状细胞bt表型的降低。例如,在一些实施例中,该scd表型包括导致血管组织损害的炎症或细胞毒性增加;voc事件触发的疼痛加剧;或scd患者的死亡率或发病率增加。
22、在任何前述方面的一些实施例中,该组合物通过静脉内施用。
23、在另一方面,本披露的特征是一种用于在缺氧条件下提高细胞活力或降低细胞死亡的方法,该方法包括使该细胞与有效量的包含补体抑制剂的组合物接触。
24、在前述方面的一些实施例中,在体内接触这些细胞。
25、在前述方面的一些实施例中,该细胞是镰状细胞
26、在任何前述方面的一些实施例中,scd的特征在于选自以下的特征:(a)补体c3和/或c5b9在受影响细胞(例如,rbc)中的沉积增加,尤其是在触发条件(例如,缺氧)下;(b)新生血管溶血增加,尤其是在触发条件(例如,缺氧)下,其中溶血增加的特征在于血浆乳酸ldh活性/水平、游离血红素和/或游离血红蛋白水平和/或总胆红素水平的增加;或(c)voc的严重程度增加,尤其是在触发条件(例如,缺氧)下。
27、在任何前述方面的一些实施例中,用补体c5抑制剂(如抗c5抗体)治疗得到选自以下的结果:(a)抑制或逆转该scd受试者的rbc中c3和c5b9的补体片段沉积,例如在缺氧条件下;(b)减弱或逆转缺氧条件下血管内溶血(如测量到血浆ldh活性/水平、游离血红素和/或游离血红蛋白水平和/或总胆红素水平增加)的水平;或(c)降低或逆转该scd受试者的肺、肾、肝和脾等重要器官血管中的血管闭塞。例如,在一些实施例中,与用包括羟基脲的标准治疗的结果相比,用补体c5抑制剂(如抗c5抗体)治疗提供了(a)-(c)中至少一个结果的可比改善;优选地,其中与用羟基脲治疗相比,用该补体c5抑制剂治疗导致(a)-(c)中至少一个结果的改善。
28、在另一方面,本披露的特征是一种包括补体c5抑制剂的组合物,该组合物用于在治疗受试者的scd或与之相关的症状中使用,特别地用于提高血细胞的活力,这些血细胞含有使其易受缺氧或低氧胁迫影响的一个或多个突变,例如,正常血红蛋白a(α2β2)到血红蛋白s(α2β6val2)的突变或rbc的β珠蛋白基因中的突变。
29、在另一方面,本披露的特征是一种包括补体抑制剂的组合物,该组合物用于在缺氧条件下提高细胞活力或降低细胞死亡中使用。
30、在前述方面的一些实施例中,该补体c5抑制剂选自由抗c5抗体或其抗原结合片段、肽、小分子、核酸分子和适配体组成的组。
31、在前述方面中任一项的一些实施例中,该核酸分子选自由小干扰rna、短发夹rna、微小rna和反义寡核苷酸组成的组。
32、在前述方面中任一项的一些实施例中,该核酸分子与编码补体c5的内源性核酸序列的一部分互补。
33、本披露至少部分地基于以下惊人发现,即补体抑制剂(例如,补体c5抑制剂,例如,抗c5抗体、核酸分子、肽、小分子或适配体)提供令人惊讶的能力来减弱与scd、bt或镰状细胞bt相关的发病机制。使用本文所述的组合物和方法,补体蛋白(例如,补体c5)可以被有效抑制,以治疗scd、bt或镰状细胞bt。还发现用抗c5抗体进行的疗法在降低ss小鼠的rbc中的血管内溶血方面与hu同样有效。更特别地,当用抗c5抗体预处理小鼠时,缺氧诱导的ldh活性、游离血红素/血红蛋白水平、和总胆红素水平的增加全都被减弱,这种效果与用已知药物如hu进行的体内预处理是可比的。关于缺氧条件下镰状细胞小鼠中的c5b9沉积,本文提供的实验证据表明,抗c5抗体疗法在抑制攻膜复合物(mac)形成方面比hu治疗更有效。用抗c5抗体预处理还抑制肺、肾、肝和脾等重要器官处缺氧诱导的血管闭塞危象。因为肺在scd的病理生理学的上下文中是主要的靶组织,所以本文的数据表明抗c5抗体在体内环境中在防止scd症状方面的显著保护效果。
- 还没有人留言评论。精彩留言会获得点赞!