非洲猪瘟病毒C717R蛋白作为免疫诱导剂或者佐剂的应用
本发明属于生物和病毒免疫学领域,尤其涉及非洲猪瘟病毒(africanswine fever virus,asfv)的c717r蛋白的新功能,即asfv c717r蛋白诱导炎性细胞因子的转录和分泌上调;同时asfv c717r诱导nlrp3炎症小体介导的il-1β的成熟。
背景技术:
1、炎症是一组复杂的可溶性因子和细胞之间的相互作用,可在任何组织中出现,以应对创伤、感染、缺血后、中毒或自身免疫损伤。炎症贯穿于机体感染-恢复-愈合整个过程,但是,如果靶向破坏和辅助修复没有达到适当的阶段,炎症可能会导致白细胞、淋巴细胞或胶原蛋白对组织的持续损伤。炎症的重要的生物标志物是细胞因子,包括肿瘤坏死因子-α(tnf-α)、白介素-1(il-1)、il-6、il-8、单核细胞趋化蛋白1等。白介素-1(il-1)家族在免疫学中是独特的,因为il-1家族和toll样受体(tlr)家族具有相似的功能。具有调控诱发炎症的功能,炎症作为宿主防御机制发挥作用。il-1家族细胞因子被认为是“早期反应”细胞因子。这意味着它们在免疫反应的早期阶段被释放,并作为后续促炎细胞因子级联的触发器。il-1β刺激il-6、tnf-α和il-17a的释放,而il-18促进ifn-γ、il-2和il-12的产生。这些下游细胞因子与高度促炎性t辅助细胞1(th1)和t辅助细胞17(th17)型免疫反应相关。
2、大部分病毒为了对抗宿主炎症应答,利用自身蛋白抑制炎症小体活化,进而降低il-1β的产生。例如,甲型流感病毒ns1蛋白抑制nlrp3炎症小体活化,最终抑制il-1β的产生。麻疹病毒v蛋白也结合nlrp3,阻遏nlrp3介导的il-1β的产生。脊髓灰质病毒3c通过其蛋白酶活性切割nlrp3抑制il-1β的产生。宿主为了启动炎症应答,也能通过结合感知病毒蛋白,激活nlrp3炎症小体介导的il-1β的产生。脊髓灰质炎病毒的基因组能够激活il-1β的产生。登革热病毒的2a、2b以及m蛋白激活nlrp3炎性小体,诱导il-1β的产生。
3、非洲猪瘟(african swine fever,asf)是由非洲猪瘟病毒(african swine fevervirus,asfv)引起猪的一种急性出血热疫病。感染家猪后死亡率高达100%,给全球的养猪业造成了巨大的打击。目前无针对强毒株对宿主产生高效保护力的疫苗或抗病毒药物。asf首次在肯尼亚被描述,进而在非洲迅速蔓延,影响多达35个非洲国家,随后席卷欧洲、南美、亚洲。在一些有野猪存在的地区,asf的防控形势更为复杂。asfv急性感染,能够引起宿主“细胞因子风暴”,导致宿主产生如脾脏充血肿大易碎、淋巴结肿大、各器官出血等系统性器官损伤和宿主死亡。而asfv慢性感染,会导致动物皮肤多灶性坏死、呼吸窘迫、关节炎等。asfv感染猪后,动物肺、肝、扁桃体和脑等组织检测存在粒细胞或单核细胞浸润肺或发生淋巴组织细胞性炎症。研究证实,asfv感染细胞诱导tnf-α、il-1β和il-6等炎症因子介导的“细胞因子风暴”,对内皮细胞造成严重损伤。asfv感染也诱导趋化因子显著增加。以上研究说明,asfv可能利用自身组分感染后期诱导炎性应答,导致机体组织功能发生紊乱。我们推测asfv调控炎症因子的产生可能是病毒大量复制以及宿主致病和病理损伤机制的重要原因之一。由于asfv早期免疫抑制严重,但后期能够形成“炎症因子风暴”,且asfv存在基因重组现象,敲除毒疫苗可能存在返强风险,因此asfv的炎性诱导蛋白的抑制剂或者亚单位疫苗的研发成为一种重要的选择,而亚单位疫苗的缺点是缺少诱发免疫应答的组分,asfv亚单位疫苗的免疫诱导剂或者佐剂的研发也至关重要。asfv是非洲猪瘟病毒科非洲猪瘟病毒属的唯一成员,为大型双链dna病毒,其基因组dna长大约150~190kb,编码150多种蛋白质,其中约五十多种蛋白质为结构蛋白,大多数蛋白仍未被鉴定。c717r蛋白是asfv的一个非常保守的病毒蛋白,该蛋白包含的一个类似于丝氨酸/苏氨酸激酶的中心结构域,除了非洲猪瘟病毒科,该蛋白在动物病毒和骨髓病毒中也保守。目前c717r的功能仍未鉴定。对其功能的研究有利于疫苗以及动物炎症相关药物的研发。
技术实现思路
1、本发明首次揭示了asfv的c717r蛋白的新功能,即c717r蛋白促进炎性细胞因子的转录与分泌,同时asfv c717r诱导nlrp3炎症小体介导的il-1β的成熟。
2、本发明构建了asfv c717r基因慢病毒表达系统,通过感染bmdms,发现c717r诱导炎性细胞因子的大量产生。将asfv c717r重组慢病毒接种balb/c小鼠后,发现il-1β、tnf-α、il-6等炎性细胞因子的转录和分泌显著增加。因此,为了控制非洲猪瘟病毒诱导炎症反应,可以设计asfv c717r的抑制药物或asfv c717r缺失减毒活疫苗;同时在疫苗设计中,为促进机体免疫应答,asfv c717r蛋白可以作为诱导剂或者佐剂使用,帮助疫苗更好产生抗体。
3、其中,asfv c717r蛋白的氨基酸序列如seq id no:1所示,编码该氨基酸的dna序列如seq id no:2所示。
4、本发明构建了asfv c717r基因慢病毒表达系统,具体构建策略如下:
5、(1)以ⅱ型非洲猪瘟病毒株asfv cn/gs 2018为模板,用引物c717r-f和c717r-r扩增含有c717r基因cds的片段,将扩增片段与pmd20 t载体连接,获得阳性克隆pmd-c717r,测序,结果显示正确;
6、(2)将pmd-c717r进行xhoi和ecori双酶切,连接到慢病毒载体(phblv-cmv-mcs-3flag-ef1-t2a-zsgreen-puro);
7、(3)将慢病毒载体进行病毒包装,收获asfv c717r重组慢病毒r-lenti-c717r(lv-c717r)。
8、同时将空载体慢病毒(empty-lenti)进行包装作为对照,空载体慢病毒的包装同asfv c717r重组慢病毒包装策略相同。
9、asfv c717r重组慢病毒感染bmdms细胞后,通过elisa和qpcr检测,发现c717r表达后,c717r诱导il-1β的分泌,il-1β、ifn-β、il-6、tnf-α等炎性细胞因子的转录显著上调。
10、c717r重组慢病毒过表达载体质粒感染bmdms后,促进nlrp3炎症小体介导的il-1β的成熟分泌。
11、本发明还发现,asfv c717r重组慢病毒感染小鼠后,小鼠血清中il-1β、tnf-α、ifn-β和ifn-γ的分泌上调。
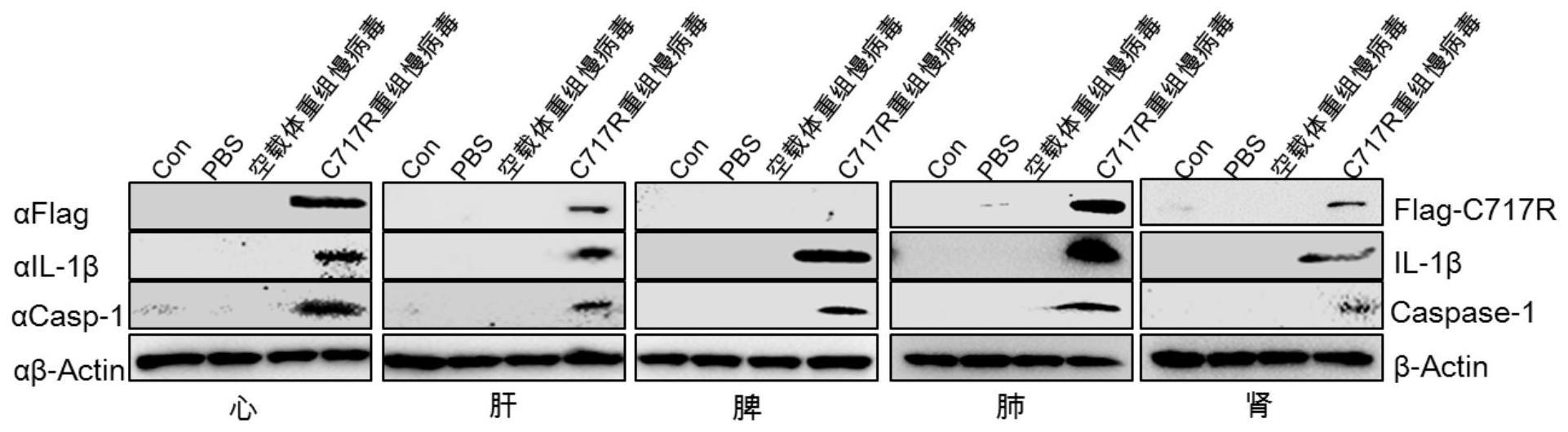
12、asfv c717r重组慢病毒感染小鼠后,小鼠组织中il-1β、tnf-α、il-6等炎性细胞因子表达量显著上升;c717r诱导小鼠肝脏、脾脏、肺脏、心脏、肾脏的il-1β和caspase-1蛋白成熟表达。这说明c717r基因表达后,c717r蛋白激活炎性细胞因子的转录和分泌。
13、另外,asfv c717r重组慢病毒感染小鼠后,c717r不引起小鼠脏器的肿大充血,但能够引发组织发生促炎性应答。
14、本发明具有以下有益效果:
15、本发明发现asfv的c717r蛋白能够诱导炎性细胞因子的转录和分泌,并通过nlrp3信号通路激活il-1β的分泌。此发明为进一步阐明asfv的基因功能以及c717r的新功能提供理论基础,同时,本发现能够为控制病毒诱导炎症反应,设计c717r的抑制药物提供新的视角,同时在疫苗设计中,为促进机体免疫应答,asfv c717r蛋白可以作为诱导剂或佐剂使用,帮助更好产生抗体。
- 还没有人留言评论。精彩留言会获得点赞!