改善细胞治疗的方法与流程
发明领域本公开涉及用于修饰细胞表面的组合物和方法,以及这些经修饰细胞在炎性病况、组织损伤/受损和癌症的基于细胞的治疗中的改善的功效和适用性。
背景技术:
0、发明背景
1、基于细胞的治疗剂(也称为“过继细胞治疗剂”)的成功取决于将足够量的相关细胞提供到需要其的位点以实现预期的生物学作用。递送用于临床适应症的细胞可以通过直接(局部)注射到所涉及的组织中,通过血管内给药(例如系统地或通过基于导管的递送到达特定血管床),或通过直接将细胞应用/放置到受影响的区域(例如用于皮肤溃疡,烧伤等)来实现。在所有形式的细胞施用中,有利的是施用的细胞具有膜分子,其能够促进细胞在施用位点内精确地在组织微环境内沉积,这些组织微环境对于达到预期效果,例如控制炎症、组织修复、消除排异反应、癌症根除至关重要。所述微环境位点之一是存在于损伤组织内的微血管内和周围的“血管周围区域”,因为众所周知,微脉管的完整性和新微血管的产生(即“血管生成”)是组织再生/修复的关键先决条件。实际上,在组织损伤、炎症和癌症的所有位点,受影响组织的微血管内的内皮细胞显示出一组特征性的粘附分子,其在募集循环(血源性)细胞至靶位时起关键作用。这些内皮分子由炎性细胞因子如肿瘤坏死因子(tnf)和白细胞介素1(il-1)上调,并且在人中其包括分子e-选择素,在小鼠包括分子e-选择素和p-选择素,这些是属于称为“选择素”的粘附分子家族的凝集素(在下文将更详细描述)。此外,已经被募集到任何炎症位点(包括癌症)或组织损伤/受损位点的白细胞显示有l-选择素,即“白细胞”选择素,因此,在被施用细胞上表达l-选择素的配体会促进这些细胞沉积到受影响组织内部的白细胞浸润物区域。
2、乍看之下,直接递送似乎可能是细胞施用最有效的方法,特别是考虑到可以将浓缩的细胞团应用到受影响的区域。然而,也存在局部注射实际上对预期的治疗效果起反作用的情况,而且局部注射仅适用于某些解剖位置:(1)通过在静水压力下将相关细胞引入培养基悬浮液中,注射程序可能伤害到递送的细胞,并且进一步降低组织完整性并破坏早期组织修复和/或宿主防御过程,从而加剧炎症状况或原位抵消适当的免疫应答;(2)凭借侵入性方法,注射针/装置(和悬浮液)可引起靶组织受损和/或引起侧支组织受损;(3)直接注射对于具有明确解剖边界(例如心脏)的器官/组织最为可行,对于没有广泛结缔组织支持(例如肺)的组织是不易实施的。(4)注射程序可能在依赖技术且耗费劳动,需要使用具有显著成像支持的复杂递送系统,尤其是对于相对不易接近和/或脆弱的器官/组织(例如中枢神经系统)而言。(5)最重要的是,许多退行性和炎性疾病实际上是广泛分布和多灶性的(如骨质疏松症、炎性肠病、多发性硬化症等),因此直接注射既不实用也不实效。因此,尽管存在局部注射可行的临床状况/情况,但脉管途径的施用对于所有广泛的“系统”疾病,以及对于局部注射很难接近和/或解剖学上不适于局部注射的任何组织(例如糖尿病中的胰腺,慢性阻塞性肺疾病中的肺)是必须的。以最小的努力重复施用细胞的能力是系统输注的另一个重要的实际优点。因此,创建优化分子效应子的表达/活性的方法学是实现所有基于细胞的疗法巨大前景的关键,所述效应子既指导了炎症环境中直接注射的细胞的粘附/沉积,也指导脉管内施用的细胞向受影响部位的生理迁移。
3、血源细胞直接迁移到预定位置的能力(“归巢”)对各种生理和病理过程有深刻的影响。循环细胞向特定解剖位点的募集是通过靶组织的流动的和脉管内皮中的细胞之间的离散的粘附相互作用引发的。介导这些接触的分子被称为“归巢受体”,并且如历史上所定义的,这些结构引导血液中的细胞对各自靶组织的向性。在历史中,描述了三种“组织特异性归巢受体”:l-选择素用于外周淋巴结,α4β7(lpam-1)用于肠和肠相关淋巴组织,以及p-选择素的一个专门的糖型p-选择素糖蛋白配体-1(psgl-1),其特别地作为促进细胞向皮肤迁移的“皮肤淋巴细胞抗原”(cla)而为人所知(r.sackstein,curr opin hematol 12,444(2005))。值得注意的是,除了这些组织,数十年来已经认识到循环细胞,特别是造血干细胞(hsc)能有效地导向骨髓(t.lapidot,a.dar,o.kollet,blood 106,1991(2005)),并且有几项研究指出了选择素的作用,主要是e-选择素与hsc e-选择素配体结合,介导hsc向骨髓的募集。
4、从生物物理角度来看,归巢受体用作分子制动器,影响初始的聚集,然后使血流中细胞以低于主要血流速率的血液流动速率向脉管内皮上进行持续滚动接触(步骤1)(r.sackstein,curr opin hematol12,444(2005))。此后,发生一系列事件,通常为通过趋化因子增强,导致整合素粘附性的激活(步骤2)、牢固粘附(步骤3)和内皮迁移(步骤4)(t.a.springer,cell 76,301(1994))。这种“多步骤范式”认为组织特异性迁移由给定循环细胞上的归巢受体和趋化因子受体表达的离散组合调节,允许识别由器官特异性形式表达于靶标内皮内的相关脉管粘附配体和趋化因子显示的相关“交通信号”。在指导细胞转运到骨髓的归巢受体参与之后,有几个证据表明一种趋化因子,具体而言是sdf-1(cxcl12)在步骤2介导的细胞向该位点的募集中起着重要作用(t.lapidot,a.dar,o.kollet,blood 106,1991(2005);a.peled等人,science 283,845(1999);d.a.sipkins等人,nature435,969(2005))。然而,sdf-1的表达不限于骨髓,并且该趋化因子通常在组织损伤/炎症的所有位点表达(r.sackstein,immunol.rev.230:140-163(2009))。
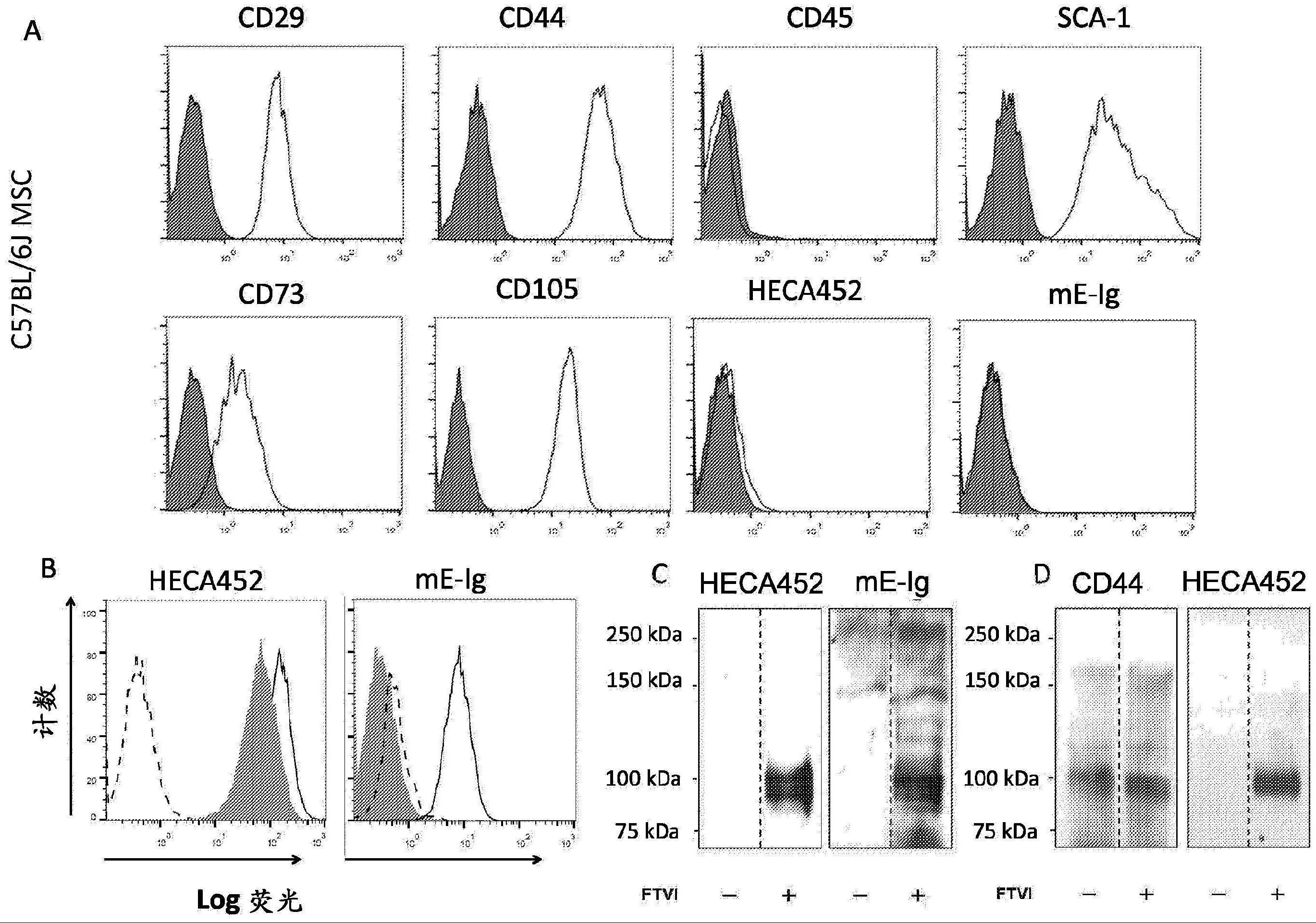
5、步骤1滚动相互作用的最有效的效应子是选择素(e-,p-和l-选择素)及其配体(r.sackstein,curr opin hematol 12,444(2005))。顾名思义,选择素是结合特异化的碳水化合物决定簇的凝集素,其由含有α(2,3)连接的唾液酸取代及α(1,3)连接的岩藻糖修饰的唾液酸岩藻糖基化构成,四糖唾液酸lewis x是其原型代表(slex;neu5acα2-3galβ1-4[fucα1-3]glcnacβ1-))(r.sackstein,curr opin hematol 12,444(2005);m.j.polley等人,proc natl acad sci usa 88,6224(1991))。slex多糖被多种单克隆抗体(mab)识别,包括称为“heca452”的mab。e-和p-选择素在脉管内皮(p-选择素还在血小板上)表达,l-选择素在循环白细胞上表达(r.sackstein,curr opin hematol 12,444(2005))。e-和p-选择素通常是可诱导的内皮细胞膜分子,其仅在组织损伤和炎症的位点显著表达,其中其表达是响应于炎性细胞因子产生的。然而,骨髓和皮肤的微血管组成型表达这些选择素,它们在这些位点的稳态募集血液细胞中起关键作用(r sackstein j invest.dermatology,122:1061-1069(2004))。重要的是,在灵长类动物(但不是啮齿动物)中所有的炎症位点和组织损伤位点,e-选择素是介导细胞募集的主要脉管选择素,因为响应于炎性细胞因子tnf和il-1的启动子元件已从p-选择素基因中删除。因此,在人的所有炎症位点,脉管e-选择素表达比p-选择素更显著(r.sackstein,immunol.rev.230:140-163(2009))。
6、已经在人造血干细胞/祖细胞(hspc)中鉴定了e-选择素的两种主要配体,即psgl-1的高唾液酸岩藻糖基化的cla糖型(z.laszik等人,blood 88,3010(1996),r.sackstein,immunol.rev.230:140-163(2009))和特异化的唾液酸岩藻糖基化的cd44糖型,称为造血细胞e-/l-选择素配体(hcell)(c.j.dimitroff,j.y.lee,s.rafii,r.c.fuhlbrigge,r.sackstein,j cell biol 153,1277(2001);c.j.dimitroff,j.y.lee,r.c.fuhlbrigge,r.sackstein,proc natl acad sci us a 97,13841(2000))。cd44是一种存在相当普遍的细胞膜蛋白,但hcell表型主要发现于人类hspc中。与hcell的限制性分布相反,cla/psgl-1在骨髓中的造血祖细胞以及更成熟的骨髓和淋巴样细胞中广泛表达(z.laszik等人,blood88,3010(1996),r.sackstein,immunol.rev.230:140-163(2009))。在操作上将hcell定义为在剪切条件下与e-选择素和l-选择素结合的cd44,并且通过细胞裂解物的蛋白质印迹分析鉴定为与e-选择素-ig嵌合体(e-ig)及mab heca452反应的cd44糖型,mab heca452识别唾液酸lewis x(除了slex之外,heca452识别slex的四糖异构体,被称为“唾液酸化的lewisa”(slea),其中岩藻糖以α(1,4)连接形式连接至1型乳糖胺骨架内的n-乙酰葡糖胺)。除了cla和hcell,人白细胞和hspc还可以表达可作为e-选择素配体的称为“cd43-e”的cd43糖型(fuhlbrigge等人blood 107:1421-1426(2006),merzaban等人blood 118:1774 -1783(2011)),并且在小鼠白细胞中,已经描述了称为e-选择素配体-1(esl-1)的另一种e-选择素配体(merzaban等人blood 118:1774-1783(2011))。在所有糖蛋白选择素配体中(例如cd43-e、cla和hcell),与e-选择素(以及l-选择素和p-选择素)的结合都严重依赖于α(2,3)-唾液酸和α(1,3)-岩藻糖修饰(c.j.dimitroff,j.y.lee,s.rafii,r.c.fuhlbrigge,r.sackstein,j cell biol 153,1277(2001);c.j.dimitroff,j.y.lee,r.c.fuhlbrigge,r.sackstein,proc natl acad sci us a 97,13841(2000);r.sackstein,c.j.dimitroff,blood 96,2765(2000);c.j.dimitroff,j.y.lee,k.s.schor,b.m.sandmaier,r.sackstein,j biol chem 276,4762(2001))。在人hspc上,hcell显示在n-聚糖上的相关的唾液酸岩藻糖基化的选择素结合决定簇(c.j.dimitroff,j.y.lee,s.rafii,r.c.fuhlbrigge,r.sackstein,j cell biol 153,1277(2001);r.sackstein,c.j.dimitroff,blood 96,2765(2000))。在血液动力学剪切应力下对e-和l-选择素结合的体外测定表明hcell是在任何人类细胞上表达的这些分子的最有效配体(c.j.dimitroff,j.y.lee,s.rafii,r.c.fuhlbrigge,r.sackstein,j cell biol153,1277(2001);c.j.dimitroff,j.y.lee,k.s.schor,b.m.sandmaier,r.sackstein,j biol chem 276,47623(2001))。重要的是,虽然e-选择素在骨髓和皮肤的微脉管内皮上组成型表达,但是在所有炎症位点——急性和慢性型的内皮层上都显著地表达这种分子——无论其由是否由以下原因引起:直接组织损伤(例如烧伤、创伤、褥疮溃疡等)、缺血/脉管事件(例如心肌梗塞、中风、休克、出血、凝血病等)、感染(例如蜂窝组织炎、肺炎、脑膜炎、sirs等)、瘤形成(例如乳腺癌、肺癌、淋巴瘤等)、免疫/自身免疫病况(例如移植物抗宿主病、多发性硬化、糖尿病、炎性肠病、红斑狼疮、类风湿关节炎、银屑病等)、退行性疾病(例如骨质疏松症、骨关节炎、阿尔茨海默氏病等)、先天性/遗传性疾病(例如肌营养不良、溶酶体贮积病、亨廷顿氏病等)、药物不良反应(例如药物诱导的肝炎、药物-诱导的心脏损伤等)、中毒性损伤(例如辐射照射、化学品接触、酒精性肝炎,酒精性胰腺炎、酒精性心肌病、可卡因心肌病等)、代谢紊乱(例如尿毒症性心包炎、代谢性酸中毒等)、医源性病况(例如辐射诱导的组织损伤、外科手术相关的并发症等),和/或特发性过程(例如肌萎缩性侧索硬化,parsonnage-turner综合征等)。
技术实现思路
1、在本公开的多个方面中,提供了用于治疗在受影响的组织内的脉管内皮细胞和/或白细胞浸润物上有e-选择素表达的疾病、障碍或医学病况的方法。e-选择素与天然存在于某些白细胞和造血干细胞/祖细胞表面上的唾液酸化的岩藻糖基化的碳水化合物(例如唾液酸化的lewis x和lewis a家族的成员)结合,所述细胞即骨髓细胞(例如嗜中性粒细胞、单核细胞、嗜酸性粒细胞、巨噬细胞等)、树突细胞(来自淋巴系和髓系)、淋巴细胞(例如初始和记忆t细胞、初始和记忆b细胞、效应t细胞、调节性t细胞、天然杀伤细胞(nk细胞)等)、造血祖细胞和造血干细胞。因此,发现这些细胞类型位于急性和慢性炎症位点,是由脉管e-选择素招募到这些炎症位点的。白细胞和hspc特征性地显示有l-选择素。l-选择素本身结合唾液酸化的岩藻糖化的碳水化合物如slex。因此,炎性位点具有表达e-选择素(内皮细胞上)和l-选择素(浸润性白细胞和hspc上)的细胞。
2、实现基于细胞的治疗剂的预期结果的能力在严重地依赖于向需要的位点递送施用的细胞,并且还涉及所述施用的细胞在特定组织微环境内的定位。因此,在本领域中需要增强施用的细胞向组织损伤/受损、向炎症位点、向癌症位点和向感染位点的脉管递送的方法。本领域还需要增强施用的细胞在受影响组织内的递送/定殖。因此,简而言之,本公开涉及治疗在受试者中表现为发炎的和/或受损的组织和/或癌症的疾病、障碍或医学病况的方法,所述方法包括向受试者施用以超过细胞的天然群体的水平表达e-选择素配体和/或l-选择素配体的细胞群体。在靶组织(例如发炎的和/或受损的组织、癌组织)内的内皮细胞上表达e-选择素的同时和/或在靶组织中白细胞积累(例如白细胞浸润物)的同时进行施用。可以通过在靶组织内的直接注射和/或通过脉管系统和/或通过如下文进一步详细描述的其它方式进行施用。
3、本公开进一步针对用表达e-选择素和/或l-选择素配体的活细胞群体治疗炎症的方法。所述活细胞群体以超过所述细胞的天然群体表达水平的水平表达e-选择素配体和/或l-选择素配体。在靶组织(例如发炎的和/或受损的组织、癌组织)内的内皮细胞上表达e-选择素的同时和/或在靶组织中白细胞积累(例如白细胞浸润物)的同时进行施用。可以通过直接注射入靶组织内和/或通过脉管系统(和/或通过如下文进一步详细描述的其它方式)进行施用,并且对所述疾病、障碍或医学病况的治疗无需伴随长期植入所述施用细胞(即可通过所述施用细胞在治疗位点的瞬时定殖或长期持续/存活,或者通过所述施用细胞在治疗位点增殖,或者通过所述施用细胞在治疗位点分化和/或成熟来实现治疗)。
4、本公开进一步针对表达e-选择素和/或l-选择素配体的活细胞群体,在制备用于治疗受试者的炎症的药物中的用途。所述活细胞群体以超过所述细胞的天然群体表达水平的水平表达e-选择素配体和/或l-选择素配体。在靶组织(例如发炎的和/或受损的组织、癌组织)内的内皮细胞上表达e-选择素的同时和/或在靶组织中白细胞积累(例如白细胞浸润物)的同时进行施用。可以通过直接注射入靶组织内和/或通过脉管系统和/或通过如下文进一步详细描述的其它方式进行施用。
5、本公开进一步针对表达e-选择素配体和/或l-选择素配体的活细胞群体,在制备用于治疗肿瘤/恶性疾病的药物中的用途,所述治疗包括向受试者施用表达e-选择素配体和/或l-选择素配体的细胞群体,其中所述群体以超过所述细胞的天然群体的表达水平的水平表达所述e-选择素配体和/或l-选择素配体,其中所述治疗包括在肿瘤/恶性组织内的内皮细胞上的e-选择素表达同时和/或在肿瘤/恶性组织中白细胞的积累同时施用所述群体。
6、本公开进一步针对表达e-选择素配体和/或l-选择素配体的活细胞群体,在制备用于治疗表现出炎症的患病状态的药物中的用途,所述治疗包括向受试者施用表达e-选择素配体和/或l-选择素配体的细胞的群体,其中所述群体以超过所述细胞的天然群体的表达水平的水平表达所述e-选择素配体和/或l-选择素配体,其中所述治疗包括在肿瘤/恶性组织内的内皮细胞上开始e-选择素表达同时和/或在肿瘤/恶性组织中白细胞的积累同时施用所述群体。
7、涉及本文所述的施用(例如通过脉管系统和/或通过直接注射到组织内和/或经由其它方式)的其它方法包括例如增强受试者中发炎的和/或受损的组织或者癌症位点(统称为“靶”组织)中细胞递送和定殖的方法,增强细胞递送至受试者靶组织和/或增强在受试者靶组织中的组织定殖的方法,增强细胞群体在受试者靶组织内归巢和植入的方法,治疗受试者的炎性病况的方法,增强受试者中组织修复/再生的方法,以及治疗受试者的肿瘤/恶性疾病的方法。
8、通常,根据本文所述的方法可以治疗多种炎性病症(例如急性和/或慢性)和/或受损的组织中的任何一种,包括但不限于由直接组织损伤(例如烧伤,创伤,褥疮溃疡等)、缺血/脉管事件(例如心肌梗塞、中风、休克、出血、凝血病等)、感染(例如蜂窝组织炎、肺炎、脑膜炎、sirs等)、瘤形成(例如乳腺癌、肺癌、淋巴瘤等)、免疫/自身免疫病症(例如移植物抗宿主病、多发性硬化、糖尿病、炎性肠病、红斑狼疮、类风湿关节炎、银屑病等)、退行性疾病(例如骨质疏松症、骨关节炎、阿尔茨海默氏病等)、先天性/遗传性疾病(例如大疱性表皮松解、成骨不全、肌营养不良、溶酶体贮积病、亨廷顿氏病等)、药物不良反应(例如药物诱导的肝炎、药物-诱导的心脏损伤等)、中毒性损伤(例如辐射照射、化学品接触、酒精性肝炎,酒精性胰腺炎、酒精性心肌病、可卡因心肌病等)、代谢紊乱(例如尿毒症性心包炎、代谢性酸中毒等)、医源性病况(例如辐射诱导的组织损伤、外科手术相关的并发症等),和/或特发性过程(例如肌萎缩性侧索硬化,parsonnage-turner综合征等)引发的那些。
9、在某些实施方案中,例如由细胞群体表达的e-选择素配体和/或l-选择素配体选自以下中的一种或多种:造血细胞e-/l-选择素配体(hcell)、神经细胞粘附分子e-选择素配体(ncam-e)、cd43e和cla。在一个实施方案中,e-选择素配体是造血细胞e-/l-选择素配体(hcell)和/或神经细胞粘附分子e-选择素配体(ncam-e)。在另一个实施方案中,e-选择素配体是hcell。在另一个实施方案中,e-选择素配体是ncam-e。在另一个实施方案中,l-选择素配体是hcell。值得注意的是,由于e-选择素在受影响组织的内皮层内表达,而且白细胞特征性表达l-选择素,所以hcell(一种有效的e-选择素和l-选择素配体)的表达将有助于明确地促进大多数强烈的免疫应答性/组织受损的微环境内的组织贮存。
10、如本文更详细地讨论的,可以使用多种方法来制备用于施用于受试者的细胞群体。在一个实施方案中,通过使细胞或细胞的群体与糖转移酶及适当的供体核苷糖接触来制备群体。例如通过糖基转移酶增强表达岩藻糖残基(岩藻糖基化)、唾液酸残基(唾液酸化)或二者(唾液酸岩藻糖基化),可以使用聚糖工程化来唾液酸岩藻糖基化cd44以增强造血细胞e-选择素配体(hcell)的表达。备选地,可使用糖基转移酶如岩藻糖基转移酶将完整的聚糖结构如唾液酸lewisx或唾液酸lewisa转移至细胞表面。此外,非酶法可以用于共价或非共价地将e-选择素和/或l-选择素配体结合到细胞表面。例如可使用生物素-链霉亲和素对将适体、slex(唾液酸lewisx)、slex聚糖的糖模拟物和/或肽模拟物、slea聚糖的(唾液酸lewisa)、slea聚糖的糖模拟物和/或肽模拟物以及结合e-选择素和/或l-选择素的其它部分非共价地结合到细胞表面,或共价地结合到细胞表面;无论是共价还是非共价,所述结合可以是直接的或经由连接子。进一步的实例,结合e-选择素和/或l-选择素的噬菌体展示颗粒或抗体可以共价地或非共价地结合到细胞表面,在每种情况下介导经处理的细胞对e-选择素和/或l-选择素的粘附。
11、通常,且与制备细胞群体的方式无关,制备方式提供了在修饰时间后24小时具有至少70%活力的修饰的细胞群体。在一个这样的实施方案中,修饰的细胞群体在修饰时间后24小时具有至少80%的活力。在一些实施方案中,修饰的细胞群体在修饰时间后24小时具有至少85%的活力。在一些实施方案中,修饰的细胞群体在修饰时间后24小时具有至少90%的活力。可以通过本领域已知的方法例如台盼蓝排除法或通过用于碘化丙啶和膜联蛋白v染色的双色流式细胞术评估来确定细胞活力。优选地,在处理后保留细胞的表型(除细胞表面修饰以外)。保留的表型是指细胞保持其天然功能和/或活性。例如如果细胞是干细胞,它保留其再生能力,例如其全能性或其多能性或其多潜能性或其单能性。
12、经修饰的细胞群体是存活的(即如上所述在修饰时间后24小时具有至少70%的活力),并且相对于所述细胞的天然群体具有增强的与e-选择素和/或l-选择素结合。可以通过脉管系统和/或通过直接注射到组织中(和/或通过下文详细描述的其它方式)进行细胞的施用。在一个实施方案中,在炎症或白细胞浸润到组织中发生的同时施用经修饰的细胞群体。在另一个实施方案中,恰好在炎症或白细胞浸润到组织中发生之前施用经修饰的细胞群体。
13、在细胞经过聚糖工程化以增强slex表达或经过用slex结构(例如通过抗生物素蛋白-亲和链霉素技术)装饰的情况下,可以通过用mab heca452或识别slex决定簇的任何其它mab进行荧光染色然后用流式细胞术检测细胞荧光强度来进行对经处理的细胞上增加的slex表达的测量。通过首先分析天然(未处理)细胞的样品来确定经修饰的细胞群体的预定荧光阈值。经处理细胞的slex的增加被定义为相比细胞的天然群体,标记物阳性细胞(例如heca452-反应细胞)比例增加超过10%,和/或平均通道荧光强度超过基线(未处理)细胞群体10%。为了检测经处理的细胞群体与e-选择素的结合是否增加,可以使用如本文所述的剪切应力条件下的平行板流动室研究或通过用e-选择素-ig嵌合体进行染色以及通过流式细胞术进行荧光强度评估,而对与e-选择素的结合进行评估。使用本文别处描述的功能性e-选择素结合测定法或通过本领域已知的另一种普遍接受的e-选择素荧光结合测定法测定对照(基线)样品细胞。测量对照(基线)群体样品的e-选择素结合荧光水平。增强的与e-选择素的结合被定义为在e-选择素特异性结合测定中具有增加的对e-选择素粘附性的经处理细胞。在一个实施方案中,增强的与e-选择素的结合可以通过使用荧光染料缀合反应剂的e-选择素结合测定中的荧光偏移来定义,例如通过流式细胞术评估与e-选择素-ig嵌合体的结合,其中具有e-选择素结合的群体内的细胞数目比基线结合的细胞数目增加至少10%(即,在标记阳性群体中增加10%)和/或平均通道荧光比(与天然细胞群体相关的)预定荧光阈值高至少10%。在另一个实施方案中,具有增加的e-选择素反应性的细胞的百分比增加25%和/或经修饰的群体超过预定的荧光阈值25%。在另一个实施方案中,经修饰的群体超过基线反应性和/或预定荧光阈值50%。在另一个实施方案中,具有增加的e-选择素反应性的细胞的百分比比e-选择素结合细胞的基线群体的百分比增加了75%,和/或经修饰的群体超过预定的荧光阈值75%。在另一个实施方案中,经修饰群体中至少90%的细胞超过基线e-选择素结合群体和/或预定荧光阈值。在另一个实施方案中,经修饰群体中至少95%的细胞超过基线e-选择素结合群体和/或预定荧光阈值。
14、可以通过使用具有高特异性的功能性l-选择素结合测定法(例如在动态剪切应力条件下的平行板流动室)或stamper-woodruff测定法来确定增强的与l-选择素结合,其中细胞处理增加了支持l-选择素介导的粘附的细胞的百分比。在平行板测定的情况下,与基线(未处理的细胞)相比,经处理的细胞群体显示与l-选择素(固定并显示在小室塑料或玻璃支撑物表面上)的栓系/滚动(tethering/rolling)粘附相互作用有至少10%的增加。在stamper-woodruff测定的情况下,增加的l-选择素淋巴细胞粘附被定义为在80rpm的旋转剪切下,经处理的细胞与l-选择素+淋巴细胞的结合有至少10%的增加;在未处理(对照)群体上评估基线细胞结合,并直接与经处理的细胞群体相比较。
15、除非另有定义,本文使用的所有技术和科学术语具有与本公开所属领域的普通技术人员通常理解的相同的含义。尽管与本文所述类似或等同的方法和材料可以用于本公开的实践或测试中,但是在下文描述了合适的方法和材料。本文提到的所有出版物、专利申请、专利和其它参考文献通过引用整体并入本文。在发生冲突的情况下,以本说明书(包括定义)为准。此外,材料、方法和实施例是仅作说明而不是限制性的。
16、将会在后文部分地展现和部分地指出其它主题和特征。
- 还没有人留言评论。精彩留言会获得点赞!