预防或治疗鼻病毒感染的药物
预防或治疗鼻病毒感染的药物
1.本技术是申请日为2018年12月28日、申请号为201880087524.5,发明名称为“预防或治疗鼻病毒感染的药物”的中国申请的分案申请。
2.本发明涉及用于预防或治疗人鼻病毒(hrv)感染、例如普通感冒的药物组合物。
3.hrv是小rna病毒科(picornaviridae)的ssrna非包膜病毒。它引起普通感冒,这是一种导致数十亿美元医疗费用的疾病(bertino,2002),它也是免疫抑制者的下呼吸道感染的致病因子(kaiser et al.,2006;liu et al.,2010),还是慢性阻塞性肺病(copd)和哮喘急性发作两者的致病因子(papi等,2006;steinke和borish,2016)。
4.迄今为止,对hrv有效的治疗手段非常有限。例如,抗病毒的普乐那利(pleconaril)对hrv可能只有很小的治疗效果,但副作用的风险却很大。因此,美国食品和药物管理局(fda)拒绝批准普乐那利用于治疗普通感冒(fleischer和laessig,2003)。
5.因此,本发明的一个目的是提供一种针对hrv感染相对安全和有效的预防或治疗,所述hrv感染例如普通感冒或下呼吸道感染,尤其是免疫抑制患者或copd患者或哮喘患者的所述感染。
6.因此,本发明提供了用于预防或治疗hrv感染的药物组合物。所述组合物包含己醛糖(aldohexose)(特别是d-己醛糖),例如葡萄糖(优选d-葡萄糖),其中所述己醛糖的碳2处的羟基被以下取代基中的任何一个取代:h、f、cl、br、i、sh、甲基(me)、甲氧基(ome)和甲基巯基(sme)。在此,根据该定义的己醛糖化合物也称为“改性己醛糖”。在一个特别优选的实施方案中,改性己醛糖是2-脱氧-葡萄糖。
7.在另一方面,本发明涉及用于鼻内给药的分配器,例如鼻喷雾剂,其容纳含有己醛糖的药物组合物,其中所述己醛糖的碳2处的羟基被h、f、cl、br、i、sh、me、ome和sme中的任何一个取代,所述己醛糖尤其是2-脱氧-d-葡萄糖。
8.在另一方面,本发明涉及一种将药物组合物优选地施用于下呼吸道的吸入装置,例如计量吸入器(metered-dose inhaler)、干粉吸入器或雾化器(nebuliser),其包括包含己醛糖的药物组合物,其中所述己醛糖的碳2处的羟基被h、f、cl、br、i、sh、me、ome和sme中的任何一个取代,所述己醛糖尤其是2-脱氧-d-葡萄糖。
9.在本发明的又一方面,提供了一种用于延迟hrv感染的发作或治疗hrv感染的方法,包括
[0010]-获得包含己醛糖的药学上可接受的制剂,其中碳2上的羟基被h、f、cl、br、i、sh、me、ome和sme中的任何一个取代;和
[0011]-对患有hrv感染或有发展hrv感染风险的个体给予有效量的所述制剂。
[0012]
在本发明的过程中,令人惊讶地发现,用改性己醛糖进行的治疗有效地抑制了hrv在体外(参见实施例1以及图1和2)以及在体内(参见实施例2以及图3和4)的复制,且同时对细胞活力没有任何可测量的影响。在体内,未观察到与本发明治疗有关的副作用。由于改性己醛糖靶向hrv复制本身,因此在hrv感染发生后(例如,个体已患普通感冒时)给药以及在hrv感染发生之前给药(例如,预防措施,以便例如延迟或完全避免发病或者改善或完全抑制疾病症状)是有效的。例如,如果家庭成员已经出现鼻炎症状,则预防性给药可能是适当
的。
[0013]
尽管在现有技术中公开了2-脱氧-葡萄糖对某些包膜病毒例如流感病毒有效(参见例如kilbourne,1959和courtney等,1973),但是现有技术根本没有暗示2-脱氧-葡萄糖对hrv感染有效。具体而言,流感病毒和hrv在结构和病理生理上都非常不同。流感病毒属于不相干的正粘病毒科,有包膜,与表达唾液酸的受体结合以感染上皮细胞(参见sun和whittaker,2013)。相比之下,hrv无被包膜,大多数亚型都结合icam-1从而进入宿主细胞(blaas和fuchs,2016)。除了这些差异外,这些病毒在内体逃逸和翻译起始过程中进化出了非常不同的策略(参见blaas和fuchs,2016;以及watanabe和kawaoka,2015)。因此,针对流感病毒感染的最新疗法奥司他韦(oseltamivir)对hrv无效。而且,2-脱氧-葡萄糖对任何人类致病性无包膜rna病毒(例如hrv)的抑制能力是现有技术中未知的(参见例如kang和hwang,2006),这使得本发明的hrv疗法的有效性更加令人意外。
[0014]
与疗法完全无关,更与预防或治疗hrv感染无关,ojima等人(annals of nuclear medicine 3(1989):143-147)描述了适于吸入的2-脱氧-2-(
18
f)氟-d-葡萄糖(
18
fdg)细粉的制备,该粉末可借助正电子发射断层扫描(pet)来诊断非感染性肺部疾病。还有venegas等(database ca,chemical abstracts service,database accession no.2013:196451)描述了
18
fdg在肺部pet成像中的用途,同样仅用于诊断目的,与病毒感染完全无关,更不用说hrv感染了。
[0015]
de 197 06 489a1也与rna病毒无关,它公开了2-脱氧-葡萄糖在由dna病毒(例如人乳头瘤病毒、乙型肝炎病毒、eb病毒)引起的病毒相关病变和/或肿瘤中抑制病毒dna转录的用途。
[0016]
kang和hwang描述了2-脱氧-葡萄糖作为抗癌和抗病毒治疗剂的作用。公开了2-脱氧-葡萄糖可通过抑制病毒包膜的生物合成和病毒体装配来抑制某些包膜病毒(流感病毒,辛德比斯病毒(sindbis virus)和塞姆利基森林病毒,单纯疱疹病毒,呼吸道合胞病毒和麻疹病毒)的增殖。未公开对任何无包膜rna病毒的抑制能力。
[0017]
现有技术已描述了2-脱氧-葡萄糖对包膜病毒的作用。例如,schnitzer等(virology 67(1975)306-309)描述了2-脱氧-葡萄糖和葡糖胺对呼吸道合胞病毒和3型副流感病毒的生长和功能的影响。kilbourne(nature 183(1959)271-272)公开了2-脱氧-葡萄糖对流感病毒增殖的抑制作用。hodes等(virology 63(1975)201-208)描述了2-脱氧-葡萄糖对呼吸道合胞病毒、3型副流感病毒和麻疹病毒的抑制作用。但是,在本发明之前,没有迹象表明2-脱氧-葡萄糖也可以有效对抗无包膜的rna病毒。
[0018]
与2-脱氧-葡萄糖无关的arita等(carbohydrate research 62(1978)143-154)公开了苯基糖苷的各种类似物和衍生物的合成以及它们对某些包膜病毒(流感病毒和单纯疱疹病毒)的抗病毒活性的检测。
[0019]
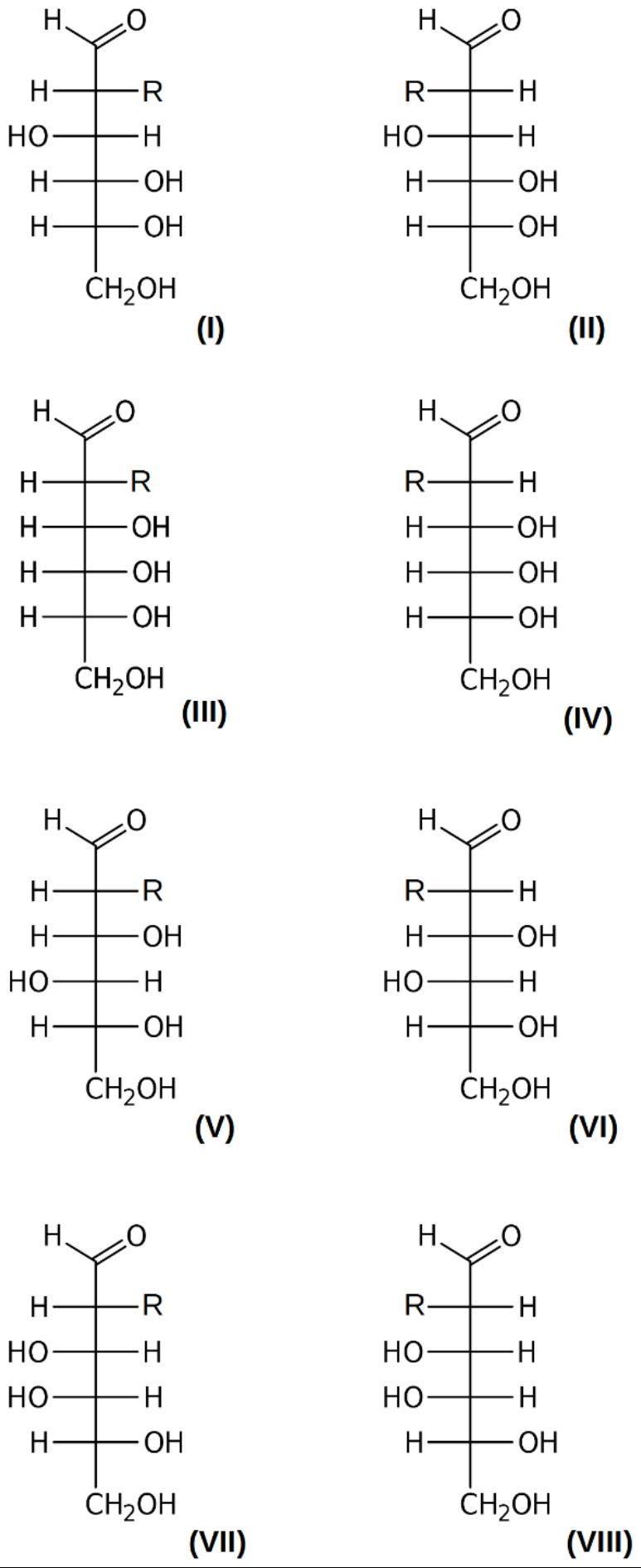
就本发明的所有方面而言,包含在药物组合物(或药学上可接受的制剂)中的改性己醛糖优选是化合物i-viii之一(描绘为费歇尔投影):
[0020][0021]
其中r是h、f、cl、br、i、sh、me、ome和sme中的任何一个。换句话说,r取代相应己醛糖的碳2处的羟基。化合物i(即基于d-葡萄糖的化合物)是特别优选的。2-脱氧-d-葡萄糖是r为h时的化合物i。2-脱氧-d-葡萄糖在本文中也称为“2-dg”。
[0022]
当前,已知三种hrv种类,即鼻病毒a、b和c。关于hrv分类学的综述在例如palmenberg等,2009中给出。优选地,就本发明的所有方面而言,打算治疗或预防的hrv是鼻病毒a或b。
[0023]
在本发明的上下文中,“药物组合物”是指包含至少一种活性剂(例如经改性己醛糖)、和优选地一种或多种赋形剂的任何组合物,其对于给个体(特别是哺乳动物,尤其人)给药(特别是对于局部给药或鼻内给药)而言是药学上可接受的。合适的赋形剂是本领域技术人员已知的,例如水(尤其是注射用水)、盐水(saline)、林格氏液(ringer's solution)、葡聚糖液(dextrose solution)、缓冲液、汉克液(hank solution)、形成囊泡的化合物(例如脂质)、固定油(fixed oils)、油酸乙酯、5%葡聚糖-盐水溶液、增强等渗性和化学稳定性的物质、缓冲液和保存剂如苯扎氯铵。根据本发明的药物组合物可以是液体或易于溶解在
0170198 a2。本文中,术语“滴鼻器(nose drop applicator)”是指适合于(尤其旨在用于)给药滴鼻剂的任何分配器。
[0031]
用于给药上述药物组合物(优选下呼吸道给药)的吸入装置优选为计量吸入器、干粉吸入器或雾化器。
[0032]
计量吸入器是一种雾化预定剂量的药物组合物(即产生相当短促地爆发的带指定剂量的气溶胶)的装置,通常由患者自行给药。例如,us 6,260,549 b1公开了计量吸入器。
[0033]
干粉吸入器是给患者吸入干粉制剂的装置。这样的装置例如在美国专利4,995,385和4,069,819中公开。成熟的干粉吸入器例如有385和4,069,819中公开。成熟的干粉吸入器例如有和
[0034]
雾化器是产生吸入用气溶胶的装置,通常只要它们被打开或通过呼吸驱动就可以连续吸入。成熟的雾化器产品包括例如和文献us 9,364,618 b2也公开了一种雾化器。
[0035]
本发明通过以下附图和实施例进一步说明,但不限于此。
[0036]
图1:2-脱氧葡萄糖在体外抑制hrv复制和hrv蛋白表达。图a)显示了2-dg对hela ohio细胞和原代人成纤维细胞中hrv 14复制的影响。将细胞感染1小时,在pbs中洗,然后施用指定浓度的所述试剂,在完全生长培养基中再温育6小时。温育期后,获得rna,逆转录成cdna,然后通过qpcr评估病毒rna负载。显示了6个独立实验的总结。对标准化数据进行wilcoxon符号秩检验(wilcoxon signed rank test)而算出,*p《0.05。图b)显示了病毒蛋白vp1-3在hrv 14感染的hela ohio细胞中的表达。细胞按上述
±
2-dg处理进行感染,然后裂解并进行蛋白质印迹分析。显示了重复进行的2个独立实验的代表性实验。
[0037]
图2:2-脱氧葡萄糖对人类细胞无毒.用10mm 2-脱氧葡萄糖(有或无hrv)处理对hela细胞的细胞活力没有显著影响。将细胞感染并按上述处理,然后加载荧光标记的活力染料并进行流式细胞仪评估。
[0038]
图3:2-脱氧葡萄糖在体内减小病毒载量并改善hrv呼吸道感染所致的炎症。c57bl/6小鼠经鼻内感染hrv 1b
±
50μl 5mm 2-dg/50μl pbs。感染24小时后,对小鼠实施安乐死,进行支气管肺泡灌洗(bal),并获取组织用于qpcr和组织学分析。显示的是归一化为次黄嘌呤核糖基转移酶(hprt)表达的肺组织中hrv1b rna的存在,其指示病毒载量,以及bal中白细胞的计数(白细胞总数=cd45+,中性粒细胞=cd45+ly6g+,b细胞=cd45+cd19+,树突细胞=cd45+cd11c+,t辅助细胞=cd45+cd3+cd4+,nk细胞=cd45+nk1.1+),其指示肺部炎症。
[0039]
图4:2-脱氧葡萄糖在体内改善hrv呼吸道感染所致炎症,如组织学所证实。描绘了受hrv攻击的小鼠用安慰剂或2-dg处理后肺组织的两种代表性苏木精和曙红(he)染色。显示了2个独立实验的代表实验。在每个实验中,每个感染组测试10只小鼠,未感染对照组测试2只小鼠。安慰剂处理的小鼠比2-dg处理的小鼠支气管周围白细胞浸润明显更多。
[0040]
实施例1
–
细胞培养和体外hrv感染
[0041]
在获得维也纳医科大学伦理委员会批准并获得参与者的书面知情同意(投票号1149/2011:从正常人类皮肤活检标本中分离和培养细胞并进行分析)后,根据赫尔辛基宣言原则进行了涉及人体材料的实验。
[0042]
hela细胞(细胞株:ohio,flow实验室)在rpmi 1640(来自gibco ltd.,paisley,苏
格兰)中培养,培养基补充有2mm l-谷氨酰胺(也来自gibco ltd.,paisley,苏格兰)、100u/ml青霉素、100μg/ml链霉素(paalaboratories,奥地利)和10%fcs(gibco)。为了分离成纤维细胞,从常规接受身体轮廓手术的患者获得包括皮肤和皮下脂肪(100
–
300cm2)的组织样本,并将其用于分离肥大细胞、成纤维细胞和角质形成细胞。皮肤在临床检查和组织学检验中都是不明显的。除去皮下组织和网状真皮,将剩余的分开厚度的皮肤切成0.5cm2的小块,置于2.4u/ml中性蛋白酶(dispase)ii(roche,维也纳,奥地利)中4℃过夜。分离表皮后,真皮在胶原酶i(gibco,维也纳,奥地利)中37℃消化2小时。cd117+肥大细胞用磁珠(macs系统;miltenyi biotec,bergisch gladbach,德国)按制造商的说明进行分离。为了提高回收细胞的纯度,从第一轮分离开始,对cd117+细胞重复进行磁分离。然后将cd117+肥大细胞接种在补充有10%fcs、青霉素/链霉素(均来自biochrom,berlin,德国)和100ng/ml重组人干细胞因子(peprotech,rocky hill,ny,美国)的dmem(gibco)中。分离肥大细胞后,cd117贴壁细胞(=成纤维细胞)如上述在已补料的rpmi 1640中培养。(gschwandtner等,2017)
[0043]
将hela ohio细胞或成纤维细胞铺在聚苯乙烯板上过夜(corning incorporated,corning,纽约,美国)。在第二天,细胞用hrv 14(属于b型鼻病毒种)感染,每个细胞感染指定量的50%组织培养感染剂量(tcid 50)的hrv 14(感染复数为3.5-10,取决于实验)。感染1小时后,细胞用37℃磷酸盐缓冲盐水(pbs)洗涤,用补充了指定浓度的指定试剂的培养基再温育6小时,然后进一步处理。为了评估细胞活力,用可固定的活力染料(65-0865-14;ebioscience,维也纳,奥地利)对细胞染色。
[0044]
蛋白质印迹分析:hela ohio细胞如上述感染。感染7小时后,细胞在冰上于0.5%triton-x缓冲液中裂解5分钟。裂解后,将悬液以13000
×
g离心5分钟,将上清液用于进一步分析。蛋白质印迹分析如前所述进行(gualdoni等,2015)。抗hrv vp1-3抗体和抗gapdh按1:1000稀释后使用。用ecl western印迹基板(thermo fisher scientific,waltham,ma)在las-4000(fujifilm,东京,日本)上进行检测。数据分析、量化和处理用fiji(imagej)图像处理软件进行。
[0045]
结果:
[0046]
2-脱氧葡萄糖强烈抑制hela细胞和原代人成纤维细胞中的hrv增殖(见图1a)。为了验证这种对增殖的影响,还对hela细胞中病毒蛋白(vp)1-3的表达所镜像反映的蛋白水平的病毒复制进行了分析,结果与rna水平的结果相似(图1a)。2-脱氧葡萄糖剂这种试剂在所用剂量下对细胞活力无可测量的影响(图2)。
[0047]
实施例2
–
鼠hrv感染模型
[0048]
所有动物实验方案均由维也纳医科大学动物伦理委员会评估,并获得经济和科学部批准(bmwfw-66.009/0356_wf/v/3b/2015)。根据实验室动物科学协会联合会的指导进行动物饲养和实验。所有实验均使用内部繁殖(in-house breeding)的6至8周龄雌性c57bl/6j小鼠(最初从the jackson laboratory,bar harbor,me,usa获得)。与本研究无关的动物护理专业人员将小鼠随机分配到各组中。
[0049]
实验按已发布的方案(bartlett等,2008)的微小改良版进行。小鼠用异氟烷使之镇静,鼻内接种5x10^6tcid50的hrv1b(属于a型鼻病毒种)的pbs溶液。同时鼻内给予溶于pbs的5mm 2-dg或单独的pbs。24小时后,对小鼠实施安乐死,进行支气管肺泡灌洗。获得一只肺叶用于pcr分析,另一只用于组织学检查。为了进行pcr分析,将材料匀浆,再用rneasy
canonical inflammasome activation.sci.rep.5,12016.
[0066]
kaiser,l.,aubert,j.-d.,pache,j.-c.,deffernez,c.,rochat,t.,garbino,j.,wunderli,w.,meylan,p.,yerly,s.,perrin,l.,et al.(2006).chronic rhinoviral infection in lung transplant recipients.am.j.respir.crit.care med.174,1392
–
1399.
[0067]
kang,hyun tae,and eun seong hwang."2-deoxyglucose:an anticancer and antiviral therapeutic,but not any more a low glucose mimetic."life sciences 78.12(2006):1392-1399.
[0068]
kilbourne,edwin d."inhibition of influenza virus multiplication with a glucose antimetabolite(2-deoxy-d-glucose)."nature 183.4656(1959):271-272.
[0069]
liu,m.,mallory,g.b.,schecter,m.g.,worley,s.,arrigain,s.,robertson,j.,elidemir,o.,and danziger-isakov,l.a.(2010).long-term impact of respiratoryviral infection after pediatric lung transplantation.pediatr.transplant.14,431
–
436.
[0070]
palmenberg,ann c.,et al."sequencing and analyses of all known humanrhinovirus genomes reveal structure and evolution."science 324.5923(2009):55-59.
[0071]
papi,a.,bellettato,c.m.,braccioni,f.,romagnoli,m.,casolari,p.,caramori,g.,fabbri,l.m.,and johnston,s.l.(2006).infections and airway inflammation inchronic obstructive pulmonary disease severe exacerbations.am.j.respir.crit.caremed.173,1114
–
1121.
[0072]
steinke,j.w.,and borish,l.(2016).immune responses in rhinovirus-inducedasthma exacerbations.curr.allergy asthma rep.16.
[0073]
sun,x.and whittaker,g.r.(2013)entry of influenza virus.adv.exp.med.biol.790,72
–
82
[0074]
watanabe,t.and kawaoka,y.(2015)influenza virus-host interactomes as abasis for antiviral drug development.curr.opin.virol.14,71
–
78.
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1