新型抗氧化抗炎和促脂质代谢协同纳米给药系统
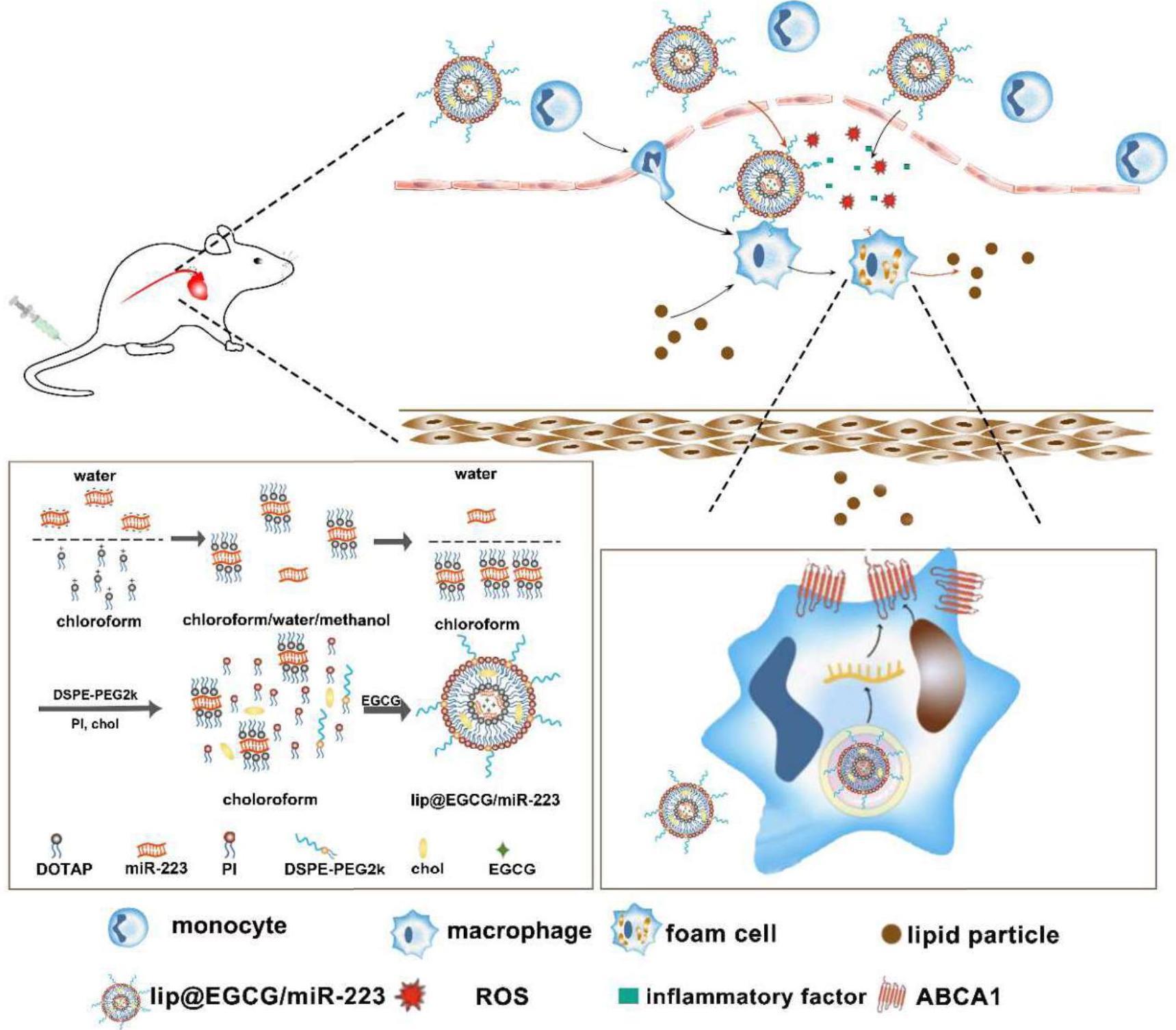
本发明涉及一种共载egcg和mir-223的新型递送体系lip@egcg/mir-223,及制备方法,纳米结构,属于生物医药学领域。涉及它的细胞摄取,涉及它的体外抗氧化抗炎和促脂质外排作用,涉及它上调abca1基因和蛋白的表达水平,进一步涉及基于apoe-/-建立动脉粥样硬化鼠的靶向作用与生长抑制作用,涉及其组织安全性相关指标。进而公开了它作为非病毒载体在动脉粥样硬化的基因治疗药物中的应用。属于生物医药学领域。
背景技术:
1、动脉粥样硬化(atherosclerosis,as)是一种慢性炎症性疾病,炎症是动脉粥样硬化发生和发展的重要诱因,抗氧化抗炎也是目前as治疗的重要研究方向。
2、在as炎症环境的诱导下单核细胞不断向病变部位蓄积,并且分化为巨噬细胞,炎症性巨噬细胞不断摄取被氧化的脂质而形成泡沫细胞,进而形成脂质斑块。因此,消除脂质斑块对于治疗as具有重要意义。
3、表没食子儿茶素没食子酸酯(epigallocatechin-3-gallate,egcg)是一种天然多酚类化合物,具有优异的抗氧化抗炎作用,有潜质成为治疗as的重要药物。但是egcg分子稳定性差,在储存和给药过程中容易分解而失效,此外,如何将egcg有效递送至作用部位也是应用过程中需要解决的问题。
4、近年来研究发现,microrna(mirna)在调节脂质代谢方面具有重要作用。作为mirna家族中的一员,mir-223可以通过上调atp结合盒转运体a1(atp-binding cassettetransporter a1,abca1)的水平促进脂质外排。但是裸mir-223因其分子量大和带负电的特性很难被递送至细胞内,且容易被体内核酸酶降解而失活,因此需要安全有效的载体用于mir-223的递送。
技术实现思路
1、本发明的目的在于提供一种具有靶向性的治疗动脉粥样硬化的基因药物递送系统:lip@egcg/mir-223。
2、本发明所述的载药系统,由上调as病变部位巨噬细胞内abca1水平的mir-223和具有抗氧化抗炎作用的药物表没食子儿茶素没食子酸酯的egcg制备而成。
3、本发明所述的靶向基因药物递送系统,dotap与mir-223的质量比为1:0.75。
4、本发明所述的载药系统lip@egcg/mir-223,为脂质体结构。
5、本发明的另一个目的在于提供载药系统lip@egcg/mir-223的制备方法。
6、本发明所述的制备方法,包括以下步骤:阳离子脂质dotap和mir-223结合,通过优化的薄膜水化法制备脂质体。
7、优选的,本发明所述载药系统的制备方法,包括以下步骤:
8、1)制备dotap-mir-223复合物:取dotap溶于氯仿,混合后加入甲醇混匀,加入mir-223和氯仿,离心提取含有dotap-mir-223复合物的有机相;
9、2)制备lip@egcg/mir-223:向dotap-mir-223复合物中加入pi、dspe-peg2k、吐温-80、chol和氯仿,旋蒸去除有机相,再加入egcg旋转水化,超声得到脂质体。
10、进一步优选的,
11、步骤1)制备dotap-mir-223复合物:
12、(1)取mir-223离心,溶于depc水中,取dotap,溶于的氯仿中,混合后加入甲醇,轻轻混匀以形成单相;其中dotap:mir-223=2-8:1-6,w/w;
13、(2)随后加入depc水溶液和氯仿以形成两个独立的相;
14、(3)离心提取,得到含有dotap-mir-223复合物的有机相。
15、步骤2)制备lip@egcg/mir-223:向dotap-mir-223复合物中加入pi、dspe-peg2k、吐温-80、胆固醇和氯仿,旋蒸去除有机相,再加入egcg水溶液旋转水化,超声得到脂质体。
16、更进一步优选的,载药系统的制备方法,包括以下步骤:
17、1)制备dotap-mir-223复合物的方法,步骤如下:
18、(1)取mir-223离心,溶于depc水中,取dotap(dotap:mir-223=4:3,w/w比),溶于的氯仿中,混合后加入甲醇,轻轻混匀以形成单相;
19、(2)室温下,摇床上孵育后,加入depc水和氯仿以形成两个独立的相;
20、(3)离心提取,得到含有dotap-mir-223复合物的有机相;
21、2)制备lip@egcg/mir-223的方法,步骤如下:
22、(1)向提取的dotap-mir-223复合物有机相中加入pi,dspe-peg2k,吐温-80,chol,转入旋蒸瓶中,再加入氯仿;
23、(2)旋蒸以除去有机相,瓶壁上形成一层薄膜;
24、(3)取egcg溶于depc水中,将egcg的水溶液加入旋蒸瓶中,旋转水化,水浴超声;
25、(4)先过微孔滤膜,然后通过聚碳酸酯膜收集,即得脂质体。
26、根据实施例之一,本发明所述的载药系统,制备方法如下:
27、1)制备dotap-mir-223复合物
28、(1)取mir-223 0.033mg(1od)离心2min(1500g)后,溶于200μl的depc水中,取dotap 0.044mg(dotap:mir-223=4:3,w/w比),溶于200μl的氯仿中,混合后加入400μl甲醇,轻轻混匀以形成单相。
29、(2)室温下,摇床上孵育30min后,加入200μl depc水和200μl氯仿以形成两个独立的相。
30、(3)以800g离心8min后,提取含有dotap-mir-223复合物的有机相。
31、2)制备lip@egcg/mir-223
32、(1)向提取的dotap-mir-223复合物有机相中加入pi 0.117mg,dspe-peg2k0.167mg,吐温-80 0.167mg,chol 0.217mg,转入旋蒸瓶中,再加入1ml氯仿。
33、(2)40℃下旋蒸20min以除去有机相,瓶壁上形成一层薄膜。
34、(3)取2mg egcg溶于1ml depc水中,将egcg的水溶液加入旋蒸瓶中,旋转水化30min。水浴超声5min,然后探头超声2min(功率:25%,超3s停3s)。
35、(4)先过0.22μm的微孔滤膜,然后通过100nm的聚碳酸酯膜挤出10次收集制得的脂质体。
36、本发明的另一个目的还在于提供载药系统在制备抑制动脉粥样硬化的药物中的应用
37、本发明的目的还在于提供载药系统lip@egcg/mir-223在制备体外抗氧化抗炎的药物中的应用。
38、本发明的目的还在于评价载药系统lip@egcg/mir-223的药物摄取效率。
39、本发明的目的还在于评价载药系统lip@egcg/mir-223的细胞毒和细胞抑制作用。
40、本发明的目的还在于评价载药系统lip@egcg/mir-223上调abca1基因和蛋白的作用。
41、本发明的目的还在于评价载药系统lip@egcg/mir-223靶向性至as病变部位,消除脂质斑块的作用。
42、对说明书中出现的以下词语作进一步的解释:
43、egcg:表没食子儿茶素没食子酸酯
44、mirna:大小为21-23个核苷酸的非编码rna
45、mir-223:mirna家族中的一员
46、abca1:atp结合盒转运蛋白a1
47、dox:阿霉素
48、lip:liposome,脂质体
49、lip@egcg/mir-223:共包载egcg和mir-223的脂质体药物载体
50、dotap:阳离子脂质
51、depc:焦碳酸二乙酯
52、pi:碘化丙啶
53、dspe-peg2k:二硬脂酰基磷脂酰乙醇胺-聚乙二醇2000
54、chol:胆固醇
55、pdi:聚合物分散性指数
56、elisa:酶联免疫吸附测定
57、cy5:花青染料荧光标记
58、pbs:phosphate buffer saline,磷酸缓冲盐溶液
59、edta:乙二胺四乙酸
60、mtt:3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐
61、dmso:二甲基亚砜
62、real time-qpcr:实时定量逆转录-聚合酶链式反应
63、od值:光密度值。
- 还没有人留言评论。精彩留言会获得点赞!