一种基于光量子计算机的分子对接方法和装置与流程
本发明涉及药物设计,尤其涉及一种基于光量子计算机的分子对接方法和装置。
背景技术:
1、传统的药物筛选是一个十分昂贵且需要消耗大量资源的过程,一般需要花费数十亿美元,而成功率则越10%。近年来,随着功能强大的分子建模工具的发展以及蛋白质小分子复合物解析结构的数目的增长,基于结构的药物设计成为新药开发中必不可少的工具。分子对接研究的重点是通过计算模拟分子识别过程。该识别过程旨在模拟蛋白质和配体之间的最佳构象,使整个系统的自由能最小化是药物筛选前期过程中的十分重要的一个环节,借助分子对接可以加快药物研发进程。
2、在制药领域的传统模型的筛选方式大多数采用启发式算法以及系统搜索算法,耗时长,且可能无法计算出最优解,在药物研发过程中假阳性居高。其缺点如下:
3、(1)使用启发式算法:需要大量的时间来进行迭代,有可能无法求出最优解,计算量大。
4、(2)使用系统搜索算法则可能面临组合爆炸的问题,传统计算机处理此类问题的能力较弱。
5、传统模型需要大量的采样才可以拿到一个能量较低的构象,且此构象有可能并非全局最优解。
技术实现思路
1、鉴于上述的分析,本发明实施例旨在提供一种基于光量子计算机的分子对接方法和装置,用以解决启发式算法消耗时间长但无法得出标准解等问题。
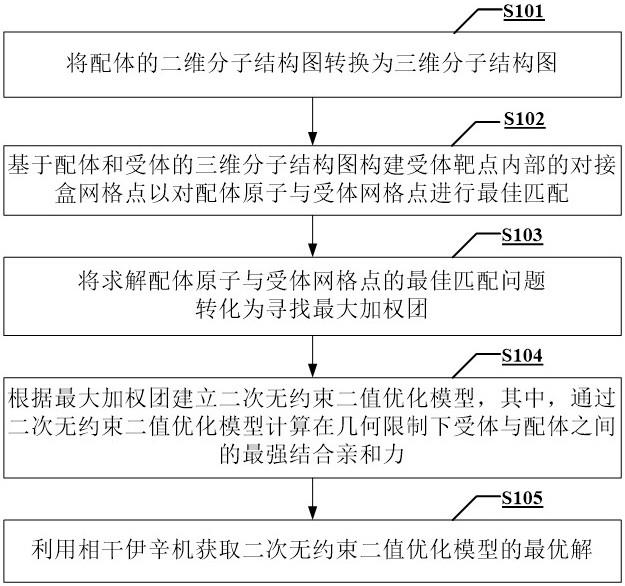
2、一方面,本发明实施例提供了一种基于光量子计算机的分子对接方法,包括:将配体的二维分子结构图转换为三维分子结构图;基于配体和受体的三维分子结构图构建受体靶点内部的对接盒网格点以对配体原子与受体网格点进行最佳匹配;将求解所述配体原子与所述受体网格点的最佳匹配问题转化为寻找最大加权团;根据所述最大加权团建立二次无约束二值优化模型,其中,通过所述二次无约束二值优化模型计算在几何限制下受体与配体之间的最强结合亲和力;以及利用相干伊辛机获取所述二次无约束二值优化模型的最优解。
3、上述技术方案的有益效果如下:根据本技术实施例的基于光量子计算机的分子对接方法使用伊辛模型求解分子模拟问题的方法更为快速和准确。使用量子计算机进行加速,可以快速的计算药物和蛋白的亲和力,帮助研究人员筛选出潜在的先导化合物,助力药物研发过程。
4、基于上述方法的进一步改进,基于配体和受体的三维分子结构图构建受体靶点内部的对接盒网格点以对配体原子与受体网格点进行最佳匹配包括:根据配体大小在受体结构空间上构建连续的对接盒;在网格点匹配过程中,将所述受体的对接盒离散为等距的网格点;将配体的每个原子放置在一个网格点上以将所述配体的每个原子与受体网格点进行匹配;以及通过将匹配结果与最佳匹配结果之间的差值最小化实现受体与配体的对接姿势。
5、基于上述方法的进一步改进,通过将匹配结果与最佳匹配结果的之间的差值最小化实现受体与配体的对接姿势包括通过以下公式表示所述配体与所述受体的对接姿势:;
6、其中, r表示所述受体与所述配体的一种可能匹配, r grid表示所述受体与所述配体的最佳匹配,‖ r- r grid‖是所述可能匹配与所述最佳匹配的差值距离,表示在所有匹配中选择一个可能匹配使得所述差值距离最小化。
7、基于上述方法的进一步改进,对配体原子与受体网格点进行最佳匹配包括当满足以下约束项1和约束项2时,确定两个顶点的匹配共存,链接所述两个顶点:所述约束项1:受体对接盒网格点与配体原子之间的距离偏差小于可调阈值参数;以及所述约束项2:一个配体原子仅与一个网格点匹配,其中,每个顶点表示一个可能的匹配。
8、基于上述方法的进一步改进,受体对接盒网格点与配体原子之间的距离偏差小于可调阈值参数包括:对于顶点集v中的两个顶点( a i, p j)和( a k, p l),当满足以下两个约束时对所述两个顶点加边:|‖ r i- r k‖-‖ pr j -pr l‖|< c dist, 其中, c dist为可调阈值参数,双竖线表示距离,单竖线表示绝对值,所述约束1表示当相对距离与配体形状协调时,两种匹配共存;以及一个配体原子仅与一个网格点匹配包括: p j≠ p l,使得一个配体原子与一个网格点匹配;其中, a={ a i}为配体中的原子集合, t i和 r i分别为原子 a i的类型和坐标, p={ p i}为对接盒网格点集合, p i的坐标是 pr i,顶点集v={( a i, p j)| van( t i, p j)<0}, van( t i, p j)是原子类型 t i放置在网格点 d i上时的范德华瓦尔斯能量,每个顶点表示一个可能的匹配。
9、基于上述方法的进一步改进,根据所述最大加权团建立二次无约束二值优化模型,其中,通过所述二次无约束二值优化模型计算在几何限制下受体与配体之间的最强结合亲和力包括通过以下公式计算能量点以获得打分函数:
10、;
11、其中,为决策变量,取值为{0,1},表示原子 a i是否放在网格顶点 d j的位置,如果是则为1,否则为0;为顶点( a i, d j)的权重,公式中的第二项和第三项分别对应约束项1和约束项2, 其中 k dist、 k mono分别为两项的惩罚系数;公式中的第一项意味着加权顶点越多越好,如果( a i, d j)和( a k, d l)符合约束项1,则,否则,类似地,如果( a i, d j)和( a k, d l)符合约束项2, 则,否则,, k dist、 k mono和 c dist为三个可调参数。
12、基于上述方法的进一步改进,利用相干伊辛机获取所述二次无约束二值优化模块的最优解包括:将所述二次无约束二值优化模块转换为伊辛模型;将所述伊辛模型编码成一组光学脉冲的幅值和相位;利用干涉效应将不同自旋之间的耦合关系传递给光学干涉;以及使用非线性光学效应将光脉冲转换为对应自旋的取值以获得所述二次无约束二值优化模块的最优解。
13、另一方面,本发明实施例提供了一种基于光量子计算机的分子对接装置,包括:分子结构转换模块,用于将配体的二维分子结构图转换为三维分子结构图;匹配模块,用于基于配体和受体的三维分子结构图构建受体靶点内部的对接盒网格点以对配体原子与受体网格点进行最佳匹配;问题转换模块,用于将求解所述配体原子与所述受体网格点的最佳匹配问题转化为寻找最大加权团;模型生成模块,用于根据所述最大加权团问题建立二次无约束二值优化模型,其中,通过所述二次无约束二值优化模型计算在几何限制下受体与配体之间的最强结合亲和力;以及模型求解模块,用于利用相干伊辛机获取所述二次无约束二值优化模块的最优解。
14、基于上述装置的进一步改进,匹配模块用于:对接网格盒构建子模块,用于根据配体大小在受体结构空间上构建连续的对接盒;离散子模块,用于在网格点匹配过程中,将所述受体的对接盒离散为等距的网格点;受配体匹配子模块,用于将配体的每个原子放置在一个网格点上以将所述配体的每个原子与受体网格点进行匹配;以及对接子模块,用于通过将匹配结果与最佳匹配结果之间的差值最小化实现受体与配体的对接姿势。
15、基于上述装置的进一步改进,对接子模块用于通过以下公式表示所述配体与所述受体的对接姿势:
16、;
17、其中, r表示所述受体与所述配体的一种可能匹配, r grid表示所述受体与所述配体的最佳匹配,‖ r- r grid‖是所述可能匹配与所述最佳匹配的差值距离,表示在所有匹配中选择一个可能匹配使得所述差值距离最小化。
18、与现有技术相比,本发明至少可实现如下有益效果之一:
19、1、根据本技术实施例的基于光量子计算机的分子对接方法使用伊辛模型求解分子模拟问题的方法更为快速和准确。
20、2、使用量子计算机进行加速,可以快速的计算药物和蛋白的亲和力,帮助研究人员筛选出潜在的先导化合物,助力药物研发过程。
21、3、本技术利用量子计算机的纠缠态和重叠态以及全联接的特性,提出了一个更为优秀的求解分子结合模式的模型,并将其放置于web端以进行展示,供给用户使用。
22、本发明中,上述各技术方案之间还可以相互组合,以实现更多的优选组合方案。本发明的其他特征和优点将在随后的说明书中阐述,并且,部分优点可从说明书中变得显而易见,或者通过实施本发明而了解。本发明的目的和其他优点可通过说明书以及附图中所特别指出的内容中来实现和获得。
- 还没有人留言评论。精彩留言会获得点赞!