一种稳定的丁苯酞口服溶液及其制备方法和应用与流程
本发明属于药物制剂,具体涉及一种丁苯酞口服溶液及其制备方法和应用。
背景技术:
1、丁苯酞(3-n-butylphthalide,简称nbp),化学名为3-丁基-1(h)-异苯并呋喃酮,化学结构式如下:
2、。
3、现有技术报告的丁苯酞具有多种确证用途,如治疗和/或预防脑缺血性疾病、肾病等;其中肾病包含急性或慢性肾功能不全、脑卒中合并伴有肾功能不全、肾衰竭等,脑缺血性疾病包括缺血性脑卒中,示例性包括但不限于轻、中、重度急性缺血性脑卒中等。尤其针对中度至重度急性脑缺血性疾病,患者极易出现昏迷、意识障碍、瘫痪、肢体麻木等症状,致使患者吞噎困难或无法经口进食,因此传统常规的口服固体制剂如片剂、胶囊剂或口服冻干粉等则不再适用。而目前我国上市的丁苯酞口服制剂,仅为石药集团的丁苯酞软胶囊(恩必普®),其单剂量规格高达200mg,人体血药浓度cmax较低,最高血药达峰时间tmax约需1.5小时;因此软胶囊无论从患者顺应性角度还是从紧急治疗效果角度,均不能满足该类疾病的治疗需求,因此,开发一种顺应性好、起效快、药效更好的丁苯酞口服溶液的液体制剂符合解决临床痛点的迫切需求。
4、此外,由于丁苯酞不溶于水,制备丁苯酞液体制剂时,首要考虑要素为增溶剂的选择。虽然现有技术讨论了大量环糊精及其衍生物的增溶能力,其中尤以羟丙基-β-环糊精和磺丁酰基倍他环糊精钠的增溶效果受到本领域的极大关注,而石药集团上市的丁苯酞氯化钠注射液也证明了羟丙基-β-环糊精的安全性。但是现有技术并没有记载任何关于这类环糊精衍生物包合丁苯酞后所形成的丁苯酞-环糊精包合物是否具有稳定释放丁苯酞的效果研究,而丁苯酞的稳定释放对于上述疾病的治疗尤其中度至重度急性缺血性脑卒中的治疗至关重要。
5、因此,开发一种不仅易于送服、起效快、疗效显著而且疗效持续稳定的丁苯酞口服溶液,提高丁苯酞治疗本领域疾病特殊情况的可靠性,是保证丁苯酞临床疗效的关键。
技术实现思路
1、为了解决现有技术存在的问题,本发明提供一种丁苯酞口服溶液,并通过控制剂量和粒径,以达到的提供一种起效快、疗效显著而且疗效持续稳定的丁苯酞口服溶液。
2、本发明提供一种丁苯酞在制备用于治疗和/或预防缺血性脑卒中的口服溶液制剂中的用途,所述口服溶液包括治疗有效量的丁苯酞和药学上可接受辅料,所述治疗有效量是单次每日剂量,在对人类受试者给予后,对于每1mg的丁苯酞,该单次每日剂量达到从1.2ng/ml至3.2ng/ml的平均cmax,所述单次每日剂量为120mg~160mg。
3、进一步地,上述单次每日剂量为125mg~160mg。
4、进一步地,在对人类受试者给予后,对于每1mg的丁苯酞,上述单次每日剂量达到从1.7ng/ml至3.2ng/ml的平均cmax。
5、进一步地,在对人类受试者给予后,对于每1mg的丁苯酞,上述单次每日剂量达到从1.5ng/ml至2.6ng/ml的平均cmax;优选为2.2ng/ml至2.6ng/ml的平均cmax。
6、进一步地,上述缺血性脑卒中包括轻、中、重度急性缺血性脑卒中。
7、进一步地,上述丁苯酞为环糊精或其衍生物的包合物,所述包合物粒径为1nm~8nm,优选为3nm~6nm。
8、进一步地,上述包合物粒径的强度峰面积不低于90%,优选不低于95%。
9、进一步地,上述环糊精或其衍生物为羟丙基-β-环糊精,所述丁苯酞与羟丙基-β-环糊精的质量比为1:19~25,优选为1:20~24。
10、进一步地,上述药学上可接受辅料为包合辅料,所述包合辅料包含无机盐、酸度剂。
11、进一步地,上述无机盐包含氯化钠、氯化钾、氯化锂、氯化镁、氯化铵、氯化铝、氯化亚铁、氯化铁、硫酸钠、硫酸镁、硫酸铵、碳酸钠或聚磷酸钠。
12、进一步地,上述酸度剂包含盐酸、硫酸、磷酸、醋酸、冰醋酸或缓冲对。
13、进一步地,上述缓冲对包含枸橼酸和枸橼酸盐、柠檬酸和磷酸盐、乳酸和乳酸盐、磷酸和磷酸盐、醋酸和醋酸盐、或酒石酸和酒石酸盐。示例性包括但不限于枸橼酸-枸橼酸钠、枸橼酸-枸橼酸钾、柠檬酸-柠檬酸二钠、柠檬酸-柠檬酸三钠、柠檬酸-磷酸氢二钠、乳酸-乳酸钠、磷酸-磷酸二氢钠、磷酸-磷酸氢二钠、醋酸-醋酸钠、或酒石酸-酒石酸钠。
14、进一步地,上述无机盐与丁苯酞的质量比为0.05~1.0:1,优选为0.2~0.7:1。
15、进一步地,上述酸度剂与丁苯酞的质量比为0.01~0.15:1。
16、进一步地,上述口服溶液的ph值为3.5~5.5,优选为4.0~5.0。
17、进一步地,上述口服溶液还包括矫味剂;所述矫味剂包括甜味剂、香精、酸味剂、咸味剂中的一种或多种。
18、进一步地,上述甜味剂包括三氯蔗糖、葡萄糖、白砂糖、甜菊糖苷、安赛蜜、木糖醇或阿斯巴甜;上述香精包括甜橙香精、苹果香精、桔子香精、香蕉香精或柠檬香精。
19、进一步地,上述口服溶液的制备方法包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌下一次性或分批加入处方量的环糊精或其衍生物和药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降温得包合物溶液,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
20、优选地,上述口服溶液的制备方法包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌加入处方量的环糊精或其衍生物使完全溶解,加入药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降温得包合物溶液,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
21、进一步地,上述口服溶液的制备方法包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌下一次性或分批加入处方量的环糊精或其衍生物和药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降温得包合物溶液;另取不超处方量10%的水,加入矫味剂,全部溶解后加至包合物溶液中,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
22、优选地,上述口服溶液的制备方法包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌加入处方量的环糊精或其衍生物使完全溶解,加入药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降温得包合物溶液;另取不超处方量10%的水,加入矫味剂,全部溶解后加至包合物溶液中,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
23、进一步地,上述治疗有效量是单次120mg每日剂量,并且其中所述单次每日剂量达到在175ng/ml的80%至125%范围内的平均cmax。
24、进一步地,上述治疗有效量是单次125mg每日剂量,并且其中所述单次每日剂量达到在272ng/ml的80%至125%范围内的平均cmax。
25、进一步地,上述治疗有效量是单次136mg每日剂量,并且其中所述单次每日剂量达到在304ng/ml的80%至125%范围内的平均cmax。
26、进一步地,上述治疗有效量是单次160mg每日剂量,并且其中所述单次每日剂量达到在410ng/ml的80%至125%范围内的平均cmax。
27、进一步地,上述治疗有效量是单次120mg每日剂量,并且其中所述单次每日剂量达到在308h*ng/ml的80%至125%范围内的平均auc(0-24h)或平均auc(0-t)。
28、进一步地,上述治疗有效量是单次125mg每日剂量,并且其中所述单次每日剂量达到从310 h*ng/ml的80%至125%范围内的平均auc(0-24h)或平均auc(0-t)。
29、进一步地,上述治疗有效量是单次136mg每日剂量,并且其中所述单次每日剂量达到从332h*ng/ml的80%至125%范围内的平均auc(0-24h)或平均auc(0-t)。
30、进一步地,上述治疗有效量是单次160mg每日剂量,并且其中所述单次每日剂量达到从478h*ng/ml的80%至125%范围内的平均auc(0-24h)或平均auc(0-t)。
31、进一步地,上述治疗有效量是单次120mg每日剂量,并且其中所述单次每日剂量达到在338h*ng/ml的80%至125%范围内的平均auc(0-inf)。
32、进一步地,上述治疗有效量是单次125mg每日剂量,并且其中所述单次每日剂量达到在340h*ng/ml的80%至125%范围内的平均auc(0-inf)。
33、进一步地,上述治疗有效量是单次136mg每日剂量,并且其中所述单次每日剂量达到在367h*ng/ml的80%至125%范围内的平均auc(0-inf)。
34、进一步地,上述治疗有效量是单次160mg每日剂量,并且其中所述单次每日剂量达到在514h*ng/ml的80%至125%范围内的平均auc(0-inf)。
35、本发明还提供一种用于制备治疗和/或预防疾病的丁苯酞口服溶液,所述口服溶液包括治疗有效量的丁苯酞和药学上可接受辅料,所述丁苯酞为环糊精或其衍生物的包合物,所述包合物粒径为1nm~8nm,丁苯酞的规格为120mg~160mg。
36、进一步地,上述丁苯酞的规格为125~160mg。
37、进一步地,上述包合物粒径的强度峰面积不低于90%,优选不低于95%。
38、进一步地,上述包合物粒径为3nm~6nm。
39、进一步地,上述环糊精或其衍生物为羟丙基-β-环糊精,所述丁苯酞与羟丙基-β-环糊精的质量比为1:19~25,优选为1:20~24。
40、进一步地,上述药学上可接受辅料为包合辅料,所述包合辅料包括无机盐、酸度剂。
41、进一步地,上述无机盐包含氯化钠、氯化钾、氯化锂、氯化镁、氯化铵、氯化铝、氯化亚铁、氯化铁、硫酸钠、硫酸镁、硫酸铵、碳酸钠或聚磷酸钠。
42、进一步地,上所述酸度剂包含盐酸、硫酸、磷酸、醋酸、冰醋酸或缓冲对。
43、进一步地,上述缓冲对包含枸橼酸和枸橼酸盐、柠檬酸和磷酸盐、乳酸和乳酸盐、磷酸和磷酸盐、醋酸和醋酸盐、或酒石酸和酒石酸盐。示例性包括但不限于枸橼酸-枸橼酸钠、枸橼酸-枸橼酸钾、柠檬酸-柠檬酸二钠、柠檬酸-柠檬酸三钠、柠檬酸-磷酸氢二钠、乳酸-乳酸钠、磷酸-磷酸二氢钠、磷酸-磷酸氢二钠、醋酸-醋酸钠、或酒石酸-酒石酸钠。
44、进一步地,上述无机盐与丁苯酞的质量比为0.05~1.0:1,优选为0.2~0.7:1。
45、进一步地,上所述酸度剂与丁苯酞的质量比为0.01~0.15:1。
46、进一步地,上述口服溶液的ph值为3.5~5.5,优选为4.0~5.0。
47、进一步地,上述口服溶液还包括矫味剂;所述矫味剂包括甜味剂、香精、酸味剂、咸味剂中的一种或多种。
48、进一步地,上述甜味剂包括三氯蔗糖、葡萄糖、白砂糖、甜菊糖苷、安赛蜜、木糖醇、蔗糖、果糖、低聚果糖、麦芽糖、淀粉糖、乳糖、糖精或阿斯巴甜;上述香精包括甜橙香精、苹果香精、桔子香精、香蕉香精或柠檬香精。
49、进一步地,上述口服溶液的制备方法,包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌下一次性或分批加入处方量的环糊精或其衍生物和药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降温得包合物溶液,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
50、优选地,上述口服溶液的制备方法包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌加入处方量的环糊精或其衍生物使完全溶解,加入药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降至室温得包合物溶液,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
51、进一步地,上述口服溶液的制备方法包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌下一次性或分批加入处方量的环糊精或其衍生物和药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降温得包合物溶液;另取不超处方量10%的水,加入矫味剂,全部溶解后加至包合物溶液中,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
52、优选地,上述口服溶液的制备方法包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌加入处方量的环糊精或其衍生物使完全溶解,加入药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降温得包合物溶液;另取不超处方量10%的水,加入矫味剂,全部溶解后加至包合物溶液中,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
53、进一步地,上述口服溶液中,所述治疗有效量是单次每日剂量,在对人类受试者给予后,对于每1mg的丁苯酞,该单次每日剂量达到从1.2ng/ml至3.2ng/ml的平均cmax;优选为从1.7ng/ml至3.2ng/ml的平均cmax;更优选为从2.2ng/ml至2.6ng/ml的平均cmax。
54、进一步地,上述口服溶液中,所述治疗有效量是单次每日剂量,在对人类受试者给予后,对于每1mg的丁苯酞,该单次每日剂量达到从1.2ng/ml至3.2ng/ml的平均cmax;优选为从1.5ng/ml至2.6ng/ml的平均cmax;更优选为从2.2ng/ml至2.6ng/ml的平均cmax。
55、进一步地,上述口服溶液中,所述治疗有效量是单次120mg每日剂量,并且其中所述单次每日剂量达到在175ng/ml的80%至125%范围内的平均cmax。
56、进一步地,上述口服溶液中,所述治疗有效量是单次125mg每日剂量,并且其中所述单次每日剂量达到在272ng/ml的80%至125%范围内的平均cmax。
57、进一步地,上述口服溶液中,所述治疗有效量是单次136mg每日剂量,并且其中所述单次每日剂量达到在304ng/ml的80%至125%范围内的平均cmax。
58、进一步地,上述口服溶液中,所述治疗有效量是单次160mg每日剂量,并且其中所述单次每日剂量达到在410ng/ml的80%至125%范围内的平均cmax。
59、进一步地,上述口服溶液中,所述治疗有效量是单次120mg每日剂量,并且其中所述单次每日剂量达到从308h*ng/ml的80%至125%范围内的平均auc(0-24h)或平均auc(0-t)。
60、进一步地,上述口服溶液中,所述治疗有效量是单次125mg每日剂量,并且其中所述单次每日剂量达到从310h*ng/ml的80%至125%范围内的平均auc(0-24h)或平均auc(0-t)。
61、进一步地,上述口服溶液中,所述治疗有效量是单次136mg每日剂量,并且其中所述单次每日剂量达到从332h*ng/ml的80%至125%范围内的平均auc(0-24h)或平均auc(0-t)。
62、进一步地,上述口服溶液中,所述治疗有效量是单次160mg每日剂量,并且其中所述单次每日剂量达到从478h*ng/ml的80%至125%范围内的平均auc(0-24h)或平均auc(0-t)。
63、进一步地,上述口服溶液中,所述治疗有效量是单次120mg每日剂量,并且其中所述单次每日剂量达到在338h*ng/ml的80%至125%范围内的平均auc(0-inf)。
64、进一步地,上述口服溶液中,所述治疗有效量是单次125mg每日剂量,并且其中所述单次每日剂量达到在340h*ng/ml的80%至125%范围内的平均auc(0-inf)。
65、进一步地,上述口服溶液中,所述治疗有效量是单次136mg每日剂量,并且其中所述单次每日剂量达到在367h*ng/ml的80%至125%范围内的平均auc(0-inf)。
66、进一步地,上述口服溶液中,所述治疗有效量是单次160mg每日剂量,并且其中所述单次每日剂量达到在514h*ng/ml的80%至125%范围内的平均auc(0-inf)。
67、进一步地,上述口服溶液中,所述疾病包含脑缺血性疾病、老年痴呆症或肾病;优选地,所述脑缺血性疾病包含缺血性脑卒中;优选为轻、中、重度急性缺血性脑卒中。
68、此外,本发明还提供上述口服溶液的制备方法,包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌下一次性或分批加入处方量的环糊精或其衍生物和药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降温得包合物溶液,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
69、优选地,上述方法包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌加入处方量的环糊精或其衍生物使完全溶解,加入药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降至室温得包合物溶液,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
70、进一步地,上述方法包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌下一次性或分批加入处方量的环糊精或其衍生物和药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降温得包合物溶液;另取不超处方量10%的水,加入矫味剂,全部溶解后加至包合物溶液中,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
71、优选地,上述方法包括如下步骤:取处方量50%~80%水加热至75℃~90℃,搅拌加入处方量的环糊精或其衍生物使完全溶解,加入药学上可接受辅料,搅拌使完全溶解,加入丁苯酞,于65~90℃搅拌90~150分钟以上,降温得包合物溶液;另取不超处方量10%的水,加入矫味剂,全部溶解后加至包合物溶液中,补水定容至全量,搅拌混匀,调节溶液ph至目标值,过滤,灌装,灭菌。
72、进一步地,上述“降温得包合物溶液”中的降温优选降至室温。
73、特别说明:
74、本发明所述“丁苯酞”包括但不限于消旋丁苯酞、左旋丁苯酞。在具体处方中丁苯酞的质量均以c12h14o2计算。
75、本发明所述水包括但不限于纯化水、超纯水、蒸馏水。
76、本发明所述室温指:20℃~35℃,优选25℃~30℃。
77、本发明所述auc(0-inf)中的“inf”指无穷的英文单词“infinite”的缩写。
78、本发明所述丁苯酞口服溶液的容器包括但不限于为钠钙玻璃管制口服液体瓶、低硼硅玻璃管制口服液体瓶、中硼硅玻璃管制口服液体瓶、口服液体药用聚酯瓶、口服液体药用聚丙烯瓶、口服液体药用高密度聚乙烯瓶等。上述丁苯酞口服溶液的容器为无色或者棕色。
79、本发明所述的“以上”或“以下”均包含本数;“不超”、“不超过”不包含本数。
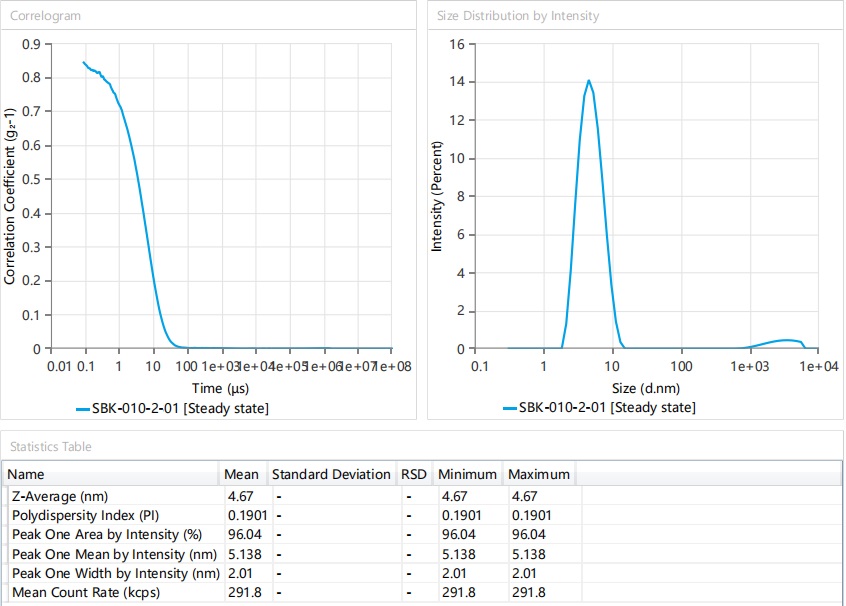
80、羟丙基-β-环糊精为口袋样结构,口袋外侧具有亲水性,内侧具有亲脂性;因此将水不溶性物质包裹在其口袋结构形成药物-环糊精包合物后可以增强不溶性物质的水溶解性。但经研究发现,为了达到丁苯酞的完全溶解(澄清溶液状态),羟丙基-β-环糊精的摩尔用量需要达到丁苯酞摩尔用量的2倍以上,也即意味着丁苯酞-羟丙基-β-环糊精包合物并非理想的1:1分子状态,而是两个或两个以上环糊精或药物-环糊精包合分子的聚集体形式或者其他形式的包合物。在某些情况下,这些包合物能产生乳光,但大多数情况下包合物的粒径还是比可见光波长小很多,因而只是以澄清溶液存在。对于澄清溶液状态,通常认为其为均质的流体,因此药品注册一般不对澄清的液体制剂进行粒径研究,而现有技术也未见任何关于丁苯酞液体制剂方面的粒径研究。但是,对于丁苯酞的口服溶液,本技术人意料之外地惊讶发现,丁苯酞口服溶液中包合物的粒径是影响丁苯酞口服溶液生物利用度稳定性的关键因素,当包合物粒径不超10nm时,不同0天样品的体内cmax、tmax、auc参数水平相似,但是当同时控制粒径及其强度峰面积(peak one area by intensity)时,不同粒径下的丁苯酞口服溶液的生物利用度稳定性则显示出巨大差异。
81、有益效果:一方面,本发明的丁苯酞口服溶液采用1nm~8nm的包合物粒径,可以稳定提高生物利用度,且起效更快、质量稳定、疗效可靠。相较于参比制剂(丁苯酞软胶囊,恩必普®),本发明的125mg的丁苯酞口服溶液即能达到与参比制剂等效的auc水平,但cmax远高于参比制剂,且tmax更小,起效更快,生物利用度更高,保证了治疗效果。尤其本发明的丁苯酞口服溶液经过长达三年的稳定性考察后,同时控制包合物粒径及其强度峰面积不低于90%时,丁苯酞口服溶液的各项生物利用度参数稳定不变,疗效稳定可靠,更适用于本领域疾病的特殊治疗需求。另一方面,本技术首次发现通过在环糊精包合丁苯酞形成丁苯酞-环糊精包合物的过程中加入无机盐和酸度剂,有利于控制包合物粒径的大小,以及粒径稳定性,使得本发明的丁苯酞口服溶液的制备过程无需考虑制备粒径的复杂设备或工艺要求,更适合工业化放大生产。
- 还没有人留言评论。精彩留言会获得点赞!