一种枸橼酸托法替布药物组合物的制作方法
本发明属于药物,具体涉及一种枸橼酸托法替布外用药物组合物。
背景技术:
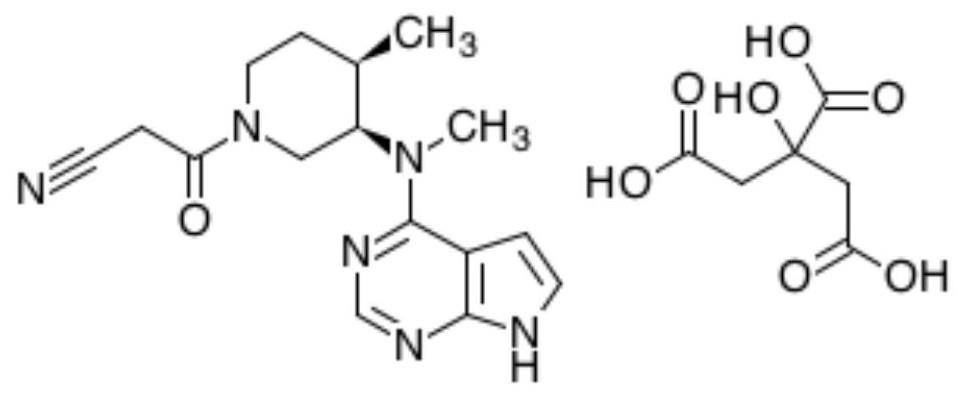
1、枸橼酸托法替布,化学名为(3r,4r)-4-甲基-3- (甲基-7h-吡咯并 [2,3-d]嘧啶-4-基氨基)-β-氧代-1-哌啶丙腈枸橼酸盐。
2、化学结构式:
3、
4、枸橼酸托法替布由美国辉瑞公司研发,作为jak抑制剂,可治疗多种自身免疫性疾病,目前,枸橼酸托法替布已在美国以商标名xeljanz®和 xeljanz®xr获批。xeljanz®为含 8mg枸橼酸托法替布 (相当于5mg托法替布)的速释片剂形式,且一天施用两次。xeljanz®xr以含 17.77mg或35.54mg的枸橼酸托法替布(相当于11mg或22mg托法替布)的缓释片剂形式获批。另外,xeljanz®新增一种1mg/ml的口服溶液,用于幼年特发性关节炎。
5、枸橼酸托法替布片可用于治疗对甲氨蝶呤反应不足或不耐受的中度至重度活动性类风湿关节炎成年患者。但口服枸橼酸托法替布片会引起多种系统性副作用如严重感染、肺结核、恶性肿瘤和淋巴增生性疾病、病毒活化、非黑色素皮肤癌、胃肠道穿孔、淋巴球减少症、嗜中性白血球减少症等。基于口服jak抑制剂的副作用较大,开发适用于斑秃、白癜风、特应性皮炎、银屑病等不需要太多全身暴露即可达到治疗作用的皮肤外用制剂显得尤为重要。目前,已有jak抑制剂获批用于治疗炎性皮肤疾病,如迪高替尼软膏已在日本获批上市治疗特应性皮炎,磷酸芦可替尼乳膏在美国获批用于特应性皮炎和白癜风的治疗。
6、当前已有多篇托法替布的外用制剂专利公开。专利cn 113730335 a公开了一种托法替布外用药物组合物,使用了过氧化值小于5且分子量低于700的聚乙二醇作为溶剂,以期望解决化合物稳定性差的问题。该组合物为无水油性软膏,有强烈的油腻感,使用依从性差。
7、专利cn103459394b公开了包含托法替布和渗透增强剂油醇的药物组合物的专利,此药物组合物以局部软膏的制剂形式治疗多种疾病,但存在药物化学稳定性差的问题。
8、专利cn113712900a公开了含有枸橼酸托法替布、聚西托醇和基质的外用油性软膏制剂,同样有强烈的油腻感,使用依从性差。
9、专利cn113975280b公开了一种含酒石酸托法替尼和促渗剂为二乙二醇单乙基醚与聚甘油脂肪酸酯的药物组合物,需要重新开发化合物的盐形。
10、专利cn111670036a公开了包含托法替尼的局部调配物,药物处方中使用了大量的二甲基亚砜(dmso)。dmso有大蒜的臭味,对皮肤有一定刺激性,易引起皮肤发红、灼痛、瘙痒和荨麻疹等问题,全身症状包括恶心、呕吐、发冷、抽筋和嗜睡。
11、专利cn116262119a公开了一种托法替布外用软膏的制备方法,为无水油性软膏,同样有强烈的油腻感,使用依从性差。
12、因枸橼酸托法替布的脂溶性较差,在ph近中性的水性基质中稳定性差等特点,开发无刺激性、无油腻感且透皮效果较好的枸橼酸托法替布外用制剂具有更高的难度和挑战。
技术实现思路
1、本发明的目的是制备一种无皮肤刺激性,无油腻感,稳定的含枸橼酸托法替布的局部用药组合物。该组合物安全性高、具有显著的抗炎效果,可用于治疗和预防包括特应性皮炎、节结性痒疹、白癜风、硬皮病、银屑病和斑秃等多种自身免疫性疾病。
2、本技术的一种药物组合物,其包含基于所述药物组合物的总重量的如下组分:
3、0.3wt%~5.0 wt %的枸橼酸托法替布;
4、1.0 wt %~70.0 wt %的促透剂;
5、0.05 wt %~5 wt %的基质;
6、0.02 wt %~2.0 wt %的稳定剂和/或抗氧剂;和
7、20 wt %~70 wt %的溶剂。
8、在一种实施方式中,所述促透剂选自油醇、油酸、氮酮、肉豆蔻酸异丙酯、二乙二醇单乙醚、碳酸丙烯酯、聚甘油脂肪酸酯、中链甘油三酯、乙醇、丙二醇中的一种或多种。
9、在一种实施方式中,所述促透剂选自肉豆蔻酸异丙酯、碳酸丙烯酯、二乙二醇单乙醚和丙二醇中的一种或多种。
10、在一种实施方式中,所述促透剂为二乙二醇单乙醚或丙二醇或者二乙二醇单乙醚与丙二醇的组合,其中,
11、当存在时,二乙二醇单乙醚的量为1.0wt%~20.0 wt %,基于所述药物组合物的总重量;和/或
12、当存在时,丙二醇的量为1.0 wt %~50.0 wt%,基于所述药物组合物的总重量。
13、在一种实施方式中,所述促透剂选自二乙二醇单乙醚和丙二醇中的一种或两种,其中,
14、当存在时,二乙二醇单乙醚的量为1.0wt%~15.0 wt %,基于所述药物组合物的总重量;和/或
15、当存在时,丙二醇的量为10.0 wt %~40.0 wt%,基于所述药物组合物的总重量。
16、在一种实施方式中,所述促透剂为二乙二醇单乙醚或丙二醇或者二乙二醇单乙醚与丙二醇的组合,其中,
17、当存在时,二乙二醇单乙醚的量为1.0wt%~15.0 wt %,基于所述药物组合物的总重量;和/或
18、当存在时,丙二醇的量为20.0 wt %~40.0 wt%,基于所述药物组合物的总重量。
19、在一种实施方式中,所述基质选自卡波姆均聚物、卡波姆共聚物、卡波姆间聚物、阿拉伯胶、黄原胶、明胶、纤维素衍生物、羧乙烯基聚合物、聚丙烯酸钠、聚乙烯醇、聚乙烯吡咯烷酮、透明质酸钠中的一种或多种。
20、在一种实施方式中,所述纤维素衍生物选自甲基纤维素、羧甲基纤维素、羟乙基纤维素和羟丙基纤维素中的一种或多种。
21、在一种实施方式中,所述基质选自卡波姆均聚物、黄原胶、羟乙基纤维素、羟丙纤维素中的一种或多种。
22、在一种实施方式中,所述基质为黄原胶或羟乙基纤维素或者黄原胶与羟乙基纤维素的组合,其中,
23、当存在时,黄原胶的量为0.05wt%~2wt%,基于所述药物组合物的总重量;和/或
24、当存在时,羟乙基纤维素的量为0.1wt%~3wt%,基于所述药物组合物的总重量。
25、在一种实施方式中,所述基质为黄原胶或羟乙基纤维素或者黄原胶与羟乙基纤维素的组合,其中,
26、当存在时,黄原胶的量为0.1wt%~1wt%,基于所述药物组合物的总重量;和/或
27、当存在时,羟乙基纤维素的量为0.5wt%~2wt%,基于所述药物组合物的总重量。
28、在一种实施方式中,所述基质为黄原胶或羟乙基纤维素或者黄原胶与羟乙基纤维素的组合,其中,
29、当存在时,黄原胶的量为0.1wt%~0.5wt%,基于所述药物组合物的总重量;和/或
30、当存在时,羟乙基纤维素的量为0.5wt%~2wt%,基于所述药物组合物的总重量。
31、在一种实施方式中,稳定剂和/或抗氧剂选自柠檬酸、柠檬酸钠、酒石酸、依地酸二钠、dl-生育酚、没食子酸丙酯、丁基羟基苯甲醚、二丁基羟基甲苯、抗坏血酸、半胱氨酸、焦亚硫酸钠、亚硫酸钠、硫代硫酸钠中的一种或多种。
32、在一种实施方式中,稳定剂和/或抗氧剂选自依地酸二钠、没食子酸丙酯、丁基羟基苯甲醚和二丁基羟基甲苯中的一种或多种的组合。
33、在一种实施方式中,稳定剂和/或抗氧剂为依地酸二钠或丁基羟基苯甲醚或者依地酸二钠与丁基羟基苯甲醚的组合;
34、当存在时,依地酸二钠的量为0.02wt%~1.0wt%,基于所述药物组合物的总重量;和/或
35、当存在时,丁基羟基苯甲醚的量为0.02wt%~1.0wt%,基于所述药物组合物的总重量。
36、在一种实施方式中,稳定剂和/或抗氧剂为依地酸二钠或丁基羟基苯甲醚或者依地酸二钠与丁基羟基苯甲醚的组合;
37、当存在时,依地酸二钠的量为0.02wt%~0.5wt%,基于所述药物组合物的总重量;和/或
38、当存在时,丁基羟基苯甲醚的量为0.02wt%~0.5wt%,基于所述药物组合物的总重量。
39、在一种实施方式中,所述溶剂为纯化水,纯化水的量为40.0wt%~60.0wt%,基于所述药物组合物的总重量。
40、在一种实施方式中,所述药物组合物包含基于所述药物组合物的总重量的如下组分:
41、0.3wt%~3.5wt%的枸橼酸托法替布;
42、1.0wt%~20.0wt%的二乙二醇单乙醚;
43、1.0%~50.0wt%的丙二醇;
44、0.05wt%~2wt%的黄原胶;
45、0.1wt%~3wt%的羟乙基纤维素;
46、0.02wt%~1.0wt%的依地酸二钠;
47、0.02wt%~1.0wt%的丁基羟基苯甲醚;
48、20 wt %~70 wt %的水。
49、在一种实施方式中,所述药物组合物还包含保湿剂,其量为1.0wt%~5.0wt%,基于所述药物组合物的总重量。
50、在一种实施方式中,所述药物组合物还任选地包含抑菌剂,其量为0wt%~0.5wt%,基于所述药物组合物的总重量。
51、在一种实施方式中,所述药物组合物包含基于所述药物组合物的总重量的如下组分:
52、0.5wt%~3.5wt%的枸橼酸托法替布;
53、5.0wt%~15.0wt%的二乙二醇单乙醚;
54、20.0wt%~40.0wt%的丙二醇
55、40.0wt%~70.0wt%的纯化水;
56、0.1wt%~0.5wt%的黄原胶;
57、0.5wt%~2wt%的羟乙基纤维素;
58、0.02wt%~0.3wt%的依地酸二钠;
59、0.02wt%~0.3wt%的丁基羟基苯甲醚;
60、1.0wt%~5.0wt%的甘油;
61、0wt%~0.3wt%的羟苯甲酯;
62、0wt%~0.1wt%的羟苯丙酯。
63、在一种实施方式中,所述药物组合物为凝胶剂。
64、本技术解决了枸橼酸托法替布剂型选择、皮肤透过和产品稳定性等方面的难题,开发了一种枸橼酸托法替布的局部用药组合物。本发明的枸橼酸托法替布组合物含量均匀度较好,产品质量稳定,且经动物皮肤或黏膜刺激性试验研究,确认本品无刺激性。
- 还没有人留言评论。精彩留言会获得点赞!