一种用于辅助区分甲状腺良恶性肿瘤的数据处理装置、系统及其应用的制作方法
本发明涉及医疗信息学领域,特别涉及一种用于辅助区分甲状腺良恶性肿瘤的数据处理装置、系统及其应用。
背景技术:
1、甲状腺癌(thyroid cancer)为一种常见的内分泌系统恶性肿瘤,包括甲状腺乳头状癌、滤泡性甲状腺癌、未分化甲状腺癌和髓样癌。其中乳头状癌(papillary thyroidcancer,ptc)最为常见,占所有甲状腺恶性肿瘤的90%以上。据统计,成年人甲状腺结节的患病率约为5-10%,60岁以上的人群最为严重,高达50-70%。影像学检查是目前普遍的甲状腺诊断方法,该方法大多依靠医生经验判断,存在一定的结果误差,而且影像学对人身体有一定辐射伤害。细针穿刺活检也是临床上常见的甲状腺癌诊断技术,该方法根据穿刺物的细胞学形态对结节的良恶性进行评估。由于甲状腺良恶性肿瘤的细胞学特征经常发生重叠,因此约有10-30%的细针穿刺诊断为不明确的细胞学结果。不确定的穿刺结果导致约60%的患者遭受过度治疗或者漏诊。这不仅增加了患者的经济和身心负担,还占据了大量的公共卫生资源,导致医疗保健系统的巨额财务成本。所以,鉴别甲状腺良恶性肿瘤有利于临床医师采取更精准的治疗方案,具有重要的临床和公共卫生意义。
2、表观遗传学是不涉及dna序列改变但可遗传的基因表达调控方式,并能遗传给下一代。dna甲基化是表观遗传调控的重要方式之一,是指在dna甲基化转移酶的作用下,在基因组cpg二核苷酸的胞嘧啶5’碳位共价键结合一个甲基基团。大量研究表明,dna甲基化能引起染色质结构、dna构象、dna稳定性及dna与蛋白质相互作用方式的改变,从而控制基因表达。
3、目前,临床上关于甲状腺癌诊断标志物的灵敏度和特异性很有限,尤其是缺乏早期诊断的标志物,因此更为敏感、特异的早期分子标记物亟待发掘。
技术实现思路
1、本发明的目的是提供一种用于辅助区分甲状腺良恶性肿瘤的数据处理装置、系统及其应用。
2、第一方面,本发明要求保护一种用于辅助区分a类型样本和b类型样本的数据处理装置。
3、本发明要求保护的数据处理装置包括单元x和单元y;
4、所述单元x用于建立数学模型,包括数据采集模块、数据分析处理模块和模型输出模块;
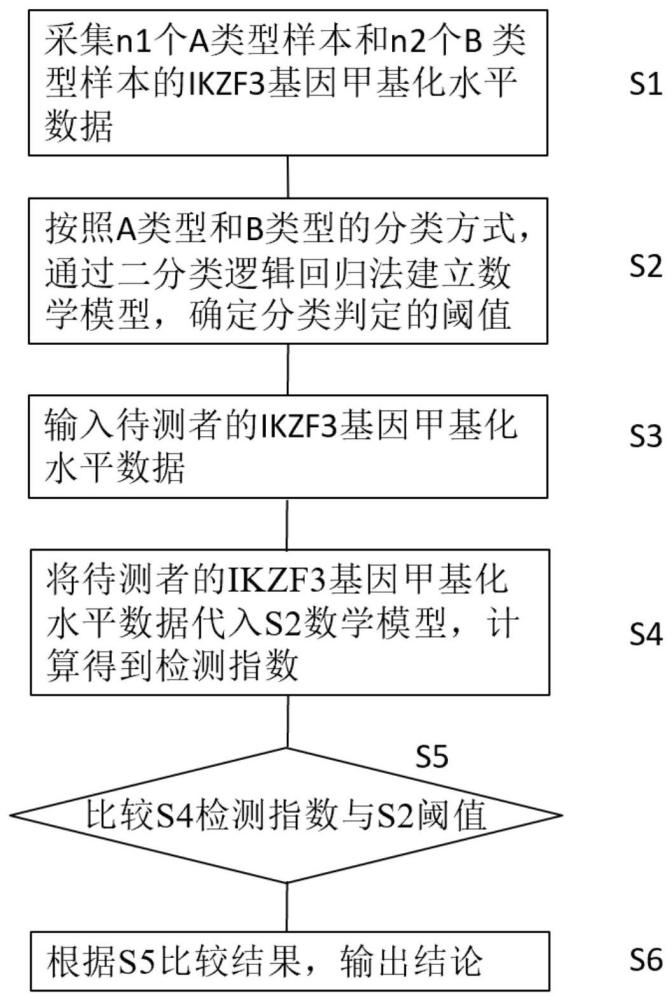
5、所述数据采集模块被配置为采集n1个所述a类型样本和n2个所述b类型样本的ikzf3基因甲基化水平数据;
6、所述数据分析处理模块被配置为接收来自于所述数据采集模块的n1个所述a类型样本和n2个所述b类型样本的ikzf3基因甲基化水平数据,按照a类型和b类型的分类方式,通过二分类逻辑回归法建立数学模型,确定分类判定的阈值;
7、其中,n1和n2均可为50以上正整数,如100以上。
8、所述模型输出模块被配置为接收来自于所述数据分析处理模块建立的所述数学模型,并进行输出;
9、所述单元y用于确定待测样本类型,包括数据输入模块、数据运算模块、数据比较模块和结论输出模块;
10、所述数据输入模块被配置为输入待测者的ikzf3基因甲基化水平数据;
11、所述数据运算模块被配置为接收来自于所述数据输入模块的所述待测者的ikzf3基因甲基化水平数据,并将所述待测者的ikzf3基因甲基化水平数据代入所述单元x中的所述数据分析处理模块建立的所述数学模型,计算得到检测指数;
12、所述数据比较模块被配置为接收来自于所述数据运算模块计算得到的检测指数,并将所述检测指数与所述单元x中的所述数据分析处理模块中确定的所述阈值进行比较;
13、所述结论输出模块被配置为接收来自于所述数据比较模块的比较结果,并根据所述比较结果输出所述待测样本的类型是a类型还是b类型的结论。
14、在本发明的具体实施方式中,所述阈值设为0.5。大于0.5归为一类,小于0.5归为另外一类,等于0.5作为不确定的灰区。其中a类型和b类型为相对应的两分类,二分类的分组,哪一组是a类型,哪一组是b类型,要根据具体的数学模型来确定,无需约定。
15、在实际应用中,所述阈值也可根据最大约登指数确定(具体可为最大约登指数对应的数值)。大于阈值归为一类,小于阈值归为另外一类,等于阈值作为不确定的灰区。其中a类型和b类型为相对应的两分类,二分类的分组,哪一组a类型,哪一组是b类型,要根据具体的数学模型来确定,无需约定。
16、所述a类型样本和所述b类型样本为如下任一种:
17、(e1)甲状腺良性肿瘤和甲状腺恶性肿瘤;
18、(e2)甲状腺良性肿瘤和不同亚型的甲状腺恶性肿瘤;
19、(e3)甲状腺良性肿瘤和不同分期的甲状腺恶性肿瘤;
20、(e4)不同亚型的甲状腺恶性肿瘤;
21、(e5)不同分期的甲状腺恶性肿瘤。
22、进一步地,(e2)和(e4)中所述不同亚型可为病理分型,如组织学分型。
23、进一步地,(e3)和(e5)中所述不同分期可为临床分期。
24、在本发明的具体实施方式中,(e2)中所述甲状腺良性肿瘤和不同亚型的甲状腺恶性肿瘤具体可为如下任一种:甲状腺良性肿瘤和甲状腺乳头状癌、甲状腺良性肿瘤和甲状腺滤泡癌、甲状腺良性肿瘤和甲状腺髓样癌、甲状腺良性肿瘤和甲状腺未分化癌。
25、在本发明的具体实施方式中,(e3)中所述甲状腺良性肿瘤和不同分期的甲状腺恶性肿瘤具体可为如下任一种:甲状腺良性肿瘤和ⅰ期甲状腺恶性肿瘤、甲状腺良性肿瘤和ⅱ期甲状腺恶性肿瘤、甲状腺良性肿瘤和ⅲ期甲状腺恶性肿瘤、甲状腺良性肿瘤和ⅳ期甲状腺恶性肿瘤。
26、在本发明的具体实施方式中,(e4)中所述甲状腺恶性肿瘤不同亚型具体可为如下任一种:甲状腺乳头状癌和甲状腺滤泡癌、甲状腺乳头状癌和甲状腺髓样癌、甲状腺乳头状癌和甲状腺未分化癌、甲状腺滤泡癌和甲状腺髓样癌、甲状腺滤泡癌和甲状腺未分化癌、甲状腺髓样癌和甲状腺未分化癌。
27、在本发明的具体实施方式中,(e5)中所述甲状腺恶性肿瘤不同分期具体可为如下任一种:ⅰ期甲状腺恶性肿瘤和ⅱ期甲状腺恶性肿瘤、ⅰ期甲状腺恶性肿瘤和ⅲ期甲状腺恶性肿瘤、ⅰ期甲状腺恶性肿瘤和ⅳ期甲状腺恶性肿瘤、ⅱ期甲状腺恶性肿瘤和ⅲ期甲状腺恶性肿瘤、ⅱ期甲状腺恶性肿瘤和ⅳ期甲状腺恶性肿瘤、ⅲ期甲状腺恶性肿瘤和ⅳ期甲状腺恶性肿瘤。
28、第二方面,本发明要求保护一种系统。
29、本发明所要求保护的系统包括:
30、(f1)用于检测ikzf3基因甲基化水平的试剂和/或仪器;
31、(f2)装置,所述装置包括单元x和单元y;
32、所述单元x用于建立数学模型,包括数据采集模块、数据分析处理模块和模型输出模块;
33、所述数据采集模块被配置为采集(f1)检测得到的n1个a类型样本和n2个b类型样本的ikzf3基因甲基化水平数据;
34、所述数据分析处理模块被配置为接收来自于所述数据采集模块的所述n1个a类型样本和n2个b类型样本的ikzf3基因甲基化水平数据,按照a类型和b类型的分类方式,通过二分类逻辑回归法建立数学模型,确定分类判定的阈值;
35、其中,n1和n2均可为50以上正整数,如100以上。
36、所述模型输出模块被配置为接收来自于所述数据分析处理模块建立的所述数学模型,并进行输出;
37、所述单元y用于确定待测样本类型,包括数据输入模块、数据运算模块、数据比较模块和结论输出模块;
38、所述数据输入模块被配置为输入(f1)检测得到的待测者的ikzf3基因甲基化水平数据;
39、所述数据运算模块被配置为接收来自于所述数据输入模块的所述待测者的ikzf3基因甲基化水平数据,并将所述待测者的ikzf3基因甲基化水平数据代入所述单元x中的所述数据分析处理模块建立的所述数学模型,计算得到检测指数;
40、所述数据比较模块被配置为接收来自于所述数据运算模块计算得到的检测指数,并将所述检测指数与所述单元x中的所述数据分析处理模块中确定的所述阈值进行比较;
41、所述结论输出模块被配置为接收来自于所述数据比较模块的比较结果,并根据所述比较结果输出所述待测样本的类型是a类型还是b类型的结论;
42、所述a类型样本和所述b类型样本为如下任一种:
43、(e1)甲状腺良性肿瘤和甲状腺恶性肿瘤;
44、(e2)甲状腺良性肿瘤和不同亚型的甲状腺恶性肿瘤;
45、(e3)甲状腺良性肿瘤和不同分期的甲状腺恶性肿瘤;
46、(e4)不同亚型的甲状腺恶性肿瘤;
47、(e5)不同分期的甲状腺恶性肿瘤。
48、其中,(e1)-(e5)的具体含义同前文第一方面中所述。
49、在本发明的具体实施方式中,所述阈值设为0.5。大于0.5归为一类,小于0.5归为另外一类,等于0.5作为不确定的灰区。其中a类型和b类型为相对应的两分类,二分类的分组,哪一组是a类型,哪一组是b类型,要根据具体的数学模型来确定,无需约定。
50、在实际应用中,所述阈值也可根据最大约登指数确定(具体可为最大约登指数对应的数值)。大于阈值归为一类,小于阈值归为另外一类,等于阈值作为不确定的灰区。其中a类型和b类型为相对应的两分类,二分类的分组,哪一组a类型,哪一组是b类型,要根据具体的数学模型来确定,无需约定。
51、第三方面,本发明要求保护一种计算机可读存储介质。
52、本发明所要求保护计算机可读存储介质存储有用于执行下述步骤的计算机程序:
53、采集n1个a类型样本和n2个b类型样本的ikzf3基因甲基化水平数据;
54、将所述n1个a类型样本和n2个b类型样本的ikzf3基因甲基化水平数据,按照a类型和b类型的分类方式,通过二分类逻辑回归法建立数学模型,确定分类判定的阈值;
55、输入待测者的ikzf3基因甲基化水平数据;
56、将所述待测者的ikzf3基因甲基化水平数据代入所述数学模型,计算得到检测指数;
57、将所述检测指数与所述阈值进行比较,得到比较结果;
58、根据所述比较结果输出待测样本的类型是a类型还是b类型的结论;
59、所述a类型样本和所述b类型样本为如下任一种:
60、(e1)甲状腺良性肿瘤和甲状腺恶性肿瘤;
61、(e2)甲状腺良性肿瘤和不同亚型的甲状腺恶性肿瘤;
62、(e3)甲状腺良性肿瘤和不同分期的甲状腺恶性肿瘤;
63、(e4)不同亚型的甲状腺恶性肿瘤;
64、(e5)不同分期的甲状腺恶性肿瘤。
65、其中,(e1)-(e5)的具体含义同前文第一方面中所述。
66、其中,n1和n2均可为50以上正整数,如100以上。
67、在本发明的具体实施方式中,所述阈值设为0.5。大于0.5归为一类,小于0.5归为另外一类,等于0.5作为不确定的灰区。其中a类型和b类型为相对应的两分类,二分类的分组,哪一组是a类型,哪一组是b类型,要根据具体的数学模型来确定,无需约定。
68、在实际应用中,所述阈值也可根据最大约登指数确定(具体可为最大约登指数对应的数值)。大于阈值归为一类,小于阈值归为另外一类,等于阈值作为不确定的灰区。其中a类型和b类型为相对应的两分类,二分类的分组,哪一组a类型,哪一组是b类型,要根据具体的数学模型来确定,无需约定。
69、在前文第一方面所述的数据处理装置或前文第二方面所述的系统或前文第三方面所述的计算机可读存储介质中,所述ikzf3基因甲基化水平可为ikzf3基因中如下(a1)-(a4)所示片段中的全部或部分cpg位点的甲基化水平:
70、(a1)seq id no.1所示的dna片段或与其具有80%以上同一性的dna片段;
71、(a2)seq id no.2所示的dna片段或与其具有80%以上同一性的dna片段;
72、(a3)seq id no.3所示的dna片段或与其具有80%以上同一性的dna片段;
73、(a4)seq id no.4所示的dna片段或与其具有80%以上同一性的dna片段。
74、进一步地,所述全部或部分cpg位点可为如下任一所示cpg位点:
75、(b1)ikzf3基因中seq id no.1、seq id no.2、seq id no.3和seq id no.4所示4个dna片段中的任意一个或多个cpg位点;
76、(b2)ikzf3基因中seq id no.2所示的dna片段上的所有cpg位点和seq id no.3所示的dna片段上的所有cpg位点;
77、(b3)ikzf3基因中seq id no.3所示的dna片段上的所有cpg位点和seq id no.4所示的dna片段上的所有cpg位点;
78、(b4)ikzf3基因中seq id no.2所示的dna片段上的所有cpg位点和seq id no.4所示的dna片段上的所有cpg位点;
79、(b5)ikzf3基因中seq id no.2所示的dna片段上的所有cpg位点、seq id no.3所示的dna片段上的所有cpg位点和seq id no.4所示的dna片段上的所有cpg位点;
80、(b6)ikzf3基因中seq id no.3所示的dna片段中的全部cpg位点或任意7个或任意6个或任意5个或任意4个或任意3个或任意2个或任意1个cpg位点;
81、(b7)ikzf3基因中seq id no.3所示的dna片段上如下6项所示cpg位点的全部或任意5项或任意4项或任意3项或任意2项或任意1项:
82、第1项:seq id no.3所示的dna片段自5’端第132-133位所示cpg位点;
83、第2项:seq id no.3所示的dna片段自5’端第203-204位所示cpg位点;
84、第3项:seq id no.3所示的dna片段自5’端第268-269位所示cpg位点;
85、第4项:seq id no.3所示的dna片段自5’端第312-313位所示cpg位点;
86、第5项:seq id no.3所示的dna片段自5’端第325-326位所示cpg位点;
87、第6项:seq id no.3所示的dna片段自5’端第357-358位所示cpg位点。
88、在本发明的具体实施方式中,有些相邻的甲基化位点在利用飞行时间质谱进行dna甲基化分析时由于几个cpg位点位于一个甲基化片段上,峰图无法区分(无法区分的位点在表6中有记载),因而在进行甲基化水平分析、以及构建和使用相关数学模型时将其按照一个甲基化位点进行处理。
89、在前文第二方面所述的系统中,所述用于检测ikzf3基因甲基化水平的试剂可包含(或为)用于扩增ikzf3基因全长或部分片段的引物组合,仪器可为飞行时间质谱检测仪。当然所述用于检测ikzf3基因甲基化水平的试剂中还可包含进行飞行时间质谱所用的其他常规试剂。
90、进一步地,所述部分片段可为如下中至少一个片段:
91、(g1)seq id no.1所示的dna片段或其包含的dna片段;
92、(g2)seq id no.2所示的dna片段或其包含的dna片段;
93、(g3)seq id no.3所示的dna片段或其包含的dna片段;
94、(g4)seq id no.4所示的dna片段或其包含的dna片段;
95、(g5)与seq id no.1所示的dna片段或其包含的dna片段具有80%以上同一性的dna片段;
96、(g6)与seq id no.2所示的dna片段或其包含的dna片段具有80%以上同一性的dna片段;
97、(g7)与seq id no.3所示的dna片段或其包含的dna片段具有80%以上同一性的dna片段;
98、(g8)与seq id no.4所示的dna片段或其包含的dna片段具有80%以上同一性的dna片段。
99、更进一步地,所述引物组合可为引物对a和/或引物对b和/或引物对c和/或引物对d;所述引物对a为引物a1和引物a2组成的引物对;所述引物a1为seq id no.5或seq idno.5的第11-35位核苷酸所示的单链dna;所述引物a2为seq id no.6或seq id no.6的第32-56位核苷酸所示的单链dna;
100、所述引物对b为引物b1和引物b2组成的引物对;所述引物b1为seq id no.7或seqid no.7的第11-35位核苷酸所示的单链dna;所述引物b2为seq id no.8或seq id no.8的第32-56位核苷酸所示的单链dna;
101、所述引物对c为引物c1和引物c2组成的引物对;所述引物c1为seq id no.9或seqid no.9的第11-35位核苷酸所示的单链dna;所述引物c2为seq id no.10或seq id no.10的第32-56位核苷酸所示的单链dna;
102、所述引物对d为引物d1和引物d2组成的引物对;所述引物d1为seq id no.11或seqid no.11的第11-35位核苷酸所示的单链dna;所述引物d2为seq id no.12或seq idno.12的第32-56位核苷酸所示的单链dna。
103、第四方面,本发明要求保护用于检测ikzf3基因甲基化水平的物质在制备产品中的应用;所述产品的用途为如下至少一种:
104、(1)区分或辅助区分甲状腺良性肿瘤和甲状腺恶性肿瘤;
105、(2)区分或辅助区分甲状腺良性肿瘤和不同亚型的甲状腺恶性肿瘤;
106、(3)区分或辅助区分甲状腺良性肿瘤和不同分期的甲状腺恶性肿瘤;
107、(4)区分或辅助区分甲状腺恶性肿瘤不同亚型;
108、(5)区分或辅助区分甲状腺恶性肿瘤不同分期。
109、进一步地,(2)和(4)中所述不同亚型可为病理分型,如组织学分型。
110、进一步地,(3)和(5)中所述不同分期可为临床分期。
111、在本发明的具体实施方式中,(2)中所述区分或辅助区分甲状腺良性肿瘤和不同亚型的甲状腺恶性肿瘤具体可为如下任一种:区分或辅助区分甲状腺良性肿瘤和甲状腺乳头状癌、区分或辅助区分甲状腺良性肿瘤和甲状腺滤泡癌、区分或辅助区分甲状腺良性肿瘤和甲状腺髓样癌、区分或辅助区分甲状腺良性肿瘤和甲状腺未分化癌。
112、在本发明的具体实施方式中,(3)中所述区分或辅助区分甲状腺良性肿瘤和不同分期的甲状腺恶性肿瘤具体可为如下任一种:区分或辅助区分甲状腺良性肿瘤和ⅰ期甲状腺恶性肿瘤、区分或辅助区分甲状腺良性肿瘤和ⅱ期甲状腺恶性肿瘤、区分或辅助区分甲状腺良性肿瘤和ⅲ期甲状腺恶性肿瘤、区分或辅助区分甲状腺良性肿瘤和ⅳ期甲状腺恶性肿瘤。
113、在本发明的具体实施方式中,(4)中所述区分或辅助区分甲状腺恶性肿瘤不同亚型具体可为如下任一种:区分或辅助区分甲状腺乳头状癌和甲状腺滤泡癌、区分或辅助区分甲状腺乳头状癌和甲状腺髓样癌、区分或辅助区分甲状腺乳头状癌和甲状腺未分化癌、区分或辅助区分甲状腺滤泡癌和甲状腺髓样癌、区分或辅助区分甲状腺滤泡癌和甲状腺未分化癌、区分或辅助区分甲状腺髓样癌和甲状腺未分化癌。
114、在本发明的具体实施方式中,(5)中所述区分或辅助区分甲状腺恶性肿瘤不同分期具体可为如下任一种:区分或辅助区分ⅰ期甲状腺恶性肿瘤和ⅱ期甲状腺恶性肿瘤、区分或辅助区分ⅰ期甲状腺恶性肿瘤和ⅲ期甲状腺恶性肿瘤、区分或辅助区分ⅰ期甲状腺恶性肿瘤和ⅳ期甲状腺恶性肿瘤、区分或辅助区分ⅱ期甲状腺恶性肿瘤和ⅲ期甲状腺恶性肿瘤、区分或辅助区分ⅱ期甲状腺恶性肿瘤和ⅳ期甲状腺恶性肿瘤、区分或辅助区分ⅲ期甲状腺恶性肿瘤和ⅳ期甲状腺恶性肿瘤。
115、进一步地,所述用于检测ikzf3基因甲基化水平的物质可包含(或为)用于扩增ikzf3基因全长或部分片段的引物组合。
116、更进一步地,所述部分片段可为如下中至少一个片段:
117、(g1)seq id no.1所示的dna片段或其包含的dna片段;
118、(g2)seq id no.2所示的dna片段或其包含的dna片段;
119、(g3)seq id no.3所示的dna片段或其包含的dna片段;
120、(g4)seq id no.4所示的dna片段或其包含的dna片段;
121、(g5)与seq id no.1所示的dna片段或其包含的dna片段具有80%以上同一性的dna片段;
122、(g6)与seq id no.2所示的dna片段或其包含的dna片段具有80%以上同一性的dna片段;
123、(g7)与seq id no.3所示的dna片段或其包含的dna片段具有80%以上同一性的dna片段;
124、(g8)与seq id no.4所示的dna片段或其包含的dna片段具有80%以上同一性的dna片段。
125、更加具体地,所述引物组合为引物对a和/或引物对b和/或引物对c和/或引物对d;
126、所述引物对a为引物a1和引物a2组成的引物对;所述引物a1为seq id no.5或seqid no.5的第11-35位核苷酸所示的单链dna;所述引物a2为seq id no.6或seq id no.6的第32-56位核苷酸所示的单链dna;
127、所述引物对b为引物b1和引物b2组成的引物对;所述引物b1为seq id no.7或seqid no.7的第11-35位核苷酸所示的单链dna;所述引物b2为seq id no.8或seq id no.8的第32-56位核苷酸所示的单链dna;
128、所述引物对c为引物c1和引物c2组成的引物对;所述引物c1为seq id no.9或seqid no.9的第11-35位核苷酸所示的单链dna;所述引物c2为seq id no.10或seq id no.10的第32-56位核苷酸所示的单链dna;
129、所述引物对d为引物d1和引物d2组成的引物对;所述引物d1为seq id no.11或seqid no.11的第11-35位核苷酸所示的单链dna;所述引物d2为seq id no.12或seq idno.12的第32-56位核苷酸所示的单链dna。
130、第五方面,本发明要求保护前文第四方面中所述用于检测ikzf3基因甲基化水平的物质和储存有数学模型和/或数学模型使用方法的介质在制备产品中的应用;所述产品的用途为如下至少一种:
131、(1)区分或辅助区分甲状腺良性肿瘤和甲状腺恶性肿瘤;
132、(2)区分或辅助区分甲状腺良性肿瘤和不同亚型的甲状腺恶性肿瘤;
133、(3)区分或辅助区分甲状腺良性肿瘤和不同分期的甲状腺恶性肿瘤;
134、(4)区分或辅助区分甲状腺恶性肿瘤不同亚型;
135、(5)区分或辅助区分甲状腺恶性肿瘤不同分期。
136、其中,(1)-(5)的具体含义同前文第四方面中所述。
137、所述数学模型可按照包括如下步骤的方法获得:
138、(c1)分别检测n1个a类型样本和n2个b类型样本的基因甲基化水平;
139、(c2)取步骤(c1)获得的所有样本的基因甲基化水平数据,按照a类型和b类型的分类方式,通过二分类逻辑回归法建立数学模型,确定分类判定的阈值;
140、其中,n1和n2均可为10以上正整数,如100以上。
141、所述数学模型使用方法可包括如下步骤:
142、(d1)检测待测样本的基因甲基化水平;
143、(d2)将步骤(d1)获得的所述待测样本的基因甲基化水平数据代入所述数学模型,得到检测指数;然后比较检测指数和阈值的大小,根据比较结果确定所述待测样本的类型是a类型还是b类型;
144、在本发明的具体实施方式中,所述阈值设为0.5。大于0.5归为一类,小于0.5归为另外一类,等于0.5作为不确定的灰区。其中a类型和b类型为相对应的两分类,二分类的分组,哪一组是a类型,哪一组是b类型,要根据具体的数学模型来确定,无需约定。
145、在实际应用中,所述阈值也可根据最大约登指数确定(具体可为最大约登指数对应的数值)。大于阈值归为一类,小于阈值归为另外一类,等于阈值作为不确定的灰区。其中a类型和b类型为相对应的两分类,二分类的分组,哪一组a类型,哪一组是b类型,要根据具体的数学模型来确定,无需约定。
146、所述a类型样本和所述b类型样本为如下任一种:
147、(e1)甲状腺良性肿瘤和甲状腺恶性肿瘤;
148、(e2)甲状腺良性肿瘤和不同亚型的甲状腺恶性肿瘤;
149、(e3)甲状腺良性肿瘤和不同分期的甲状腺恶性肿瘤;
150、(e4)不同亚型的甲状腺恶性肿瘤;
151、(e5)不同分期的甲状腺恶性肿瘤。
152、其中,(e1)-(e5)的具体含义同前文第一方面中所述。
153、第六方面,本发明要求保护前文第五方面中所述储存有数学模型和/或数学模型使用方法的介质在制备产品中的应用;所述产品的用途为如下至少一种:
154、(1)区分或辅助区分甲状腺良性肿瘤和甲状腺恶性肿瘤;
155、(2)区分或辅助区分甲状腺良性肿瘤和不同亚型的甲状腺恶性肿瘤;
156、(3)区分或辅助区分甲状腺良性肿瘤和不同分期的甲状腺恶性肿瘤;
157、(4)区分或辅助区分甲状腺恶性肿瘤不同亚型;
158、(5)区分或辅助区分甲状腺恶性肿瘤不同分期。
159、其中,(1)-(5)的具体含义同前文第四方面中所述。
160、第七方面,本发明要求保护甲基化ikzf3基因作为标志物在制备产品中的应用;所述产品的用途为如下至少一种:
161、(1)区分或辅助区分甲状腺良性肿瘤和甲状腺恶性肿瘤;
162、(2)区分或辅助区分甲状腺良性肿瘤和不同亚型的甲状腺恶性肿瘤;
163、(3)区分或辅助区分甲状腺良性肿瘤和不同分期的甲状腺恶性肿瘤;
164、(4)区分或辅助区分甲状腺恶性肿瘤不同亚型;
165、(5)区分或辅助区分甲状腺恶性肿瘤不同分期。
166、其中,(1)-(5)的具体含义同前文第四方面中所述。
167、以上任一所述数学模型在实际应用中可能会根据dna甲基化的检测方法以及拟合方式不同有所改变,要根据具体的数学模型来确定,无需约定。
168、在本发明的实施例中,所述模型具体为ln(y/(1-y))=b0+b1x1+b2x2+b3x3+…+bnxn,其中y为因变量即将待测样品的一个或者多个甲基化位点的甲基化值代入模型以后得出的检测指数,b0为常量,x1~xn为自变量即为该测试样品的一个或者多个甲基化位点的甲基化值(每一个值为0-1之间的数值),b1~bn为模型赋予每一个位点甲基化值的权重。
169、本发明的实施例中建立的一个具体模型为用于区分或辅助区分甲状腺良性肿瘤和甲状腺恶性肿瘤的模型,所述模型具体为:ln(y/(1-y))=5.493–1.617*ikzf3_c_3+1.582*ikzf3_c_4-9.615*ikzf3_c_5 -1.509*ikzf3_c_6+6.229*ikzf3_c_7 -3.371*ikzf3_c_8。
170、所述ikzf3_c_3为seq id no.3所示的dna片段自5’端第132-133位所示cpg位点的甲基化水平;所述ikzf3_c_4为seq id no.3所示的dna片段自5’端第203-204位所示cpg位点的甲基化水平;所述ikzf3_c_5为seq id no.3所示的dna片段自5’端第268-269位所示cpg位点的甲基化水平;所述ikzf3_c_6为seq id no.3所示的dna片段自5’端第312-313位所示cpg位点的甲基化水平;所述ikzf3_c_7为seq id no.3所示的dna片段自5’端第325-326位所示cpg位点的甲基化水平;所述ikzf3_c_8为seq id no.3所示的dna片段自5’端第357-358位所示cpg位点的甲基化水平。所述模型的阈值为0.5。通过模型计算的检测指数大于0.5的患者候选为甲状腺恶性肿瘤患者,小于0.5的患者候选为甲状腺良性肿瘤患者。
171、在上述各方面中,所述检测ikzf3基因甲基化水平为检测肿瘤组织样本中ikzf3基因甲基化水平。
172、在本发明中,甲状腺恶性肿瘤组织中的ikzf3基因中seq id no.1、2、3和4所示的dna片段上甲基化位点的甲基化水平明显低于甲状腺良性肿瘤。
173、在本发明中,不同临床特征甲状腺癌如:乳头状癌、滤泡癌、髓样癌和未分化癌肿瘤组织中的ikzf3基因中seq id no.1、2、3和4所示的dna片段上甲基化位点的甲基化水平越来越低。
174、在本发明中,随着甲状腺恶性肿瘤的分期的增加组织中的ikzf3基因中seq idno.1、2、3和4所示的dna片段上甲基化位点的甲基化水平越来越低。
175、以上任一所述ikzf3基因具体可参见genbank登录号:nm_012481.5(gi:1519312216),转录变体1;nm_183228.3(gi:1676325075),转录变体2;nm_183229.3(gi:1675158667),转录变体3;nm_183230.3(gi:1675136892),转录变体4;nm_183231.3(gi:1676318702),转录变体5;nm_183232.3(gi:1676439909),转录变体6;nm_001257408.2(gi:1675151003),转录变体7;nm_001257409.2(gi:1676318954),转录变体8;nm_001257410.2(gi:1676317062),转录变体9;nm_001257411.2(gi:1676440050),转录变体10;nm_001257412.2(gi:1675034824),转录变体11;nm_001257413.2(gi:1675134475),转录变体12;nm_001257414.2(gi:1676317122),转录变体13;nm_001284514.2(gi:1890273863),转录变体14;nm_001284515.2(gi:1674989040),转录变体15;nm_001284516.1(gi:548962173),转录变体16。
176、本发明证明活检样本ikzf3甲基化可作为甲状腺良性肿瘤和甲状腺恶性肿瘤、不同亚型或不同分期的甲状腺恶性肿瘤的鉴别诊断的潜在标志物。本发明对鉴别甲状腺良性肿瘤和甲状腺恶性肿瘤、不同亚型或不同分期的甲状腺恶性肿瘤,以及指导制定合理的临床治疗方案均有重要的科学意义和临床应用价值。
- 还没有人留言评论。精彩留言会获得点赞!