人白介素-4受体α抗体糖皮质激素缀合物的制作方法
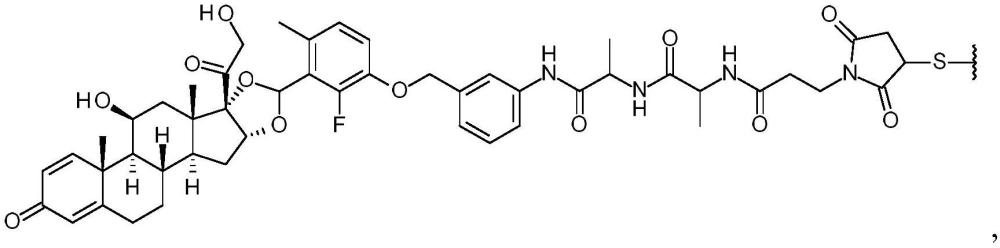
本公开提供了人白介素-4受体α抗体糖皮质激素受体激动剂缀合物;使用这些缀合物治疗炎性疾病的方法,这些炎性疾病如2型炎性疾病,如特应性皮炎、嗜酸细胞性食管炎、鼻息肉病、哮喘、慢性鼻窦炎、过敏性疾病、慢性阻塞性肺病或慢性自发性荨麻疹;用于制备这些缀合物的方法;以及包含这些缀合物的药物组合物。
背景技术:
1、特应性皮炎是一种慢性、瘙痒性复发和缓解型炎性皮肤病,其在儿童中频繁发生,但也影响许多成人。目前对特应性皮炎的治疗包括光疗法、含有皮质类固醇或钙调神经磷酸酶抑制剂的局部乳膏或称为度普利尤单抗(dupilumab)的可皮下注射生物制剂。尽管在治疗特应性皮炎方面取得了进展,但是仍然非常需要新的化合物来治疗特应性皮炎和其他炎性及自身免疫性疾病,并且其最大限度地减少或消除目前批准的治疗所具有的缺点。
2、wo2017/210471公开了可用于治疗炎性疾病的某些糖皮质激素受体激动剂(gc)及其免疫缀合物。wo2018/089373公开了新的类固醇、其蛋白缀合物以及用于治疗疾病、障碍和病症的方法,该方法包括施用类固醇和缀合物。迄今为止,还没有已知的正在开发中的用于治疗炎性疾病的人il-4rαgc缀合物。
技术实现思路
1、本公开提供某些新型人il-4rα抗体gc缀合物,其中抗体与人il-4rα结合。本公开还提供包含新型抗人il-4rα抗体gc缀合物的组合物以及使用此类抗人il-4rα抗体gc缀合物和其组合物的方法。本公开还提供了某些新型抗人il-4rαgc缀合物,其可用于治疗炎性疾病,如2型炎性疾病,如特应性皮炎、嗜酸细胞性食管炎、鼻息肉病、哮喘、慢性鼻窦炎、过敏性疾病、慢性阻塞性肺病或慢性自发性荨麻疹。
2、本文提供的某些抗人il-4rα抗体gc缀合物具有以下特性中的一种或多种:1)结合跨越人和/或食蟹猴il-4rα的n-末端纤连蛋白iii型结构域1和2的新表位,2)以期望的结合亲和力结合人il-4rα,3)以期望的结合亲和力结合食蟹猴il-4rα,4)结合细胞表面上的人il-4rα并内化到细胞中,5)结合人il-4rα并抑制il-4和il-13与il-4rα的结合,6)在体外结合人il-4rα并抑制il-4r介导的反应(b和t细胞中的pstat6、b细胞增殖、cd23表达、细胞因子产生(例如,mdc、gm-csf)),7)结合人和/或食蟹猴il-4rα上的独特功能表位,8)在体外调节糖皮质激素受体激动剂介导的反应(诱导cd163表达、抑制b细胞增殖、抑制细胞因子产生(例如,il-5、gm-csf)),9)调节糖皮质激素受体激动剂介导的基因表达(上调:tsc22d3、fkbp5、zbtb16;下调:il-5),10)不显著诱导adcc或cdc活性,11)保留fcγ受体与b细胞和/或髓样细胞的结合,12)抑制体内炎性反应,或13)具有良好的开发性特征,例如可接受的粘度、溶解度和聚集稳定性,以有助于开发、制造和/或配制。
3、因此,在一个实施方案中,本公开提供了式i的缀合物:
4、
5、其中ab是结合人白介素-4受体α的抗体(“抗人il-4rα抗体”),并且其中
6、为:
7、或
8、
9、并且n为1至5。
10、在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的一个或多个氨基酸残基:d12、m14、s15、i16、y37、l39、f41、l42、l43、e45、h47、t48、c49、i50、e52、h62、l64、m65、d66、d67、v68、v69、d72、r99、p121、p123、p124、d125、p192(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的至少一个、至少两个、至少三个、至少四个、或至少五个或更多个氨基酸残基:d12、m14、s15、i16、y37、l39、f41、l42、l43、e45、h47、t48、c49、i50、e52、h62、l64、m65、d66、d67、v68、v69、d72、r99、p121、p123、p124、d125、p192(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的一个或多个氨基酸残基:d12、m14、s15、i16、l39、f41、l42、t48、c49、i50、e52、h62、l64、m65、d66、d67、v68、v69、d72、r99、p121、p123、p124、d125、p192(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的至少一个、至少两个、至少三个、至少四个、至少五个或更多个氨基酸残基:d12、m14、s15、i16、l39、f41、l42、t48、c49、i50、e52、h62、l64、m65、d66、d67、v68、v69、d72、r99、p121、p123、p124、d125、p192(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的一个或多个氨基酸残基:d12、m14、s15、i16、y37、l39、f41、l43、e45、h47、t48、c49、i50、h62、l64、m65、d66、d67、v69、d72、r99、p121、p123、p124、d125(氨基酸残基位置对应于seqid no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的至少一个、至少两个、至少三个、至少四个、至少五个或更多个氨基酸残基:d12、m14、s15、i16、y37、l39、f41、l43、e45、h47、t48、c49、i50、h62、l64、m65、d66、d67、v69、d72、r99、p121、p123、p124、d125(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的一个或多个氨基酸残基:d12、m14、s15、i16、y37、l39、t48、c49、i50、e52、h62、m65、r99、p121、p123、p124、d125、p192(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的至少一个、至少两个、至少三个、至少四个、至少五个或更多个氨基酸残基:d12、m14、s15、i16、y37、l39、t48、c49、i50、e52、h62、m65、r99、p121、p123、p124、d125、p192(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的一个或多个氨基酸残基:r99、p121、p123、p124、d125、p192(氨基酸残基位置对应于seq id no:15),其中这些残基位于il-4rα的n-末端纤连蛋白iii型结构域的结构域2中。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的一个或多个氨基酸残基:d66、d67和d125(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的至少一个氨基酸残基:d66和d67(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含选自以下的至少一个氨基酸残基:d66和d125(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,式i的缀合物中的ab与人il-4rα的表位结合,其中表位包含氨基酸残基d66(氨基酸残基位置对应于seq id no:15)。在又其他实施方案中,式i的缀合物中的ab结合人il-4rα的新的结构和/或功能表位,其中表位跨越il-4rα的n-末端纤连蛋白iii型结构域的结构域1和结构域2。在特定实施方案中,式i的缀合物中的ab结合人il-4rα的新的结构和/或功能表位,其中表位与il-4rα的il-4结合位点重叠。在此类实施方案中,式i的缀合物中的ab阻断il-4与人il-4rα的结合。在特定实施方案中,式i的缀合物中的ab结合人il-4rα的新的结构和/或功能表位,其中表位与il-4rα的il-13结合位点重叠。在此类实施方案中,式i的缀合物中的ab阻断il-13与人il-4rα的结合。在特定实施方案中,式i的缀合物中的ab结合人il-4rα的新的结构和/或功能表位,其中表位与il-4rα的il-4和il-13结合位点重叠。在此类实施方案中,式i的缀合物中的ab阻断il-4和il-13与人il-4rα的结合。在一些实施方案中,式i的缀合物,其中il-4rα表位通过x-射线晶体学、丙氨酸扫描诱变、位阻诱变和/或hdx-ms确定。在又其他实施方案中,il-4rα表位通过定点诱变确定。
11、在另外的实施方案中,本公开提供了式i的缀合物:
12、
13、其中ab是结合人白介素-4受体α的抗体(“抗人il-4rα抗体”),其中ab包含重链可变区(vh)和轻链可变区(vl),其中vh包含重链互补决定区hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区lcdr1、lcdr2和lcdr3,其中:
14、hcdr1包含seq id no:1、19或42;
15、hcdr2包含seq id no:2或20;
16、hcdr3包含seq id no:3;
17、lcdr1包含seq id no:4或22;
18、lcdr2包含seq id no:5;并且
19、lcdr3包含seq id no:6或24;
20、并且其中
21、为:
22、或
23、
24、并且n为1至5。
25、在另外的实施方案中,本公开提供了式ia的缀合物:
26、
27、其中ab是结合人il-4rα的抗体,其中ab包含重链可变区(vh)和轻链可变区(vl),其中vh包含重链互补决定区hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区lcdr1、lcdr2和lcdr3,其中:
28、hcdr1包含seq id no:1、19或42;
29、hcdr2包含seq id no:2或20;
30、hcdr3包含seq id no:3;
31、lcdr1包含seq id no:4或22;
32、lcdr2包含seq id no:5;并且
33、lcdr3包含seq id no:6或24;
34、并且其中
35、为:
36、或
37、
38、并且n为1至5。
39、在另外的实施方案中,本公开提供了式ib的缀合物:
40、
41、其中ab是结合人il-4rα的抗体,其中ab包含重链可变区(vh)和轻链可变区(vl),其中vh包含重链互补决定区hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区lcdr1、lcdr2和lcdr3,其中:
42、hcdr1包含seq id no:1、19或42;
43、hcdr2包含seq id no:2或20;
44、hcdr3包含seq id no:3;
45、lcdr1包含seq id no:4或22;
46、lcdr2包含seq id no:5;并且
47、lcdr3包含seq id no:6或24;
48、并且其中
49、为:
50、或
51、
52、并且n为1至5。
53、在另外的实施方案中,本公开提供了式ic的缀合物:
54、
55、其中ab是结合人il-4rα的抗体,其中ab包含重链可变区(vh)和轻链可变区(vl),其中vh包含重链互补决定区hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区lcdr1、lcdr2和lcdr3,其中:
56、hcdr1包含seq id no:1、19或42;
57、hcdr2包含seq id no:2或20;
58、hcdr3包含seq id no:3;
59、lcdr1包含seq id no:4或22;
60、lcdr2包含seq id no:5;并且
61、lcdr3包含seq id no:6或24;
62、并且其中
63、为:
64、或
65、
66、并且n为1至5。
67、在另外的实施方案中,本公开提供了式id的缀合物:
68、
69、其中ab是结合人il-4rα的抗体,其中ab包含重链可变区(vh)和轻链可变区(vl),其中vh包含重链互补决定区hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区lcdr1、lcdr2和lcdr3,其中:
70、hcdr1包含seq id no:1、19或42;
71、hcdr2包含seq id no:2或20;
72、hcdr3包含seq id no:3;
73、lcdr1包含seq id no:4或22;
74、lcdr2包含seq id no:5;并且
75、lcdr3包含seq id no:6或24;
76、并且其中
77、为:
78、或
79、
80、并且n为1至5。
81、在另外的实施方案中,本公开提供了式ie的缀合物:
82、
83、其中ab是结合人il-4rα的抗体,其中ab包含重链可变区(vh)和轻链可变区(vl),其中vh包含重链互补决定区hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区lcdr1、lcdr2和lcdr3,其中:
84、hcdr1包含seq id no:1、19或42;
85、hcdr2包含seq id no:2或20;
86、hcdr3包含seq id no:3;
87、lcdr1包含seq id no:4或22;
88、lcdr2包含seq id no:5;并且
89、lcdr3包含seq id no:6或24;
90、并且其中
91、为:
92、
93、并且n为1至5。
94、在另外的实施方案中,本公开提供了式if的缀合物:
95、
96、其中ab是结合人il-4rα的抗体,其中ab包含重链可变区(vh)和轻链可变区(vl),其中vh包含重链互补决定区hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区lcdr1、lcdr2和lcdr3,其中:
97、hcdr1包含seq id no:1、19或42;
98、hcdr2包含seq id no:2或20;
99、hcdr3包含seq id no:3;
100、lcdr1包含seq id no:4或22;
101、lcdr2包含seq id no:5;并且
102、lcdr3包含seq id no:6或24;
103、并且其中
104、为:
105、
106、并且n为1至5。
107、在实施方案中,n为2至5。
108、在实施方案中,n为3至5。
109、在实施方案中,n为3至4。
110、在实施方案中,n为约4。
111、在实施方案中,n为约3。
112、在实施方案中,n为约2。
113、在一些实施方案中,ab包含vh和vl,其中vh包含重链互补决定区hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区lcdr1、lcdr2和lcdr3,其中hcdr1包含seq id no:1,hcdr2包含seq id no:2,hcdr3包含seq id no:3,lcdr1包含seq id no:4,lcdr2包含seqid no:5,并且lcdr3包含seq id no:6。在一些实施方案中,ab包含含有seq id no:7的vh和含有seq id no:8的vl。在一些实施方案中,ab是ab1,其中ab1包含含有seq id no:9的hc和含有seq id no:10的lc。在一些实施方案中,ab是ab2,其中ab2包含含有seq id no:50的hc和含有seq id no:10的lc。在一些实施方案中,ab是ab3,其中ab3包含含有seq id no:37的hc和含有seq id no:10的lc。在一些实施方案中,ab是ab4,其中ab4包含含有seq id no:31的hc和含有seq id no:10的lc。在一些实施方案中,ab是ab5,其中ab5包含含有seq id no:35的hc和含有seq id no:10的lc。在一些实施方案中,ab是ab6,其中ab6包含含有seq idno:33的hc和含有seq id no:10的lc。在一些实施方案中,ab是ab7,其中ab7包含含有seqid no:13的hc和含有seq id no:10的lc。在一些实施方案中,ab是ab8,其中ab8包含含有seq id no:52的hc和含有seq id no:10的lc。
114、在一些实施方案中,ab包含vh和vl,其中vh包含重链互补决定区hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区lcdr1、lcdr2和lcdr3,其中hcdr1包含seq id no:42,hcdr2包含seq id no:2,hcdr3包含seq id no:3,lcdr1包含seq id no:22,lcdr2包含seqid no:5,并且lcdr3包含seq id no:6。在一些实施方案中,ab包含含有seq id no:44的vh和含有seq id no:45的vl。在一些实施方案中,ab是ab9,其中ab9包含含有seq id no:46的hc和含有seq id no:47的lc。
115、在一些实施方案中,ab包含vh和vl,其中vh包含重链互补决定区hcdr1、hcdr2和hcdr3,并且vl包含轻链互补决定区lcdr1、lcdr2和lcdr3,其中hcdr1包含seq id no:19,hcdr2包含seq id no:20,hcdr3包含seq id no:3,lcdr1包含seq id no:22,lcdr2包含seqid no:5,并且lcdr3包含seq id no:24。在一些实施方案中,ab包含含有seq id no:25的vh和含有seq id no:26的vl。在一些实施方案中,ab是ab10,其中ab10包含含有seq id no:27的hc和含有seq id no:28的lc。
116、在一些实施方案中,式i的缀合物中的ab结合人il-4rα并且抑制人il-4和人il-13与人il-4rα的结合。在一些实施方案中,式i的缀合物中的ab结合人il-4rα并且抑制il-4r受体介导的反应(例如,抑制b和t细胞中的pstat6,抑制b细胞增殖,抑制cd23表达,抑制细胞因子分泌(例如,mdc、gm-csf)。在一些实施方案中,式i的缀合物中的ab结合人il-4rα并且不显著诱导adcc或cdc活性。在一些实施方案中,式i的缀合物中的ab结合细胞表面上的人il-4rα并且将式i的缀合物内化到细胞中。
117、在本公开的一些实施方案中,式i的缀合物中的ab是完全人抗体。在本公开的一些实施方案中,式i的缀合物中的ab具有人igg4或人igg1同种型。
118、在本公开的一些实施方案中,式i的缀合物中的ab具有修饰的人igg4铰链区,其包含s228p取代(eu编号),也称为igg4p,其减少体内igg4fab-臂交换(参见labrijn等人,nat.biotechnol.2009,27(8):767)。在一些实施方案中,当与具有效应子空主链的人igg4和/或人igg4p il-4rα抗体相比时,具有人igg4p主链的ab具有改善的与b细胞和/或髓样细胞的结合。
119、在本公开的一些实施方案中,式i的缀合物中的ab具有修饰的人igg1fc区,其包含氨基酸残基322处的丙氨酸(k322a取代)(eu编号)(也称为igg1a)。在此类实施方案中,ab具有降低的或消除的补体活性。在一些实施方案中,ab具有修饰的人igg1 fc区,其包含l234a、l235a和/或p329a(也分别称为igg1aa或iggiaaa),其具有降低或消除的与fcγ和c1q受体的结合(所有残基均根据eu编号来编号)。在一些实施方案中,当与具有人igg1aaa效应子空主链的抗人il-4rα抗体相比时,具有人igg1a主链的ab显示改善的与b细胞和/或髓样细胞的结合。
120、在本公开的一些实施方案中,式i的缀合物中的ab具有修饰的人igg4hc恒定区,与具有野生型人igg4 hc恒定区的相同抗体相比,其降低抗体的粘度。在此类实施方案中,ab具有修饰的人igg4 hc恒定区,其包含在以下氨基酸残基中的任何一个或多个处的氨基酸取代:e137g、d203n、q274k、q355r、e419q(所有位置均根据eu编号来编号)。在一些实施方案中,ab具有修饰的人igg4 hc恒定区,其包含在以下氨基酸残基处的氨基酸取代:e137g、d203n、q274k、q355r、e419q(所有位置均根据eu编号来编号)。在一些实施方案中,ab具有修饰的人igg4 hc恒定区,其包含在以下氨基酸残基中的任何一个或多个处的氨基酸取代:q274k、q355r、e419q(所有位置均根据eu编号来编号)。在一些实施方案中,ab具有修饰的人igg4 hc恒定区,其包含在以下氨基酸残基处的氨基酸取代:q274k、q355r、e419q(所有位置均根据eu编号来编号)。
121、在另外的实施方案中,式i的缀合物中的ab具有修饰的人igg1或人igg4恒定结构域,其包含一个或多个工程化半胱氨酸残基(参见wo 2018/232088al)。在此类实施方案中,ab包含重链恒定结构域1(ch1)中的氨基酸残基124(eu编号)处的半胱氨酸,或重链恒定结构域2(ch2)中的氨基酸残基378(eu编号)处的半胱氨酸。在其他实施方案中,ab包含ch1结构域中的氨基酸残基124(eu编号)处的半胱氨酸和ch2结构域中的氨基酸残基378(eu编号)处的半胱氨酸。
122、在一些实施方案中,式i的缀合物中的ab选自ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10。在一些实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7和ab8具有相同的hcdr和lcdr氨基酸序列。因此,如下所示,ab1、ab2、ab3、ab4、ab5、ab6、ab7和ab8与包含选自以下的氨基酸残基的表位结合:d12、m14、s15、i16、l39、f41、l42、t48、c49、i50、e52、h62、l64、m65、d66、d67、v68、v69、d72、r99、p121、p123、p124、d125、p192(氨基酸残基位置对应于seqid no:15)。在如下所示的一些实施方案中,ab9和ab10与人il-4rα的表位结合,其中表位包含选自以下的一个或多个氨基酸残基:d12、m14、s15、i16、y37、l39、f41、l43、e45、h47、t48、c49、i50、h62、l64、m65、d66、d67、v69、d72、r99、p121、p123、p124、d125(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,如下所示,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10与人il-4rα的表位结合,其中表位包含选自以下的一个或多个氨基酸残基:d12、m14、s15、i16、y37、l39、t48、c49、i50、e52、h62、m65、r99、p121、p123、p124、d125、p192(氨基酸残基位置对应于seq id no:15)。在一些实施方案中,如下所示,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10与人il-4rα的表位结合,其中表位包含选自以下的一个或多个氨基酸残基:r99、p121、p123、p124、d125、p192(氨基酸残基位置对应于seq id no:15),其中这些残基位于il-4rα的n-末端纤连蛋白iii型结构域的结构域2中。在如下所示的一些实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10与人il-4rα的表位结合,其中表位包含选自以下的一个或多个氨基酸残基:d66、d67和d125(氨基酸残基位置对应于seq idno:15)。在如下所示的另外的实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10与人il-4rα的表位结合,其中表位包含选自以下的至少一个氨基酸残基:d66和d67(氨基酸残基位置对应于seq id no:15)。在如下所示的又一实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10与人il-4rα的表位结合,其中表位包含选自以下的至少一个氨基酸残基:d66和d125(氨基酸残基位置对应于seq id no:15)。在如下所示的又一实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10与人il-4rα的表位结合,其中表位包含氨基酸残基d66(氨基酸残基位置对应于seq id no:15)。在此类实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10与人il-4rα的新的结构和/或功能表位结合,其中表位跨越il-4rα的n-末端纤连蛋白iii型结构域的结构域1和结构域2。在特定实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10与人il-4rα的新的结构和/或功能表位结合,其中表位与il-4rα的il-4结合位点重叠。在此类实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10抑制il-4与人il-4rα的结合。在特定实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10与人il-4rα的新的结构和/或功能表位结合,其中表位与il-4rα的il-13结合位点重叠。在此类实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10抑制il-13与人il-4rα的结合。在一些实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10与人il-4rα的新的结构和/或功能表位结合,其中表位与il-4rα的il-4和il-13结合位点重叠。在此类实施方案中,ab1、ab2、ab3、ab4、ab5、ab6、ab7、ab8、ab9和ab10抑制il-4和il-13与人il-4rα的结合。在一些实施方案中,il-4rα表位通过x-射线晶体学、丙氨酸扫描诱变、位阻诱变和/或hdx-ms确定。在又其他实施方案中,il-4rα表位通过定点诱变确定。
123、在一些实施方案中,本公开提供了编码结合人il-4rα的抗体的hc或lc、或者vh或vl的核酸,或包含此类核酸的载体。
124、在一些实施方案中,本公开提供了包含seq id no:11、12、14、29、30、32、34、36、38、48、49、51或53的序列的核酸。
125、在一些实施方案中,提供了编码结合人il-4rα的抗体的重链或轻链的核酸。在一些实施方案中,提供了包含编码seq id no:9、10、13、27、28、31、33、35、37、46、47、50或52的序列的核酸。在一些实施方案中,提供了包含编码包含seq id no:9、13、27、31、33、35、37、46、50或52的抗体重链的序列的核酸。例如,核酸可包含seq id no:11、14、29、32、34、36、38、48、51或53的序列。在一些实施方案中,提供了包含编码包含seq id no:10、28或47的抗体轻链的序列的核酸。例如,核酸可包含seq id no:12、30或49的序列。
126、在本公开的一些实施方案中,提供了编码特异性结合人il-4rα的抗体的vh或vl的核酸。在一些实施方案中,提供了包含编码seq id no:7、8、25、26、44或45的序列的核酸。在一些实施方案中,提供了包含编码包含seq id no:7、25或44的抗体vh的序列的核酸。在一些实施方案中,提供了包含编码包含seq id no:8、26或45的抗体vl的序列的核酸。
127、本公开的一些实施方案提供了包含编码抗体重链或轻链的核酸序列的载体。例如,此类载体可包含编码seq id no:9、13、27、31、33、35、37、46、50或52的核酸序列。在一些实施方案中,载体包含编码seq id no:10、28或47的核酸序列。
128、本文还提供了包含编码抗体vh或vl的核酸序列的载体。例如,此类载体可包含编码seq id no:7、25或44的核酸序列。在一些实施方案中,载体包含编码seq id no:8、26或45的核酸序列。
129、本文还提供了包含编码抗体重链的第一核酸序列和编码抗体轻链的第二核酸序列的载体。在一些实施方案中,载体包含编码seq id no:9、13、27、31、33、35、37、46、50或52的第一核酸序列和编码seq id no:10、28或47的第二核酸序列。在一些实施方案中,载体包含编码seq id no:9的第一核酸序列和编码seq id no:10的第二核酸序列。在一些实施方案中,载体包含编码seq id no:13的第一核酸序列和编码seq id no:10的第二核酸序列。在一些实施方案中,载体包含编码seq id no:27的第一核酸序列和编码seq id no:28的第二核酸序列。在一些实施方案中,载体包含编码seq id no:31的第一核酸序列和编码seqid no:10的第二核酸序列。在一些实施方案中,载体包含编码seq id no:33的第一核酸序列和编码seq id no:10的第二核酸序列。在一些实施方案中,载体包含编码seq id no:35的第一核酸序列和编码seq id no:10的第二核酸序列。在一些实施方案中,载体包含编码seq id no:37的第一核酸序列和编码seq id no:10的第二核酸序列。在一些实施方案中,载体包含编码seq id no:50的第一核酸序列和编码seq id no:10的第二核酸序列。在一些实施方案中,载体包含编码seq id no:52的第一核酸序列和编码seq id no:10的第二核酸序列。在一些实施方案中,载体包含编码seq id no:46的第一核酸序列和编码seq id no:47的第二核酸序列。
130、本文还提供了组合物,该组合物包含含有编码抗体重链的核酸序列的第一载体以及含有编码抗体轻链的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq id no:9、13、27、31、33、35、37、46、50或52的核酸序列的第一载体以及含有编码seq idno:10、28或47的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq idno:9的核酸序列的第一载体以及含有编码seq id no:10的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq id no:13的核酸序列的第一载体以及含有编码seqid no:10的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq id no:27的核酸序列的第一载体以及含有编码seq id no:28的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq id no:31的核酸序列的第一载体以及含有编码seq idno:10的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq id no:33的核酸序列的第一载体以及含有编码seq id no:10的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq id no:35的核酸序列的第一载体以及含有编码seq id no:10的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq id no:37的核酸序列的第一载体以及含有编码seq id no:10的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq id no:50的核酸序列的第一载体以及含有编码seq id no:10的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq id no:52的核酸序列的第一载体以及含有编码seq id no:10的核酸序列的第二载体。在一些实施方案中,该组合物包含含有编码seq id no:46的核酸序列的第一载体以及含有编码seq id no:47的核酸序列的第二载体。
131、本文还提供了组合物,该组合物包含含有编码抗体重链的核酸序列以及编码抗体轻链的核酸序列的载体。在一些实施方案中,该组合物包含含有编码seq id no:9、13、27、31、33、35、37、46、50或52的核酸序列以及编码seq id no:10、28或47的第二核酸序列的载体。
132、如本文所用,式中的“gc”:
133、
134、是指合适的糖皮质激素受体激动剂有效负载,并且包括下式iia、iib或iic:
135、
136、和
137、
138、如本文所用,式中的“l”
139、
140、是指将ab连接至gc的合适的接头基团。本领域普通技术人员已知的合适接头包括例如可裂解和不可裂解的接头。更具体地,合适的接头“l”包括下式iiia至iiif:
141、
142、和
143、
144、在实施方案中,本公开提供了式iv的糖皮质激素受体激动剂有效负载-接头:
145、
146、在实施方案中,本公开提供了式iva的糖皮质激素受体激动剂有效负载-接头:
147、
148、在实施方案中,本公开提供了式ivb的糖皮质激素受体激动剂有效负载-接头:
149、
150、在实施方案中,本公开提供了式ivc的糖皮质激素受体激动剂有效负载-接头:
151、
152、在实施方案中,本公开提供了式ivd的糖皮质激素受体激动剂有效负载-接头:
153、
154、在实施方案中,本公开提供了式v的化合物:
155、
156、在另外的实施方案中,本公开提供了式va的化合物:
157、
158、在实施方案中,本公开还提供了治疗对其有需要的受试者的炎性疾病的方法,该方法包括向受试者施用有效量的式i的缀合物或其药学上可接受的盐。在实施方案中,本公开还提供了治疗炎性疾病的方法,其中炎性疾病是对其有需要的受试者的2型炎性疾病,该方法包括向受试者施用有效量的式i的缀合物或其药物或盐。在某些实施方案中,2型炎性疾病是例如特应性皮炎、嗜酸细胞性食管炎、鼻息肉病、哮喘、慢性鼻窦炎、过敏性疾病、慢性阻塞性肺病或慢性自发性荨麻疹。在实施方案中,本公开还提供了治疗对其有需要的受试者的特应性皮炎的方法,该方法包括向受试者施用有效量的式i的缀合物或其药学上可接受的盐。在实施方案中,本公开还提供了治疗对其有需要的受试者的嗜酸细胞性食管炎的方法,该方法包括向受试者施用有效量的式i的缀合物或其药学上可接受的盐。在实施方案中,本公开还提供了治疗对其有需要的受试者的鼻息肉病的方法,该方法包括向受试者施用有效量的式i的缀合物或其药学上可接受的盐。在实施方案中,本公开还提供了治疗对其有需要的受试者的哮喘的方法,该方法包括向受试者施用有效量的式i的缀合物或其药学上可接受的盐。在实施方案中,本公开还提供了治疗对其有需要的受试者的慢性鼻窦炎的方法,该方法包括向受试者施用有效量的式i的缀合物或其药学上可接受的盐。在实施方案中,本公开还提供了治疗对其有需要的受试者的过敏性疾病的方法,该方法包括向受试者施用有效量的式i的缀合物或其药学上可接受的盐。在实施方案中,本公开还提供了治疗对其有需要的受试者的慢性阻塞性肺病的方法,该方法包括向受试者施用有效量的式i的缀合物或其药学上可接受的盐。在实施方案中,本公开还提供了治疗对其有需要的受试者的慢性自发性荨麻疹的方法,该方法包括向受试者施用有效量的式i的缀合物或其药学上可接受的盐。
159、在实施方案中,本公开还提供了式i的缀合物或其药学上可接受的盐,用于疗法。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐,用于治疗炎性疾病。在某些实施方案中,炎性疾病是2型炎性疾病。在某些实施方案中,2型炎性疾病是例如特应性皮炎、嗜酸细胞性食管炎、鼻息肉病、哮喘、慢性鼻窦炎、过敏性疾病、慢性阻塞性肺病或慢性自发性荨麻疹。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐,用于治疗特应性皮炎。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐,用于治疗嗜酸细胞性食管炎。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐,用于治疗鼻息肉病。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐,用于治疗哮喘。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐,用于治疗慢性鼻窦炎。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐,用于治疗过敏性疾病。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐,用于治疗慢性阻塞性肺病。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐,用于治疗慢性自发性荨麻疹。
160、在实施方案中,本公开还提供了式i的缀合物或其药学上可接受的盐用于制造用于治疗炎性疾病的药物的用途。在某些实施方案中,炎性疾病是2型炎性疾病。在某些实施方案中,2型炎性疾病是例如特应性皮炎、嗜酸细胞性食管炎、鼻息肉病、哮喘、慢性鼻窦炎、过敏性疾病、慢性阻塞性肺病或慢性自发性荨麻疹。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐用于制造用于治疗特应性皮炎的药物的用途。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐用于制造用于治疗嗜酸细胞性食管炎的药物的用途。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐用于制造用于治疗鼻息肉病的药物的用途。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐用于制造用于治疗哮喘的药物的用途。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐用于制造用于治疗慢性鼻窦炎的药物的用途。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐用于制造用于治疗过敏性疾病的药物的用途。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐用于制造用于治疗慢性阻塞性肺病的药物的用途。在实施方案中,本公开提供了式i的缀合物或其药学上可接受的盐用于制造用于治疗慢性自发性荨麻疹的药物的用途。
161、本公开的核酸可以在宿主细胞中表达,例如,在核酸已经可操作地连接到表达控制序列之后。能够表达与其可操作地连接的核酸的表达控制序列是本领域所熟知的。表达载体可包括编码促进多肽从宿主细胞分泌的一种或多种信号肽的序列。含有感兴趣核酸(例如,编码抗体的重链或轻链的核酸)的表达载体可通过众所周知的方法(例如,稳定或瞬时转染、转化、转导或感染)转移到宿主细胞中。另外,表达载体可包含一种或多种选择标记物,例如四环素、新霉素和二氢叶酸还原酶,以帮助检测用期望的核酸序列转化的宿主细胞。
162、在另一个方面,本文提供了包含本文所述的核酸、载体或核酸组合物的细胞,例如宿主细胞。宿主细胞可以是用表达本文所述抗体的全部或一部分的一种或多种表达载体稳定地或瞬时地转染、转化、转导或感染的细胞。在一些实施方案中,宿主细胞可以用表达本公开的抗体的hc和lc多肽的表达载体稳定地或瞬时地转染、转化、转导或感染。在一些实施方案中,宿主细胞可以用表达本文所述抗体的hc多肽的第一载体和表达本文所述抗体的lc多肽的第二载体稳定地或瞬时地转染、转化、转导或感染。此类宿主细胞(例如,哺乳动物宿主细胞)可表达如本文所述的结合人il-4rα的抗体。已知能够表达抗体的哺乳动物宿主细胞包括cho细胞、hek293细胞、cos细胞和ns0细胞。
163、在一些实施方案中,细胞(例如,宿主细胞)包含含有编码seq id no:9、13、27、31、33、35、37、46、50或52的第一核酸序列以及编码seq id no:10、28或47的第二核酸序列的载体。
164、在一些实施方案中,细胞(例如,宿主细胞)包含含有编码seq id no:9、13、27、31、33、35、37、46、50或52的核酸序列的第一载体以及含有编码seq id no:10、28或47的核酸序列的第二载体。
165、本公开还提供了用于通过以下方式生产本文所述的结合人il-4rα的抗体的方法:在使得抗体被表达的条件下培养上述宿主细胞,例如哺乳动物宿主细胞,并且从培养基回收表达的抗体。可通过常规技术纯化其中已分泌了抗体的培养基。可以采用各种蛋白质纯化方法,并且此类方法是本领域已知的并且描述于例如deutscher,methods inenzymology 182:83-89(1990)以及scopes,protein purification:principles andpractice,第3版,springer,ny(1994)中。
166、本公开提供了产生缀合物的方法,该方法包括使本公开的化合物与抗人il-4rα抗体缀合。
167、本公开提供了产生缀合物的方法,该方法包括使式iv的化合物与抗人il-4rα抗体缀合。本公开提供了产生缀合物的方法,该方法包括使式iva的化合物与抗人il-4rα抗体缀合。本公开提供了产生缀合物的方法,该方法包括使式ivb的化合物与抗人il-4rα抗体缀合。本公开提供了产生缀合物的方法,该方法包括使式ivc的化合物与抗人il-4rα抗体缀合。本公开提供了产生缀合物的方法,该方法包括使式ivd的化合物与抗人il-4rα抗体缀合。
168、在一些实施方案中,所产生的缀合物是式i的缀合物。
169、本公开提供了产生缀合物的方法,该方法包括以下步骤:
170、(a)用还原剂还原抗人il-4rα抗体以产生还原的抗人il-4r抗体,其中抗人il-4rα抗体包含一个或多个工程化半胱氨酸残基;
171、(b)用氧化剂氧化还原的抗人il-4rα抗体,以产生氧化的抗人il-4r抗体;以及
172、(c)使氧化的抗人il-4rα抗体与本公开的化合物接触以产生缀合物。
173、本公开提供了产生缀合物的方法,该方法包括以下步骤:
174、(a)用还原剂还原抗人il-4rα抗体,其中抗人il-4rα抗体包含一个或多个工程化半胱氨酸残基;
175、(b)用氧化剂氧化抗人il-4rα抗体,以产生氧化的抗人il-4r抗体;
176、以及
177、(c)使氧化的抗人il-4rα抗体与下式的化合物接触
178、
179、以产生缀合物。
180、在一些实施方案中,还原剂是二硫苏糖醇。在一些实施方案中,氧化剂是脱氢抗坏血酸。在一些实施方案中,还原剂是二硫苏糖醇,并且氧化剂是脱氢抗坏血酸。
181、本公开还提供了通过本文所述的方法中的任何方法产生的抗体或其抗原结合片段。
182、在实施方案中,本公开还提供药物组合物,其包含本文所述的式i的缀合物或其药学上可接受的盐或抗体、核酸或载体与一种或多种药学上可接受的载剂、稀释剂或赋形剂。在实施方案中,本公开还提供药物组合物,其包含式i的缀合物或其药学上可接受的盐与一种或多种药学上可接受的载剂、稀释剂或赋形剂。在实施方案中,本公开还提供了药物组合物,其包含式i的缀合物与一种或多种药学上可接受的载剂、稀释剂或赋形剂。在实施方案中,本公开还提供了用于制备药物组合物的方法,该方法包括将式i的缀合物或其药学上可接受的盐与一种或多种药学上可接受的载剂、稀释剂或赋形剂混合。在实施方案中,本公开还包括用于合成式i的缀合物的新型中间体和方法。
- 还没有人留言评论。精彩留言会获得点赞!