一种肝细胞癌患者经肝切除术和TACE治疗疗效的方法
本发明属于肝癌治疗,具体为一种肝细胞癌患者经肝切除术和tace治疗疗效的方法。
背景技术:
1、肝癌是全球第三大癌症相关死亡原因且发病率呈上升趋势,预计到2025年将超过100万人受到肝癌的影响。其中肝细胞癌(hcc)约占75%—85%,是肝癌最常见的病理类型。为不同预后的肝癌患者提供合适的治疗方案,国内外学者提出了不同的诊疗指南,如中国肝癌分期(cnlc)和巴塞罗那肝癌分级(bclc)。在诊疗指南中,单发肝癌无论大小均被归类为肝癌早期(cnlc i或bclc a),但孤立性大肝癌患者(>5cm)的总生存期小于其他早期hcc患者(31.0月vs 49.0月,p<0.0001)。由于同一分期的患者之间仍存在异质性,即使采用同样治疗方式患者的生存时间也有差异。在临床实践中肝切除术和tace的适应症不断扩大,两者的适用范围存在重叠。虽然肝切除术是早期hcc患者的主要治疗方式,但由于患者年龄、慢性肝病、未来肝残余量以及患者一般状况等因素,对所有早期肝癌患者均采用肝切除术并不合适。同时早期hcc患者可以从tace和肝切除术治疗中获得相似的生存益处,tace可以作为一些早期肝癌患者的治疗方法。另外肝切除术可以延长部分中晚期肝癌患者的生存期。对于伴有门静脉癌栓(pvtt)且原发病灶可切除的肝癌患者,肝切除术也是可行的,中国肝癌协会也认为肝切除术是伴有i型/ⅱ型pvtt肝癌患者的首选治疗方案。而tace对伴有pvtt的晚期肝癌患者存在潜在的安全性和适用性,有显著的生存益处。越来越多的患者可以采取肝切除术和tace治疗,所以发现能从肝切除术或tace治疗中获得益处的患者是改善肝癌预后的关键。
2、但是传统的决策支持系统(如cnlc分期和bclc分期)将患者分为不同等级,并推荐相应的治疗策略。虽然临床指南对预后和治疗很重要,但决策能力可能不足。因此,许多方法比较了肝切除术与tace治疗对同一分期患者的疗效,但即使是随机对照试验也无法避免因果推断问题。尽管之前关于hcc的影像组学或深度学习研究已建立了预后模型,但它们并未考虑治疗方案的影响。虽有研究基于反事实原则考虑了治疗方案的影响,但只估计了治疗的平均效果。该研究只评估了不同治疗方法的总体疗效,因此无法根据患者的实际情况给出个性化的治疗建议。
技术实现思路
1、本发明的目的在于:为了解决上述提出的问题,提供一种肝细胞癌患者经肝切除术和tace治疗疗效的方法。
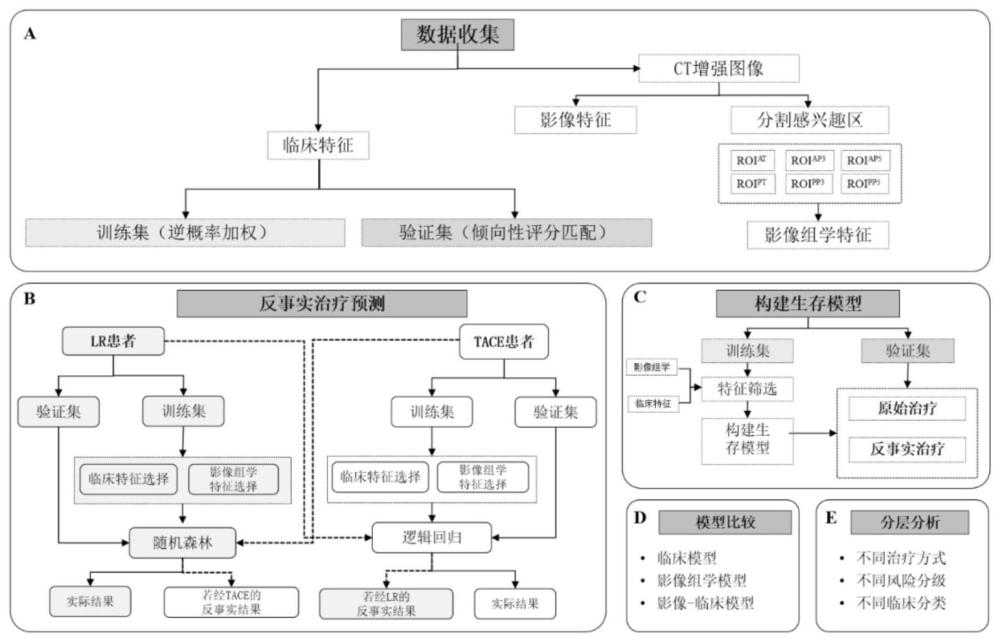
2、本发明采用的技术方案如下:一种肝细胞癌患者经肝切除术和tace治疗疗效的方法,所述肝细胞癌患者经肝切除术和tace治疗疗效的方法包括以下步骤:
3、步骤1:通过倾向性评分和逆概率加权控制不同治疗组患者间的混淆因素;
4、步骤2:对ct图像预处理、感兴趣区的分割及影像组学特征的提取;
5、步骤3:构建个体治疗效应分析模型,预测患者经两种治疗的死亡概率,并为患者选择最佳治疗方案;
6、步骤4:构建加速失效时间模型预测患者的生存时间;
7、步骤5:通过生存分析评估模型预测性能,并进一步利用分层分析评估。
8、在一优选的实施方式中,所述步骤s1中,为确保疗效和治疗方案的因果效应,通过倾向评分匹配(propensity score matching,psm)筛选出基线特征相似的患者,并将其作为独立的测试队列。对于其余未匹配的患者,采用逆概率加权法(inverse probability oftreatment weighting,iptw)平衡治疗组间的混杂因素,并将加权后的患者作为训练队列。
9、在一优选的实施方式中,所述步骤s1中,临床医生的主观判断可能会影响治疗方案的选择。为确保生存时间受治疗方案而非混杂因素的影响,对患者进行psm。计算基线特征与治疗方案、生存时间和生存状态的相关系数。结果显示,cnlc、肝外转移、门静脉瘤栓、肿瘤数目、albi分级、肝硬化和alb与治疗方案、生存时间和生存状态显著相关(p<0.05)。上述明显相关的基线特征被用作匹配特征。采用非参数匹配法,以1:1的比例筛选出肝切除术组和tace组中匹配特征相似的患者。
10、在一优选的实施方式中,所述步骤s1中,未配对的患者通过iptw校正混杂因素,从而收敛治疗组之间的内部混杂分布。上述匹配特征被用作需要平衡的混杂因素。以治疗方案为因变量,混杂因素为自变量,通过逻辑回归构建倾向得分模型。为每位患者计算倾向得分(propensityscore,ps)(患者接受肝切除术治疗的概率)。使用ps对每位患者进行加权:权重=1/ps(肝切除术组),权重=1/(1-ps)(tace组)。iptw治疗后,各治疗组的基线临床特征无明显差异,混杂因素导致的偏倚已得到控制。因此,肝切除术组和tace组的疗效相当。iptw加权患者被用作训练队列。
11、在一优选的实施方式中,所述步骤s2中具体内容包括:
12、步骤2.1:采集患者ct图像并进行图像预处理。采用患者术前一个月内的增强ct图像进行分析。为减少图像间的异质性,提高研究可重复性,对图像进行以下预处理,首先通过线性插值算法将所有图像重采样为统一体素大小,随后使用固定面源宽度(25hu)对体素强度进行离散化。
13、步骤2.2:在预处理后的ct图像上勾画肿瘤感兴趣区。利用3dslicer软件在预处理后的图像上由两名放射科医生沿肿瘤边缘勾画感兴趣区(regionsofinterest,roi)。随后利用侵蚀扩张算法向外扩张3mm,5mm得到瘤周roi。最终获得6个rois:动脉期肿瘤roi(roiat),动脉期瘤周3mmroi(roiap3),动脉期瘤周5mmroi(roiap5),静脉期肿瘤roi(roipt),静脉期瘤周3mmroi(roipp3),静脉期瘤周5mmroi(roipp5)。
14、步骤2.3:采用组间和组内相关系数(icc)评估放射科医生勾画roi的可重复性,即随机抽取20例患者,两位医生同时勾画roi并计算组间相关系数;随后间隔1个月后,再次勾画所抽取的20例患者的roi并计算组内相关系数。组内和组间icc同时大于0.7的影像组学特征被认为受勾画可变性的影响较小。
15、步骤2.4:提取ct影像组学特征。影像组学特征的提取由pyradiomics包实现。提取的影像组学特征分为两组:基于原始图像和基于滤波图像的特征。基于原始图像特征包括14个形状特征、18个一阶特征和75个纹理特征,共计107个特征。纹理特征包括24个glcm特征、14个gldm特征、16个glrlm特征、16个glszm特征和5个ngtdm特征。基于滤波图像的特征,使用小波变换和对数变换将原始图像分别分解为8个和5个滤波图像,然后提取一阶特征和纹理特征。各特征的计算公式见网页:https://pyradiomics.readthedocs.io/en/latest/features.html。
16、步骤2.5:采取z-score标准化对影像组学特征值进行预处理,减少变量间量纲差异的影响。
17、在一优选的实施方式中,所述步骤s3中,对于两种治疗方案(肝切除术组和tace组)的患者,分别构建了两个生存预测模型(deathhepatectomy和deathtace),以便根据患者的临床特征和影像组学特征预测其生存状况。然后,使用deathhepatectomy和deathtace模型预测每位患者的死亡概率和假设治疗方案转换后的反事实死亡概率。比较两种死亡概率,为患者选择较优治疗方案。
18、在一优选的实施方式中,所述步骤s3中,具体内容包括:
19、步骤3.1:构建deathhepatectomy模型。每次实验都使用随机生存森林(rsf)来选择预测准确率大于0的特征,实验重复100次。被选中80次及以上的特征被用作治疗方案的预测因子。在临床特征中,生存时间、门静脉肿瘤血栓、肝硬化、融合性病变、瘤内坏死、肿瘤数目、肿瘤直径、年龄和alb被用作治疗方案的预测因子。radscores由特征和权重(radscore_a、radscore_p、radscore_a3、radscore_p3、radscore_a5和radscore_p5)线性相乘计算得出。将所选的临床特征和具有不同radscores的放射组学特征结合起来,构建不同的随机森林模型。用接收者操作特征曲线下面积(auc)、f1分数、精确度、灵敏度、特异度和准确度来比较上述模型的性能。性能最佳的模型被选为deathhepatectomy模型。
20、综上所述,由于采用了上述技术方案,本发明的有益效果是:
21、本发明中,提供一种基于反事实理论的机器学习模型以预测肝细胞癌患者经肝切除术和tace治疗疗效的方法。在该方法中以临床数据和ct影像组学特征为输入数据,分别构建预测患者经肝切除术或tace治疗的死亡概率的机器学习模型,基于反事实理论为患者推荐最佳治疗方案,同时以加速失效时间模型为预后模型框架从而预测患者的生存时间。将auc值作为模型功效评价指标,以评估模型区分度;基于反事实理论,建立了肝癌患者肝切除术与tace治疗的预测模型。比较了采用真实治疗方案和反事实治疗方案的患者的预后。我们的机器学习模型估计了可能从首选治疗方案(肝切除术和tace)中获益的患者,从而为患者推荐可能获益更大的治疗方案。此外,还构建了一个预测hcc患者os的预后模型。该预后模型不仅具有较高的预测能力,还能将hcc患者分为生存时间差异显著的亚组。对于高危组患者,术后应采取更严格的随访策略或考虑额外的辅助治疗。对于低风险组患者,考虑到风险收益比,可采取更合理的随访方案。
- 还没有人留言评论。精彩留言会获得点赞!