一种共载双硫仑和硫化铜的温敏纳米给药系统及其制备和应用
本发明属于纳米载药,涉及一种共载双硫仑和硫化铜的温敏纳米给药系统及其制备和应用,具体涉及一种含有双硫仑和硫化铜的上临界温敏给药系统和制备方法,以及双硫仑和硫化铜的上临界温敏给药系统能够进行对肿瘤的选择性靶向给药和激光照射下的药物在肿瘤部位的控释。
背景技术:
1、据全球最新癌症统计报告显示,结直肠癌已成为仅次于肺癌的第三大常见癌症。据估计每年全世界有超过100万人被新确诊为结直肠癌,其发病率位居全球癌症发病率第3位,死亡率位居第2位。据调查显示,造成结直肠癌发病率和死亡率高的一大原因是公众缺少对结直肠癌高危因素的认知以及其早筛早诊的意识薄弱。在中国,结直肠癌也是常见的恶性肿瘤之一,其新发病人数仅次于肺癌,成为第二大癌症,每年有超过28万人死于结直肠癌,占全球该类癌症死亡人数的30.6%。
2、双硫仑(disulfiram,dsf)是fda批准的用于治疗酒精中毒的药物,在临床前研究中已被证实对多种癌症有效。dsf在体内被代谢成为二乙基二硫代氨基甲酸盐,该代谢产物可以与体内的cu2+螯合形成二乙基二硫代氨基甲酸铜络合物。在目前的研究中已经证实cu(ddc)2是dsf的主要抗癌活性物质。
3、已有研究已经表明,dsf的抗肿瘤作用具有铜离子依赖性,但是人体内的cu2+浓度太低,因此需要额外补充铜离子来增强dsf的抗肿瘤效果。最近,超小硫化铜纳米粒子因其在近红外区的优异的光热转换性能、良好的生物降解性、低毒性和低成本而被广泛应用于光疗和化疗的协同治疗中。在激光照射下,硫化铜纳米粒子可释放出cu2+,其可以与特定的前药配位,表现出优异的抗癌效果。因此,硫化铜纳米粒子的引入可以解决基于dsf的癌症治疗的铜源问题,且能实现化疗和光热疗法的协同治疗。
4、在化疗和光热疗法的联合治疗中,药物递送系统的应用可以有效提高药物的抗肿瘤效果。在目前的dsf和cus nps联合使用的递送系统中,大多是以cus nps作为载体进行dsf的负载。一些研究团队开发了负载有dsf的中空硫化铜纳米粒子,但这种中空硫化铜纳米粒子往往粒径较大,不能迅速地从体内清除出去。也有研究团队合成了一种能被肾脏快速清除的超小硫化铜纳米粒子,并且利用dsf的代谢物ddc与cus nps之间的配位作用,将ddc直接负载在cus nps的表面。但是这种方式需要对ddc和cus nps的投料比进行严格把控,若ddc稍有过量,便会产生过多的具有细胞毒性的cu(ddc)2复合物,而cu(ddc)2复合物是一种疏水性物质,会影响该药物递送系统的稳定性。此外,这种递送系统在体内递送过程中,可能会有部分生成的cu(ddc)2复合物泄漏出来,对正常组织产生毒性。
技术实现思路
1、本发明的目的是针对目前药物递送缓释和靶部位速释的矛盾、dsf的抗肿瘤作用对铜离子依赖性以及单一治疗效果有限的问题,提供一种共载双硫仑和硫化铜的温敏纳米给药系统,采用上临界溶解温度型材料聚(丙烯腈-丙烯酰胺)-聚乙二醇聚合物包封双硫仑(dsf)和硫化铜纳米粒子(cus nps)得到共载胶束,该胶束在聚合物的上临界溶解温度以下时可以在体循环中保持稳定,防止药物泄漏;选择性靶向至肿瘤部位并能通过近红外激光照射使硫化铜发生光热转换,实现热疗;温度升高达到上临界溶解温度实现肿瘤部位的定位控释,并进一步借助生成的cu2+在肿瘤部位与双硫仑原位合成具有抗肿瘤活性的二乙基二硫代氨基甲酸铜(cu(ddc)2)复合物,用于肿瘤化疗。这种共载双硫仑和硫化铜纳米粒的上临界溶解温度型胶束,实现了药物的定位控释的同时,还能达到化疗和光热疗法的协同治疗,有效提高肿瘤治疗效果。
2、本发明的上述目的通过以下技术方案实现:
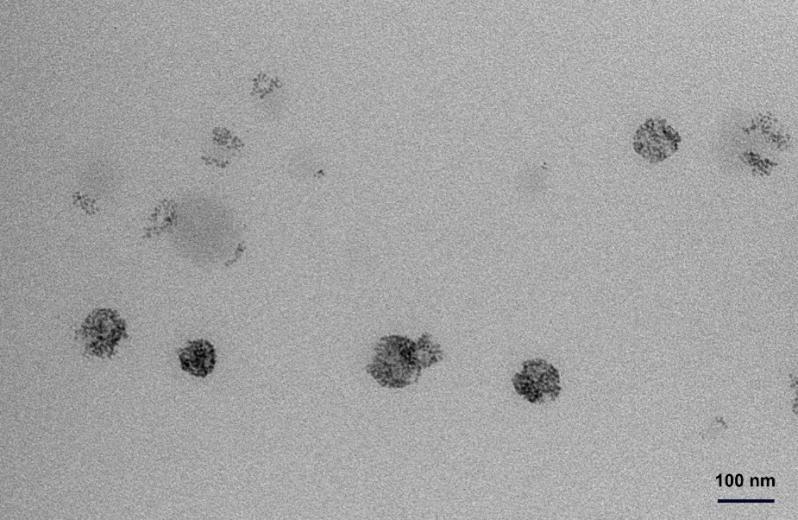
3、一种共载双硫仑和硫化铜的温敏纳米给药系统,粒径大小为90~100nm,由双硫仑、硫化铜纳米粒子和包封所述双硫仑、硫化铜纳米粒子的上临界溶解温度型胶束载体材料在水中自组装得到,其中双硫仑的质量百分比为0.1%~8.3%,硫化铜纳米粒子的质量百分比为8.3%~33.3%,上临界溶解温度型胶束载体材料的质量百分比为62.5%~83.4%;所述上临界溶解温度型胶束载体材料采用聚(丙烯腈-丙烯酰胺)-聚乙二醇聚合物,由丙烯酰胺、丙烯腈、偶氮二异丁腈和端基琥珀酰亚胺功能化的聚乙二醇混合制备得到。
4、作为优选,硫化铜纳米粒子粒径大小为2~5nm。
5、作为优选,所述端基琥珀酰亚胺功能化的聚乙二醇的分子量为5000~10000。
6、作为优选,所述双硫仑和硫化铜纳米粒子的质量比为1:(1~333);所述双硫仑和胶束载体材料的质量比为1:(7.5~834);所述硫化铜和胶束载体材料的质量比为1:(1.8~10)。
7、本发明的第二个目的是提供上述共载双硫仑和硫化铜的温敏纳米给药系统的制备方法,采用空白胶束载药法联合溶剂挥发法,具体包括以下步骤:
8、步骤(1)、制备空白胶束溶液
9、将聚(丙烯腈-丙烯酰胺)-聚乙二醇聚合物(p(aam-co-an)-peg)溶于水中,充分溶解并搅拌,得到空白胶束溶液;
10、步骤(2)、制备单载双硫仑胶束溶液
11、在搅拌条件下,将双硫仑(dsf)和无水乙醇的混合溶液加入空白胶束溶液中,反应后挥发除去无水乙醇,得到单载双硫仑胶束溶液;
12、步骤(3)、制备共载双硫仑和硫化铜的温敏纳米给药系统
13、将硫化铜纳米粒子(cus nps)分散在二氯甲烷中,然后加入单载双硫仑胶束溶液中超声得到乳化液,乳化液挥发除去二氯甲烷后得到所述共载双硫仑和硫化铜的温敏纳米给药系统。
14、作为优选,所述聚(丙烯腈-丙烯酰胺)-聚乙二醇聚合物采用丙烯酰胺、丙烯腈、偶氮二异丁腈和端基琥珀酰亚胺功能化的聚乙二醇混合制备得到。
15、作为优选,所述聚(丙烯腈-丙烯酰胺)-聚乙二醇聚合物采用以下步骤制备得到:
16、将丙烯酰胺和丙烯腈溶解于无水二甲基亚砜中,均匀混合后,加入引发剂偶氮二异丁腈,充分溶解后通氮气30~40min,然后置于60~70℃水浴中搅拌反应8~10h;反应结束后冷却到室温,用甲醇作为沉淀剂将聚合物沉淀出来,离心洗涤干燥,即得聚(丙烯腈-丙烯酰胺)聚合物;
17、将所得聚(丙烯腈-丙烯酰胺)聚合物和端基琥珀酰亚胺功能化的聚乙二醇溶于二甲基亚砜中,充分溶解后,转移至50~60℃水浴中反应8~10h;反应结束后用纯水透析,随后冷冻干燥,即得所述聚(丙烯腈-丙烯酰胺)-聚乙二醇聚合物。
18、作为优选,丙烯腈和丙烯酰胺的摩尔比为1:(3~5),端基琥珀酰亚胺功能化的聚乙二醇与聚(丙烯腈-丙烯酰胺)聚合物的摩尔比为1:(5~6)。
19、作为优选,所述硫化铜纳米粒子采用以下步骤制备得到:
20、在加热条件下,将硫粉、乙酰丙酮铜溶于油胺和氯仿中进行反应,反应结束后离心洗涤,即得所述硫化铜纳米粒子。
21、本发明的第三个目的是提供上述共载双硫仑和硫化铜的温敏纳米给药系统在制备治疗肿瘤药物中的应用。
22、本发明由于采用上述方案,将dsf和cus nps共同包裹在同一温敏胶束中,实现了给药后有效靶向递送至肿瘤部位,达到体循环缓释和肿瘤部位速释目的,又具有联合治疗肿瘤的效果。
23、本发明配方简单,制造容易,操作简便,起到治疗肿瘤疾病的作用。
24、本发明的有益效果为:
25、1.本发明提供的dsf和cus nps共载的上临界溶解温度型胶束,其疏水性的核可以提高dsf与cus nps的载药量和包封率,能阻止dsf和cus nps在递送过程中的泄露,并将其共同靶向递送至肿瘤部位,经近红外激光照射后(温度高于上临界溶解温度)促使药物在靶区控释,cus nps中的铜离子释放,与无毒的dsf结合,原位生成具有细胞毒性的cu(ddc)2,产生原位化疗效果,胶束结构被破坏,进而将药物从胶束疏水性的核中完全释放出来,其中过量的超小cus nps还可以被肾脏快速清除,与将ddc直接负载在cus nps表面相比具有更好的生物安全性;同时,cu2+与肿瘤部位过量的过氧化氢(h2o2)发生类芬顿反应,会导致细胞内ros水平升高,发挥化学动力学疗法的作用;更重要的是,cu2+导致细胞内铜离子过量,还能实现肿瘤铜死亡。dsf/cus@m在提高药物原位化疗的同时有效联合光热治疗、化学动力学疗法和铜死亡,能够实现肿瘤的安全高效治疗。
26、2.本发明采用的具有上临界溶解温度的聚(丙烯腈-丙烯酰胺)-聚乙二醇聚合物胶束,提高了双硫仑和硫化铜纳米粒子在水中的溶解性。采用的cus nps作为光热剂,具有高的光热转换效率,因其所具有的超小粒径,具有快速的肾脏可清除性。
27、3.本发明采用空白胶束溶液载药法和乳化溶剂挥发法制备药物胶束,制备方法简单,制备时间短,所制备得到的共载胶束水溶性好,具有被动靶向功能,实现了载药胶束体内药物的控释,抗癌效果显著,具有良好的应用前景。
28、4.本发明配方简单、合理,加工制造方法容易、使用方便,产品质量可靠,采用空白胶束溶液载药法和乳化溶剂挥发法制备,产量较高,载药量、包封率较高,靶向控释性能和联合治疗效果良好。
- 还没有人留言评论。精彩留言会获得点赞!