金诺芬在制备错配修饰缺陷或ARID1A缺陷肿瘤药物中的应用
背景技术:
0、技术背景:
1、癌症的治疗是医学领域的重要挑战之一,相关研究人员一直在寻找更有效的治疗策略。金诺芬(auranofin)作为一种白金类化合物,在抗癌治疗中显示出通过与dna结合干扰复制和转录过程,诱导癌细胞凋亡的潜力,但其临床应用受限于可能引发的严重副作用,如肾脏、神经毒性和听力损伤,以及长期使用可能导致的癌细胞耐药性问题,这些问题不仅影响患者生活质量,还可能降低治疗效果,使得金诺芬在实际应用中面临挑战。
2、在肿瘤的发生和发展过程中,复制压力对肿瘤细胞的生存和增殖具有重要影响。肿瘤细胞在快速增殖过程中,其dna复制机制面临内源性损伤,导致复制压力的产生。这种压力是细胞维持基因组稳定性的关键因素。肿瘤细胞由于g1/s检查点的缺陷,使得它们在dna复制过程中更容易出错,从而更加依赖有效的复制压力应对机制以避免基因组突变的累积。如果复制压力得不到有效管理,肿瘤细胞可能因有丝分裂崩溃而死亡。因此,复制压力的分子机制是肿瘤细胞生存的一个脆弱点,为开发新的肿瘤治疗策略提供了潜在的靶点。
3、肿瘤细胞的发生、发展和增殖通常与遗传性缺陷有关,特别是与错配修复缺陷(mismatch repair deficiency,mmrd)或者arid1a(at-rich interactive domain-containing protein 1a)关系密切。其中mmrd是一种遗传性缺陷,是指细胞内错配修复(mmr)系统功能受损,导致dna碱基配对错误无法得到及时纠正。mmrd肿瘤在临床上具有高度微卫星不稳定性(msi-h)等特征,这种不稳定性导致肿瘤的发生和发展。对于mmrd肿瘤的治疗一直是一个挑战,传统的治疗手段效果有限。mmrd缺陷通常是包括mlh1,msh2,msh6,pms2等基因缺失引起的。其中mlh1的突变频率相对较高,在所有癌症中的突变率约为1.28%,其中结肠癌、肺癌、子宫内膜癌、乳腺浸润性导管癌和常规型多形性胶质母细胞瘤突变发生率最高。然而对于这些mmrd肿瘤,目前并没有太多很好的靶向治疗策略。
4、arid1a是在dna染色质重塑过程中起关键作用的基因。arid1a是swi/snf染色质重塑复合物的一个组成部分,参与调节基因表达、dna修复和细胞周期控制。arid1a的突变通常导致其功能丧失,影响染色质重塑和基因表达调控,从而促进肿瘤发生。大约6%的人类癌症患者携带arid1a基因失活突变。一些癌症类型显示出最高的arid1a失活突变和表达丧失发生频率,包括卵巢癌(约50%)、子宫内膜癌(约37%)、胃癌(20-30%)、膀胱癌(约20%)、肝细胞癌(约14%)、黑色素瘤(约12%)、结直肠癌(约9%)和肺癌(约8%)。那么如何对含有arid1a突变的癌症患者进行更加有效的靶向治疗,是目前临床研究的重点之一。
5、本发明创造性的发现金诺芬可以竞争性的结合topbp1,通过抑制atr信号通路的激活,使得肿瘤细胞频繁复制产生的复制压力不能有效缓解最终导致肿瘤细胞的死亡。本发明创造性地发现在arid1a缺陷或者错配修复通路缺陷的肿瘤细胞中,使用金诺芬治疗会增加肿瘤的敏感性,在较低的剂量下使用金诺芬就可以杀伤肿瘤细胞,增加病人的生存期,克服了金诺芬副作用大且会耐药的缺点。
技术实现思路
0、
技术实现要素:
1、本发明保护提供一种topbp1的竞争性的抑制剂在制备用于治疗和/或改善肿瘤药物组合物中的应用,所述肿瘤选自:
2、i)错配修复缺陷(mmrd)肿瘤;
3、或者ii)arid1a缺陷的肿瘤。
4、进一步的,所述错配修复缺陷肿瘤为mlh1缺陷肿瘤。
5、进一步的,所述topbp1的竞争性的抑制剂的结合位点为topbp1的brct7-8口袋。
6、进一步的,所述topbp1的竞争性的抑制剂具有破坏phf8-topbp1,fancj-topbp1的结合的作用。
7、进一步的,所述topbp1的竞争性的抑制剂为金诺芬。
8、本发明第二个方面提供一种治疗装置,其特征在于,包含模块i)和模块ii):
9、模块i)为检测模块,所述模块i)包括检测离体样品是否为arid1a缺陷、mlh1缺陷所
10、需的检测试剂;
11、模块ii)为鉴定给药模块,所述模块ii)将topbp1的竞争性的抑制剂施用于模块i)鉴定为arid1a缺陷、mlh1缺陷的离体样本患者。
12、进一步的,所述装置中的模块i)中所述的检测试剂为arid1a或mlh1基因、arid1a或mlh1基因表达产物特异性杂交的生物分子,和/或以arid1a或者mlh1基因为检测目的物的检测试剂。
13、进一步的,所述装置中的模块ii),所述topbp1的竞争性的抑制剂具有结合到topbp1的brct7-8口袋的作用或者所述topbp1的竞争性的抑制剂具有破坏phf8-topbp1,
14、fancj-topbp1的结合的作用;优选的所述topbp1的竞争性的抑制剂为金诺芬。
15、本发明第三个方面提供检测生物标志物的试剂在制备金诺芬抗肿瘤疗效预测试剂盒中的应用,所述生物标志物为:
16、i)arid1a或mlh1基因;或者
17、ii)arid1a或mlh1基因表达产物。
18、进一步的,所述肿瘤包括结肠癌、肺癌、子宫内膜癌、乳腺浸润性导管癌、常规型多形性胶质母细胞瘤、卵巢癌、胃癌、膀胱癌、肝细胞癌、黑色素瘤、和/或结直肠癌。
19、本发明第四个方面提供一种药物组合物,其包含组分1和组分2,
20、所述组分1为金诺芬;
21、所述组分2为mlh1抑制剂或者arid1a抑制剂。
22、本发明第五个方面提供金诺芬与mlh1抑制剂和/或arid1a抑制剂在制备抗肿瘤药物中的应用,所述肿瘤为arid1a缺陷或mlh1缺陷型肿瘤。
23、本发明具有以下优势:
24、1.发现了金诺芬新的作用机制:本发明打破了金诺芬传统意义上的作用是通过抑制硫氧还蛋白还原酶(thioredoxin reductase,trxr)来发挥其药理效应的作用的局限,揭示了金诺芬作为一种小分子化合物,能够结合到topbp1的brct7-8口袋,占据phf8与
25、fancj的关键结合位点,从而抑制phf8-topbp1和fancj-topbp1复合体的形成。
26、2.发现金诺芬影响复制压力应答:金诺芬通过干扰topbp1的功能,抑制了atr信号的激活和rpa在受损染色质上的积累,这对于复制压力的调控和细胞对dna损伤的响应至关重要。
27、3.发现金诺芬在特定遗传背景下具有增强的抗肿瘤活性:金诺芬显示出对错配修复缺陷比如mlh1缺陷的结直肠癌或者arid1a缺陷的结直肠癌具有合成致死效应。
28、4.金诺芬在arid1a缺陷或mlh1缺陷的肿瘤的治疗方面展现出增强的肿瘤抑制效果:
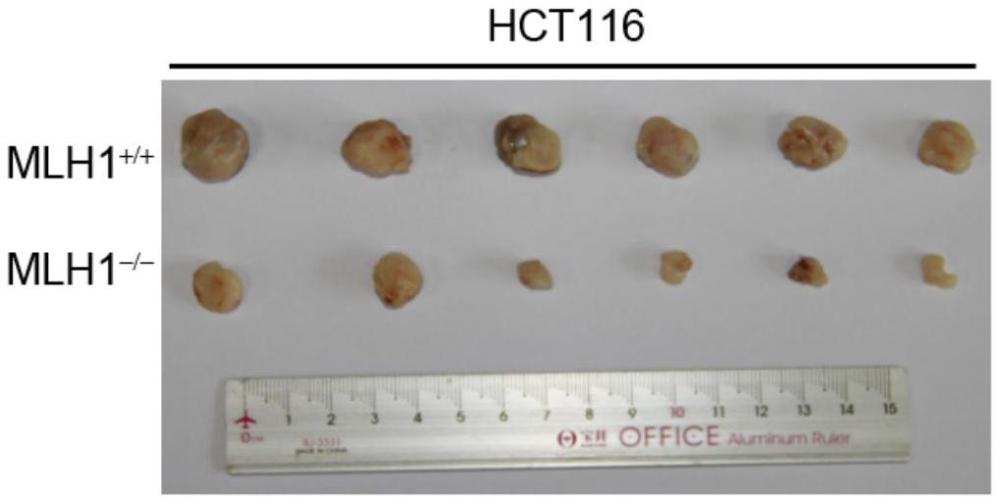
29、在细胞实验和异种移植动物模型中,金诺芬与arid1a缺陷或mlh1缺陷的结直肠癌细胞共处理时,显示出比单独处理更显著的肿瘤生长抑制效果。
30、5.本发明创造性的发现,在治疗中有较高的副作用以及耐药性的金诺芬对于携带arid1a或mlh1突变的肿瘤患者有良好的敏感性,因此开发了将金诺芬在低剂量的抗肿瘤作用应用在实现精准医疗的同时,也将实现老药新用,促进了化疗药高疗效、低副作用的治疗潜力。
31、6.临床应用潜力:由于金诺芬已经作为fda批准的药物用于治疗类风湿性关节炎,本发明开发的该药物在制备肿瘤药物中的应用可能会加速临床转化过程。
- 还没有人留言评论。精彩留言会获得点赞!