间充质干细胞注射液、制备工艺及治疗自身免疫病应用的制作方法
本发明属于生物医药,具体涉及间充质干细胞注射液、制备工艺及治疗自身免疫病应用。
背景技术:
1、脐带间充质干细胞(human umbilical cordmensenchymalstemcell,huc-mscs)来源广泛,取材方便,对供着无损伤,具有独特的免疫调节功能,可以抑制多种免疫细胞的功能,如t细胞、b细胞、nk细胞、中性粒细胞、单核巨噬细胞、抗原提呈细胞等。在众多体内或体外研究中表明,间充质干细胞对免疫系统表现出很强的抑制作用,因而广泛应用于临床治疗免疫相关性疾病,如移植物抗宿主病、类风湿关节炎等。
2、碱性成纤维细胞生长因子(bfgf)可促进干细胞生长、增殖和并维持干细胞干性;基质细胞衍生因子-1α(sdf-1α)具有促进干细胞归巢、趋化和增殖的作用,在间充质干细胞分离培养早期使用可加快干细胞从脐带等组织中分离获取的速度并有利于保持干细胞活性;叶酸(维生素b9)对细胞的dna合成和细胞分裂有重要作用;而甲基-β-环糊精(mβcd)在细胞培养中可改善细胞膜的流动性和完整性、提高细胞培养效率,并调节细胞膜上的胆固醇水平。
3、肿瘤坏死因子(tumor necrosis factor,tnf-α)是一种多效细胞因子,生物学和医学研究证明,tnf-α参与了免疫调节、炎症、感染性休克、凋亡和自身免疫等生理和病理过程,对机体稳态和疾病发生发展起重要作用。tnf-α与两型tnf受体(tnfr1和tnfr2)的相互作用及下游信号通路的异常激活是类风湿关节炎、溃疡性结肠炎等自身免疫性疾病发生发展的重要因素。总体上说,tnf-α引起的炎症、凋亡或程序性坏死反应,主要是通过与tnfr1的结合而触发。可溶性肿瘤坏死因子ⅰ型受体(stnfr1)是tnfr1的胞外区域,它可以竞争性阻断tnfr1与tnf-α结合,降低tnf-α对细胞的毒性。因此,stnfr1可以作为tnf-α的拮抗剂,用于疾病的治疗,在医学领域具有重要的研究价值。
4、c-met具有酪氨酸激酶的活性,被配体激活后介导细胞信息传递,是细胞增殖、分化和运动的重要调节因素。肝细胞生长因子(hepatocyte growth factor,hgf)是一种多效性细胞因子,能够通过激活其受体c-met来诱发多种细胞反应,包括增殖、迁移和存活。已有研究表明hgf/c-met信号转导通路具有促炎作用,能够直接影响炎症中的白细胞反应。因此,靶向抑制hgf/c-met途径可能是的一种免疫相关性疾病有潜力的治疗方法。
5、目前,对于脐带间充质干细胞在临床治疗免疫相关性疾病的研究初见成效,但需开发一种治疗免疫相关性疾病更有效的间充质干细胞注射液。
技术实现思路
1、基于现有技术中存在的问题和不足,本发明旨在提供间充质干细胞注射液、制备工艺及治疗自身免疫病应用。本发明提供的间充质干细胞注射液采用完全培养液-1、完全培养液-2、完全培养液-3在特定的培养条件下制备得到;所述的完全培养液-1包括:含有fbs、bfgf、sdf-1α和叶酸的基础培养液;完全培养液-2包括:含有fbs、bfgf、sdf-1α、叶酸和氢气的基础培养液;完全培养液-3包括:含有fbs、bfgf、甲基-β-环糊精和叶酸的基础培养液。本发明用于制备间充质干细胞注射液的间充质干细胞工作库细胞安全性好,具有较好的细胞增殖能力,高表达cd73、cd90、cd105,不表达cd19、cd34、cd45、cd11b、hla-dr,具有成骨成脂的分化能力和较好的生物学效力。本发明提供的间充质干细胞注射液符合药典标准,hgf、stnfr1含量高,能够起到防治自身免疫病的效果。
2、本发明的技术方案如下:
3、一方面,本发明提供了一种间充质干细胞注射液,所述的间充质干细胞注射液的制备方法包括如下步骤:
4、s1、脐带组织置于培养瓶孵育后,加入完全培养液-1培养传代,得到p0代人脐带间充质干细胞;
5、s2、p0代人脐带间充质干细胞用完全培养液-2培养传代,获得p1代人脐带间充质干细胞;
6、s3、p1代人脐带间充质干细胞用完全培养液-3培养传代,获得p2代人脐带间充质干细胞,离心后弃去上清液,收集细胞作为种子库细胞;
7、s4、种子库细胞用完全培养液-3继续培养至p5代并冻存,得到间充质干细胞工作库细胞;
8、s5、将间充质干细胞工作库细胞用细胞保存液重悬,得间充质干细胞注射液。
9、具体地,步骤s1所述的完全培养液-1包括:含有fbs、bfgf、sdf-1α和叶酸的基础培养液。
10、优选地,步骤s1所述的完全培养液-1包括:含有10%-15%v/v fbs、5-10μg/lbfgf、10-100μg/l sdf-1α和0.35-0.80mg/l叶酸的基础培养液。
11、进一步优选地,步骤s1所述的完全培养液-1包括:含有10%v/v fbs、7.5μg/lbfgf、50μg/l sdf-1α和0.35mg/l叶酸的基础培养液。
12、具体地,步骤s2所述的完全培养液-2包括:含有fbs、bfgf、sdf-1α、叶酸和氢气的基础培养液。
13、优选地,步骤s2所述的完全培养液-2包括:含有10%-15%v/v fbs、5-10μg/lbfgf、10-100μg/l sdf-1α、0.35-0.80mg/l叶酸和0.5-2mg/l氢气的基础培养液。
14、进一步优选地,步骤s2所述的完全培养液-2包括:含有10%v/v fbs、7.5μg/lbfgf、50μg/l sdf-1α、0.35mg/l叶酸和1mg/l氢气的基础培养液。
15、具体地,步骤s3和步骤s4所述的完全培养液-3包括:含有fbs、bfgf、甲基-β-环糊精和叶酸的基础培养液。
16、优选地,步骤s3和步骤s4所述的完全培养液-3包括:含有10%-15%v/v fbs、5-10μg/l bfgf、1-2mg/l甲基-β-环糊精和0.35-0.80mg/l叶酸的基础培养液。
17、进一步优选地,步骤s3和步骤s4所述的完全培养液-3包括:含有10%v/vfbs、7.5μg/l bfgf、1mg/l甲基-β-环糊精和0.35mg/l叶酸的基础培养液。
18、优选地,所述的基础培养液包括但不限于dmem/f12培养液、dmem培养液、msc生长培养基、rpmi 1640或e8。
19、进一步优选地,所述的基础培养液为dmem/f12培养液。
20、具体地,步骤s1所述的培养条件包括5%co2,1%-2%o2。
21、优选地,步骤s1所述的培养条件包括5%co2,1%o2。
22、具体地,步骤s1包括:脐带组织置于培养瓶5%co2孵育24h后,加入完全培养液-1在5%co2,1%-2%o2条件下培养传代,得到p0代人脐带间充质干细胞。
23、优选地,步骤s1包括:脐带组织置于培养瓶5%co2孵育24h后,加入完全培养液-1在5%co2,1%o2条件下培养传代,得到p0代人脐带间充质干细胞。
24、具体地,步骤s1中所述的培养包括:加入5ml完全培养液-1,过夜培养后补加10ml完全培养液-1继续培养。
25、具体地,步骤s2中所述的培养条件包括5%co2,5%-10%o2;
26、优选地,步骤s2中所述的培养条件包括5%co2,5%o2。
27、具体地,步骤s3中所述的培养条件包括5%co2,18%-20%o2。
28、优选地,步骤s3中所述的培养条件包括5%co2,18%o2。
29、具体地,步骤s5所述的细胞保存液由人血白蛋白、肝素、右旋糖酐-40和复方电解质溶液组成。
30、优选地,步骤s5所述的细胞保存液包括10-20mg/ml人血白蛋白,50-100iu/ml肝素和50-100mg/ml右旋糖酐-40。
31、进一步优选地,步骤s5所述的细胞保存液包括10mg/ml人血白蛋白,50iu/ml肝素和60mg/ml右旋糖酐-40。
32、具体地,所述的间充质干细胞注射液中间充质干细胞的密度为0.5×106-1×108cells/ml。
33、优选地,所述的间充质干细胞注射液中间充质干细胞的密度为1×106cells/ml。
34、另一方面,本发明提供了上述间充质干细胞注射液的制备方法。
35、具体地,所述的制备方法包括如下步骤:
36、s1、脐带组织置于培养瓶孵育后,加入完全培养液-1培养传代,得到p0代人脐带间充质干细胞;
37、s2、p0代人脐带间充质干细胞用完全培养液-2培养传代,获得p1代人脐带间充质干细胞;
38、s3、p1代人脐带间充质干细胞用完全培养液-3培养传代,获得p2代人脐带间充质干细胞,离心后弃去上清液,收集细胞作为种子库细胞;
39、s4、种子库细胞用完全培养液-3继续培养至p5代并冻存,得到间充质干细胞工作库细胞;
40、s5、将间充质干细胞工作库细胞用细胞保存液重悬,得间充质干细胞注射液。
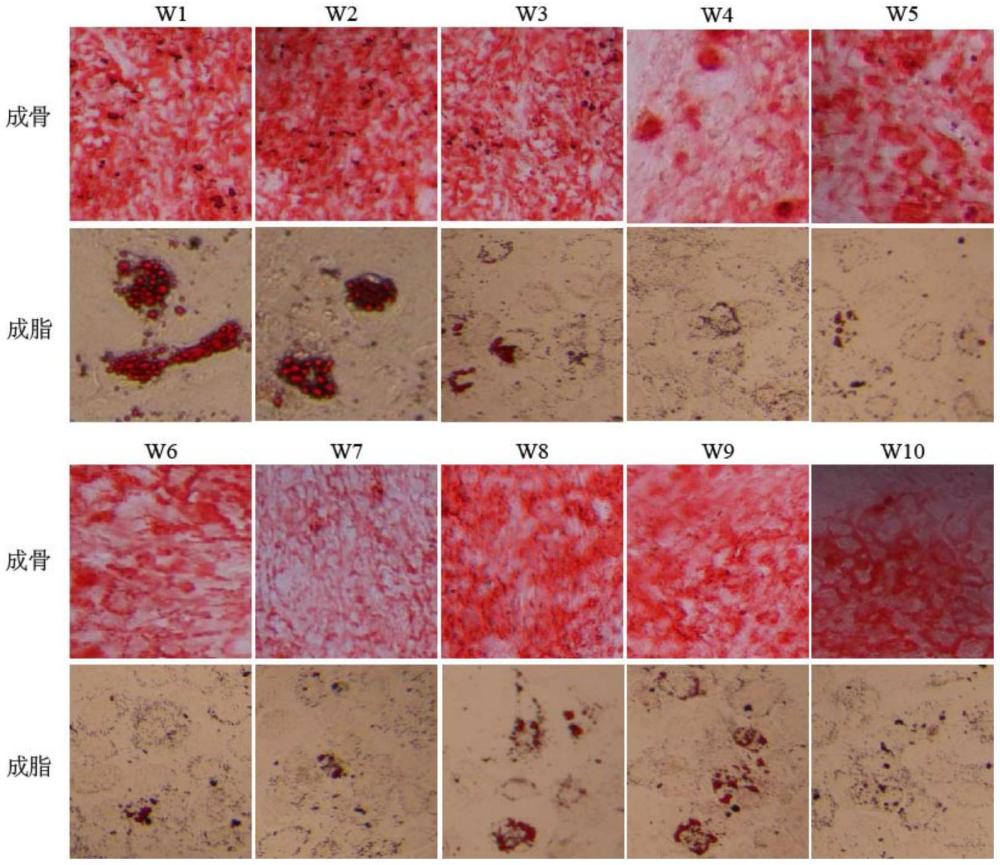
41、又一方面,本发明提供了上述间充质干细胞注射液的细胞活性鉴定方法,所述的细胞活性鉴定方法包括对间充质干细胞进行细胞形态、细胞活率、流式表型、成骨成脂分化能力或生物学效力的检测。
42、具体地,所述的流式表型的检测包括对cd73、cd90、cd105、cd19、cd34、cd45、cd11b、hla-dr中的一种或多种进行检测。
43、优选地,所述的流式表型的检测标准为高标达cd73、cd90和cd105,不表达cd19、cd34、cd45、cd11b和hla-dr。
44、具体地,所述的生物学效力的检测包括对hgf或stnfr1进行检测。
45、优选地,所述的hgf的生理范围为10-30ng/1e+6cells。
46、优选地,所述的stnfr1的生理范围为220-800pg/1e+6cells。
47、又一方面,本发明提供了上述的间充质干细胞注射液、制备方法制备得到的间充质干细胞注射液或符合细胞活性鉴定方法的标准的间充质干细胞注射液在制备含有间充质干细胞的药物的应用。
48、具体地,所述的药物包括预防或治疗自身免疫病的药物。
49、优选地,所述的自身免疫病包括但不限于系统性红斑狼疮、类风湿性关节炎、多发性硬化症、重症肌无力、炎症性肠病、i型糖尿病、自身免疫性肝炎、多发性神经炎、原发性血小板紫癜或自身免疫性溶血性贫血。
50、进一步优选地,所述的自身免疫病为类风湿性关节炎和系统性红斑狼疮。
51、本发明的有益效果为:
52、(1)本发明用于制备间充质干细胞注射液的间充质干细胞工作库细胞安全性好,具有较好的细胞增殖能力,高表达cd73、cd90、cd105,不表达cd19、cd34、cd45、cd11b、hla-dr,具有成骨成脂的分化能力和较好的生物学效力。
53、(2)本发明提供的间充质干细胞注射液符合《中华人民共和国药典》标准,hgf、stnfr1含量高,能够起到防治自身免疫病的效果。
- 还没有人留言评论。精彩留言会获得点赞!