筒状织物的制作方法
本发明涉及筒状织物。更详细而言,涉及在流体、粉体移送用和金属线、线缆、电线管等线状物保护用软管、筒状过滤器、人工血管的基材等中有用的筒状织物。
背景技术:
软管、补强材料、保护材料等各种产业用途中利用了筒状织物,但根据其使用情况,有时弯曲、或卷绕成旋涡状、或与空间匹配而配置为蛇行状等形状。因此,前述的筒状织物在与使用情况匹配的形状中,提出了提高耐扭折性(易弯曲性)以使得不发生破损、扭曲的手段。
例如,专利文献1中,公开了能够提供下述人工血管的技术:所述人工血管包含热塑性树脂纤维制的布且实施了卷曲加工,通过采取特定的卷曲形状,柔软,且缝合针的通过性良好,随时间的拉伸少。
此外,专利文献2中,公开了能够提供下述编织制造的人工血管的技术:所述编织制造的人工血管的特征在于,具有通过多个纵纱和横纱编织制成的织物,前述织物包含通过熔融而对该织物赋予对松解的抵抗性的可熔化元素,并且前述横纱包括遍及织成的全长对前述织物赋予自保持性而不需实施卷曲加工的固化元素,通过所述编织制造的人工血管,在裁切时不存在松解的倾向,也不需要卷曲加工,为自保持型且保持开放管腔。
生物体移植后的人工血管为了追随周围组织的活动,此外还考虑到移植至弯曲部位的情况,要求具有柔软性,但如果例如减小纤维密度、或使用极细纤维等而使人工血管具有柔软性,则存在血液容易从纤维间隙泄漏的问题。因此,考虑了各种防止血液泄漏的方法,专利文献3、4和5中报告了通过赋予在生物体内被吸收的胶原蛋白、明胶等凝胶,从而填埋纤维的间隙以防止漏血的方法。
现有技术文献
专利文献
专利文献1:日本特公平6-24587号公报
专利文献2:日本专利第2960586号公报
专利文献3:日本专利第1450789号公报
专利文献4:日本特开平1-34360号公报。
专利文献5:日本专利第1563185号公报。
技术实现要素:
发明所要解决的课题
然而,上述专利文献1记载的人工血管对热塑性树脂纤维制的布实施了卷曲加工,人工血管内表面的凹凸变大。因此,如果用作人工血管时内径细,则血流中产生湍流,存在形成血栓的问题。
另一方面,上述专利文献2记载的编织制造的人工血管据信不需要卷曲加工,具有能够防止松解的平滑的内表面。使纬纱具有熔融元素,在后加工的热定型中熔融的纬纱与经纱熔接,使纬纱的纤度变细,由此赋予伸缩性和耐松解性。然而,本技术中,熔融成分无法与经纱均匀熔接,有在纤度变细的纬纱与经纱的交错部分产生有孔部分的问题。
此外,针对血液泄漏这一问题,专利文献3记载了通过对拉伸强度20kg/cm2以上的可挠性管覆盖胶原蛋白或明胶从而防止漏血的人工血管。然而,专利文献3中记载的人工血管的管本身硬,因此不仅难以追随脏器的活动,而且在狭窄手术视野中进行移植时也难以缝合,难以自由选择吻合部位。
专利文献4和5中,记载了通过对多孔质的人工血管覆盖明胶而防止漏血的人工血管,但没有记载用于兼顾人工血管所要求的机械特性和防漏血的具体明胶覆盖的结构。
本发明的目的在于,改善所述现有技术的问题,提供筒状织物内表面的凹凸小、且伸缩性、柔软性、耐扭折性(易弯曲性)优异的筒状织物和人工血管,尤其是兼具机械特性和低漏血性的人工血管。
解决课题的手段
为了解决所述课题,本发明具有下述结构。
(1)筒状织物,其是使经纱和纬纱交错而织造的筒状织物,该筒状织物的经纱方向的外径之差为10%以内,所述筒状织物满足下式,
(l2-l1)/l1≥0.1
l1:以在不向上述筒状织物施加应力的状态下测定时的织物外径中的、该织物外径的最大值的5倍的距离在筒状织物的外周上画出标线,沿该筒状织物的经纱方向以0.01cn/dtex的应力压缩时的标线间距离;
l2:以在不向上述筒状织物施加应力的状态下测定时的织物外径中的、该织物外径的最大值的5倍的距离在筒状织物的外周上画出标线,沿该筒状织物的经纱方向以0.01cn/dtex的应力伸长时的标线间距离。
(2)根据(1)所述的筒状织物,其中,沿经纱方向以0.01cn/dtex的应力压缩筒状织物时的该筒状织物的最大外径a与沿经纱方向以0.01cn/dtex的应力伸长该筒状织物时的该筒状织物的最小外径b的下式表示的变动指数c为0.03以上且不足0.2,
变动指数c=(a-b)/a。
(3)根据(1)或(2)所述的筒状织物,其中,筒状织物的内表面的凹凸为100μm以下。
(4)根据(1)~(3)中任一项所述的筒状织物,其中,筒状织物不具有波纹结构。
(5)根据(1)~(4)中任一项所述的筒状织物,其中,筒状织物中使用的经纱和纬纱为合成纤维。
(6)根据(5)所述的筒状织物,其中,筒状织物中使用的合成纤维为非弹性纱的聚酯。
(7)根据(5)或(6)所述的筒状织物,其中,构成筒状织物的经向的合成纤维的单纱直径的一部分或全部为5μm以下的复丝。
(8)人工血管,其以(1)~(7)中任一项所述的筒状织物为基材。
(9)人工血管,其以(1)~(7)中任一项所述的筒状织物为基材,在该基材的内表面具有抗血栓性材料的层。
(10)根据(9)所述的人工血管,其中,前述抗血栓性材料包含:包含硫原子的阴离子性的具有抗凝血活性的化合物。
(11)根据(9)或(10)所述的人工血管,其中,前述抗血栓性材料包含:含有选自烯化亚胺、乙烯基胺、烯丙基胺、赖氨酸、鱼精蛋白和二烯丙基二甲基氯化铵中的化合物作为单体单元的阳离子性聚合物,前述阳离子性聚合物与构成前述内表面与血液接触的筒状织物的经纱和纬纱共价键合。
(12)人工血管,其以(8)~(11)中任一项所述的筒状织物为基材,在该基材的外表面具有生物体吸收性材料的层。
(13)根据(12)所述的人工血管,其扭折半径为15mm以下。
(14)根据(12)或(13)所述的人工血管,其中,在25℃向内表面施加120mmhg的压力时的透水性为10ml/cm2/min以下。
(15)根据(12)~(14)中任一项所述的人工血管,其中,上述生物体吸收性材料为包含选自乳酸、羟基乙酸、己酸、草酸、丙二酸、琥珀酸、戊二酸、马来酸、富马酸、乙二醇、丙二醇、乙烯基吡咯烷酮和乙烯醇中的单体单元的均聚物或共聚物。
(16)根据(12)~(15)中任一项所述的人工血管,其中,上述生物体吸收性材料为多糖类或蛋白质。
(17)根据(16)所述的人工血管,其中,上述蛋白质选自胶原蛋白、去端肽胶原蛋白和明胶。
发明的效果
根据本发明,可以得到筒状织物内表面的凹凸小、且伸缩性、柔软性、耐扭折性(易弯曲性)优异的筒状织物。并且,所述筒状织物能够在流体、粉体移送用和金属线、线缆、电线管等线状物保护用软管、筒状过滤器、人工血管的基材等中有用地使用,其中特别是在人工血管中有用地使用。本发明的人工血管即使在移植到弯曲部位的情况中也维持柔软性,能够防止血液从纤维间隙泄漏,即使对紧急手术也可以合适地利用。
附图说明
图1是用于在筒状织物上画出标线的说明图。
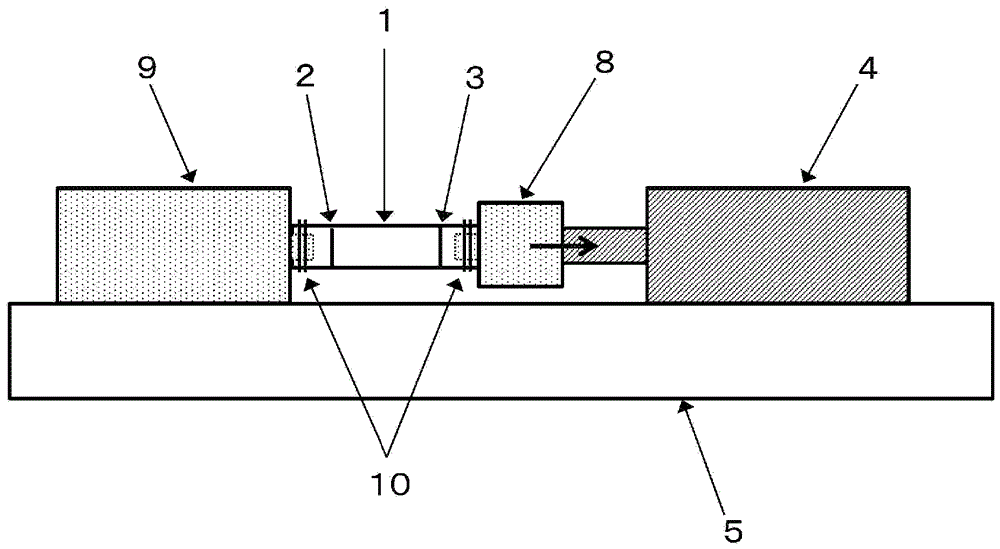
图2是用于测定筒状织物的压缩时标线间距离的装置的概念图。
图3是用于测定筒状织物的伸长时标线间距离的装置的概念图。
图4是针对筒状织物的内表面的凹凸的含义进行说明的图。
具体实施方式
根据本发明所述的筒状织物是使经纱和纬纱交错而织造的筒状织物,不实施通常进行的卷曲加工。因此,可以使该筒状织物的经纱方向的外径之差为10%以内。
应予说明,上述“外径之差为10%以内”是指沿经纱方向以50mm间隔进行5个部位的测定,用最大值和最小值进行评价,将最大值减去最小值并将该值除以最大值而用百分数表示的值记作“外径之差”。
并且,其特征在于,以在不向该筒状织物施加应力的状态下测定时的织物外径最大值的5倍的距离在筒状织物的外周上画出标线,沿该筒状织物的经纱方向以0.01cn/dtex的应力压缩时的标线间距离l1、和沿经纱方向以0.01cn/dtex的应力伸长时的标线间距离l2的关系以下式表示,
(l2-l1)/l1≥0.1。
此外,上述(l2-l1)/l1的值从能够更进一步提高伸缩性、柔软性的观点出发,优选为0.15以上、更优选为0.18以上。作为上限,优选为1.0。
通过将前述标线间距离l1与l2的关系设为上述的范围,能够提供伸缩性、柔软性、耐扭折性(易弯曲性)优异的筒状织物。即,使筒状织物弯折而弯曲时,在弯曲的内周侧沿压缩方向施加应力,同时在外周侧沿伸长方向施加应力,但通过设为上述范围,外周相对于内周可以充分伸长,因此意味着耐扭折性优异。并且,0.01cn/dtex的应力下的伸长操作或压缩操作通常相当于人沿经纱方向轻轻地用手伸长或压缩该筒状织物时的应力,处于上述范围的情况中,人用手进行弯曲操作时操作性也良好,意味着伸缩性、柔软性优异。
此外,本发明的筒状织物从人用手轻轻地拉伸时容易感到手感方面考虑,优选沿经纱方向以0.01cn/dtex的应力伸长时的伸长率为30%以下。进一步优选为20%以下、更优选为10%左右。此外,作为沿经纱方向以0.01cn/dtex的应力伸长时的下限,从人轻轻地用手拉伸时感到伸长感的方面考虑,优选为5%以上、更优选为8%以上。
此外,沿经纱方向以0.01cn/dtex的应力压缩筒状织物时的该筒状织物的最大外径a、与沿经纱方向以0.01cn/dtex的应力伸长该筒状织物时的该筒状织物的最小外径b的下式表示的变动指数c优选为0.03以上且不足0.2、更优选为0.05以上且不足0.15,
变动指数c=(a-b)/a。
通过将前述最大外径a与最小外径b的关系设为上述的范围,弯曲等伸长、压缩同时产生时筒状织物的内径差也小,能够确保无变化的流路。
此外,筒状织物的内表面的凹凸优选为100μm以下、进一步优选为80μm以下、更优选为60μm以下。作为内表面的凹凸的下限,从用作人工血管时的内皮形成的观点出发,优选为3μm以上。通过将筒状织物的内表面的凹凸设为上述的范围,即使在内径小的情况中,流体中也不产生湍流,特别是即使在用作细人工血管的情况中,在血流中也不产生湍流,具有难以生成血栓的优点。
此外,筒状织物优选不具有波纹结构。通过不具有波纹结构,内表面没有凹凸、在细间隙流体流动时也不产生湍流,特别是在用于细人工血管时,在血流中不产生乱流,具有难以生成血栓的优点。
应予说明,“不具有波纹结构”是指没有在纤维筒状物中插入具有螺旋状或环状的波形槽的芯棒并加热而进行波形定型加工的结构的织物、或没有进行褶皱加工的织物。
本发明的筒状织物中使用的经纱和纬纱优选使用合成纤维,具体而言,可以举出尼龙纤维、聚酯纤维等,更优选使用所谓非弹性纱。“非弹性纱”是不具有所谓橡胶弹性的纤维,是不同于由聚醚系弹性体、聚硫醚系弹性体和聚氨酯系弹性体等所代表的热塑性弹性体那样伸长性和恢复性优异的原材料构成的具有橡胶弹性的纤维、即所谓弹性纱的纤维。
其中,本发明中从强度、尺寸稳定性的方面考虑,优选非弹性纱的聚酯纤维。作为非弹性纱的聚酯纤维,可以举出例如包含聚对苯二甲酸乙二醇酯、聚对苯二甲酸丁二醇酯、聚对苯二甲酸丙二醇酯、它们的共聚物等的纤维。
本发明中,即使使用非弹性纱,筒状织物本身也具有伸缩性。
本发明的筒状织物例如可以以下述方式制造。
织造步骤中,作为经纱,优选使用至少2种(经纱a、经纱b)。针对这些,也如上所述,优选为非弹性纱。
作为经纱a,可以由例如尼龙纤维、聚酯纤维等各种合成纤维构成。其中,从强度、尺寸稳定性方面考虑,优选为非弹性纱的聚酯纤维。作为非弹性纱的聚酯纤维,可以举出例如包含聚对苯二甲酸乙二醇酯、聚对苯二甲酸丁二醇酯、聚对苯二甲酸丙二醇酯、它们的共聚物等的纤维。
在此,构成织物的经纱a可以是直接纺丝得到的极细纤维,也可以是将海岛复合纤维进行脱海处理而得到的极细纤维。其中,优选为经向的合成纤维的单纱直径的一部分或全部为5μm以下的复丝。通过将单纱直径设为上述的范围,筒状织物的柔软性提高,能够制成更致密的结构。
作为经纱b,优选由可溶纱(
作为各经纱的总纤度,优选为560dtex以下、进一步优选为235dtex以下、更优选为100dtex以下。
作为后加工后的经纱a的织密度(
此外,作为纬纱,优选使用至少2种(纬纱c、纬纱d)。
此时,优选制成2层结构的筒状织物。此时的优选的方式是纬纱c位于筒状织物的内层、且纬纱d位于外层的情况。
作为上述位于内层的纬纱c和位于外层的纬纱d,可以由例如尼龙纤维、聚酯纤维等各种合成纤维构成,但优选为非弹性纱。其中,从强度、尺寸稳定性方面考虑,优选为非弹性纱的聚酯纤维。作为非弹性纱的聚酯纤维,可以举出例如包含聚对苯二甲酸乙二醇酯、聚对苯二甲酸丁二醇酯、聚对苯二甲酸丙二醇酯、它们的共聚物等的纤维。
此外,位于内层的纬纱c可以是将海岛复合纤维或直接纺丝而得到的极细纤维用作原纱、并且进行海岛复合纤维的脱海处理后或直接纺丝而得到的极细纤维。优选为这些纬纱c的合成纤维的单纱直径的一部分或全部为5μm以下的复丝。通过将单纱直径设为上述的范围,筒状织物的柔软性提高,能够制成更致密的结构。
位于外层的纬纱d的单纱直径优选为10~20μm的范围内。通过将单纱直径设为上述的范围,相对于内层而言刚性提高,此外,抑制了因水解而导致的劣化,能够提高耐久性。
作为各纬纱的总纤度,优选为560dtex以下、进一步优选为235dtex以下、更优选为100dtex以下。
作为后加工后的各纬纱的织密度,优选为200根/英寸(2.54cm)以下、进一步优选为180根/英寸(2.54cm)以下、更优选为150根/英寸(2.54cm)以下。
并且,织造时,优选提高经纱b的张力,同时经纱a在不对开口造成阻碍的范围降低张力。例如,优选经纱b的张力设为0.5~1.5cn/dtex、经纱a的张力设为0.05~0.15cn/dtex。应予说明,经纱a与经纱b的配置优选以相对于2~10根经纱a而言经纱b为1根的比率进行配置。
一般而言,高密度的织物中,为了增大经纱的卷曲率,如果在织造时降低经纱的张力,则因回织(
进一步,经纱b优选在位于内层的纬纱c和位于外层的纬纱d之间配置。
此外,纬纱通过使用筒状织物的位于内层的纬纱c和位于外层的纬纱d的至少2种,由于纬纱c和纬纱d的周长不同,从而产生结构上的应变。由此,能够对筒状织物赋予伸长性。
作为筒状织物的内径,优选为100mm以下、进一步优选为50mm以下、更优选为10mm以下。作为筒状织物的内径的优选下限,从织造性的观点出发为1.5mm左右。
后加工步骤例如优选经过下述步骤。应予说明,下述实施方式中,例示出筒状织物的内径为3mm的情况。
(a)热水洗
通过热水洗,脱去原纱油剂,使经纱b收缩。处理条件优选温度为80~98℃、时间为15~40分钟。
(b)预热定型
通过预热定型,使伴随经纱b的收缩而卷曲率变大的经纱a的形状变得稳定。将外径2.8mm的圆棒插入筒状织物中,将两端用金属丝等固定,进行热处理。热处理条件优选温度为160~190℃、时间为3~10分钟。应予说明,前述圆棒的材质可以举出例如sus。
(c)脱海处理
根据需要,进行前述的经纱a、纬纱c的脱海处理,同时进行经纱b的溶解去除。
脱海处理和溶解去除通过下述步骤进行。
(c-1)酸处理
通过酸处理,使海岛复合纤维的海成分变脆。作为酸,可以举出马来酸。酸处理条件优选浓度为0.1~1质量%、温度为100~150℃、时间为10~50分钟。不使用海岛复合纤维时,可以省略酸处理。
(c-2)碱处理
通过碱处理,使可溶纱和通过酸处理而变脆的海岛复合纤维的海成分溶出。作为碱,可以举出氢氧化钠。碱处理条件优选浓度为0.5~2质量%、温度为70~98℃、时间为60~100分钟。
(d)热定型(第1次)
通过第1次热定型,目的在于使因脱海处理而平缓的经纱的卷曲再次最大化。将外径3mm的圆棒插入筒状织物中,以不引入褶皱的方式,在沿经纱方向最大限度压缩的状态下,将两端用金属丝等固定,进行热处理。热处理条件优选温度为160~190℃、时间为3~10分钟。应予说明,前述圆棒的材质可以举出例如sus。
(e)热定型(第2次)
通过第2次热定型,目的在于制成在残留卷曲的弯曲点的同时具有收缩容许量的织物,但也可以不实施第2次热定型。将外径3mm的圆棒插入筒状织物中,在沿经纱方向伸长20~50%的状态下,将两端用金属丝等固定,进行热处理。热处理条件优选设为比第1次热定型低10~20℃的温度,时间优选为3~10分钟。应予说明,前述圆棒的材质可以举出例如sus。
以这样的方式得到的筒状织物形成内表面的凹凸小、且伸缩性、柔软性、耐扭折性(易弯曲性)优异的筒状织物,能够在流体、粉体移送用和金属线、线缆、电线管等线状物保护用软管、筒状过滤器、人工血管的基材等中有用地使用,特别地能够适合地用作人工血管。
将本发明用作人工血管时,优选通过在与血液接触的筒状织物的内表面键合具有抗凝血活性的化合物,从而具有抗血栓性材料的层。在此,抗血栓性是指在与血液接触的表面血液不凝固的性质,是例如抑制因血小板的凝集、凝血酶所代表的凝血因子的活化等而进行的凝血的性质。形成抗血栓性材料的层的方法没有特别限定,有使筒状织物的内表面改性后使筒状织物的内表面与肝素或肝素衍生物共价键合的方法(日本特表2009-545333号公报、日本专利第4152075号公报、日本专利第3497612号公报);使筒状织物的内表面与肝素或肝素衍生物离子键合的方法、或涂布在胶原蛋白、明胶等凝胶中包含的肝素或肝素衍生物方法(日本专利第3799626号公报和日本特公平8-24686号公报);将筒状织物浸渗在溶解于有机溶剂中的嵌段聚氨酯中并将筒状织物的内表面用嵌段聚氨酯涂布的方法(日本特开平7-265338号公报);使筒状织物的内表面与抑制参与凝血反应的多个凝血因子和血栓形成的阶段中所涉及的凝血酶等的化合物结合的方法(日本专利第4461217号公报、wo08/032758号公报、wo12/176861号公报)等,特别优选使筒状织物的内表面通过离子键而与肝素或肝素衍生物键合的方法。
抗血栓性材料优选为具有抗凝血活性的化合物。作为具有抗凝血活性的化合物,只要是具有抑制因血小板的凝集、凝血酶所代表的凝血因子的活化等而进行的凝血的性质的化合物即可,可以例示出阿司匹林、氯吡格雷硫酸盐、普拉格雷硫酸盐、盐酸噻氯匹定、双嘧达莫、西洛他唑、贝前列素钠、利马前列素阿法环糊精、奥扎格雷钠、盐酸沙格雷酯、二十碳五烯酸乙酯、曲匹地尔、华法林钾、肝素钠、肝素钾、达肝素钠、帕肝素钠、利巴韦林钠(レバピリンナトリウム)、利伐沙班、阿哌沙班、依度沙班、达比加群、阿加曲班、硫酸葡聚糖、聚乙烯基磺酸和聚苯乙烯磺酸等,其中,优选为包含硫原子的阴离子性的具有抗凝血活性的化合物。除此之外,优选包含阳离子性聚合物,具体而言,更优选包含:含有选自烯化亚胺、乙烯基胺、烯丙基胺、赖氨酸、鱼精蛋白和二烯丙基二甲基氯化铵中的化合物作为单体单元的阳离子性聚合物。
这些单体单元具有阳离子性的氮原子,因此聚合物是阳离子性的,另一方面,具有抗凝血活性的包含硫原子的化合物是阴离子性的,因此两者可以离子键合。包含硫原子的阴离子性的具有抗凝血活性的化合物可以举出肝素、肝素衍生物、硫酸葡聚糖、聚乙烯基磺酸和聚苯乙烯磺酸等,更优选为肝素或肝素衍生物。此外,肝素或肝素衍生物可以提纯,也可以不提纯,只要能够抑制凝血反应则没有特别限定,除了临床上一般而言广泛使用的肝素、未分级肝素、低分子量肝素之外,还包括对抗凝血酶iii高亲和性的肝素等。作为肝素的具体例,可以举出“肝素钠”(organonapi公司制)等。
阳离子性聚合物由于具有阳离子性而可能表现出溶血毒性等,因此在血液中溶出是不优选的。因此,阳离子性聚合物优选与构成内侧与血液接触的筒状织物的经纱和纬纱键合,更优选共价键合。
在此,共价键合是指原子彼此通过共享相互的电子而产生的化学键。本发明中,是构成抗血栓性材料的聚合物和基材的表面所具有的碳、氮、氧、硫等原子彼此的共价键,可以是单键也可以是多重键。共价键的种类没有限定,可以举出例如胺键、叠氮键、酰胺键和亚胺键等。其中,特别是从共价键的形成容易性、键合后的稳定性等观点出发,更优选为酰胺键。
阳离子性聚合物可以是均聚物,也可以是共聚物。阳离子性聚合物是共聚物时,可以是无规共聚物、嵌段共聚物、接枝共聚物或交替共聚物中任一者,但包含氮原子的重复单元连续的嵌段的情况中,该嵌段的部分与包含硫原子的阴离子性的具有抗凝血活性的化合物相互作用而牢固地离子键合,因此更优选为嵌段共聚物。
在此,均聚物是指1种单体单元聚合而得到的高分子化合物,共聚物是指2种以上的单体共聚而得到的高分子化合物。其中,嵌段共聚物是指重复单元不同的至少2种以上的聚合物通过共价键连接从而形成长链那样的分子结构的共聚物,嵌段是指构成嵌段共聚物的重复单元不同的至少2种以上的各个聚合物。
本发明中,阳离子性聚合物的结构可以为直链状,也可以为支链状。本发明中,由于能够与包含硫原子的阴离子性的具有抗凝血活性的化合物在多个点形成稳定的离子键,因此更优选为支链状。
本发明中,阳离子性聚合物具有伯至叔氨基和季铵基之中的至少一种官能团,但其中,季铵基与伯至叔氨基相比,与包含硫原子的阴离子性的具有抗凝血活性的化合物的离子相互作用牢固,容易控制包含硫原子的阴离子性的具有抗凝血活性的化合物的溶出速度,故而优选。
本发明中,构成季铵基的3个烷基的碳原子数没有特别限定,通过不使疏水性和空间位阻过大,容易使季铵基与包含硫原子的阴离子性的具有抗凝血活性的化合物有效地离子键合。此外,为了减小溶血毒性,构成季铵基的氮原子上键合的平均1个烷基的碳原子数优选为1~12、进一步优选为2~6。构成季铵基的氮原子上键合的3个烷基可以全部为相同碳原子数,也可以不同。
本发明中,基于与包含硫原子的阴离子性的具有抗凝血活性的化合物的离子相互作用而吸附的量多,因此作为阳离子性聚合物,优选使用聚烯化亚胺。作为聚烯化亚胺,可以举出聚乙烯亚胺(以下称为“pei”)、聚丙烯亚胺(
作为pei的具体例,可以举出“lupasol”(注册商标)(basf公司制)、“epomin”(注册商标)(株式会社日本触媒公司制)等,在不妨碍本发明的效果的范围,可以为与其他单体形成的共聚物,也可以为改性体。在此,改性体是指构成阳离子性聚合物的单体的重复单元相同,但例如通过后述的放射线的照射,从而其一部分发生自由基分解、再键合等的物质。
本发明中,如果阳离子性聚合物的重均分子量过小,则与包含硫原子的阴离子性的具有抗凝血活性的化合物相比分子量小,因此无法形成稳定的离子键,难以得到目标的抗血栓性。另一方面,如果阳离子性聚合物的重均分子量过大,则包含硫原子的阴离子性的具有抗凝血活性的化合物被阳离子性聚合物包覆在内,抗血栓性材料被掩埋。因此,阳离子性聚合物的重均分子量优选为600~2000000、更优选为1000~1500000、更进一步优选为10000~1000000。阳离子性聚合物的重均分子量可以通过例如凝胶渗透色谱法、光散射法等测定。
抗血栓性材料的制造方法示于如下。例如,为了对作为基材的筒状织物覆盖抗血栓性材料,可以在包含含有选自烯化亚胺、乙烯基胺、烯丙基胺、赖氨酸、鱼精蛋白和二烯丙基二甲基氯化铵中的化合物作为单体单元的聚合物、和包含硫原子的阴离子性的具有抗凝血活性的化合物的溶液中,浸渍目标基材而进行覆盖,但也可以在上述聚合物与包含硫原子的阴离子性的具有抗凝血活性的化合物之间,通过使其全部或任意一部分预先反应后的抗血栓性材料覆盖基材的内表面,从而在基材的内表面形成抗血栓性材料的层。
其中,为了以良好的效率在基材的表面表现出抗血栓性,更优选为作为第1覆盖步骤,使包含选自烯化亚胺、乙烯基胺、烯丙基胺、赖氨酸、鱼精蛋白和二烯丙基二甲基氯化铵中的化合物作为单体单元的阳离子性聚合物与基材的内表面共价键合后,作为第2覆盖步骤,使包含硫原子的阴离子性的具有抗凝血活性的化合物与上述阳离子性聚合物离子键合的方法。
此外,阳离子性聚合物包含伯至叔氨基时,为了使与包含硫原子的阴离子性的具有抗凝血活性的化合物的离子相互作用变得牢固,容易控制肝素的溶出速度,在第1覆盖步骤后,可以追加将阳离子性聚合物制成季铵的步骤。
使用作为第1覆盖步骤,使包含选自烯化亚胺、乙烯基胺、烯丙基胺、赖氨酸、鱼精蛋白和二烯丙基二甲基氯化铵中的化合物作为单体单元的阳离子性聚合物与基材的内表面共价键合后,作为第2的覆盖步骤,使包含硫原子的阴离子性的具有抗凝血活性的化合物与上述阳离子性聚合物离子键合的方法的情况中的制造方法示于如下。
使阳离子性聚合物与基材的内表面共价键合的方法没有特别限定,基材具有官能团(羟基、硫醇基、氨基、羧基、醛基、异氰酸酯基和异硫氰酸酯等)时,有通过与阳离子性聚合物进行化学反应而共价键合的方法。例如,基材的内表面具有羧基等时,只要使具有羟基、硫醇基和氨基等的聚合物与基材的内表面共价键合即可,可以举出使具有羟基、硫醇基和氨基等的化合物与聚合物共价键合后,在具有羧基等的基材的内表面上共价键合的方法等。
此外,基材不具有官能团时,有通过等离子体、电晕等而对基材的内表面进行处理后,使阳离子性聚合物共价键合的方法;通过照射放射线而在基材的内表面和阳离子性聚合物中产生自由基,通过其再键合反应而使基材的内表面与阳离子性聚合物共价键合的方法。作为放射线,主要使用γ射线、电子射线。使用γ射线时,γ射线源量优选为250万~1000万ci、更优选为300万~750万ci。此外,使用电子射线时,电子射线的加速电压优选为5mev以上、更优选为10mev以上。作为放射线剂量,优选为1~50kgy、更优选为5~35kgy。照射温度优选为10~60℃、更优选为20~50℃。
通过照射放射线而共价键合的方法的情况中,为了控制自由基产生量,可以使用抗氧化剂。在此,抗氧化剂是指具备容易对其他分子给予电子的性质的分子。所使用的抗氧化剂没有特别限定,可以举出例如维生素c等水溶性维生素类、多元酚类、甲醇、乙醇、丙醇、乙二醇、丙二醇和丙三醇等醇类、葡萄糖、半乳糖、甘露糖和海藻糖等糖类、连二亚硫酸钠、焦亚硫酸钠、连二硫酸钠等无机盐类、尿酸、半胱氨酸、谷胱甘肽、双(2-羟基乙基)亚氨基三(羟基甲基)甲烷(以下称为“bis-tris”)等缓冲剂等。然而,从处理性、残留性等观点出发,特别优选为甲醇、乙醇、丙二醇、bis-tris,更优选为丙二醇、bis-tris。这些抗氧化剂可以单独使用,也可以混合使用2种以上。此外,抗氧化剂优选添加至水溶液中。
作为筒状织物的材质而使用聚酯纤维时,没有特别限定,还可以使用通过在加热条件下使阳离子性聚合物接触从而利用氨解反应进行共价键合的方法。此外,还可以通过酸和碱处理而使基材的内表面的酯键水解,使在基材的内表面上产生的羧基与阳离子性聚合物的氨基进行缩合反应而共价键合。这些方法中,可以使阳离子性聚合物与基材的内表面接触而反应,也可以在溶解于溶剂中的状态下接触而反应。作为溶剂,优选为水、醇等,从处理性、残留性等观点出发,特别优选为水。此外,也可以在使构成阳离子性聚合物的单体与基材的内表面接触的状态下聚合后,进行反应而共价键合。
加热的手段没有特别限定,可以举出电加热、微波加热、远红外线加热等。通过氨解反应而使聚酯纤维与阳离子性聚合物共价键合时,加热温度优选为玻璃化转变点附近以上且熔点以下。
本发明中,可知在第1覆盖步骤之前,将基材的内表面的酯键进行水解和氧化的步骤是重要的。具体而言,适合使用通过酸或碱和氧化剂进行处理的方法。特别的,为了在不使补体活化的情况下提高阳离子性聚合物的覆盖量而提高抗血栓性,特别适合使用通过酸或碱和氧化剂进行处理的方法。
作为本发明中的通过酸或碱和氧化剂而将基材的内表面的酯键进行水解和氧化的步骤的组合,发现最适合的是通过酸和氧化剂进行处理的方法。此外,也可以在通过碱对基材的内表面进行处理后,通过酸和氧化剂进行处理。
所使用的酸的种类没有特别限定,可以举出例如盐酸、氢溴酸、氢碘酸、次氯酸、亚氯酸、高氯酸、硫酸、氟磺酸、硝酸、磷酸、六氟锑酸、四氟硼酸、铬酸和硼酸等无机酸;甲磺酸、乙磺酸、苯磺酸、对甲苯磺酸、三氟甲磺酸和聚苯乙烯磺酸钠等磺酸、乙酸、柠檬酸、甲酸、葡糖酸、乳酸、草酸和酒石酸等羧酸、抗坏血酸和麦氏酸等乙烯基性羧酸、脱氧核糖核酸和核糖核酸等核酸等。其中,从处理性等观点出发,更优选为盐酸、硫酸等。
所使用的碱的种类没有特别限定,可以举出例如氢氧化锂、氢氧化钠、氢氧化钾、氢氧化铷和氢氧化铯等碱金属的氢氧化物、氢氧化四甲基铵和氢氧化四乙基铵等四烷基铵的氢氧化物、氢氧化钙、氢氧化锶、氢氧化钡、氢氧化铕和氢氧化铊等碱土金属的氢氧化物、胍化合物、二氨合银(i)氢氧化物和四氨合铜(ii)氢氧化物等氨合络合物的氢氧化物、三甲基锍氢氧化物和二苯基碘鎓氢氧化物等。其中,从处理性等观点出发,更优选为氢氧化锂、氢氧化钠和氢氧化钾等。
所使用的氧化剂的种类没有特别限定,可以举出例如硝酸钾、次氯酸、亚氯酸、高氯酸、氟、氯、溴和碘等卤素、高锰酸钾、高锰酸钠三水合物、高锰酸铵、高锰酸银、高锰酸锌六水合物、高锰酸镁、高锰酸钙和高锰酸钡等高锰酸盐、硝酸铈铵、铬酸、二铬酸、过氧化氢水等过氧化物、土伦试剂和二氧化硫等,其中,从能够适度地防止氧化剂的强度、抗血栓性材料的劣化等观点出发,更优选为高锰酸盐。
作为使包含聚酯纤维的筒状织物的内表面与阳离子性聚合物共价键合的方法,有例如使用脱水缩合剂等而进行缩合反应的方法。
所使用的脱水缩合剂的种类没有特别限定,可以举出例如n,n'-二环己基碳二亚胺、n,n'-二异丙基碳二亚胺、1-醚-3-(3-二甲基氨基丙基)碳二亚胺、1-醚-3-(3-二甲基氨基丙基)碳二亚胺盐酸盐(以下称为“edc”)、1,3-双(2,2-二甲基-1,3-二氧杂环戊烷-4-基甲基)碳二亚胺、n-{3-(二甲基氨基)丙基-}-n'-乙基碳二亚胺、n-{3-(二甲基氨基)丙基-}-n'-乙基碳二亚胺甲碘化物、n-叔丁基-n'-乙基碳二亚胺、n-环己基-n'-(2-吗啉代乙基)碳二亚胺间对甲苯磺酸盐、n,n'-二叔丁基碳二亚胺或n,n'-二对甲苯基碳二亚胺等碳二亚胺系化合物;4(-4,6-二甲氧基-1,3,5-三嗪-2-基)-4-甲基吗啉鎓氯化物n水合物(以下称为“dmt-mm”)等三嗪系化合物。
脱水缩合剂可以与脱水缩合促进剂一同使用。所使用的脱水缩合促进剂没有特别限定,可以举出例如吡啶、4-二甲基氨基吡啶(以下称为“dmap”)、三乙基胺、异丙基胺、1-羟基苯并三唑或n-羟基琥珀酰亚胺。
阳离子性聚合物、脱水缩合剂和脱水缩合促进剂可以制成混合水溶液而反应,也可以依次添加而进行反应。
此外,阳离子性聚合物包含伯至叔氨基时,使与肝素或肝素的衍生物的离子相互作用变得牢固,容易控制肝素的溶出速度的情况中,可以追加将聚合物制成季铵的步骤。
作为将阳离子性聚合物制成季铵的方法,可以在将阳离子性聚合物共价键合于基材的内表面之前制成季铵,也可以在将阳离子性聚合物共价键合于基材的内表面之后制成季铵,但为了使阳离子性聚合物与包含硫原子的阴离子性的具有抗凝血活性的化合物的离子相互作用变得牢固,优选阳离子性聚合物所具有的季铵基存在于抗血栓性材料的最内表面,因此优选在共价键合于基材的内表面后制成季铵。具体而言,将阳离子性聚合物共价键合于基材的内表面之后,可以直接接触氯化醚、溴化醚等卤代烷化合物或含有缩水甘油基的季铵盐,也可以溶解于水溶液或有机溶剂中而接触。
作为使包含硫原子的阴离子性的具有抗凝血活性的化合物与阳离子性聚合物离子键合的第2覆盖步骤,没有特别限定,优选为在水溶液的状态下接触的方法。
本发明中,作为示出抗血栓性的指标,使用抗血栓性材料的抗xa因子活性。在此,抗xa因子活性是表示抑制第xa因子的活性的程度的指标,所述第xa因子促进从凝血酶原转化为凝血酶,可以知晓抗血栓性材料中的肝素或肝素的衍生物的活性单位的表面量。测定中使用“テストチーム(注册商标)ヘパリンs”(积水メディカル株式会社制)。
如果抗xa因子活性过低,则抗血栓性材料中的肝素或肝素的衍生物的表面量少,难以得到目标的抗血栓性。另一方面,如果抗xa因子活性过高,则肝素或肝素的衍生物的表面量存在用于表现出目标的抗血栓性的充分量,但由于抗血栓性材料的厚度增加,导致有时无法保持基材的表面的微细结构。即,抗血栓性材料的表面的基于抗xa因子活性的总覆盖量相对于基材的单位重量优选为10miu/mg以上且20000miu/mg以下,总覆盖量更优选为50miu/mg以上且10000miu/mg。在此的总覆盖量是指将裁切为约0.5cm×1cm的基材浸渍于人正常血浆5ml中,在37度氛围下振荡24小时后,将人正常血浆中的溶出肝素量与在基材表面残留的表面肝素量加和,从而算出。
本发明的人工血管优选在作为基材的筒状织物的外表面上具有生物体吸收性材料的层。覆盖筒状织物的外表面的生物体吸收性材料实现防止血液从人工血管的内侧漏出的功能,为了即使将人工血管移植至体内血液也不会漏出,不必说在体温以下,在体温以上的温度下也必须具有不溶于水的性质。生物体吸收性是指随时间地分解而在体内被吸收的性质,是通过水解、酶解或基于免疫细胞的吞噬作用等而被分解吸收的性质。可以在防止漏血的功能结束后分解消失。生物体吸收性材料的层从具有适度的形状保持性、优选容易追随筒状织物且容易防止漏血的结构的理由出发,优选具有适度的厚度,不必为无空隙的结构,可以为包含连通孔等微多孔的多孔质结构。
生物体吸收性材料没有特别限定,从上述那样的追随性、覆盖加工性的观点出发,优选为高分子化合物,可以使用合成高分子、天然高分子。作为合成高分子,从具有临床实绩的观点出发,特别优选为包含选自乳酸、羟基乙酸、己酸、草酸、丙二酸、琥珀酸、戊二酸、马来酸、富马酸、乙二醇、丙二醇、乙烯基吡咯烷酮、乙烯醇中的单体单元的均聚物或共聚物。作为天然高分子,优选使用多糖类或蛋白质,特别是从具有临床实绩的观点出发,优选使用胶原蛋白、去端肽胶原蛋白、明胶。作为明胶,为了避免生物体内的炎症反应而优选为低内毒素含量,更优选为ビーマトリックス(注册商标)明胶(ls-h,ls-w)(新田ゼラチン株式会社制)、rm-明胶(rm-50、rm-100、rm-100b)(ゼライス株式会社制)。
在体内留置人工血管时,生物体吸收性材料的层优选为在体温下不溶解的高分子化合物。为了表现出这样的性质,优选至少高分子化合物对37℃的水是不溶性的。作为将生物体吸收性材料制成水不溶性的高分子化合物的方法,可以适合地使用使高分子化合物中的亲水性成分的组成比率比非亲水性成分的比率低的方法、或者化学或物理地导入交联结构的方法。特别地,在生物体吸收性材料为蛋白质的情况中,已知通过化学交联而制成水不溶性的方法。化学交联的方法没有限定,可以采用利用包含二价性官能团的物质的化学交联、或利用γ射线等放射线的放射线交联等。化学交联时使用的包含二价性官能团的物质没有特别限定,可以使用包含选自氨基、羧基、羟基、硫醇基、异氰酸酯基、异硫氰酸酯基、醛基、环氧基和胍基中的2种以上反应性官能团的物质。其中,优选使用在医疗用途中也具有实绩的戊二醛或甲醛。
对于生物体吸收性材料的层的厚度,用相对于长度方向垂直的截面裁切人工血管,将该截面使用扫描型电子显微镜(株式会社日立ハイテクロノジーズ制miniscopetm3000),以300倍的倍率观察而测定。更具体而言,将位于筒状织物的最外周的任意纱中,位于与人工血管的中心相反一侧的生物体吸收性材料接触的边界的点记作p1,以穿过p1的方式画出的与筒状织物的切线垂直的线和生物体吸收性材料的外周相交的点记作p2时,在5个部位测定p1至p2的垂线的长度,将所得平均值记作生物体吸收性材料的层的厚度(μm)。生物体吸收性材料的层的厚度在提高对血压的耐久性方面,优选为10μm以上,在提高人工血管的柔软性方面,优选为300μm以下。此外,生物体吸收性材料的厚度特别优选为30μm以上且200μm以下。
本发明的人工血管的扭折半径优选为15mm以下。满足该范围时,在体内留置时能够具有良好的耐屈曲性(耐扭折性)。耐扭折性能够将用人工血管形成环并逐渐缩小环的直径时不屈曲的最小环半径作为指标,将逐渐缩小环的直径时不屈曲的最小环半径定义为扭折半径。扭折半径按照is07198的指南,测定最小环半径。
作为表示埋植时的血液从人工血管中泄露的指标,使用透水性。人工血管的透水性越低越好,优选为10ml/cm2/min以下。透水性的测定方法按照iso7198,将人工血管的在25℃向内表面施加120mmhg的压力时流出到人工血管的外表面的水量(ml)除以单位面积(cm2)和单位时间(30sec.)而得到。
实施例
以下,将本发明的实施例与比较例一同说明。
应予说明,本实施例中使用的各种特性的测定方法如下所述。
(1)纤度、丝数
纤度基于jisl1013:20108.3.1公量纤度(a法)而测定。
丝数基于jisl1013:20108.4而测定。
(2)单纱直径
基于将所使用的复丝的单纱侧面用キーエンス制显微镜vhx-2000放大至400倍得到的照片进行测定,以μm单位算出。此时,扁平纱等不规则截面纱在侧面达到最小的部分进行测定。
(3)筒状织物的内径
按照iso7198的指南,将锥度为1/10以下的圆锥垂直放置,在其上以覆盖将筒状织物沿径向裁切得到的截面的方式垂直平缓落下,测定停止的样品的下端位置的圆锥直径。
沿经纱方向以50mm间隔裁切,进行5个部位的测定,用最大值和最小值进行评价。
(4)筒状织物的外径
通过游标卡尺测定筒状织物的外径。
在未对筒状织物施加应力的状态下,沿经纱方向以50mm间隔进行5个部位的测定,用最大值和最小值进行评价。
外径之差设为最大值减去最小值并将该值除以最大值而得到的值。
(5)筒状织物的压缩时标线间距离l1、伸长时标线间距离l2
首先,通过上述(4),求出织物外径的最大值(未对筒状织物施加应力的状态下测定时的织物外径最大部分)。
接着,图1是用于在筒状织物上画出标线的说明图,如该图1所示,在从筒状织物1的一个端部起5mm的织物外周画出第一根标线2。从该第一根标线2起以织物外径的最大值的5倍的距离x在织物外周画出第二根标线3。在从该第二根标线3起朝向外侧(将虚线箭头的位置相对于标线3记作内侧时,为其相反侧)5mm的位置处,沿径向裁切筒状织物1。图1的标线2与标线3之间的距离是本发明中的标线间距离。
并且,图2是用于测定筒状织物的压缩时标线间距离的装置的概念图,如该图2所示,该装置中,作为载重测定器(测力计)4,将日本计测システム株式会社制handydigitalforcegaugehf-1(额定容量10n)设置在架台5上,将具有芯棒部分的压缩用夹持夹具6安装在载重测定器4上,将具有能够插入前述芯棒部分的孔部分的压缩用接受夹具7安装在架台5。
并且,在筒状织物1中穿过压缩用夹持夹具6的芯棒部分而设置在上述装置上,通过游标卡尺测定沿经纱方向以0.01cn/dtex的应力压缩时的标线间距离l1(压缩时标线间距离)。
在此,压缩用夹持夹具6的插入筒状织物1中的芯棒部分的外径设为筒状织物1的织物内径最小部位的数值减去“0.1mm±0.03mm”而得到的数值,压缩用接受夹具7的孔部分与筒状织物的织物内径最小部位为等径。在此,等径不必严格地为相同直径,±0.03mm程度的差异当作相同直径处理。此外,图3是用于测定筒状织物的伸长时标线间距离的装置的概念图,如该图3所示,该装置中,作为载重测定器(测力计)4,将日本计测システム株式会社制handydigitalforcegaugehf-1(额定容量10n)设置在架台5上,将具有能够插入筒状织物1中的芯棒部分的伸长用夹持夹具8安装在载重测定器4上,将具有能够插入筒状织物1中的芯棒部分的伸长用接受夹具9安装在架台5上。并且,将筒状织物1的标线2与3的外侧用固定绳10固定,通过游标卡尺测定沿经纱方向以0.01cn/dtex的应力伸长时的标线间距离l2(伸长时标线间距离)。
改变试样进行5次测定,用平均值进行评价。
应予说明,上述应力下算出的载重通过下式算出。
载重(cn)=0.01×经纱纤度×经纱根数。
(6)筒状织物的压缩时织物外径a、伸长时织物外径b
通过与上述(5)相同的流程,通过游标卡尺测定沿经纱方向以0.01cn/dtex的应力压缩筒状织物时的筒状织物的外径。
改变试样进行5次测定,将最大值记作“最大外径a(压缩时织物外径a)”。
此外,通过游标卡尺测定沿经纱方向以0.01cn/dtex的应力伸长筒状织物时的筒状织物的外径。
改变试样进行5次测定,将最小值记作“最小外径b(伸长时织物外径b)”。
任意情况中,外径的测定位置均设为在筒状织物1上标记的2个标线2、3间的中央部位和从标线起5mm内侧的3个部位。由于改变5次试样而进行测定,因此测定进行15次。
(7)筒状织物的内表面的凹凸
用电子显微镜将把筒状织物沿经纱方向裁切而得到的纬纱截面放大至150倍,基于得到的照片,测定筒状织物内表面的相邻经纱的头顶部与纬纱的头顶部的高度之差。使用图4,针对筒状织物的内表面的凹凸的含义进行说明。这样的筒状织物的内表面中,相邻的经纱11与纬纱12的内壁面起算的高度之差y被称为内表面的凹凸。
改变试样进行5次测定,用平均值进行评价。将使用图4说明的该头顶部的高度之差的平均值记作“筒状织物的内表面凹凸”。
(8)织密度
基于jisl1096:20108.6.1而测定。
将试样放置在平坦的台上,去除不自然的褶皱、张力,针对5个不同部位数出0.5cm间的经纱和纬纱的根数,算出各自的平均值,换算为平均2.54cm的根数。
(9)耐扭折性
按照iso7198的指南,耐扭折性测定扭折半径。使筒状织物成环,使用半径已知的圆筒状夹具测定外观上明显发生弯折的半径。为了评价织造管状体本身的特性,不进行内压维持。
[实施例1]
织造步骤中,使用下述的经纱(经纱a、经纱b)和纬纱(纬纱c、纬纱d)。
·经纱a(海岛复合纤维):聚对苯二甲酸乙二醇酯纤维、66dtex、9丝(脱海处理后:52.8dtex、630丝)
·经纱b(可溶纱):共聚了间苯二甲酸5-磺酸钠的碱易溶性的聚酯纤维、84dtex、24丝
·纬纱c(内层)(海岛复合纤维):聚对苯二甲酸乙二醇酯纤维、66dtex、9丝(脱海处理后:52.8dtex、630丝)
·纬纱d(外层):聚对苯二甲酸乙二醇酯纤维、56dtex、18丝
并且,织造时,将经纱b的张力设为0.9cn/dtex,将经纱a的张力设为0.1cn/dtex,后加工后的织密度达到经纱a、201根/英寸(2.54cm)、纬纱c、121根/英寸(2.54cm)、纬纱d、121根/英寸(2.54cm)的内径3mm的筒状织物。应予说明,经纱a和经纱b的配置以相对于3根经纱a为1根经纱b的比率进行配置。此外,经纱b配置于位于内层的纬纱c与位于外层的纬纱d之间。
接着,通过下述的步骤,进行后加工。
(a)热水洗
处理条件在温度98℃、时间20分钟的条件下进行。
(b)预热定型
将外径2.8mm的圆棒插入筒状织物中,将两端用金属丝固定,进行热处理。处理条件为温度180℃、时间5分钟。应予说明,前述圆棒的材质为sus。
(c)脱海处理
进行前述的经纱a、纬纱c的脱海处理,同时进行经纱b的溶解去除。
(c-1)酸处理
作为酸,使用马来酸。处理条件为浓度0.2质量%、温度130℃、时间30分钟。
(c-2)碱处理
作为碱,使用氢氧化钠。处理条件为浓度1质量%、温度80℃、时间90分钟。
(d)热定型(第1次)
将外径3mm的圆棒插入筒状织物,以沿经纱方向不引入褶皱的方式,在最大限度压缩的状态下,将两端用金属丝等固定,进行热处理。处理条件为温度180℃、时间5分钟。应予说明,前述圆棒的材质为sus。
(e)热定型(第2次)
将外径3mm的圆棒插入筒状织物中,在沿经纱方向伸长30%的状态下,将两端用金属丝等固定,进行热处理。处理条件为温度170℃、时间5分钟。应予说明,前述圆棒的材质为sus。
所得筒状织物的特性示于表1。
将所得筒状织物用手弯曲时,操作性良好,伸缩性、柔软性优异。
此外,将该筒状织物彼此缝合时,经纱方向的外径、内径之差小,因此包含筒状织物的人工血管不需要考虑裁切部位,容易缝合。
[实施例2]
实施例1中,将筒状织物的内径设为5mm,不实施第2次热定型,除此之外,以与实施例1相同的方式,得到筒状织物。
将所得筒状织物用手弯曲时,操作性良好,伸缩性、柔软性优异。
此外,将该筒状织物彼此缝合时,经纱方向的外径、内径之差小,因此包含筒状织物的人工血管不需要考虑裁切部位,容易缝合。
所得筒状织物的特性示于表1。
[实施例3]
实施例1中,将筒状织物的内径设为7mm,第2次热定型中伸长20%,除此之外,以与实施例1相同的方式,得到筒状织物。
所得筒状织物的特性示于表1。
将所得筒状织物用手弯曲时,操作性良好,伸缩性、柔软性优异。
此外,将该筒状织物彼此缝合时,经纱方向的外径、内径之差小,因此包含筒状织物的人工血管不需要考虑裁切部位,容易缝合。
[比较例1]
使用实施例1中使用的经纱a和纬纱c,将经纱a的张力设为0.9cn/dtex,后加工后的织密度达到经纱a、201根/英寸(2.54cm)、纬纱c、121根/英寸(2.54cm)的平纹组织的筒状织物(内径3mm)。其后,以与实施例1相同的方式,得到筒状织物。
所得筒状织物的特性示于表1。
将所得筒状织物用手弯曲时,与实施例1相比,无法容易地弯曲,伸缩性、柔软性差。
此外,将该筒状织物彼此缝合时,经纱方向的外径、内径之差小,因此包含筒状织物的人工血管不需要考虑裁切部位,容易缝合。
[比较例2]
实施例1中,将织造时的经纱b的张力设为0.9cn/dtex,将经纱a的张力设为0.9cn/dtex,除此之外,以与实施例1相同的方式,得到筒状织物(内径3mm)。
所得筒状织物的特性示于表1。
将所得筒状织物用手弯曲时,与实施例1相比,无法容易地弯曲,伸缩性、柔软性差。
此外,将该筒状织物彼此缝合时,经纱方向的外径、内径之差小,因此包含筒状织物的人工血管不需要考虑裁切部位,容易缝合。
[比较例3]
织造步骤中,使用下述的经纱e和纬纱f。
·经纱e:聚对苯二甲酸乙二醇酯纤维、66dtex、72丝
·纬纱f:聚对苯二甲酸乙二醇酯纤维、140dtex、144丝
并且,织造时,将经纱e的张力设为0.9cn/dtex,后加工后的织密度达到经纱a、180根/英寸(2.54cm)、纬纱c、120根/英寸(2.54cm)的内径7mm的筒状织物。
接着,通过下述的步骤,进行后加工。
(a)热水洗
处理条件在温度98℃、时间20分钟的条件下进行。
(b)热定型
将外径7.0mm的iso公制螺丝插入筒状织物中,从其上沿着螺纹槽,将聚乙烯制的纱以1kg的张力卷附,进行热处理。处理条件为温度170℃、时间30分钟。应予说明,前述iso公制螺丝的材质为sus。
所得筒状织物的特性示于表1。
将所得筒状织物用手弯曲时,操作性良好,伸缩性、柔软性优异。
此外,该筒状织物彼此缝合时,沿经纱方向外径、内径之差大,因此需要考虑包含筒状织物的人工血管裁切部位,斜向(bias)裁切时,由于凹凸而难以缝合。
[实施例4]
将实施例1中得到的筒状织物浸渍于5.0重量%高锰酸钾(和光纯药工业株式会社制)、0.6mol/l硫酸(和光纯药工业株式会社制)的水溶液中,在60℃下进行3小时反应,将筒状织物进行水解和氧化。
接着,浸渍于0.5重量%dmt-mm(和光纯药工业株式会社制)、5.0重量%pei(lupasol(注册商标)p;basf公司制)的水溶液中,在30℃下进行2小时反应,通过使实施例1中得到的筒状织物的内表面与pei进行缩合反应,进行共价键合。
进一步,浸渍于溴乙烷(和光纯药工业株式会社制)的1重量%甲醇水溶液中,在35℃下进行1小时反应后,升温至50℃而进行4小时反应,将共价键合于实施例1中得到的筒状织物的pei制成季铵。
最后,浸渍于0.75重量%肝素钠(organonapi公司制)、0.1mol/l氯化钠的水溶液(ph=4)中,在70℃下进行6小时反应,通过与制成季铵的pei的离子键,得到在内表面具有抗血栓性材料的层的筒状织物。该筒状织物的肝素总覆盖量为1100miu/mg。
[实施例5]
在实施例4中得到的筒状织物的外表面上,作为生物体吸收性材料,涂布制备为20wt%的浓度的乳酸/羟基乙酸共聚物(溶剂:氯仿),涂布后在室温下干燥一夜,形成生物体吸收性材料的层。所形成的生物体吸收性材料的层的厚度为65μm。对具有所得生物体吸收性材料的层的筒状织物,测定在25℃向内表面施加120mmhg的压力时的透水性时,透水性为0ml/cm2/min.。按照iso7198的指南测定的扭折半径为15mm。
[实施例6]
在实施例4中得到的筒状织物的外表面上,作为生物体吸收性材料,涂布制备为20wt%的浓度的乳酸/ε-己内酯共聚物(溶剂:四氢呋喃),涂布后在40度下干燥2小时,形成生物体吸收性材料的层。所形成的生物体吸收性材料的层的厚度为45μm。对具有所得生物体吸收性材料的层的筒状织物,测定在25℃向内表面施加120mmhg的压力时的透水性时,透水性为0ml/cm2/min.。按照iso7198的指南测定的扭折半径为10mm。
[实施例7]
在实施例4中得到的筒状织物的外表面上,作为生物体吸收性材料,涂布制备为30wt%的明胶溶液(ビーマトリックス(注册商标)明胶ls-h;新田ゼラチン株式会社制),涂布后在4度下冷却1小时,由此使明胶固化,浸渍于0.2%戊二醛溶液中30分钟,将固化的明胶交联。交联后,在40度下干燥一夜。所形成的生物体吸收性材料的层的厚度为120μm。对具有所得生物体吸收性材料的层的筒状织物,测定在25℃向内表面施加120mmhg的压力时的透水性时,透水性为0ml/cm2/min.。按照iso7198的指南测定的扭折半径为7mm。
[实施例8]
对实施例1中得到的筒状织物,测定在25℃向内表面施加120mmhg的压力时的透水性时,透水性为188ml/cm2/min.。
[表1]
表1中,经纱a、纬纱c、纬纱d、经纱e和纬纱f的纱种为聚对苯二甲酸乙二醇酯。
工业实用性
根据本发明所述的筒状织物能够适合地用于人工血管,但其应用范围不限于此。
附图标记说明
1筒状织物
2第一根标线
3第二根标线
4载重测定器
5架台
6压缩用夹持夹具
7压缩用接受夹具
8伸长用夹持夹具
9伸长用接受夹具
10固定绳
x织物外径的最大值的5倍的距离
y内表面的凹凸
- 还没有人留言评论。精彩留言会获得点赞!