聚合性液晶组合物、聚合性液晶组合物的制造方法、光学各向异性膜、光学膜、偏振片及图像显示装置与流程
本发明涉及一种聚合性液晶组合物、聚合性液晶组合物的制造方法、光学各向异性膜、光学膜、偏振片及图像显示装置。
背景技术:
对于显示逆波长分散性的聚合性化合物,由于具有能够进行广波长范围内的准确的光线波长的转换、及由于具有高折射率而能够使相位差膜薄膜化等的特征,因此积极地进行研究。
并且,作为显示逆波长分散性的聚合性化合物,通常采用t型分子设计指南,并且要求将分子长轴的波长进行短波长化,且将位于分子中央处的短轴的波长进行长波长化。
因此,已知在位于分子中央处的短轴的骨架(以下,还称为“逆波长分散显现部”。)与分子长轴的连结中,利用没有吸收波长的亚环烷基骨架(例如,参考专利文献1~专利文献3)。
以往技术文献
专利文献
专利文献1:日本特开2010-031223号公报
专利文献2:国际公开第2014/010325号
专利文献3:日本特开2016-081035号公报
技术实现要素:
发明要解决的技术课题
本发明人等对专利文献1~专利文献3进行研究的结果,发现了具有如下耐久性的问题:有时根据聚合性化合物的种类而聚合性液晶组合物的溶解性差,且根据聚合性化合物的种类、聚合引发剂的种类、及固化温度等聚合条件,所形成的光学各向异性膜暴露在高温高湿下时,导致双折射率发生变化。
因此,本发明的课题在于提供一种用于形成耐久性优异的光学各向异性膜的溶解性优异的聚合性液晶组合物及其制造方法、以及光学各向异性膜、光学膜、偏振片及图像显示装置。
用于解决技术课题的手段
为了实现上述课题,本发明人等进行深入研究的结果发现了,若与以逆波长分散表达部作为中心而沿长轴方向延伸的2个基团(侧链)的结构互不相同,且至少一个侧链为疏水性的不对称结构的聚合性液晶化合物一起,配合具有每一个不对称侧链作为对称结构的2种聚合性液晶化合物,则溶解性良好,所形成的光学各向异性膜的耐久性也得到提高,以完成了本发明。
即,发现了通过以下结构能够实现上述课题。
[1]一种聚合性液晶组合物,其含有由后述的式(1)表示的聚合性液晶化合物p1、由后述的式(2)表示的聚合性液晶化合物p2及由后述的式(3)表示的聚合性液晶化合物p3。
[2]根据[1]所述的聚合性液晶组合物,其中,相对于聚合性液晶组合物的总固体成分质量,聚合性液晶化合物p1、聚合性液晶化合物p2及聚合性液晶化合物p3的含量分别为1质量%以上,且总计为50质量%以上。
[3]根据[1]或[2]所述的聚合性液晶组合物,其中,相对于聚合性液晶组合物的总固体成分质量,聚合性液晶化合物p2的含量为10质量%以上。
[4]根据[1]至[3]中任一项所述的聚合性液晶组合物,其中,后述的式(1)~(3)中的a及b的至少一个表示由后述的式(6)表示的侧链。
[5]根据[4]所述的聚合性液晶组合物,其中,后述的式(6)中的g1及g2均表示环己烷环。
[6]一种聚合性液晶组合物的制造方法,其中,使由后述的式(i)表示的羧酸化合物及由后述的式(ii)表示的羧酸化合物与由后述的式(iii)表示的酚化合物同时反应,制备[1]至[5]中任一项所述的聚合性液晶组合物。
[7]一种光学各向异性膜,其通过使[1]至[5]中任一项所述的聚合性液晶组合物聚合而获得。
[8]根据[7]所述的光学各向异性膜,其满足后述的式(7)。
[9]一种光学膜,其具有[7]或[8]所述的光学各向异性膜。
[10]一种偏振片,其具有[9]所述的光学膜和起偏器。
[11]一种图像显示装置,其具有[9]所述的光学膜或[10]所述的偏振片。
发明效果
根据本发明,能够提供一种用于形成耐久性优异的光学各向异性膜的溶解性优异的聚合性液晶组合物及其制造方法、以及光学各向异性膜、光学膜、偏振片及图像显示装置。
附图说明
图1a是表示本发明的光学膜的一例的示意性剖视图。
图1b是表示本发明的光学膜的一例的示意性剖视图。
图1c是表示本发明的光学膜的一例的示意性剖视图。
具体实施方式
以下,对本发明进行详细说明。
以下所记载的构成要件的说明有时是基于本发明的代表性实施方式来进行的,但本发明并不限定于这种实施方式。
另外,本说明书中,使用“~”来表示的数值范围是指将“~”的前后所记载的数值作为下限值及上限值而包含的范围。
并且,在本说明书中,除了指定键合位置的情况以外,所标记的二价的基团(例如,-o-co-)的键合方向并无特别限制,例如,在后述式(4)中的d1为-co-o-的情况下,若将键合于ar侧的位置设为*1,且将键合于a1侧的位置设为*2,则d1可以是*1-co-o-*2,也可以是*1-o-co-*2。
[聚合性液晶组合物]
本发明的聚合性液晶组合物为含有由下述式(1)表示的聚合性液晶化合物p1、由下述式(2)表示的聚合性液晶化合物p2及由下述式(3)表示的聚合性液晶化合物p3的聚合性液晶组合物。
a-ar-a……(1)
a-ar-b……(2)
b-ar-b……(3)
上述式(1)及(2)中,a表示clogp值均显示相同值的由后述的式(4)表示的侧链,上述式(2)及(3)中,b表示clogp值均显示相同值的由后述的式(5)表示的侧链。其中,a及b表示clogp值互不相同,a的clogp值大于b的clogp值,且至少一个clogp值成为3.3以上的侧链,
在此,clogp值是指通过计算对1-辛醇和水的分配系数p的常用对数logp而求出的值。关于用于计算clogp值的方法和软件,能够使用公知的方法和软件,但是只要并无特别说明,则在本发明中使用在cambridgesoft公司的chembiodrawultra13.0中编入的clogp程序。
并且,关于式中的a,“clogp值均显示相同值”是指上述式(1)中的2个a及上述式(2)中的a为clogp值显示相同值的结构,并且是指由后述的式(4)表示的侧链结构为相同结构或者结构异构体。另外,关于式中的b,也同样地进行解释。
本发明中,如上所述,通过与由上述式(2)表示的聚合性液晶化合物p2一起配合由上述式(1)及(3)表示的聚合性液晶化合物p1及聚合性液晶化合物p3,聚合性液晶组合物的溶解性得到提高,所形成的光学各向异性膜的耐久性良好。
虽然其详细内容尚不明确,但是本发明人等推测如下。
即,推测为:通过配合侧链结构不对称的聚合性液晶化合物p2,分子彼此的堆积得到阻碍,其结果,聚合性液晶化合物对有机溶剂的溶解性得到提高。并且,推测为:通过设为与聚合性液晶化合物p3一起配合有具有聚合性液晶化合物p3中的每一个不对称侧链作为对称结构的聚合性液晶化合物p1及p3的3种类型的混合物,溶解性得到进一步提高。
另一方面,推测为:由于聚合性液晶化合物p1及p3的侧链中的至少一个为疏水性,且聚合性液晶化合物p2的不对称侧链中的至少一个也为疏水性,因此所形成的光学各向异性膜的水分吸收减少,其结果,光学各向异性膜的耐久性得到提高。
以下,对本发明的聚合性液晶组合物的各成分进行详细说明。
〔聚合性液晶化合物〕
本发明的聚合性液晶组合物含有由下述式(1)表示的聚合性液晶化合物p1、由下述式(2)表示的聚合性液晶化合物p2及由下述式(3)表示的聚合性液晶化合物p3。
a-ar-a……(1)
a-ar-b……(2)
b-ar-b……(3)
上述式(1)及(2)中,a表示clogp值均显示相同值的由下述式(4)表示的侧链,上述式(2)及(3)中,b表示clogp值均显示相同值的由下述式(5)表示的侧链。
其中,a及b表示clogp值互不相同,a的clogp值大于b的clogp值,且至少一个clogp值成为3.3以上的侧链。
*-d1-(a1-e1)n-sp1-l1……(4)
*-d2-(a2-e2)m-sp2-l2……(5)
上述式(4)及(5)中,*表示与ar的键合位置,n及m分别独立地表示1以上的整数。
并且,上述式(4)及(5)中,d1、d2、e1及e2分别独立地表示单键或-co-、-o-、-s-、-c(=s)-、-cr1r2-、-cr3=cr4-、-nr5-或者包含它们中的2个以上的组合的2价的连结基团,r1~r5分别独立地表示氢原子、氟原子或碳原子数1~4的烷基。在n为2以上的整数的情况下,多个e1可以分别相同,也可以不同,在m为2以上的整数的情况下,多个e2可以分别相同,也可以不同。
并且,上述式(4)及(5)中,a1及a2分别独立地表示可以具有取代基的碳原子数6以上的芳香环、或可以具有取代基的碳原子数6以上的环烷烃环。在n为2以上的整数的情况下,多个a1可以分别相同,也可以不同,在m为2以上的整数的情况下,多个a2可以分别相同,也可以不同。
并且,上述式(4)及(5)中,sp1及sp2分别独立地表示单键或碳原子数1~20的直链状或支链状的亚烷基、碳原子数2~20的直链状或支链状的亚烯基、碳原子数2~20的直链状或支链状的亚炔基或构成亚烷基、亚烯基及亚炔基的1个以上的-ch2-被-o-、-s-、-nh-、-n(q)-或-co-取代而得的2价的连结基团,q表示取代基。
并且,上述式(4)及(5)中,l1及l2分别独立地表示1价的有机基团,l1及l2的至少一个表示聚合性基团。其中,在上述式(1)~(3)中的ar为由后述的式(ar-3)表示的芳香环的情形下,l1及l2以及后述的式(ar-3)中的l3及l4的至少一个表示聚合性基团。
上述式(4)及(5)中,n及m分别独立地表示1以上的整数,优选为1~3的整数,更优选为1或2,进一步优选为2。
上述式(4)及(5)中,作为d1、d2、e1及e2所表示的2价的连结基团,例如,可举出-co-o-、-c(=s)o-、-cr1r2-、-cr1r2-cr1r2-、-o-cr1r2-、-cr1r2-o-cr1r2-、-co-o-cr1r2-、-o-co-cr1r2-、-cr1r2-o-co-cr1r2-、-cr1r2-co-o-cr1r2-、-nr5-cr1r2-及-co-nr5-等。r1、r2及r5分别独立地表示氢原子、氟原子或碳原子数1~4的烷基。
其中,d1及d2优选为-co-o-,e1及e2优选为-o-、-co-o-、-co-nr5-,更优选为-co-o-。
上述式(4)及(5)中,作为a1及a2所表示的碳原子数6以上的芳香环,例如可举出苯环、萘环、蒽环、菲咯啉环等芳香族烃环;呋喃环、吡咯环、噻吩环、吡啶环、噻唑环、苯并噻唑环等芳香族杂环。其中,优选苯环(例如,1,4-苯基等)。
并且,上述式(4)及(5)中,a1及a2所表示的碳原子数6以上的环烷烃环,例如可举出环己烷环、环戊烷环、环辛烷环、环十二烷环、二十二烷环等。其中,优选环己烷环(例如,1,4-亚环己基等),更优选反式-1,4-亚环己基。
另外,作为碳原子数6以上的芳香环或碳原子数6以上的环烷烃环可以具有的取代基,可举出与后述的式(ar-1)中的y1可以具有的取代基相同的基团。
上述式(4)及(5)中,作为sp1及sp2所表示的碳原子数1~20的直链状或支链状的亚烷基,优选碳原子数1~12的直链状或支链状的亚烷基,例如,可优选举出亚甲基、亚乙基、亚丙基、亚丁基、亚戊基、亚己基、甲基己烯基、庚烯基等。
并且,作为sp1及sp2所表示的碳原子数2~20的直链状或支链状的亚烯基,优选碳原子数2~20的直链状或支链状的亚烯基,例如,可优选举出亚乙烯基、亚丙烯基、亚丁烯基等。
并且,作为sp1及sp2所表示的碳原子数2~20的直链状或支链状的亚炔基,例如,可优选举出亚乙炔基。
另外,如上所述,sp1及sp2可以是构成亚烷基、亚烯基及亚炔基的1个以上的-ch2-被-o-、-s-、-nh-、-n(q)-或-co-取代而得的2价的连结基团,作为由q表示的取代基,可举出与后述的式(ar-1)中的y1可以具有的取代基相同的基团。
上述式(4)及(5)中,作为l1及l2所示的1价的有机基团,例如,能够举出烷基、芳基、杂芳基等。烷基可以是直链状、支链状或环状,但是优选直链状。烷基的碳原子数优选1~30,更优选1~20,进一步优选1~10。并且,芳基可以是单环,也可以是多环,但是优选单环。芳基的碳原子数优选6~25,更优选6~10。并且,杂芳基可以是单环,也可以是多环。构成杂芳基的杂原子的数量优选1~3。构成杂芳基的杂原子优选氮原子、硫原子、氧原子。杂芳基的碳原子数优选6~18,更优选6~12。并且,烷基、芳基及杂芳基可以未经取代,也可以具有取代基。作为取代基,可举出与后述的式(ar-1)中的y1可以具有的取代基相同的取代基。
上述式(4)及(5)中,l1及l2的至少一个所表示的聚合性基团,并无特别限定,但是优选能够进行自由基聚合或阳离子聚合的聚合性基团。
作为自由基聚合性基团,能够使用众所周知的自由基聚合性基团,作为优选的自由基聚合性基团,能够举出丙烯酰基或甲基丙烯酰基。已知在该情况下,通常丙烯酰基的聚合速度快,从提高生产率的观点出发,优选丙烯酰基,但是甲基丙烯酰基也能够同样地用作聚合性基团。
作为阳离子聚合性基团,能够使用众所周知的阳离子聚合性基团,具体而言,能够举出脂环式醚基、环状缩醛基、环状内酯基、环状硫醚基、螺环原酸酯基及乙烯氧基等。其中,优选脂环式醚基或乙烯氧基,尤其优选环氧基、氧杂环丁基或乙烯氧基。
作为尤其优选的聚合性基团的例,可举出下述。
[化学式1]
本发明中,从所形成的光学各向异性膜的耐久性得到进一步提高的理由出发,由上述式(4)表示的侧链即上述式(1)及(2)中的a的clogp值优选为4.0以上,更优选为4.0~6.0。
并且,只要由上述式(5)表示的侧链即上述式(2)及(3)中的b的clogp值为比上述式(1)及(2)中的a的clogp值小的值,则并无特别限定,但是优选为1.0~5.0,更优选为2.5~4.5。
另一方面,上述式(1)~(3)中,ar表示选自包含由下述式(ar-1)~(ar-5)表示的基团的组中的任一个芳香环。另外,下述式(ar-1)~(ar-5)中,*表示与上述式(4)及(5)中的d1或d2的键合位置。
[化学式2]
在此,上述式(ar-1)中,q1表示n或ch,q2表示-s-、-o-或-n(r6)-,r6表示氢原子或碳原子数1~6的烷基,y1表示可以具有取代基的碳原子数6~12的芳香族烃基、或碳原子数3~12的芳香族杂环基。
作为r6所表示的碳原子数1~6的烷基,具体而言,例如可举出甲基、乙基、丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基及正己基等。
作为y1所表示的碳原子数6~12的芳香族烃基,例如可举出苯基、2,6-二乙基苯基、萘基等芳基。
作为y1所表示的碳原子数3~12的芳香族杂环基,例如可举出噻吩基、噻唑基、呋喃基、吡啶基等杂芳基。
并且,作为y1可以具有的取代基,例如可举出烷基、烷氧基、卤素原子等。
作为烷基,例如优选碳原子数1~18的直链状、分支链状或环状的烷基,更优选碳原子数1~8的烷基(例如,甲基、乙基、丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、环己基等),进一步优选碳原子数1~4的烷基,尤其优选甲基或乙基。
作为烷氧基,例如优选碳原子数1~18的烷氧基,更优选碳原子数1~8的烷氧基(例如,甲氧基、乙氧基、正丁氧基、甲氧基乙氧基),进一步优选碳原子数1~4的烷氧基,尤其优选甲氧基或乙氧基。
作为卤素原子,例如可举出氟原子、氯原子、溴原子、碘原子等,其中,优选氟原子、氯原子。
并且,上述式(ar-1)~(ar-5)中,z1、z2及z3分别独立地表示氢原子、碳原子数1~20的1价的脂肪族烃基、碳原子数3~20的1价的脂环式烃基、碳原子数6~20的1价的芳香族烃基、卤素原子、氰基、硝基、-or7、-nr8r9或-sr10,r7~r10分别独立地表示氢原子或碳原子数1~6的烷基,z1及z2可以相互键合而形成芳香环。
作为碳原子数1~20的1价的脂肪族烃基,优选碳原子数1~15的烷基,更优选碳原子数1~8的烷基,具体而言,进一步优选甲基、乙基、异丙基、叔戊基(1,1-二甲基丙基)、叔丁基、1,1-二甲基-3,3-二甲基-丁基,尤其优选甲基、乙基、叔丁基。
作为碳原子数3~20的1价的脂环式烃基,例如可举出环丙基、环丁基、环戊基、环己基、环庚基、环辛基、环癸基、甲基环己基、乙基环己基等单环式饱和烃基;环丁烯基、环戊烯基、环己烯基、环庚烯基、环辛烯基、环癸烯基、环戊二烯基、环己二烯基、环辛二烯基、环癸二烯等单环式不饱和烃基;双环[2.2.1]庚基、双环[2.2.2]辛基、三环[5.2.1.02,6]癸基、三环[3.3.1.13,7]癸基、四环[6.2.1.13,6.02,7]十二烷基、金刚烷基等多环式饱和烃基等。
作为碳原子数6~20的1价的芳香族烃基,具体而言,例如可举出苯基、2,6-二乙基苯基、萘基、联苯基等,优选碳原子数6~12的芳基(尤其,苯基)。
作为卤素原子,例如可举出氟原子、氯原子、溴原子、碘原子等,其中,优选氟原子、氯原子、溴原子。
另一方面,作为r7~r10所表示的碳原子数1~6的烷基,具体而言,例如可举出甲基、乙基、丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基及正己基等。
并且,上述式(ar-2)及(ar-3)中,a3及a4分别独立地表示选自包含-o-、-n(r11)-、-s-及-co-的组中的基团,r11表示氢原子或取代基。
作为r11所表示的取代基,可举出与上述式(ar-1)中的y1可以具有的取代基相同的取代基。
并且,上述式(ar-2)中,x表示氢原子或可以键合取代基的第14~16族的非金属原子。
并且,作为x所表示的第14~16族的非金属原子,例如可举出氧原子、硫原子、具有取代基的氮原子、具有取代基的碳原子,作为取代基,具体而言,例如可举出烷基、烷氧基、烷基取代烷氧基、环状烷基、芳基(例如,苯基、萘基等)、氰基、氨基、硝基、烷基羰基、磺基、羟基等。
并且,上述式(ar-3)中,d3及d4分别独立地表示单键或-co-、-o-、-s-、-c(=s)-、-cr1r2-、-cr3=cr4-、-nr5-或者包含它们中的2个以上的组合的2价的连结基团,r1~r5分别独立地表示氢原子、氟原子或碳原子数1~4的烷基,
在此,作为2价的连结基团,可举出与在上述式(4)及(5)中的d1及d2中说明的基团相同的基团。
并且,上述式(ar-3)中,sp3及sp4分别独立地表示单键或碳原子数1~20的直链状或支链状的亚烷基、碳原子数2~20的直链状或支链状的亚烯基、碳原子数2~20的直链状或支链状的亚炔基或构成亚烷基、亚烯基及亚炔基的1个以上的-ch2-被-o-、-s-、-nh-、-n(q)-或-co-取代而得的2价的连结基团,q表示取代基。
在此,作为亚烷基、亚烯基及亚炔基,可举出与在上述式(4)及(5)中的sp1及sp2中说明的基团相同的基团。
并且,作为取代基,可举出与上述式(ar-1)中的y1可以具有的取代基相同的取代基。
并且,上述式(ar-3)中,l3及l4分别独立地表示1价的有机基团,l3及l4以及上述式(4)及(5)中的l1及l2的至少一个表示聚合性基团。
作为1价的有机基团,可举出与在上述式(4)及(5)中的l1及l2中说明的基团相同的基团。
并且,作为聚合性基团,可举出与在上述式(4)及(5)中的l1及l2中说明的基团相同的基团。
并且,上述式(ar-4)~(ar-5)中,ax表示具有选自包含芳香族烃环及芳香族杂环的组中的至少1个芳香环的碳原子数2~30的有机基团。
并且,上述式(ar-4)~(ar-5)中,ay表示氢原子、可以具有取代基的碳原子数1~12的烷基、或具有选自包含芳香族烃环及芳香族杂环的组中的至少一个芳香环的碳原子数2~30的有机基团。
在此,ax及ay中的芳香环可以具有取代基,也可以ax与ay键合而形成环。
并且,q3表示氢原子、或可以具有取代基的碳原子数1~6的烷基。
作为ax及ay,可举出专利文献2(国际公开第2014/010325号)的[0039]至[0095]段中所记载的基团。
并且,作为q3所表示的碳原子数1~6的烷基,具体而言,例如可举出甲基、乙基、丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、正戊基及正己基等,作为取代基,可举出与上述式(ar-1)中的y1可以具有的取代基相同的取代基。
本发明中,从所形成的光学各向异性膜的耐久性得到进一步提高的理由出发,优选上述式(1)~(3)中的a及b的至少一个表示由下述式(6)表示的侧链。另外,即使在上述式(1)~(3)中的a及b这两者表示由下述式(6)表示的侧链的情况下,如上所述,本发明中,a及b也表示clogp值互不相同,a的clogp值大于b的clogp值,且至少一个clogp值成为3.3以上的侧链。
*-d5-g1-g2-d6-sp5-l5……(6)
上述式(6)中,*表示与ar的键合位置,
并且,上述式(6)中,d5及d6分别独立地表示单键或-co-、-o-、-s-、-c(=s)-、-cr1r2-、-cr3=cr4-、-nr5-或者包含它们中的2个以上的组合的2价的连结基团,r1~r5分别独立地表示氢原子、氟原子或碳原子数1~4的烷基。另外,作为2价的连结基团,可举出与在上述式(4)及(5)中的d1及d2中说明的基团相同的基团。
并且,上述式(6)中,g1及g2分别独立地表示可以具有取代基的碳原子数6以上的环烷烃环,另外,作为取代基及环烷烃环,可分别举出与在上述式(4)及(5)中的a1及a2中说明的取代基及环相同的取代基及环。
并且,上述式(6)中,sp5表示单键或碳原子数1~20的直链状或支链状的亚烷基、碳原子数2~20的直链状或支链状的亚烯基、碳原子数2~20的直链状或支链状的亚炔基或构成亚烷基、亚烯基及亚炔基的1个以上的-ch2-被-o-、-s-、-nh-、-n(q)-或-co-取代而得的2价的连结基团,q表示取代基。另外,作为亚烷基、亚烯基及亚炔基,可分别举出与在上述式(4)及(5)中的sp1及sp2中说明的基团相同的基团。
并且,上述式(6)中,l5表示1价的有机基团或聚合性基团。另外,作为1价的有机基团及聚合性基团,可分别举出与在上述式(4)及(5)中的l1及l2中说明的基团相同的基团。
并且,本发明中,从所形成的光学各向异性膜的耐久性得到进一步提高的理由出发,优选上述式(6)中的g1及g2均表示环己烷环。
作为由上述式(1)~(3)表示的聚合性液晶化合物中的由上述式(2)表示的聚合性液晶化合物p2,具体而言,例如,可举出将下述表1中的1-1~1-16中所示的侧链a及侧链b的组合导入到由下述式(c1)~(c9)表示的ar结构的两个侧链上而得的化合物。
另外,下述表1中的1-1、1-11及1-16中所示的侧链b的结构中,分别与丙烯酰氧基及甲基丙烯酰基相邻的基团表示亚丙基(甲基取代亚乙基而得的基团),且表示甲基位置不同的位置异构体的混合物。
[化学式3]
[表1]
并且,作为由上述式(1)表示的聚合性液晶化合物p1,具体而言,例如,可分别举出将上述表1中所示的侧链a导入到由上述的式(c1)~(c9)表示的ar结构的两个侧链上而得的化合物。
同样地,作为由上述式(3)表示的聚合性液晶化合物p3,具体而言,例如,可分别举出将上述表1中所示的侧链b导入到由上述的式(c1)~(c9)表示的ar结构的两个侧链上而得的化合物。
本发明中,从溶解性变得更良好,且所形成的光学各向异性膜的耐久性得到进一步提高的理由出发,优选相对于聚合性液晶组合物的总固体成分质量,聚合性液晶化合物p1、聚合性液晶化合物p2及聚合性液晶化合物p3的含量分别为1质量%以上,且总计为50质量%以上,更优选相对于聚合性液晶组合物的总固体成分质量,聚合性液晶化合物p1、聚合性液晶化合物p2及聚合性液晶化合物p3的含量分别为3质量%以上,且总计为50质量%以上,进一步优选总计为75~100质量%,特别优选总计为85~100质量%。
并且,本发明中,从溶解性变得更良好,且所形成的光学各向异性膜的耐久性得到进一步提高的理由出发,相对于聚合性液晶组合物的总固体成分质量,聚合性液晶化合物p2的含量优选为10质量%以上,更优选为10~50质量%。
〔其他聚合性化合物〕
除了上述的聚合性液晶化合物p1~p3以外,本发明的聚合性液晶组合物还可以包含具有1个以上的聚合性基团的其他聚合性化合物。
在此,其他聚合性化合物所具有的聚合性基团并无特别限定,例如可举出丙烯酰基、甲基丙烯酰基、乙烯基、苯乙烯基、烯丙基等。其中,优选具有丙烯酰基、甲基丙烯酰基。
作为其他聚合性化合物,从所形成的光学各向异性膜的耐湿热性得到进一步提高的理由出发,优选具有1个~4个聚合性基团的其他聚合性化合物,更优选具有2个聚合性基团的其他聚合性化合物。
作为其他聚合性化合物,可举出日本特开2016-053709号公报的[0073]~[0074]段中所记载的化合物。
并且,作为其他聚合性化合物,可举出日本特开2014-077068号公报的[0030]~[0033]段中所记载的由式(m1)、(m2)、(m3)表示的化合物,更具体而言,可举出日本特开2014-077068号公报的[0046]~[0055]段中所记载的具体例。
并且,作为其他聚合性化合物,还能够优选使用日本特开2014-198814号公报中所记载的式(1)~(3)的结构的聚合性化合物,更具体而言,可举出日本特开2014-198814号公报的[0020]~[0035]、[0042]~[0050]、[0056]~[0057]段中所记载的具体例。
相对于包括上述的聚合性液晶化合物p1~p3在内的总质量,含有这种其他聚合性化合物时的含量优选小于50质量%,更优选为40质量%以下,进一步优选为10~30质量%。
〔聚合引发剂〕
优选本发明的聚合性液晶组合物含有聚合引发剂。
优选所使用的聚合引发剂为通过紫外线照射而能够引发聚合反应的光聚合引发剂。
作为光聚合引发剂,例如可举出α-羰基化合物(记载于美国专利第2367661号、美国专利第2367670号的各说明书)、偶姻醚(记载于美国专利第2448828号说明书)、α-烃取代芳香族偶姻化合物(记载于美国专利第2722512号说明书)、多核醌化合物(记载于美国专利第3046127号、美国专利第2951758号的各说明书)、三芳基咪唑二聚体和对氨基苯基酮的组合(记载于美国专利第3549367号说明书)、吖啶及吩嗪化合物(记载于日本特昭60-105667号公报、美国专利第4239850号说明书)及噁二唑化合物(记载于美国专利第4212970号说明书)、酰基膦氧化合物(记载于日本特公昭63-040799号公报、日本特公平5-029234号公报、日本特开平10-095788号公报、日本特开平10-029997号公报)等。
并且,本发明中,聚合引发剂也优选为肟型聚合引发剂,作为其具体例,可举出国际公开第2017/170443号的[0049]至[0052]段中所记载的引发剂。
〔溶剂〕
从形成光学各向异性膜的操作性等的观点出发,优选本发明的聚合性液晶组合物含有溶剂。
作为溶剂,具体而言,例如可举出酮类(例如,丙酮、2-丁酮、甲基异丁基酮、环己酮、环戊酮等)、醚类(例如,二噁烷、四氢呋喃等)、脂肪族烃类(例如,己烷等)、脂环式烃类(例如,环己烷等)、芳香族烃类(例如,甲苯、二甲苯、三甲苯等)、卤代碳类(例如,二氯甲烷、二氯乙烷、二氯苯、氯甲苯等)、酯类(例如,乙酸甲酯、乙酸乙酯、乙酸丁酯等)、水、醇类(例如,乙醇、异丙醇、丁醇、环己醇等)、溶纤剂类(例如,甲基溶纤剂、乙基溶纤剂等)、溶纤剂乙酸酯类、亚砜类(例如,二甲基亚砜等)、酰胺类(例如,二甲基甲酰胺、二甲基乙酰胺等)等,可以单独使用它们中的1种,也可以同时使用2种以上。
〔流平剂〕
从将光学各向异性膜的表面保持为平滑,并使取向控制变得容易的观点出发,优选本发明的聚合性液晶组合物含有流平剂。
作为这种流平剂,从相对于添加量的流平效果高的理由出发,优选氟系流平剂或硅系流平剂,从难以引起渗出(起霜、渗漏)的观点出发,更优选氟系流平剂。
作为流平剂,具体而言,例如可举出日本特开2007-069471号公报的[0079]~[0102]段中所记载的化合物、日本特开2013-047204号公报中所记载的由通式(i)表示的化合物(尤其,[0020]~[0032]段中所记载的化合物)、日本特开2012-211306号公报中所记载的由通式(i)表示的化合物(尤其,[0022]~[0029]段中所记载的化合物)、日本特开2002-129162号公报中所记载的由通式(i)表示的液晶取向促进剂(尤其,[0076]~[0078]及[0082]~[0084]段中所记载的化合物)、日本特开2005-099248号公报中所记载的由通式(i)、(ii)及(iii)表示的化合物(尤其,[0092]~[0096]段中所记载的化合物)等。另外,可以兼备作为后述的取向控制剂的功能。
〔取向控制剂〕
根据需要,本发明的聚合性液晶组合物能够含有取向控制剂。
通过取向控制剂,除了均匀取向以外,还能够形成垂直取向(vertical取向)、倾斜取向、混合取向、胆甾醇取向等各种取向状态,并且,能够更均匀且更精密地控制并实现特定的取向状态。
作为促进均匀取向的取向控制剂,例如能够使用低分子的取向控制剂或高分子的取向控制剂。
作为低分子的取向控制剂,例如能够参考日本特开2002-020363号公报的[0009]~[0083]段、日本特开2006-106662号公报的[0111]~[0120]段、及日本特开2012-211306公报的[0021]~[0029]段的记载,且该内容被编入本申请说明书中。
并且,作为高分子的取向控制剂,例如能够参考日本特开2004-198511号公报的[0021]~[0057]段、及日本特开2006-106662号公报的[0121]~[0167]段,且该内容被编入本申请说明书中。
并且,作为形成或促进垂直取向的取向控制剂,例如可举出硼酸化合物、鎓盐化合物,具体而言,能够参考日本特开2008-225281号公报的[0023]~[0032]段、日本特开2012-208397号公报的[0052]~[0058]段、日本特开2008-026730号公报的[0024]~[0055]段、日本特开2016-193869号公报的[0043]~[0055]段等中所记载的化合物,且该内容被编入本申请说明书中。
另一方面,关于胆甾醇取向,能够通过在本发明的聚合性组合物中加入手性剂来实现,且能够根据其手性方向来控制胆甾醇取向的回旋方向。另外,能够根据手性剂的取向限制力来控制胆甾醇取向的间距。
相对于聚合性液晶组合物中的总固体成分质量,含有取向控制剂时的含量优选为0.01~10质量%,更优选为0.05~5质量%。若含量在该范围内,则能够获得实现所期望的取向状态,并且没有析出、相分离、取向缺陷等,而均匀且高透明性的光学各向异性膜。
这些取向控制剂还能够赋予聚合性官能团、尤其能够赋予能够与构成本发明的聚合性液晶组合物的聚合性液晶化合物聚合的聚合性官能团。
〔其他成分〕
本发明的聚合性液晶组合物还可以含有除了上述的成分以外的成分,例如可举出除了上述的聚合性液晶化合物以外的液晶化合物、表面活性剂、倾斜角控制剂、取向助剂、增塑剂及交联剂等。
[聚合性液晶组合物的制造方法]
本发明的聚合性液晶组合物的制造方法为使由下述式(i)表示的羧酸化合物及由下述式(ii)表示的羧酸化合物与由下述式(iii)表示的酚化合物同时反应,制备上述的本发明的聚合性液晶组合物的方法,且为通过一锅法制备含有上述的聚合性液晶化合物p1~p3的聚合性液晶组合物的制造方法。
在此,“同时反应”是指在存在由下述式(i)表示的羧酸化合物及由下述式(ii)表示的羧酸化合物这两者的条件下使它们与由下述式(iii)表示的酚化合物进行反应。
ho-c(=o)-(a1-e1)n-sp1-l1……(i)
ho-c(=o)-(a2-e2)m-sp2-l2……(ii)
ho-ar-oh……(iii)
上述式(i)及(ii)中,n、m、a1、a2、e1、e2、sp1、sp2、l1及l2均与作为上述的式(4)及(5)中的n、m、a1、a2、e1、e2、sp1、sp2、l1及l2而说明的内容相同。
并且,上述式(iii)中,ar与作为上述的式(1)~(3)中的ar而说明的内容相同。
〔羧酸化合物〕
作为由上述式(i)及(ii)表示的羧酸化合物的组合,可举出下述表2中的2-1~2-16中所示的羧酸化合物的组合。
另外,下述表2中的2-1、2-11及2-16中所示的式(ii)的羧酸化合物中,分别与丙烯酰氧基及甲基丙烯酰基相邻的基团表示亚丙基(甲基取代亚乙基而得的基团),且表示甲基位置不同的位置异构体的混合物。
[表2]
〔酚化合物〕
作为由上述式(iii)表示的酚化合物,具体而言,例如,可举出由下述式(d1)~(d9)表示的化合物。
[化学式4]
〔反应条件〕
由上述式(i)表示的羧酸化合物及由上述式(ii)表示的羧酸化合物与由上述式(iii)表示的酚化合物同时反应的反应条件并无特别限定,能够适当地采用以往公知的酯化反应条件。
例如,可举出:在酸性条件下使羧酸化合物和酚化合物进行脱水缩合的方法;使羧酸化合物与亚硫酰氯等氯化剂进行反应而衍生为酰氯之后与酚化合物进行酯化的方法;使羧酸化合物与甲磺酰氯或甲苯磺酰氯进行反应而衍生为混合酸酐之后与酚化合物进行酯化的方法;使用缩合剂将羧酸化合物与酚化合物进行酯化的方法等。
例如,关于反应温度,优选在-10~150℃下进行,更优选在-5~120℃下进行,进行一步优选在-5~100℃下进行。
并且,关于反应时间,优选进行10分钟~24小时,更优选进行20分钟~10小时,进一步优选进行30分钟~8小时。
[光学各向异性膜]
本发明的光学各向异性膜为将上述的本发明的聚合性液晶组合物聚合而获得的光学各向异性膜。
作为光学各向异性膜的形成方法,例如可举出使用上述的本发明的聚合性液晶组合物,设为所期望的取向状态之后,通过聚合进行固定化的方法等。
在此,聚合条件并无特别限定,但是通过光照射的聚合中,优选使用紫外线。照射量优选为10mj/cm2~50j/cm2,更优选为20mj/cm2~5j/cm2,进一步优选为30mj/cm2~3j/cm2,尤其优选为50~1000mj/cm2。并且,为了促进聚合反应,可以在加热条件下实施。
另外,本发明中,光学各向异性膜能够形成于后述的本发明的光学膜中的任意的支撑体上、后述的本发明的偏振片中的起偏器上。
本发明的光学各向异性膜优选满足下述式(7)。
0.50<re(450)/re(550)<1.00……(7)
其中,上述式(7)中,re(450)表示光学各向异性膜的波长450nm下的面内延迟,re(550)表示光学各向异性膜的波长550nm下的面内延迟。另外,在本说明书中,在未指定延迟的测定波长的情况下,测定波长设为550nm。
并且,面内延迟及厚度方向的延迟的值是指使用axoscanopmf-1(optoscience,inc.制造)并使用测定波长的光测定的值。
具体而言,通过使用axoscanopmf-1输入平均折射率((nx+ny+nz)/3)和膜厚(d(μm))来计算如下:
慢轴方向(°)
re(λ)=r0(λ)
rth(λ)=((nx+ny)/2-nz)×d。
另外,r0(λ)显示为利用axoscanopmf-1计算的数值,但是指re(λ)。
本发明的光学各向异性膜优选正a板或正c板,更优选正a板。
在此,正a板(positiveaplate)和正c板(positivecplate)定义为如下。
当将薄膜面内的慢轴方向(面内的折射率最大的方向)的折射率设为nx,将在面内与面内的慢轴正交的方向的折射率设为ny,将厚度方向的折射率设为nz时,正a板满足式(a1)的关系,正c板满足式(c1)的关系。另外,正a板的rth表示正值,正c板的rth表示负值。
式(a1)nx>ny≈nz
式(c1)nz>nx≈ny
另外,所谓上述“≈”,不仅包含两者完全相同的情况,还包含两者实质上相同的情况。
所谓“实质上相同”,在正a板中,例如,即使在(ny-nz)×d(其中,d为薄膜的厚度)为-10~10nm、优选为-5~5nm的情况下也包含于“ny≈nz”中,即使在(nx-nz)×d为-10~10nm、优选为-5~5nm的情况下也包含于“nx≈nz”中。并且,在正c板中,例如,即使在(nx-ny)×d(其中,d为薄膜的厚度)为0~10nm、优选为0~5nm的情况下也包含于“nx≈ny”中。
在本发明的光学各向异性膜为正a板的情况下,从作为λ/4板发挥功能的观点出发,re(550)优选为100~180nm,更优选为120~160nm,进一步优选为130~150nm,尤其优选为130~140nm。
在此,“λ/4板”是指具有λ/4功能的板,具体而言,是指具有将某一特定的波长的直线偏振光转换为圆偏振光(或将圆偏振光转换为直线偏振光)的功能的板。
[光学膜]
本发明的光学膜为具有本发明的光学各向异性膜的光学膜。
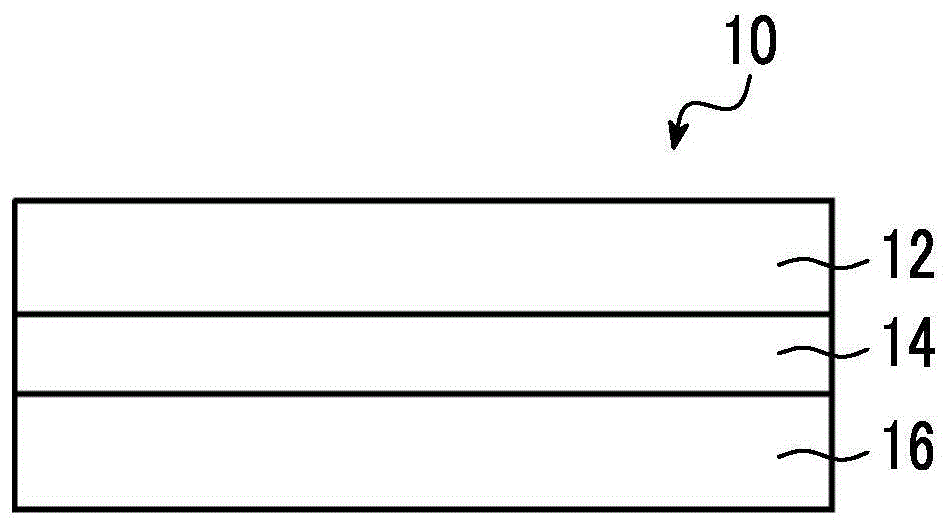
图1a、图1b及图1c(以下,在无需特别区分这些附图的情况下,简称为“图1”。)分别是表示本发明的光学膜的一例的示意性剖视图。
另外,图1为示意图,各层的厚度的关系、位置关系等不一定与实际一致,图1中所示的支撑体、取向膜及硬涂层均为任意的构成部件。
图1中所示的光学膜10依次具有支撑体16、取向膜14及光学各向异性膜12。
并且,如图1b所示,光学膜10可以在支撑体16的与设置有取向膜14的侧相反的一侧具有硬涂层18,如图1c所示,可以在光学各向异性膜12的与设置有取向膜14的侧相反的一侧具有硬涂层18。
以下,对本发明的光学膜中所使用的各种部件进行详细说明。
〔光学各向异性膜〕
本发明的光学膜所具有的光学各向异性膜为上述的本发明的光学各向异性膜。
本发明的光学膜中,对于上述光学各向异性膜的厚度,并无特别限定,但是优选为0.1~10μm,更优选为0.5~5μm。
〔支撑体〕
如上所述,本发明的光学膜可以具有支撑体,来作为用于形成光学各向异性膜的基材。
优选这种支撑体为透明,具体而言,优选透光率为80%以上。
作为这种支撑体,例如可举出玻璃基板、聚合物薄膜,作为聚合物薄膜的材料,可举出纤维素系聚合物;聚甲基丙烯酸甲酯、含有内酯环的聚合物等具有丙烯酸酯聚合物的丙烯酸系聚合物;热塑性降冰片烯系聚合物;聚碳酸酯系聚合物;聚对苯二甲酸乙二酯、聚萘二甲酸乙二醇酯等聚酯系聚合物;聚苯乙烯、丙烯腈-苯乙烯共聚物(as树脂)等苯乙烯系聚合物;聚乙烯、聚丙烯、乙烯-丙烯共聚物等聚烯烃系聚合物;氯乙烯系聚合物;尼龙、芳香族聚酰胺等酰胺系聚合物;酰亚胺系聚合物;砜系聚合物;聚醚砜系聚合物;聚醚醚酮系聚合物;聚苯硫醚系聚合物;偏二氯乙烯系聚合物;乙烯醇系聚合物;乙烯醇缩丁醛系聚合物;芳酯系聚合物;聚甲醛系聚合物;环氧系聚合物;或混合这些聚合物而成的聚合物。
并且,也可以是后述的起偏器兼作这种支撑体的方式。
本发明中,对于上述支撑体的厚度,并无特别限定,但是优选为5~60μm,更优选为5~30μm。
〔取向膜〕
本发明的光学膜具有上述的任意的支撑体时,优选在支撑体与光学各向异性膜之间具有取向膜。另外,也可以是上述的支撑体兼作取向膜的方式。
取向膜通常将聚合物作为主要成分。作为取向膜用聚合物材料,在多个文献中有记载,能够获得多个市售品。
优选本发明中所利用的聚合物材料为聚乙烯醇或聚酰亚胺及其衍生物。尤其优选改性或未改性的聚乙烯醇。
关于本发明中能够使用的取向膜,例如可举出国际公开第01/088574号的43页24行~49页8行中所记载的取向膜;日本专利第3907735号公报的[0071]至[0095]段中所记载的改性聚乙烯醇;日本特开2012-155308号公报中所记载的通过液晶取向剂形成的液晶取向膜等。
本发明中,从通过在形成取向膜时不与取向膜表面接触而能够防止面形态恶化的理由出发,还优选利用光取向膜来作为取向膜。
作为光取向膜,并无特别限定,但是能够使用国际公开第2005/096041号的[0024]至[0043]段中所记载的聚酰胺化合物、聚酰亚胺化合物等聚合物材料;日本特开2012-155308号公报中所记载的通过具有光取向性基团的液晶取向剂形成的液晶取向膜;rolictechnologies公司制造的商品名称lpp-jp265cp等。
并且,本发明中,上述取向膜的厚度,并无特别限定,但是从缓和能够存在于支撑体上的表面凹凸来形成膜厚均匀的光学各向异性膜的观点出发,优选为0.01~10μm,更优选为0.01~1μm,进一步优选为0.01~0.5μm。
〔硬涂层〕
为了赋予薄膜的物理强度,优选本发明的光学膜具有硬涂层。具体而言,可以在支撑体的与设置有取向膜的侧相反的一侧具有硬涂层(参考图1b),也可以在光学各向异性膜的与设置有取向膜的侧相反的一侧具有硬涂层(参考图1c)。
作为硬涂层,能够使用日本特开2009-098658号公报的[0190]至[0196]段中所记载的硬涂层。
〔其他光学各向异性膜〕
本发明的光学膜还可以具有与本发明的光学各向异性膜不同的其他光学各向异性膜。
即,本发明的光学膜可以具有本发明的光学各向异性膜与其他光学各向异性膜的层叠结构。
关于这种其他光学各向异性膜,只要为不配合上述的聚合性液晶化合物(i)及聚合性化合物(ii)中的任一个,而使用上述的其他聚合性化合物(尤其,液晶化合物)获得的光学各向异性膜,则并无特别限定。
在此,通常,液晶化合物能够根据其形状分为棒状类型和圆盘状类型。而且,分别具有低分子和高分子类型。高分子通常是指聚合度为100以上的高分子(高分子物理·相变动力学,土井正男著,第2页,岩波书店,1992)。本发明中,还能够使用任何液晶化合物,但是优选使用棒状液晶化合物或盘状液晶化合物(圆盘状液晶化合物)。还可以使用2种以上的棒状液晶化合物、2种以上的圆盘状液晶化合物、或棒状液晶化合物与圆盘状液晶化合物的混合物。为了上述液晶化合物的固定化,更优选使用具有聚合性基团的棒状液晶化合物或圆盘状液晶化合物来形成,进一步优选液晶化合物在1分子中具有2个以上的聚合性基团。在液晶化合物为2种以上的混合物的情况下,优选至少1种液晶化合物在1分子中具有2个以上的聚合性基团。
作为棒状液晶化合物,例如能够优选使用日本特表平11-513019号公报的方案1或日本特开2005-289980号公报的[0026]至[0098]段中所记载的化合物,作为盘状液晶化合物,例如能够优选使用日本特开2007-108732号公报的[0020]至[0067]段、日本特开2010-244038号公报的[0013]至[0108]段中所记载的化合物,但是并不限定于这些。
〔紫外线吸收剂〕
考虑外部光(尤其,紫外线)的影响,本发明的光学膜优选包含紫外线(uv)吸收剂。
紫外线吸收剂可以包含于本发明的光学各向异性膜中,也可以包含于构成本发明的光学膜的光学各向异性膜以外的部件中。作为除光学各向异性膜以外的部件,例如可优选举出支撑体。
作为紫外线吸收剂,能够使用能够显现紫外线吸收性的任何现有公知的紫外线吸收剂。这种紫外线吸收剂中,从获得紫外线吸收性高且图像显示装置中所使用的紫外线吸收能力(紫外线截止能力)的观点考虑,优选使用苯并三唑系或羟基苯基三嗪系紫外线吸收剂。
并且,为了扩大紫外线的吸收宽度,能够同时使用2种以上的极大吸收波长不同的紫外线吸收剂。
作为紫外线吸收剂,具体而言,例如可举出日本特开2012-018395公报的[0258]至[0259]段中所记载的化合物、日本特开2007-072163号公报的[0055]至[0105]段中所记载的化合物等。
并且,作为市售品,能够使用tinuvin400、tinuvin405、tinuvin460、tinuvin477、tinuvin479及tinuvin1577(均由basf公司制造)等。
[偏振片]
本发明的偏振片具有上述的本发明的光学膜和起偏器。
并且,在上述的本发明的光学各向异性膜为λ/4板(正a板)的情况下,本发明的偏振片能够用作圆偏振片。
并且,关于本发明的偏振片,在上述的本发明的光学各向异性膜为λ/4板(正a板)的情况下,λ/4板的慢轴与后述的起偏器的吸收轴所形成的角度优选为30~60°,更优选为40~50°,进一步优选为42~48°,尤其优选为45°。
在此,λ/4板的“慢轴”是指在λ/4板的面内折射率成为最大的方向,起偏器的“吸收轴”是指吸光度最高的方向。
〔起偏器〕
关于本发明的偏振片所具有的起偏器,只要为具有将光转换为特定的直线偏振光的功能的部件,则并无特别限定,能够利用以往公知的吸收型起偏器及反射型起偏器。
作为吸收型起偏器,可使用碘系起偏器、利用了二色性染料的染料系起偏器及多烯系起偏器等。在碘系起偏器及染料系起偏器中,具有涂布型起偏器和拉伸型起偏器,均能够应用,但是优选使碘或二色性染料吸附于聚乙烯醇上并进行拉伸而制作的起偏器。
并且,作为通过在基材上形成有聚乙烯醇层的层叠薄膜的状态下实施拉伸及染色而获得起偏器的方法,能够举出日本专利第5048120号公报、日本专利第5143918号公报、日本专利第4691205号公报、日本专利第4751481号公报、日本专利第4751486号公报,还能够优选利用与这些起偏器相关的公知的技术。
作为反射型起偏器,可使用层叠双折射不同的薄膜而得的起偏器、线栅型起偏器、组合具有选择性反射区域的胆甾醇液晶和1/4波长板而得的起偏器等。
其中,从密合性更加优异的观点出发,优选包含聚乙烯醇系树脂(包含-ch2-choh-来作为重复单元的聚合物。尤其,选自包含聚乙烯醇及乙烯-乙烯醇共聚物的组中的至少一个)的起偏器。
本发明中,起偏器的厚度并无特别限定,但是优选为3μm~60μm,更优选为5μm~30μm,进一步优选为5μm~15μm。
〔粘合剂层〕
本发明的偏振片可以在本发明的光学膜中的光学各向异性膜与起偏器之间配置有粘合剂层。
作为用于层叠光学各向异性膜和起偏器的层叠的粘合剂层,例如表示通过动态粘弹性测定装置测定的储能模量g’与损耗弹性模量g”之比(tanδ=g”/g’)为0.001~1.5的物质,包含所谓的粘合剂或容易蠕变的物质等。作为本发明中能够使用的粘合剂,例如可举出聚乙烯醇系粘合剂,但是并不限定于此。
[图像显示装置]
本发明的图像显示装置为具有本发明的光学膜或本发明的偏振片的图像显示装置。
本发明的图像显示装置中所使用的显示元件,并无特别限定,例如可举出液晶单元、有机电致发光(以下,简称为“el”。)显示面板、等离子显示面板等。
它们中,优选液晶单元、有机el显示面板,更优选液晶单元。即,作为本发明的图像显示装置,优选作为显示元件使用了液晶单元的液晶显示装置、作为显示元件使用了有机el显示面板的有机el显示装置,更优选液晶显示装置。
〔液晶显示装置〕
作为本发明的图像显示装置的一例的液晶显示装置为具有上述的本发明的偏振片和液晶单元的液晶显示装置。
另外,本发明中,在设置于液晶单元的两侧的偏振片中,优选使用本发明的偏振片来作为前侧的偏振片,更优选使用本发明的偏振片来作为前侧及后侧的偏振片。
以下,对构成液晶显示装置的液晶单元进行详细叙述。
<液晶单元>
液晶显示装置中所利用的液晶单元优选为va(verticalalignment:垂直取向)模式、ocb(opticallycompensatedbend:光学补偿弯曲)模式、ips(in-plane-switching:面内切换)模式、或tn(twistednematic:扭曲向列),但并不限定于这些。
tn模式的液晶单元中,在未施加电压时棒状液晶性分子实质上水平取向,进而扭曲取向为60~120°。tn模式的液晶单元最常用作色彩tft液晶显示装置,并在多个文献中有记载。
va模式的液晶单元中,在未施加电压时棒状液晶性分子实质上垂直取向。在va模式的液晶单元中,除了包含(1)在未施加电压时使棒状液晶性分子实质上垂直取向,在施加电压时使其实质上水平取向的狭义的va模式的液晶单元(日本特开平2-176625号公报中所记载)以外,还包含(2)为了扩大视角,对va模式进行了多域化的(mva模式的)液晶单元(sid97,digestoftech.papers(论文集)28(1997)845中所记载)、(3)在未施加电压时使棒状液晶性分子实质上垂直取向,在施加电压时使其扭曲多域取向的模式(n-asm模式)的液晶单元(日本液晶讨论会的论文集58~59(1998)中所记载)及(4)survival模式的液晶单元(lcdinternational98中发表)。并且,可以是pva(patternedverticalalignment:图像垂直调整)型、光取向型(opticalalignment:光学对准)及psa(polymer-sustainedalignment:聚合物稳定取向)中的任一种。关于这些模式的详细内容,在日本特开2006-215326号公报及日本特表2008-538819号公报中有详细的记载。
关于ips模式的液晶单元,棒状液晶分子相对于基板而实质上平行取向,且通过施加与基板面平行的电场而使液晶分子平面响应。关于ips模式,在未施加电场的状态下成为黑色显示,且上下一对偏振片的吸收轴正交。在日本特开平10-054982号公报、日本特开平11-202323号公报、日本特开平9-292522号公报、日本特开平11-133408号公报、日本特开平11-305217号公报、日本特开平10-307291号公报等中公开有使用光学补偿片来降低斜方向上的黑色显示时的漏光并改善视角的方法。
〔有机el显示装置〕
关于作为本发明的图像显示装置的一例的有机el显示装置,例如可优选举出从视觉辨认侧依次具有起偏器、包含本发明的光学各向异性膜的λ/4板(正a板)及有机el显示面板的方式。
并且,有机el显示面板为使用在电极间(阴极及阳极间)夹持有机发光层(有机电致发光层)而成的有机el元件构成的显示面板。有机el显示面板的构成并无特别限制,可采用公知的结构。
实施例
以下,基于实施例对本发明进行进一步详细说明。关于以下的实施例中所示的材料、用量、比例、处理内容、处理顺序等,只要不脱离本发明的主旨,则能够进行适当变更。因此,本发明的范围不应由以下所示的实施例限定性地进行解释。
〔羧酸化合物的合成〕
<羧酸化合物(viii-1)的合成>
[化学式5]
如上述方案所示,在室温(23℃)下混合化合物(viii-1a)10.0g(39.3mmol)、乙酸乙酯(ea)100ml、n,n-二甲基乙酰胺(dmac)18.2ml及2,6-二-叔丁基-4-甲基苯酚433mg,并将内部温度冷却至5℃。在混合物中滴加了亚硫酰氯(socl2)6.24ml(86.5mmol),以免内部温度上升至10℃以上。在5℃条件下搅拌1小时之后,加入了4-羟基丁基丙烯酸酯5.67g(39.3mmol)。滴加n,n-二异丙基乙胺(dipea)37.7ml(216mmol)之后,在室温下搅拌了2小时。搅拌之后,加入1n盐酸水100ml而停止反应,并进行了分液。利用10%食盐水清洗有机层之后,利用硫酸镁进行干燥,并在减压下蒸馏除去了溶剂。通过硅胶柱色谱法对所获得的粗产物进行纯化,而获得了羧酸化合物(viii-1)4.49g(11.8mmol)(产率为30%)。
<羧酸化合物(viii-2)的合成>
关于由下述式表示的羧酸化合物(viii-2)即日本特开2016-081035号公报的[0122]段中所记载的混合物(i-4c)的合成,通过日本特开2016-081035号公报的[0123]~[0125]段中所记载的方法进行了合成。
[化学式6]
<羧酸化合物(viii-3)的合成>
由下述式表示的羧酸化合物(viii-3)通过日本特开2016-081035号公报的[0109]段中所记载的方法来合成。
[化学式7]
<羧酸化合物(viii-4)的合成>
由下述式表示的羧酸化合物(viii-4)通过日本特开2010-031223号公报的[0392]段中所记载的方法来合成。
[化学式8]
<羧酸化合物(viii-5)的合成>
由下述式表示的羧酸化合物(viii-5)通过日本专利第4397550号公报的[0085]至[0087]段中所记载的方法来合成。
[化学式9]
<羧酸化合物(viii-6)的合成>
[化学式10]
如上述方案所示,将羧酸化合物(viii-1)的合成法中的4-羟基丁基丙烯酸酯变更为6-羟基己基丙烯酸酯,除此以外,通过与羧酸侧链(viii-1)相同的合成法,获得了羧酸化合物(viii-6)。
<羧酸化合物(viii-7)的合成>
[化学式11]
如上述方案所示,将羧酸化合物(viii-1)的合成法中的4-羟基丁基丙烯酸酯变更为5-羟基-3-甲基戊基丙烯酸酯,除此以外,通过与羧酸化合物(viii-1)相同的合成法,获得了羧酸化合物(viii-7)。
<羧酸化合物(viii-8)的合成>
[化学式12]
如上述方案所示,将羧酸化合物(viii-1)的合成法中的4-羟基丁基丙烯酸酯变更为2-羟基乙基丙烯酸酯,除此以外,通过与羧酸化合物(viii-1)相同的合成法,获得了羧酸化合物(viii-8)。
<羧酸化合物(viii-9)的合成>
关于由下述式表示的羧酸化合物(viii-9)的合成,通过日本特开2016-053149号公报的[0113]至[0115]段中所记载的方法来进行。
[化学式13]
〔酚化合物的合成〕
<酚化合物(x-1)的合成>
关于由下述式表示的酚化合物(x-1)的合成,通过“journalofchemicalcrystallography”(1997);27(9);p.515-526.中所记载的方法来进行。
[化学式14]
<酚化合物(x-2)的合成>
关于由下述式表示的酚化合物(x-2)的合成,通过日本特开2016-081035号公报的[0169]段(实施例15)中所记载的方法来进行。
[化学式15]
<酚化合物(x-3)的合成>
关于由下述式表示的酚化合物(x-3)的合成,按照日本特开2016-081035号公报的[0175]段(实施例17)中所记载的方法进行了合成。
[化学式16]
<酚化合物(x-4)的合成>
关于由下述式表示的酚化合物(x-4)的合成,通过日本特开2008-273925号公报的[0240]至[0244]段中所记载的方法来进行。
[化学式17]
<酚化合物(x-5)的合成>
关于由下述式表示的酚化合物(x-5)的合成,按照日本特开2011-207765号公报的[0463]段中所记载的方案进行了合成。
[化学式18]
[实施例1]
[化学式19]
如上述方案所示,在室温(23℃)下混合化合物(viii-1)3.42g(9.00mmol)、化合物(viii-2)0.50g(1.00mmol)、乙酸乙酯(ea)40ml、n,n-二甲基乙酰胺(dmac)5ml及2,6-二-叔丁基-4-甲基苯酚110mg,并将内部温度冷却至5℃。在混合物中滴加了亚硫酰氯(socl2)1.19g(10.0mmol),以免内部温度上升至10℃以上。在5℃条件下搅拌1小时之后,加入了化合物(x-1)1.13g(4.55mmol)的thf溶液(30ml)。滴加n,n-二异丙基乙胺(dipea)2.58g(20.0mmol)之后,在室温下搅拌了2小时。搅拌之后,加入1n盐酸水50ml而停止反应,并进行了分液。利用10%食盐水清洗有机层之后,利用硫酸镁进行干燥,并在减压下蒸馏除去了溶剂。在所获得的粗产物中添加甲醇,并对所析出的固体进行过滤,由此获得了3.5g的混合物1。
通过高速液相色谱法(highperformanceliquidchromatography:hplc)测定混合物1中的聚合性液晶化合物(p1-1)、聚合性液晶化合物(p2-1)、聚合性液晶化合物(p3-1)之比的结果,为(p1-1):(p2-1):(p3-1)=81:18:1。将该结果示于下述表3中。
[实施例2]
将化合物(viii-1):化合物(viii-2)的混合比变更为8:2,除此以外,通过与实施例1相同的方法获得了混合物2。
通过hplc测定混合物2中的聚合性液晶化合物(p1-1)、聚合性液晶化合物(p2-1)、聚合性液晶化合物(p3-1)之比的结果,为(p1-1):(p2-1):(p3-1)=64:32:4。
[实施例3]
将化合物(viii-1):化合物(viii-2)的混合比变更为7:3,除此以外,通过与实施例1相同的方法获得了混合物3。
通过hplc测定混合物3中的聚合性液晶化合物(p1-1)、聚合性液晶化合物(p2-1)、聚合性液晶化合物(p3-1)之比的结果,为(p1-1):(p2-1):(p3-1)=49:42:9。
[实施例4]
将化合物(viii-1):化合物(viii-2)的混合比变更为5:5,除此以外,通过与实施例1相同的方法获得了混合物4。
通过hplc测定混合物4中的聚合性液晶化合物(p1-1)、聚合性液晶化合物(p2-1)、聚合性液晶化合物(p3-1)之比的结果,为(p1-1):(p2-1):(p3-1)=25:50:25。
[实施例5]
[化学式20]
将化合物(viii-1):化合物(viii-2)的混合比变更为7:3,且将酚化合物(x-1)变更为酚化合物(x-4),除此以外,通过与实施例1相同的方法获得了混合物5。
通过hplc测定混合物5中的聚合性液晶化合物(p1-5)、聚合性液晶化合物(p2-5)、聚合性液晶化合物(p3-5)之比的结果,为(p1-5):(p2-5):(p3-5)=49:42:9。
[实施例6]
[化学式21]
将化合物(viii-1):化合物(viii-4)的混合比变更为7:3,且将酚化合物(x-1)变更为酚化合物(x-5),除此以外,通过与实施例1相同的方法获得了混合物6。
通过hplc测定混合物6中的聚合性液晶化合物(p1-6)、聚合性液晶化合物(p2-6)、聚合性液晶化合物(p3-6)之比的结果,为(p1-6):(p2-6):(p3-6)=49:42:9。
[实施例7]
[化学式22]
将化合物(viii-1):化合物(viii-4)的混合比变更为7:3,且将酚化合物(x-1)变更为2,5―二羟基苯甲醛,除此以外,通过与实施例1相同的方法获得了混合物7a。
[化学式23]
接着,如上述方案所示,在室温下混合混合物7a(5g)、thf50ml,并加入了浓盐酸0.93ml(0.48mmol)。经15分钟将通过日本专利第6055569号公报的[0304]至[0306]段中所记载的方法合成的化合物(x-6a)1.25g(5.0mmol)的thf10ml溶液滴加到该溶液中,滴加结束之后,进一步在室温下搅拌了1小时。反应结束之后,将反应液投入到甲醇800ml中,滤取所析出的固体,而获得了混合物7。
通过hplc测定混合物7中的聚合性液晶化合物(p1-7)、聚合性液晶化合物(p2-7)、聚合性液晶化合物(p3-7)之比的结果,为(p1-7):(p2-7):(p3-7)=49:42:9。
[实施例8]
[化学式24]
将化合物(viii-1):化合物(viii-4)的混合比变更为7:3,除此以外,通过与实施例1相同的方法获得了混合物8。
通过hplc测定混合物8中的聚合性液晶化合物(p1-8)、聚合性液晶化合物(p2-8)、聚合性液晶化合物(p3-8)之比的结果,为(p1-8):(p2-8):(p3-8)=49:42:9。
[实施例9]
[化学式25]
将化合物(viii-1):化合物(viii-5)的混合比变更为8:2,除此以外,通过与实施例1相同的方法获得了混合物9。
通过hplc测定混合物9中的聚合性液晶化合物(p1-9)、聚合性液晶化合物(p2-9)、聚合性液晶化合物(p3-9)之比的结果,为(p1-9):(p2-9):(p3-9)=64:32:4。
[实施例10]
[化学式26]
将化合物(viii-6):化合物(viii-1)的混合比变更为3:7,除此以外,通过与实施例1相同的方法获得了混合物10。
通过hplc测定混合物10中的聚合性液晶化合物(p1-10)、聚合性液晶化合物(p2-10)、聚合性液晶化合物(p3-10)之比的结果,为(p1-10):(p2-10):(p3-10)=9:42:49。
[实施例11]
[化学式27]
将化合物(viii-7):化合物(viii-1)的混合比变更为3:7,除此以外,通过与实施例1相同的方法获得了混合物11。
通过hplc测定混合物11中的聚合性液晶化合物(p1-11)、聚合性液晶化合物(p2-11)、聚合性液晶化合物(p3-11)之比的结果,为(p1-11):(p2-11):(p3-11)=9:42:49。
[实施例12]
[化学式28]
将化合物(viii-1):化合物(viii-2)的混合比变更为7:3,且将芯部变更为(x-2),除此以外,通过与实施例1相同的方法获得了混合物12。
通过hplc测定混合物12中的聚合性液晶化合物(p1-12)、聚合性液晶化合物(p2-12)、聚合性液晶化合物(p3-12)之比的结果,为(p1-12):(p2-12):(p3-12)=49:42:9。
[实施例13]
[化学式29]
将化合物(viii-1):化合物(viii-2)的混合比变更为8:2,且将芯部变更为(x-3),除此以外,通过与实施例1相同的方法获得了混合物13。
通过hplc测定混合物13中的聚合性液晶化合物(p1-13)、聚合性液晶化合物(p2-13)、聚合性液晶化合物(p3-13)之比的结果,为(p1-13):(p2-13):(p3-13)=64:32:4。
[实施例14]
[化学式30]
将化合物(viii-1):化合物(viii-9)的混合比变更为5:5,除此以外,通过与实施例1相同的方法获得了混合物14。
通过hplc测定混合物14中的聚合性液晶化合物(p1-14)、聚合性液晶化合物(p2-14)、聚合性液晶化合物(p3-14)之比的结果,为(p1-14):(p2-14):(p3-14)=25:50:25。
[实施例15]
[化学式31]
将化合物(viii-4):化合物(viii-9)的混合比变更为5:5,且将芯部变更为化合物(x-2),除此以外,通过与实施例1相同的方法获得了混合物15。
通过hplc测定混合物15中的聚合性液晶化合物(p1-15)、聚合性液晶化合物(p2-15)、聚合性液晶化合物(p3-15)之比的结果,为(p1-15):(p2-15):(p3-15)=25:50:25。
[实施例16]
[化学式32]
将化合物(viii-10):化合物(viii-2)的混合比变更为2:8,除此以外,通过与实施例1相同的方法获得了混合物16。
通过hplc测定混合物16中的聚合性液晶化合物(p1-16)、聚合性液晶化合物(p2-16)、聚合性液晶化合物(p3-16)之比的结果,为(p1-16):(p2-16):(p3-16)=4:32:64。
[实施例17]
[化学式33]
将化合物(viii-10):化合物(viii-4)的混合比变更为2:8,且将酚化合物(x-1)变更为酚化合物(x-5),除此以外,通过与实施例1相同的方法获得了混合物17。
通过hplc测定混合物17中的聚合性液晶化合物(p1-17)、聚合性液晶化合物(p2-17)、聚合性液晶化合物(p3-17)之比的结果,为(p1-17):(p2-17):(p3-17)=4:32:64。
[实施例18]
[化学式34]
将化合物(viii-10):化合物(viii-4)的混合比变更为2:8,除此以外,通过与实施例7相同的方法获得了混合物18。
通过hplc测定混合物18中的聚合性液晶化合物(p1-18)、聚合性液晶化合物(p2-18)、聚合性液晶化合物(p3-18)之比的结果,为(p1-18):(p2-18):(p3-18)=4:32:64。
[实施例19]
[化学式35]
将化合物(viii-4):化合物(viii-2)的混合比变更为7:3,且将芯部变更为化合物(x-5),除此以外,通过与实施例1相同的方法获得了混合物19。
通过hplc测定混合物19中的聚合性液晶化合物(p1-19)、聚合性液晶化合物(p2-19)、聚合性液晶化合物(p3-19)之比的结果,为(p1-19):(p2-19):(p3-19)=49:42:9。
[实施例20]
[化学式36]
将化合物(viii-4):化合物(viii-2)的混合比变更为7:3,除此以外,通过与实施例7相同的方法获得了混合物20。
通过hplc测定混合物20中的聚合性液晶化合物(p1-20)、聚合性液晶化合物(p2-20)、聚合性液晶化合物(p3-20)之比的结果,为(p1-20):(p2-20):(p3-20)=49:42:9。
[实施例21]
[化学式37]
将化合物(viii-4):化合物(viii-2)的混合比变更为7:3,除此以外,通过与实施例1相同的方法获得了混合物21。
通过hplc测定混合物21中的聚合性液晶化合物(p1-21)、聚合性液晶化合物(p2-21)、聚合性液晶化合物(p3-21)之比的结果,为(p1-21):(p2-21):(p3-21)=49:42:9。
[实施例22]
将化合物(viii-1):化合物(viii-2)的混合比变更为9.5:0.5,除此以外,通过与实施例1相同的方法获得了混合物22。
通过hplc测定混合物22中的聚合性液晶化合物(p1-1)、聚合性液晶化合物(p2-1)、聚合性液晶化合物(p3-1)之比的结果,为(p1-1):(p2-1):(p3-1)=90:9:1。
[比较例1]
通过日本特开2010-084032号公报的[0161]~[0163]段中所记载的方法,合成了下述式中的n为1的化合物c。
[化学式38]
[比较例2]
按照日本特开2011-207765号公报的[0463]段中所记载的方案,合成了由下述式表示的聚合性液晶化合物。
[化学式39]
[比较例3]
通过日本特开2016-081035号公报的[0122]段(实施例4)中所记载的方法,合成了由下述式表示的聚合性液晶化合物。
[化学式40]
〔溶解性〕
通过以下所示的方法进行了在实施例1~实施例21中制备的混合物(聚合性液晶组合物)及在比较例1~比较例3中合成的聚合性液晶化合物的溶解性测定。将结果示于下述表3及表4中。
具体而言,向1.5ml的样品瓶中称取50mg化合物,直至固体成分成为40wt%为止加入溶剂(75mg)。
在50℃的条件下利用手充分摇晃并混合,并在室温(23℃)下放置10分钟之后,通过肉眼观察,若为纯净的,则结束,判定了溶解性为40wt%。若存在溶解残留物,则以固体成分成为35wt%的方式加入了溶剂(+18mg)。在50℃的条件下利用手充分摇晃并混合,并在室温(23℃)下放置10分钟之后,通过肉眼观察,若为纯净的,则结束,判定为35wt%。若存在溶解残留物,则以成为30wt%的方式加入了溶剂。以每5wt%进行相同的操作,反复进行至成为5wt%,在存在溶解残留物的情况下,判定溶解性小于5wt%(<5wt%),并结束了操作。作为溶解性测定的溶剂,使用了mek(甲乙酮)、cpn(环戊酮)。
a:对mek或cpn的溶解性为30%以上
b:对mek或cpn的溶解性为15%以上且小于30%
c:对mek或cpn的溶解性小于15%
〔表面形态〕
制备具有下述组成的聚合性组合物(光学各向异性膜用涂布液),并通过旋涂法涂布于带有经摩擦处理的聚酰亚胺取向膜(nissanchemicalindustries,ltd.制造的se-150)的玻璃基板上。在140℃条件下对涂膜进行取向处理,形成了液晶层。然后,冷却至60℃并进行基于1000mj/cm2的紫外线照射的取向固定化,形成光学各向异性膜,而获得了波长分散测定用光学膜。
[化学式41]
对于所制作的光学膜,通过光学显微镜及肉眼观察确认表面形态,并根据以下基准进行了评价。将结果示于下述表3及表4中。
a:未观察到亮点、条纹状缺陷
b:局部观察到亮点、条纹状缺陷
c:亮点、条纹状缺陷多
〔耐久性〕
关于耐久性的试验条件,进行了在100℃、相对湿度95%的环境下放置144小时的试验。将结果示于下述表3及表4中。
a:试验后的re(550)相对于初始相位差值的变化量小于初始值的15%
b:试验后的re(550)相对于初始相位差值的变化量为初始值的15%以上且小于30%
c:试验后的re(550)相对于初始相位差值的变化量为初始值的30%以上且小于45%
d:试验后的re(550)相对于初始相位差值的变化量为初始值的45%以上
〔波长分散〕
关于所制作的光学膜,利用自动双折射仪(kobra-21adh,ojiscientificinstruments制造),测定波长为450nm的延迟值(re(450))和波长为550nm的延迟值(re(550)),并计算了re(450)/re(550)。将结果示于下述表3及表4中。
a:re(450)/re(550)小于0.67
b:re(450)/re(550)为0.67以上且小于0.8
c:re(450)/re(550)为0.8以上
[表3]
[表4]
由表3及表4中所示的结果发现:在仅配合1种对应于聚合性液晶化合物p1或聚合性液晶化合物p3的聚合性液晶化合物的情况下,溶解性差或所形成的光学各向异性膜的耐久性差(比较例1~比较例3)。
相对于此,发现:在均配合聚合性液晶化合物p1~p3的情况下,溶解性良好,所形成的光学各向异性膜的耐久性也优异(实施例1~实施例22)。
符号说明
10-光学膜,12-光学各向异性膜,14-取向膜,16-支撑体,18-硬涂层。
- 还没有人留言评论。精彩留言会获得点赞!