一种N,N-二烷基酰胺羧酸类化合物的应用及方法与流程
一种n,n
‑
二烷基酰胺羧酸类化合物的应用及方法
技术领域
1.本发明涉及金属分离和提纯领域,具体涉及一种n,n
‑
二烷基酰胺羧酸类化合物的应用及方法。
背景技术:
2.目前,从稀土料液中萃取去除铝和铁的主要方法是环烷酸萃取法。
3.如cn101979680a公开了一种从稀土料液中除铝的方法,属于稀土料液处理技术,旨在提供一种除铝效果好,除铝成本低,稀土回收率高,操作控制方便,工序简单,设备投资少的稀土料液除铝方法,其技术方案的要点包括下述步骤:(1)按体积比为15~25%环烷酸—15~25%醇—煤油配制有机相;(2)将上述配制好的有机相与稀土料液按体积比2~5∶1加入至搅拌槽中,开启搅拌,混合均匀;(3)在搅拌条件下,向步骤(2)所得的混合液中加入碱性溶液,加入的碱摩尔总数为稀土料液中稀土元素摩尔总数的50~100%;(4)加碱完毕后继续搅拌一段时间,然后停止搅拌,静置一段时间,溶液分离为水相和有机相,水相即为除铝后的稀土料液。
4.同时cn105200249a还公开了一种高稳定的环烷酸萃取分离高纯钇的方法,该方法在环烷酸萃取分离高纯钇过程中油水相比较大或者发生严重波动时依然可以保证混合室有合适的相比以保证混合室处于发粘状态,而使混合相在澄清室快速澄清分相。采用简单的操作步骤便能快速稳定的调节环烷酸萃取分离高纯钇槽体混合室的相比,重新快速构建混合室发粘体系,保证澄清室正常分相,其操作简单、稳定性好,降低了对操作工的技术要求,利于企业稳定生产。
5.虽然现有技术中通过采用各种手段对环烷酸萃取分离体系进行优化,然而现有的环烷酸萃取分离中仍存在除铝效果差,萃取过程中有机相容易乳化等问题。
技术实现要素:
6.鉴于现有技术中存在的问题,本发明的目的在于提供一种n,n
‑
二烷基酰胺羧酸类化合物的应用及方法,通过采用n,n
‑
二烷基酰胺羧酸类化合物作为萃取剂分离稀土溶液中铁和/或铝,对溶液中的铝和铁具有良好的去除效果,萃取过程有机相没有乳化现象发生。
7.为达此目的,本发明采用以下技术方案:
8.第一方面,本发明提供了一种n,n
‑
二烷基酰胺羧酸类化合物的应用,所述应用为用于萃取稀土溶液中的铁元素和/或铝元素。
9.所述n,n
‑
二烷基酰胺羧酸类化合物具有如下所示的结构:
[0010][0011]
式中,r1和r2分别为独立的c1
‑
c9烷基,n为1
‑
6的自然数。
[0012]
本发明中,通过采用n,n
‑
二烷基酰胺羧酸类化合物作为稀土溶液中铁和/或铝元素的萃取剂,对溶液中的铝和铁具有良好的去除效果。
[0013]
本发明中,所述r1和r2分别为独立的c1
‑
c9烷基,例如可以是甲基,乙基,丙基,异丙基,正丁基,异丁基,仲丁基,叔丁基,正戊基,正己基,正庚基,正辛基,环丙基,环丁基,环戊基或环己基等,可以均为链状烷基(可以相同或不同),或均为环烷基(可以相同或不同),或是链状烷基和环烷基的组合(碳原子数可以相同或不同),如r1和r2分别为乙基和乙基,如r1和r2分别为乙基和甲基,如r1和r2分别为丙基和乙基,如r1和r2分别为正丁基和丙基,如r1和r2分别为叔丁基和叔丁基,如r1和r2分别为丙基和环丙基,如r1和r2分别为乙基和环丁基,如r1和r2分别为环丙基和环丁基,但不限于所列举的的烷基,该范围内其他未列举的组合同样适用。
[0014]
本发明中,式i中的n可以是1、2、3、4、5或6等,但不限于所列举的数值,该范围内其他未列举的组合同样适用。
[0015]
本发明中,所述n,n
‑
二烷基酰胺羧酸类化合物可采用常规现有合成方法进行合成。
[0016]
作为本发明优选的技术方案,所述n,n
‑
二烷基酰胺羧酸类化合物结构式中n为2或3。
[0017]
作为本发明优选的技术方案,所述n,n
‑
二烷基酰胺羧酸类化合物结构式中r1和r2分别为独立的c2
‑
c8烷基。
[0018]
第二方面,本发明提供了一种从稀土溶液中萃取铁和/或铝的方法,所述方法包括如下步骤:
[0019]
将含如第一方面所述n,n
‑
二烷基酰胺羧酸类化合物的稀释液和含铝和/或铁的稀土溶液混合,之后加入碱液进行萃取。
[0020]
本发明提供的萃取溶液中铝和/或铁的方法中,通过采用n,n
‑
二烷基酰胺羧酸类化合物作为萃取剂,并且在将水相和有机相混合后加入碱液相配合,避免了萃取溶液中铝和/或铁的过程中出现有机相乳化的问题。
[0021]
作为本发明优选的技术方案,所述稀释液中的稀释剂包括正己烷、正庚烷、甲苯、260#溶剂煤油或航空煤油中的1种或至少2种的组合。
[0022]
作为本发明优选的技术方案,所述稀释液中n,n
‑
二烷基酰胺羧酸类化合物和稀释剂的体积比为(1
‑
50):(50
‑
99),例如可以是1:50、1:60、1:70、1:80、1:90、1:10、1:12、1:14、1:16、1:18、1:5、1:6、1:7、1:8、1:9、2:5、1:3、2:7、1:4、2:9、3:5、1:2、3:7、3:8、4:5、2:3、4:7、4:9、1:1、5:6、5:7、5:8或5:9等,但不限于所列举的数值,该范围内其他未列举的组合同样适用。
[0023]
作为本发明优选的技术方案,所述稀土溶液中稀土元素的总浓度为0.1
‑
2mol/l,例如可以是0.1mol/l、0.2mol/l、0.3mol/l、0.4mol/l、0.5mol/l、0.6mol/l、0.7mol/l、0.8mol/l、0.9mol/l、1mol/l、1.1mol/l、1.2mol/l、1.3mol/l、1.4mol/l、1.5mol/l、1.6mol/l、1.7mol/l、1.8mol/l、1.9mol/l或2mol/l等,但不限于所列举的数值,该范围内其他未列举的组合同样适用。
[0024]
优选地,所述稀土溶液中铝元素的浓度以氧化铝计为0.1
‑
10g/l,例如可以是0.1g/l、0.2g/l、0.3g/l、0.4g/l、0.5g/l、0.6g/l、0.7g/l、0.8g/l、0.9g/l、1g/l、1.5g/l、
2g/l、2.5g/l、3g/l、3.5g/l、4g/l、4.5g/l、5g/l、5.5g/l、6g/l、6.5g/l、7g/l、7.5g/l、8g/l、8.5g/l、9g/l、9.5g/l或10g/l等,但不限于所列举的数值,该范围内其他未列举的组合同样适用。
[0025]
优选地,所述稀土溶液中铁元素的浓度以氧化铁计为0.01
‑
2g/l,例如可以是0.01g/l、0.02g/l、0.03g/l、0.04g/l、0.05g/l、0.06g/l、0.07g/l、0.08g/l、0.09g/l、0.1g/l、0.2g/l、0.3g/l、0.4g/l、0.5g/l、0.6g/l、0.7g/l、0.8g/l、0.9g/l、1g/l、1.1g/l、1.2g/l、1.3g/l、1.4g/l、1.5g/l、1.6g/l、1.7g/l、1.8g/l、1.9g/l或2g/l等,但不限于所列举的数值,该范围内其他未列举的组合同样适用。
[0026]
作为本发明优选的技术方案,所述碱液包括氨水、氢氧化钠溶液、氢氧化钾溶液、碳酸钠溶液或碳酸钾溶液中的1种或至少2种的组合。
[0027]
优选地,所述碱液的浓度为0.5
‑
10mol/l,例如可以是0.5mol/l、0.6mol/l、0.7mol/l、0.8mol/l、0.9mol/l、1mol/l、1.5mol/l、2mol/l、2.5mol/l、3mol/l、3.5mol/l、4mol/l、4.5mol/l、5mol/l、5.5mol/l、6mol/l、6.5mol/l、7mol/l、7.5mol/l、8mol/l、8.5mol/l、9mol/l、9.5mol/l或10mol/l等,但不限于所列举的数值,该范围内其他未列举的组合同样适用。
[0028]
优选地,所述碱液的添加量为所述稀土溶液体积的1
‑
20%,例如可以是1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、11%、12%、13%、14%、15%、16%、17%、18%、19%或20%等,但不限于所列举的数值,该范围内其他未列举的组合同样适用。
[0029]
优选地,所述萃取中水相和有机相的体积比为(0.1
‑
10):1,例如可以是0.1:1、0.2:1、0.3:1、0.4:1、0.5:1、0.6:1、0.7:1、0.8:1、0.9:1、1:1、1.5:1、2:1、2.5:1、3:1、3.5:1、4:1、4.5:1、5:1、5.5:1、6:1、6.5:1、7:1、7.5:1、8:1、8.5:1、9:1、9.5:1或10:1等,但不限于所列举的数值,该范围内其他未列举的组合同样适用。
[0030]
作为本发明优选的技术方案,所述萃取结束后采用无机酸对负载有机相进行反萃。
[0031]
优选地,所述无机酸包括盐酸、硝酸或硫酸中的1种或至少2种的组合。
[0032]
优选地,所述无机酸的浓度为0.5
‑
10mol/l,例如可以是0.5mol/l、0.6mol/l、0.7mol/l、0.8mol/l、0.9mol/l、1mol/l、1.5mol/l、2mol/l、2.5mol/l、3mol/l、3.5mol/l、4mol/l、4.5mol/l、5mol/l、5.5mol/l、6mol/l、6.5mol/l、7mol/l、7.5mol/l、8mol/l、8.5mol/l、9mol/l、9.5mol/l或10mol/l等,但不限于所列举的数值,该范围内其他未列举的组合同样适用。
[0033]
优选地,所述反萃后得到的有机相返回萃取过程,水相为富含铝和/或铁的溶液。
[0034]
作为本发明优选的技术方案,所述方法包括如下步骤:
[0035]
将含如第一方面所述n,n
‑
二烷基酰胺羧酸类化合物的稀释液和含铝和/或铁的稀土溶液混合,之后加入碱液进行萃取;
[0036]
所述稀释液中的稀释剂包括正己烷、正庚烷、甲苯、260#溶剂煤油或航空煤油中的1种或至少2种的组合;所述稀释液中n,n
‑
二烷基酰胺羧酸类化合物和稀释剂的体积比为(1
‑
50):(50
‑
99);所述稀土溶液中稀土元素的总浓度为0.1
‑
2mol/l;所述稀土溶液中铝元素的浓度以氧化铝计为0.1
‑
10g/l;所述稀土溶液中铁元素的浓度以氧化铁计为0.01
‑
2g/l;所述碱液包括氨水、氢氧化钠溶液、氢氧化钾溶液、碳酸钠溶液或碳酸钾溶液中的1种或
至少2种的组合;所述碱液的浓度为0.5
‑
10mol/l;所述碱液的添加量为所述稀土溶液体积的1
‑
20%;所述萃取中水相和有机相的体积比为(0.1
‑
10):1。
[0037]
与现有技术方案相比,本发明至少具有以下有益效果:
[0038]
(1)n,n
‑
二烷基酰胺羧酸萃取剂的合成所需的化工原料来源广泛,合成简单,成本低廉。
[0039]
(2)n,n
‑
二烷基酰胺羧酸萃取剂对杂质铝和铁离子具有很高的选择性,铝、铁与稀土的分离系数高,铝和铁的去除率较高。
[0040]
(3)萃取剂在使用后,用无机酸使其再生,即可循环使用。
具体实施方式
[0041]
为更好地说明本发明,便于理解本发明的技术方案,本发明的典型但非限制性的实施例如下:
[0042]
实施例1
[0043]
本实施例提供的萃取剂为n,n
‑
二乙基酰胺丁酸,即r1和r2为乙基,n=2,结构式如下:
[0044][0045]
采用下述过程进行溶液中铁和铝的分离:
[0046]
(1)配制有机相。将20ml n,n
‑
二乙基酰胺丁酸萃取剂与80ml甲苯稀释剂混合,组成100ml有机相。萃取剂与稀释剂体积比为1:4。
[0047]
(2)萃取过程:取含有铝和铁元素的稀土溶液100ml,与所述有机相混合,缓慢加入6.0mol/l氢氧化钠溶液,进行萃取。萃取时间30分钟。稀土料液与液碱的体积比为25:4。稀土元素的总浓度为1.85mol/l,铝元素的浓度为4.025g/l(以al2o3计算),铁元素的浓度为0.45g/l(以fe2o3计算)。稀土溶液与所述有机相的体积比为1:1。铝和铁元素被萃取到有机相中,形成负载有机相,而稀土仍然留在溶液中;
[0048]
(3)反萃取过程:取4.0mol/l的盐酸25ml,对负载有机相进行反萃取,使铝和铁元素进入无机酸溶液中。铝和铁元素与稀土元素得到有效分离。反萃取时间5分钟,使萃取剂再生。
[0049]
经过测定,萃取前后水相中铝浓度和铁浓度的变化详见表1。
[0050]
实施例2
[0051]
萃取剂采用n,n
‑
二正辛基酰胺丁酸,即r1和r2为正辛基,n=2,结构式如下:
[0052][0053]
采用下述过程进行溶液中铁和铝的分离:
[0054]
(1)配制有机相。将50ml n,n
‑
二正辛基酰胺丁酸萃取剂与50ml航空煤油稀释剂混合,组成100ml有机相。萃取剂与稀释剂体积比为1:1。
[0055]
(2)萃取过程:取含有铝和铁元素的稀土溶液10ml,与所述有机相混合,缓慢加入0.5mol/l氢氧化钠溶液,进行萃取。萃取时间30分钟。稀土料液与液碱的体积比为5:1。稀土元素的总浓度为0.3mol/l,铝元素的浓度为4.025g/l(以al2o3计算),铁元素的浓度为0.45g/l(以fe2o3计算)。稀土溶液与所述有机相的体积比为0.1:1。铝和铁元素被萃取到有机相中,形成负载有机相,而稀土仍然留在溶液中;
[0056]
(3)反萃取过程:取4mol/l的盐酸25ml,对负载有机相进行反萃取,使铝和铁元素进入无机酸溶液中。铝和铁元素与稀土元素得到有效分离。反萃取时间5分钟,使萃取剂再生。
[0057]
经过测定,萃取前后水相中铝浓度和铁浓度的变化详见表1。
[0058]
实施例3
[0059]
萃取剂采用n,n
‑
二环戊基酰胺丁酸,即r1和r2为均为环戊基,n=2,结构式如下,萃取剂的来源为自制,纯度和收率均大于98%。
[0060][0061]
采用下述过程进行溶液中铁和铝的分离:
[0062]
(1)配制有机相。将1ml萃取剂与9ml甲苯稀释剂混合,组成10ml有机相。萃取剂与稀释剂体积比为1:9。
[0063]
(2)萃取过程:取含有铝和铁元素的稀土溶液100ml,与所述有机相混合,缓慢加入8mol/l氢氧化钠溶液,进行萃取。萃取时间30分钟。稀土料液与液碱的体积比为10:1。稀土元素的总浓度为2mol/l,铝元素的浓度为4.025g/l(以al2o3计算),铁元素的浓度为0.45g/l(以fe2o3计算)。稀土溶液与所述有机相的体积比为10:1。铝和铁元素被萃取到有机相中,形成负载有机相,而稀土仍然留在溶液中;
[0064]
(3)反萃取过程:取4mol/l的盐酸25ml,对负载有机相进行反萃取,使铝和铁元素进入无机酸溶液中。铝和铁元素与稀土元素得到有效分离。反萃取时间5分钟,使萃取剂再生。
[0065]
经过测定,萃取前后水相中铝浓度和铁浓度的变化详见表1。
[0066]
实施例4
[0067]
萃取剂中r1为正丁基,r2为乙基,n=3,结构式如下,萃取剂的来源为自制,纯度和收率均大于98%。
[0068][0069]
采用下述过程进行溶液中铁和铝的分离:
[0070]
(1)配制有机相。将30ml萃取剂与70ml甲苯稀释剂混合,组成100ml有机相。萃取剂与稀释剂体积比为3:7。
[0071]
(2)萃取过程:取含有铝和铁元素的稀土溶液100ml,与所述有机相混合,缓慢加入2mol/l氢氧化钠溶液,进行萃取。萃取时间30分钟。稀土料液与液碱的体积比为20:1。稀土元素的总浓度为1.5mol/l,铝元素的浓度为4.025g/l(以al2o3计算),铁元素的浓度为0.45g/l(以fe2o3计算)。稀土溶液与所述有机相的体积比为1:1。铝和铁元素被萃取到有机相中,形成负载有机相,而稀土仍然留在溶液中;
[0072]
(3)反萃取过程:取10mol/l的盐酸10ml,对负载有机相进行反萃取,使铝和铁元素进入无机酸溶液中。铝和铁元素与稀土元素得到有效分离。反萃取时间5分钟,使萃取剂再生。
[0073]
经过测定,萃取前后水相中铝浓度和铁浓度的变化详见表1。
[0074]
实施例5
[0075]
萃取剂中r1为异丙基,r2为正丁基,n=4,结构式如下,萃取剂的来源为自制,纯度和收率均大于98%。
[0076][0077]
采用下述过程进行溶液中铁和铝的分离:
[0078]
(1)配制有机相。将20ml萃取剂与80ml甲苯稀释剂混合,组成100ml有机相。萃取剂与稀释剂体积比为1:4。
[0079]
(2)萃取过程:取含有铝和铁元素的稀土溶液500ml,与所述有机相混合,缓慢加入1mol/l氢氧化钠溶液,进行萃取。萃取时间30分钟。稀土料液与液碱的体积比为25:4。稀土元素的总浓度为1.85mol/l,铝元素的浓度为4.025g/l(以al2o3计算),铁元素的浓度为0.45g/l(以fe2o3计算)。稀土溶液与所述有机相的体积比为5:1。铝和铁元素被萃取到有机相中,形成负载有机相,而稀土仍然留在溶液中;
[0080]
(3)反萃取过程:取6mol/l的盐酸15ml,对负载有机相进行反萃取,使铝和铁元素进入无机酸溶液中。铝和铁元素与稀土元素得到有效分离。反萃取时间5分钟,使萃取剂再生。
[0081]
经过测定,萃取前后水相中铝浓度和铁浓度的变化详见表1。
[0082]
实施例6
[0083]
萃取剂中r1为叔丁基,r2为正戊基,n=5,结构式如下,萃取剂的来源为自制,纯度和收率均大于98%。
[0084][0085]
采用下述过程进行溶液中铁和铝的分离:
[0086]
(1)配制有机相。将20ml萃取剂与80ml甲苯稀释剂混合,组成100ml有机相。萃取剂与稀释剂体积比为1:4。
[0087]
(2)萃取过程:取含有铝和铁元素的稀土溶液100ml,与所述有机相混合,缓慢加入3mol/l氢氧化钠溶液,进行萃取。萃取时间30分钟。稀土料液与液碱的体积比为25:4。稀土元素的总浓度为1.85mol/l,铝元素的浓度为4.025g/l(以al2o3计算),铁元素的浓度为0.45g/l(以fe2o3计算)。稀土溶液与所述有机相的体积比为1:1。铝和铁元素被萃取到有机相中,形成负载有机相,而稀土仍然留在溶液中;
[0088]
(3)反萃取过程:取5mol/l的盐酸20ml,对负载有机相进行反萃取,使铝和铁元素进入无机酸溶液中。铝和铁元素与稀土元素得到有效分离。反萃取时间5分钟,使萃取剂再生。
[0089]
经过测定,萃取前后水相中铝浓度和铁浓度的变化详见表1。
[0090]
实施例7
[0091]
萃取剂中r1为叔丁基,r2为异丙基,n=2,结构式如下,萃取剂的来源为自制,纯度和收率均大于98%。
[0092][0093]
采用下述过程进行溶液中铁和铝的分离:
[0094]
(1)配制有机相。将20ml萃取剂与80ml甲苯稀释剂混合,组成100ml有机相。萃取剂与稀释剂体积比为1:4。
[0095]
(2)萃取过程:取含有铝和铁元素的稀土溶液20ml,与所述有机相混合,缓慢加入6mol/l氢氧化钠溶液,进行萃取。萃取时间30分钟。稀土料液与液碱的体积比为25:4。稀土元素的总浓度为1.85mol/l,铝元素的浓度为4.025g/l(以al2o3计算),铁元素的浓度为0.45g/l(以fe2o3计算)。稀土溶液与所述有机相的体积比为0.2:1。铝和铁元素被萃取到有机相中,形成负载有机相,而稀土仍然留在溶液中;
[0096]
(3)反萃取过程:取4mol/l的盐酸25ml,对负载有机相进行反萃取,使铝和铁元素进入无机酸溶液中。铝和铁元素与稀土元素得到有效分离。反萃取时间5分钟,使萃取剂再
生。
[0097]
经过测定,萃取前后水相中铝浓度和铁浓度的变化详见表1。
[0098]
实施例8
[0099]
萃取剂中r1为叔丁基,r2为异己基,n=2,结构式如下,萃取剂的来源为自制,纯度和收率均大于98%。
[0100][0101]
采用下述过程进行溶液中铁和铝的分离:
[0102]
(1)配制有机相。将20ml萃取剂与80ml甲苯稀释剂混合,组成100ml有机相。萃取剂与稀释剂体积比为1:4。
[0103]
(2)萃取过程:取含有铝和铁元素的稀土溶液100ml,与所述有机相混合,缓慢加入6mol/l氢氧化钠溶液,进行萃取。萃取时间30分钟。稀土料液与液碱的体积比为25:4。稀土元素的总浓度为1.85mol/l,铝元素的浓度为4.025g/l(以al2o3计算),铁元素的浓度为0.45g/l(以fe2o3计算)。稀土溶液与所述有机相的体积比为1:1。铝和铁元素被萃取到有机相中,形成负载有机相,而稀土仍然留在溶液中;
[0104]
(3)反萃取过程:取6mol/l的盐酸15ml,对负载有机相进行反萃取,使铝和铁元素进入无机酸溶液中。铝和铁元素与稀土元素得到有效分离。反萃取时间5分钟,使萃取剂再生。
[0105]
经过测定,萃取前后水相中铝浓度和铁浓度的变化详见表1。
[0106]
实施例9
[0107]
萃取剂中r1为乙基,r2为异戊基,n=2,结构式如下,萃取剂的来源为自制,纯度和收率均大于98%。
[0108][0109]
采用下述过程进行溶液中铁和铝的分离:
[0110]
(1)配制有机相。将20ml萃取剂与80ml甲苯稀释剂混合,组成100ml有机相。萃取剂与稀释剂体积比为1:4。
[0111]
(2)萃取过程:取含有铝和铁元素的稀土溶液100ml,与所述有机相混合,缓慢加入6mol/l氢氧化钠溶液,进行萃取。萃取时间30分钟。稀土料液与液碱的体积比为25:4。稀土元素的总浓度为1.85mol/l,铝元素的浓度为4.025g/l(以al2o3计算),铁元素的浓度为0.45g/l(以fe2o3计算)。稀土溶液与所述有机相的体积比为1:1。铝和铁元素被萃取到有机
相中,形成负载有机相,而稀土仍然留在溶液中;
[0112]
(3)反萃取过程:取5mol/l的盐酸20ml,对负载有机相进行反萃取,使铝和铁元素进入无机酸溶液中。铝和铁元素与稀土元素得到有效分离。反萃取时间5分钟,使萃取剂再生。
[0113]
经过测定,萃取前后水相中铝浓度和铁浓度的变化详见表1。
[0114]
对比例1
[0115]
萃取剂采用环烷酸。其它条件同实施例1。
[0116]
经过测定,萃取前后水相中铝浓度和铁浓度的变化详见表1。
[0117]
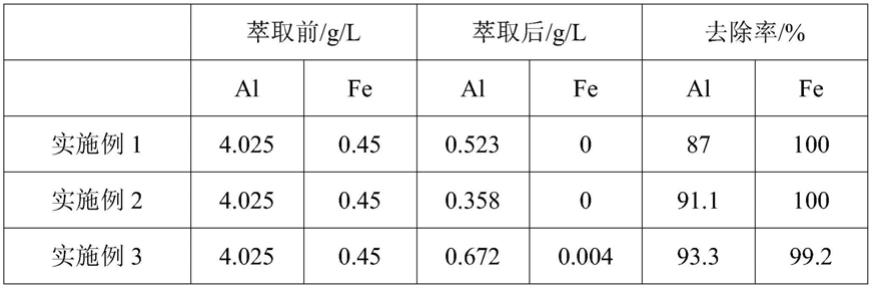
表1
[0118][0119][0120]
通过上述实施例和对比例的结果可知,通过采用n,n
‑
二烷基酰胺羧酸类化合物作为萃取剂分离稀土溶液中铁和/或铝,对溶液中的铝和铁的去除率分别可达84%以上和99.2%以上,萃取过程有机相没有乳化现象发生。
[0121]
申请人声明,本发明通过上述实施例来说明本发明的详细结构特征,但本发明并不局限于上述详细结构特征,即不意味着本发明必须依赖上述详细结构特征才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明所选用部件的等效替换以及辅助部件的增加、具体方式的选择等,均落在本发明的保护范围和公开范围之内。
[0122]
以上详细描述了本发明的优选实施方式,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,这些简单变型均属于本发明的保护范围。
[0123]
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛
盾的情况下,可以通过任何合适的方式进行组合,为了避免不必要的重复,本发明对各种可能的组合方式不再另行说明。
[0124]
此外,本发明的各种不同的实施方式之间也可以进行任意组合,只要其不违背本发明的思想,其同样应当视为本发明所公开的内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1