一种基于电渗析原理的卤水或海水提锂方法及装置
1.本发明属于材料科学及化学工程技术领域,具体涉及一种基于电渗析原理的应用锂离子固态电解质的卤水或海水提锂方法及装置。
背景技术:
2.锂离子电池相较其他电化学体系,具有高能量密度、长循环寿命等优点,是目前电化学储能装置的优选,但受限于li2co3、lioh等原料价格较贵,正极活性材料及电芯成本较高。随着储能市场及电动汽车市场持续增长,锂资源需求量将远超现有市场水平的供给量,将进一步抬高电池成本,影响锂离子电池产业的良性发展。
3.全球陆地锂资源中,70%左右蕴含在盐湖及地下卤水中,剩余的锂资源主要存在于伟晶岩矿石中。矿石中锂资源储量少且提锂成本高,因此,盐湖卤水提锂是锂产出的主要方式。此外,海水中蕴含大量锂资源,远超陆地锂资源储量,是锂资源供应的潜在原料。但卤水、海水中含有大量与li
+
性质相似的mg
2+
,需要进行mg
2+
、li
+
分离后方可提锂。目前,我国盐湖卤水提锂(mg
2+
、 li
+
分离)技术主要有沉淀法、纳滤膜分离、电渗析分离、萃取法、离子交换法和电化学脱嵌法等。沉淀法适用于低mg/li比的卤水,难以直接应用于我国大部分高mg/li比的盐湖;纳滤膜分离和电渗析分离需要昂贵的离子交换膜;萃取法和离子交换法中萃取剂和离子交换树脂的寿命较短,增加了生产成本;电化学脱嵌法需要较长时间提锂,效率较低。因此,需要开发低成本、快速的盐湖卤水提锂方法,以满足市场对li2co3、lioh快速增长的需求。
4.锂离子固态电解质是一类具备迅速导锂能力的固体含锂化合物,对li
+
具有优先选择透过性,可实现mg
2+
、li
+
分离。尽管已有应用固态电解质进行盐湖提锂的工作(cn 109097791 b等),但该方法需要对装置施加高电压,同时体系内发生电解盐水反应,耗能较大且产生氯气等有害物质,易对环境造成二次污染。
技术实现要素:
5.本发明的目的是提供一种基于电渗析原理的应用锂离子固态电解质的卤水或海水提锂方法,旨在利用锂离子固态电解质对li
+
的优先选择透过性,通过外加电场使正极区域的卤水中li
+
、mg
2+
等阳离子向负极方向移动,由于固态电解质优先通过li
+
,从而实现卤水中mg
2+
、li
+
分离及li
+
在负极区域的富集。经过一次或多次富集后,li
+
浓度到达提取浓度,经沉淀或蒸发等方式提取li2co3、lioh等目标产物。
6.为实现上述目的,本发明提出了一种基于电渗析原理的卤水或海水提锂方法,所述方法包括以下步骤:
7.1)在正极区提供循环的卤水或海水,负极区为无锂或少锂溶液,正负极区域用锂离子固态电解质分隔,其中,所述少锂水溶液由下一级电渗析槽的正极所返回,用于分隔的锂离子固态电解质包括柔性的电解质膜或者刚性的电解质片;
8.2)对正极施加2.0v以下电压,基于电渗析原理利用电场对阳离子的迁移作用和固
态电解质对li
+
的高选择透过性,在负极区实现li
+
的富集;
9.3)将负极区富集的锂溶液引入下一级电渗析槽的正极区,在该电渗析槽重复步骤1)和步骤2);
10.4)经过大于等于零次的步骤3)后,当负极区li
+
达到一定浓度时,向负极溶液添加无锂化合物将li
+
提取。
11.优选地,应用的锂离子固态电解质为氧化物无机固态电解质、聚合物有机固态电解质及无机-有机复合固态电解质中的一种,其中,有机-无机复合固态电解质由上述氧化物无机固态电解质和聚合物有机固态电解质组成。
12.优选地,氧化物无机固态电解质为石榴石型li7la3zr2o
12
、钙钛矿型 li
3x
la
2/3
–
x
tio3、li
1+x
al
x
ti
2-x
(po4)3、li
1+x
al
x
ge
2-x
(po4)3及以上物质经其他元素掺杂后所得电解质中的一种或多种。
13.优选地,聚合物有机固态电解质由聚合物和导电锂盐组成,聚合物为聚环氧乙烷、聚丙烯腈、聚偏氟乙烯、聚甲基丙烯酸甲酯中的一种或多种,导电锂盐为六氟磷酸锂、高氯酸锂、双三氟甲烷磺酰亚胺锂中的一种或多种,聚合物与导电锂盐的摩尔比为(5~20):1。
14.优选地,电解质膜或电解质片的厚度为1μm~10mm。
15.优选地,负极区的溶液为纯水、nacl溶液、kcl溶液、na2co3溶液、k2co3溶液中的一种或多种。
16.优选地,所述无锂化合物包括氢氧化物、氯化物、硫酸类化合物、硝酸盐类化合物、碳酸类化合物、磷酸类化合物、醋酸类化合物、草酸类化合物、硼酸类化合物中的一种或多种。
17.优选地,所述步骤4)中,通过对含li
+
溶液进行沉淀过滤、蒸发结晶、加热分解中的一种或多种操作,以获得含锂化合物。
18.优选地,含锂化合物为氢氧化锂、氧化锂、过氧化锂、氯化锂、硫酸锂、硝酸锂、碳酸锂、磷酸锂、醋酸锂、草酸锂、硼酸锂中的一种或多种。
19.本发明还提出了一种基于电渗析原理的卤水或海水提锂装置,所述装置用于上述任一项所述的方法,所述装置包括多个电渗析槽,所述电渗析槽由外壳、正负极电极、锂离子固态电解质组成,利用锂离子固态电解质将正极溶液和负极溶液分隔开,并且利用树脂类化合物固定、封装固态电解质;将卤水或海水从第一级电渗析槽的正极区下部注入,从正极区上部流出少锂溶液;将无锂水溶液或者下一级电渗析槽得到的少锂溶液从负极区下部注入,电渗析后的多锂溶液从负极区上部流出进入下一级电渗析槽的正极区下部,实现循环提锂。
20.相对现有技术,本发明技术方案带来的有益效果如下:
21.(1)本发明中使用的锂离子固态电解质制造门槛低,易于规模化生产,且成本较低;
22.(2)本发明对装置施加的电压低,电耗成本低,且li
+
提取过程中不发生氧化还原反应,不产生有害物质如氯气等,对环境友好;
23.(3)本发明提锂速率快,单次循环用时少,大大提高了提锂效率。
附图说明
24.图1为本发明提锂的其中一种工艺流程图;
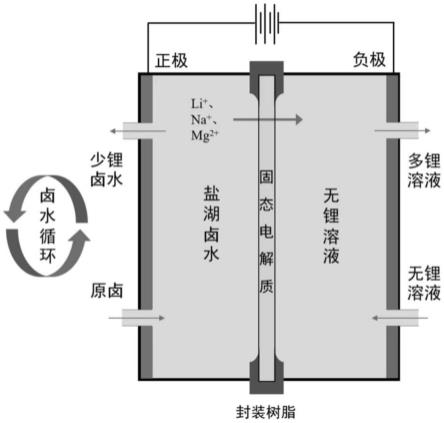
25.图2为本发明提锂的单级电渗析槽示意图;
26.图3为本发明提锂的多级电渗析槽示意图;
27.图4为本发明实施例1所得的首次循环时正极溶液(原卤)、负极溶液(提取液)中li
+
/mg
2+
随时间变化关系图,其中,箭头对线条的纵坐标起指示作用;
28.图5为本发明实施例1所得的装置分离系数、锂回收率随时间变化关系图,其中,箭头对线条的纵坐标起指示作用。
具体实施方式
29.下面结合附图和实施例对本发明作进一步的详细说明。可以理解的是,此处所描述的具体实施例仅仅用于解释本发明,而非对本发明的限定。
30.实施例1:
31.请参照图2,以300μm厚的li
1.5
al
0.5
ge
1.5
(po4)3(lagp)固态电解质片分隔正极卤水(mg
2+
浓度为10g/l,li
+
浓度为0.2g/l)、负极nacl溶液;对正极施加1.0v电压,通电0.5h;分别于10min、20min、30min时取负极溶液检测li
+
、mg
2+
浓度,结果如图4和表1所示。图5和表2可看出装置分离系数(提取液li/mg与原卤li/mg的比值),用于判断装置对li
+
的选择透过性,分离系数越高越好。图5和表3可看出锂回收率随时间的变化关系(提取液中li
+
浓度与初始原卤中li
+
浓度的比值),回收率越高越好。
32.表1原卤与提取液中离子浓度
[0033][0034]
表2分离系数
[0035] 10min20min30min分离系数19.8222.6324.33
[0036]
表3装置对li
+
的回收率
[0037] 10min20min30min回收率%7.410.4514.55
[0038]
实施例2:
[0039]
请参照图3,以1mm厚的li7la3zr2o
12
(llzo)固态电解质片分隔正极卤水(mg
2+
浓度为15g/l,li
+
浓度为0.2g/l)、负极nacl溶液;对正极施加 1.2v电压,通电1.5h;经5次富集后,取出负极溶液,向溶液中添加na3po4粉末使li
+
以li3po4沉淀形式析出。
[0040]
实施例3:
[0041]
请参照图3,以3mm厚的li
1.5
al
0.5
ti
1.5
(po4)3(latp)固态电解质片分隔正极卤水(mg
2+
浓度为10g/l,li
+
浓度为0.1g/l)、负极nacl溶液;对正极施加0.8v电压,通电0.5h;经8
次富集后,取出负极溶液,向溶液中添加naoh粉末并将溶液加热至60℃蒸发,使li
+
以lioh晶体形式析出。
[0042]
实施例4:
[0043]
请参照图3,以10mm厚的li
0.33
la
0.557
tio3(llto)固态电解质片分隔正极卤水(mg
2+
浓度为20g/l,li
+
浓度为0.1g/l)、负极nacl溶液;对正极施加1.0v电压,通电2h;经10次富集后,取出负极溶液,向溶液中添加 na2co3粉末并将溶液加热至80℃蒸发,使li
+
以li2co3晶体形式析出。
[0044]
实施例5:
[0045]
请参照图3,以100μm厚的聚合物固态电解质膜(peo与litfsi的摩尔比为15:1)分隔正极卤水(mg
2+
浓度为10g/l,li
+
浓度为0.2g/l)、负极nacl 溶液;对正极施加1.7v电压,通电2h;经10次富集后,取出负极溶液,向溶液中添加naoh粉末并将溶液加热至60℃蒸发,使li
+
以lioh晶体形式析出。
[0046]
实施例6:
[0047]
请参照图3,以150μm厚的无机-有机复合固态电解质膜(peo与litfsi 的摩尔比为12:1,聚合物占复合电解质总质量的85%)分隔正极卤水(mg
2+
浓度为15g/l,li
+
浓度为0.3g/l)、负极kcl溶液;对正极施加1.0v电压,通电1.5h;经8次富集后,取出负极溶液,向溶液中添加na2co3粉末并将溶液加热至80℃蒸发,使li
+
以li2co3晶体形式析出。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1