氮化碳纳米材料及其制备方法和应用与流程
本发明涉及材料化学
技术领域:
,具体涉及一种氮化碳纳米材料及其制备方法和应用。
背景技术:
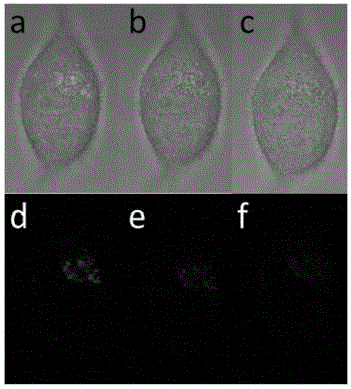
:石墨相氮化碳(g-c3n4),是一种不含金属的聚合物半导体,具有合适的带隙位置、独特的化学结构和优异的稳定性,这些优点使g-c3n4被广泛应用于光催化以及光电转换领域,如光催化水产氢产氧、光催化co2还原和光催化有机染料降解等。由于石墨相氮化碳比表面积小,不利于进一步修饰,且体相石墨相氮化碳材料很难溶于绝大多数溶剂,限制了其在生物传感、成像等方向的应用。因此,氮化碳纳米材料的制备具有重要意义。然而,目前针对氮化碳纳米材料的合成方法往往比较复杂,且大多数方法只针对于合成某种特定形貌的氮化碳纳米材料,很少有一种方法可以适用于合成多种形貌的氮化碳纳米材料。并且,由于量子限域效应的影响,由石墨相氮化碳出发制备得到的氮化碳量子点往往存在不利于成像应用的蓝移现象。因此,开发适用于合成多种形貌的氮化碳纳米材料,包括碳氮量子点、碳氮纳米片、碳氮纳米棒等,并能够改善氮化碳纳米材料光学性质的新方法具有重要意义。技术实现要素:发明目的:本发明的第一个目的是提供一种适于合成多种形貌的氮化碳纳米材料,并能够改善氮化碳纳米材料光学性质的方法。本发明的第二个目的是提供上述方法制得的氮化碳纳米材料。本发明的第三个目的是提供上述方法制得的氮化碳纳米材料的应用。技术方案:本发明提供一种氮化碳纳米材料的制备方法,包括以下步骤:1)将前驱体在惰性气氛中650℃-710℃热处理1h-4h;前驱体为石墨相氮化碳、三聚氰胺、双氰胺、尿素、氰胺和三聚氰酸中的一种或多种;2)根据目标氮化碳纳米材料种类选择溶剂,利用溶剂从步骤1)热处理产物中筛选氮化碳纳米材料。步骤1)中,上述前驱体可以是由已知的方法制得的石墨相氮化碳,也可以是含碳氮元素的分子如三聚氰胺、双氰胺、尿素、氰胺和三聚氰酸等;优选地,上述前驱体可以为由已知的方法,如400℃~600℃热缩聚等,以已知化合物为原料制得的石墨相氮化碳;上述已知的化合物可以包括三聚氰胺、双氰胺、尿素、氰胺和三聚氰酸中的一种或多种;进一步优选地,上述前驱体可以是三聚氰胺、双氰胺、氰胺和三聚氰酸中的一种或多种在450℃保温4小时然后研磨成粉得到的石墨相氮化碳cn450,也可以是三聚氰胺、双氰胺、氰胺和三聚氰酸中的一种或多种在550℃保温4小时然后研磨成粉得到的石墨相氮化碳cn550。步骤1)中,热处理温度优选为680℃-710℃,热处理时间优选为2小时-4小时;惰性气氛为氮气或氩气气氛。步骤2)中,溶剂为水、n,n-二甲基甲酰胺、甲苯、甲酰胺或乙腈等;利用溶剂从步骤1)热处理产物中筛选氮化碳纳米材料的方法包括:将步骤1)热处理产物得到的产物分散在溶剂中,超声,离心,取上清液,即为氮化碳纳米材料溶液,还可根据目标氮化碳纳米材料种类选择是否在离心后对上清液进行透析。将前驱体在惰性气氛中650℃~710℃热处理1小时-48小时和利用溶剂从步骤1)热处理产物中收集和筛选氮化碳纳米材料的具体方法为:将前驱体置于方舟中,将方舟置于管式炉中,拧紧管式炉密封圈,将管式炉的气体出口连接通气管一端,通气管另一端插入用于收集和筛选氮化碳纳米材料的溶剂中,以5l/h-30l/h的流速向管式炉中通入惰性气体,以1℃/min-20℃/min的升温速度升温至600℃~750℃保温1小时~48小时,保温过程中热剪裁产物被惰性气体流吹入至所述溶剂中,保温结束后,对所述溶剂超声,离心,取上清液;用于收集和筛选氮化碳纳米材料的溶剂可根据前驱体的量进行设置;上述通气管可以是硅胶管、乳胶管或玻璃管;升温速度优选为5℃/min-11℃/min。优选地,上述超声功率400w,超声时间为30min;离心转速为13000rpm,离心时间为30min。本发明另一方面提供一种氮化碳纳米材料,该氮化碳纳米材料由上述方法制得。上述氮化碳纳米材料包括但不限于氮化碳量子点、氮化碳纳米片、氮化碳纳米叶子、氮化碳纳米网络、氮化碳纳米纤维和氮化碳纳米棒中的一种或多种。本发明另一方面提供上述氮化碳纳米材料在细胞成像或信息加密中的应用。有益效果:(1)本发明的方法可通过前驱体和收集溶剂的选择获得多种不同形貌的氮化碳纳米材料,具有广泛的可调控性和适用性。(2)利用本发明方法制备得到的氮化碳量子点呈现出最大发光位置向长波长方向移动的特点,长波长荧光材料更有利于减小对生物组织的光照伤害,更有利于细胞成像等应用的开展;该氮化碳量子点应用于溶酶体成像时表现出比商业化溶酶体荧光探针lyso-trackerred更好的光稳定性,更有利于长时间实时溶酶体成像应用的开展;该氮化碳量子点可应用于信息加密方向,并可通过合理设计实现双层信息加密、解密应用。附图说明图1为氮化碳纳米材料制备过程示意图;图2为不同形貌的氮化碳纳米材料的透射电子显微镜照片,其中,a图为实施例1制备的氮化碳量子点-h2o的透射电子显微镜照片,b图为实施例2制备的氮化碳量子点-dmf的透射电子显微镜照片,c图为实施例3制备的氮化碳纳米叶子的透射电子显微镜照片,d图为实施例4制备的氮化碳纳米棒的透射电子显微镜照片,e图为实施例5制备的氮化碳纳米纤维的透射电子显微镜照片,f图为实施例6制备的氮化碳纳米网络的透射电子显微镜照片;图3为实施例1制备的氮化碳量子点-h2o、实施例2制备的氮化碳量子点-dmf与前驱体材料石墨相氮化碳cn450的荧光发射对照图;三者最大发射峰分别位于448nm、521nm、432nm,与石墨相氮化碳cn450相比,两种氮化碳量子点材料最大发射峰位置均发生红移,分别红移16nm、89nm;图4为氮化碳量子点-h2o的荧光发射图;其中,(a)图为实施例9制备的氮化碳量子点-h2o在激发光波长分别为320nm、340nm、360nm下的荧光发射图,(b)图为实施例1、实施例7和实施例8制备的氮化碳量子点-h2o的荧光发射图;由图4可以看出,氮化碳量子点-h2o表现为带隙发光,最大发射峰位于456nm,比石墨相氮化碳cn450红移了24nm;图5为氮化碳量子点-h2o与lyso-trackerred共同应用于人乳腺癌细胞mcf-7细胞溶酶体成像时间对比图;其中,a,b,c图分别为激光持续照射0s,60s,120s时,全光通道下lyso-trackerred及氮化碳量子点-h2o对mcf-7细胞的成像及溶酶体共定位效果;d,e,f图分别为激光持续照射0s,60s,120s时,红光及蓝光双通道下lyso-trackerred及氮化碳量子点-h2o对mcf-7细胞的成像及溶酶体共定位效果;图6为实施例1制备的氮化碳量子点-h2o应用在信息加密中应用的情况,其中,(a)图为滤纸上滴加氮化碳量子点-h2o干燥后在日光下的照片;(b)图为滤纸上滴加氮化碳量子点-h2o干燥后在uv光下的照片;(c)图为滤纸上滴加氮化碳量子点-h2o干燥后用cucl2进行二层加密后在日光下的照片;(d)图为滤纸上滴加氮化碳量子点-h2o干燥后用cucl2进行二层加密后在uv光照射下的照片;(e)图为用edta解密后紫外灯照射下的滤纸照片。具体实施方式下面通过具体实施方式对本发明进一步说明。图1显示了制备氮化碳纳米材料的流程,其中,热剪裁程序中,1+4表示匀速升温的时间为1h,保温的时间为4h;2+4表示匀速升温的时间为2h,保温的时间为4h;1+2表示匀速升温的时间为1h,保温的时间为2h。实施例1水溶性氮化碳量子点(氮化碳量子点-h2o)的制备(1)石墨相氮化碳cn450的制备将双氰胺于坩埚中置于马弗炉中,以10℃/min的升温速度升温至450℃,保温4小时,得到淡黄色石墨相氮化碳,研磨成粉备用。(2)将步骤(1)制备得到的石墨相氮化碳cn450粉末置于方舟中,将方舟置于管式炉石英管中央,拧紧法兰垫圈,法兰出气口外接30cm长的硅胶管,将硅胶管的另一端插入盛有50ml收集溶剂超纯水的100ml的广口锥形瓶中,使硅胶管口完全浸没在水中。(3)设置管式炉程序:第一阶段室温下以16l/h的流速向管式炉中通氮气1小时以排空石英管内的空气;第二阶段保持16l/h的流速通氮气,以11℃/min的升温速率升温至680℃,在680℃保温4小时以收集热剪裁产生的氮化碳量子点。(4)将步骤(3)收集到的氮化碳量子点及其他形貌材料的分散液在400w功率下超声30min,使其分散得更均匀。(5)将步骤(4)得到的分散液在13000rpm的转速下离心30min,取上清液。(6)取20ml步骤(5)得到的上清液,封于3000da的透析袋中,在磁力搅拌器上搅拌透析12h,取透析外液,即为氮化碳量子点-h2o的水溶液。氮化碳量子点-h2o的透射电子显微镜照片如图2a所示。实施例2发光比石墨相氮化碳cn450红移89nm的氮化碳量子点(氮化碳量子点-dmf)的制备。(1)石墨相氮化碳cn450的制备将双氰胺于坩埚中置于马弗炉中,以10℃/min的升温速度升温至450℃,保温4小时,得到淡黄色石墨相氮化碳,研磨成粉备用。(2)将步骤(1)制备得到的石墨相氮化碳cn450粉末置于方舟中,将方舟置于管式炉石英管中央,拧紧法兰垫圈,法兰出气口外接30cm长的硅胶管,将硅胶管的另一端插入盛有50ml收集溶剂n,n-二甲基甲酰胺(dmf)的100ml的广口锥形瓶中,使硅胶管口完全浸没在n,n-二甲基甲酰胺中。(3)设置管式炉程序:第一阶段室温下以16l/h的流速向管式炉中通氮气1小时以排空石英管内的空气;第二阶段保持16l/h的流速通氮气,以11℃/min的升温速率升温至680℃,在680℃保温4小时以收集热剪裁产生的氮化碳量子点。(4)将步骤(3)收集到的氮化碳量子点及其他形貌材料的分散液在400w功率下超声30min,使其分散得更均匀。(5)将步骤(4)得到的分散液在13000rpm的转速下离心30min,取离心上清液。(6)取20ml步骤(5)得到的上清液,封于3000da的超滤管中,13000rpm的转速下离心30min,取超滤外液,即为氮化碳量子点-dmf溶液。氮化碳量子点-dmf的透射电子显微镜照片如图2b所示。图3显示了实施例1制备的氮化碳量子点-h2o、实施例2制备的氮化碳量子点-dmf与前驱体材料石墨相氮化碳cn450的荧光发射对照图;三者最大发射峰分别位于448nm、521nm、432nm,与石墨相氮化碳cn450相比,两种氮化碳量子点材料最大发射峰位置均发生红移,分别红移16nm,89nm。实施例3氮化碳纳米叶子的制备(1)将双氰胺置于方舟中,将方舟置于管式炉石英管中央,拧紧法兰垫圈,法兰出气口外接30cm长的硅胶管,将硅胶管的另一端插入盛有50ml收集溶剂超纯水的100ml的广口锥形瓶中,使硅胶管口完全浸没在水中。(2)设置管式炉程序:第一阶段室温下以10l/h的流速向管式炉中通氮气1小时以排空石英管内的空气;第二阶段保持10l/h的流速通氮气,以11℃/min的升温速率升温至680℃,在680℃保温4小时以收集热剪裁产生的氮化碳纳米叶子。(3)将步骤(2)收集到的氮化碳纳米叶子及其他形貌材料的分散液在400w功率下超声30min,使其分散得更均匀。(4)将步骤(3)得到的分散液在13000rpm转速下离心30min,取上层清液,即为氮化碳纳米叶子的分散液。氮化碳纳米叶子的透射电子显微镜照片如图2c所示。实施例4氮化碳纳米棒的制备(1)石墨相氮化碳cn550的制备将双氰胺前驱物于坩埚中,置于马弗炉中,以2.2℃/min的升温速度升温至550℃,保温4小时,得到淡黄色石墨相氮化碳(石墨相氮化碳cn550),研磨成粉备用。(2)将步骤(1)制备得到的石墨相氮化碳cn550粉末置于方舟中,将方舟置于管式炉石英管中央,拧紧法兰垫圈,法兰出气口外接30cm长的硅胶管,将硅胶管的另一端插入盛有50ml收集溶剂超纯水的100ml的广口锥形瓶中,使硅胶管口完全浸没在水中。(3)设置管式炉程序:第一阶段室温下以20l/h的流速向管式炉中通氮气1小时以排空石英管内的空气;第二阶段保持20l/h的流速通氮气,以11℃/min的升温速率升温至680℃,在680℃保温4小时以收集热剪裁产生的氮化碳纳米棒。(4)将步骤(3)收集到的氮化碳纳米棒及其他形貌材料的分散液在400w功率下超声30min,使其分散得更均匀。(5)将步骤(4)得到的分散液在13000rpm转速下离心30min,取上层清液,即为氮化碳纳米棒的分散液。氮化碳纳米棒的透射电子显微镜照片如图2d所示。实施例5氮化碳纳米纤维的制备(1)石墨相氮化碳cn450的制备将双氰胺于坩埚中置于马弗炉中,以10℃/min的升温速度升温至450℃,保温4小时,得到淡黄色石墨相氮化碳,研磨成粉备用。(2)将步骤(1)制备得到的石墨相氮化碳cn450粉末置于方舟中,将方舟置于管式炉石英管中央,拧紧法兰垫圈,法兰出气口外接30cm长的硅胶管,将硅胶管的另一端插入盛有50ml收集溶剂乙腈的100ml的广口锥形瓶中,使硅胶管口完全浸没在乙腈中。(3)设置管式炉程序:第一阶段室温下以20l/h的流速向管式炉中通氮气1小时以排空石英管内的空气;第二阶段保持20l/h的流速通氮气,以11℃/min的升温速率升温至680℃,在680℃保温4小时以收集热剪裁产生的氮化碳纳米纤维。(4)将步骤(3)收集到的氮化碳纳米纤维及其他形貌材料的分散液在400w功率下超声30min,使其分散得更均匀。(5)将步骤(4)得到的分散液在13000rpm转速下离心30min,取上层清液,即为氮化碳纳米纤维的分散液。氮化碳纳米纤维的透射电子显微镜照片如图2e所示。实施例6氮化碳纳米网络的制备(1)石墨相氮化碳cn450的制备将双氰胺于坩埚中置于马弗炉中,以10℃/min的升温速度升温至450℃,保温4小时,得到淡黄色石墨相氮化碳,研磨成粉备用。(2)将步骤(1)制备得到的石墨相氮化碳cn450粉末置于方舟中,将方舟置于管式炉石英管中央,拧紧法兰垫圈,法兰出气口外接30cm长的硅胶管,将硅胶管的另一端插入盛有50ml收集溶剂甲苯的100ml的广口锥形瓶中,使硅胶管口完全浸没在甲苯中。(3)设置管式炉程序:第一阶段室温下以20l/h的流速向管式炉中通氮气1小时以排空石英管内的空气;第二阶段保持20l/h的流速通氮气,以11℃/min的升温速率升温至680℃,在680℃保温4小时以收集热剪裁产生的氮化碳纳米网络。(4)将步骤(3)收集到的氮化碳纳米网络及其他形貌材料的分散液在200w超声1h,使其分散得更均匀。(5)将步骤(4)得到的分散液在13000rpm转速离心30min,取上清液,即为氮化碳纳米网络的分散液。氮化碳纳米网络的透射电子显微镜照片如图2f所示。实施例1~实施例6的实验条件汇总如表1所示,其中,热剪裁程序一列中的1+4表示匀速升温的时间为1小时,保温时间为4小时。实施例7水溶性氮化碳量子点(氮化碳量子点-h2o)的制备(1)石墨相氮化碳cn450的制备将双氰胺于坩埚中置于马弗炉中,以10℃/min的升温速度升温至450℃,保温4小时,得到淡黄色石墨相氮化碳,研磨成粉备用。(2)将步骤(1)制备得到的石墨相氮化碳cn450粉末置于方舟中,将方舟置于管式炉石英管中央,拧紧法兰垫圈,法兰出气口外接30cm长的硅胶管,将硅胶管的另一端插入盛有50ml收集溶剂超纯水的100ml的广口锥形瓶中,使硅胶管口完全浸没在水中。(3)设置管式炉程序:第一阶段室温下以16l/h的流速向管式炉中通氮气1小时以排空石英管内的空气;第二阶段保持16l/h的流速通氮气,以11℃/h的升温速率升温至680℃,在680℃保温2小时以收集热剪裁产生的氮化碳量子点。(4)将步骤(3)收集到的氮化碳量子点及其他形貌材料的分散液在400w功率下超声30min,使其分散得更均匀。(5)将步骤(4)得到的分散液在13000rpm的转速下离心30min,取上清液。(6)取20ml步骤(5)得到的上清液,封于3000da的透析袋中,在磁力搅拌器上搅拌透析12h,取透析外液,即为氮化碳量子点-h2o的水溶液。实施例8水溶性氮化碳量子点(氮化碳量子点-h2o)的制备(1)石墨相氮化碳cn450的制备将双氰胺于坩埚中置于马弗炉中,以10℃/min的升温速度升温至450℃,保温4小时,得到淡黄色石墨相氮化碳,研磨成粉备用。(2)将步骤(1)制备得到的石墨相氮化碳cn450粉末置于方舟中,将方舟置于管式炉石英管中央,拧紧法兰垫圈,法兰出气口外接30cm长的硅胶管,将硅胶管的另一端插入盛有50ml收集溶剂超纯水的100ml的广口锥形瓶中,使硅胶管口完全浸没在水中。(3)设置管式炉程序:第一阶段室温下以16l/h的流速向管式炉中通氮气1小时以排空石英管内的空气;第二阶段保持16l/h的流速通氮气,以5℃/min的升温速率升温至680℃,在680℃保温2小时以收集热剪裁产生的氮化碳量子点。(4)将步骤(3)收集到的氮化碳量子点及其他形貌材料的分散液在400w功率下超声30min,使其分散得更均匀。(5)将步骤(4)得到的分散液在13000rpm的转速下离心30min,取上清液。(6)取20ml步骤(5)得到的上清液,封于3000da的透析袋中,在磁力搅拌器上搅拌透析12h,取透析外液,即为氮化碳量子点-h2o的水溶液。实施例9水溶性氮化碳量子点(氮化碳量子点-h2o)的制备(1)石墨相氮化碳cn450的制备将双氰胺于坩埚中置于马弗炉中,以10℃/min的升温速度升温至450℃,保温4小时,得到淡黄色石墨相氮化碳,研磨成粉备用。(2)将步骤(1)制备得到的石墨相氮化碳cn450粉末置于方舟中,将方舟置于管式炉石英管中央,拧紧法兰垫圈,法兰出气口外接30cm长的硅胶管,将硅胶管的另一端插入盛有50ml收集溶剂超纯水的100ml的广口锥形瓶中,使硅胶管口完全浸没在水中。(3)设置管式炉程序:第一阶段室温下以12l/h的流速向管式炉中通氮气1小时以排空石英管内的空气;第二阶段保持12l/h的流速通氮气,以11℃/min的升温速率升温至710℃,在710℃保温4小时以收集热剪裁产生的氮化碳量子点。(4)将步骤(3)收集到的氮化碳量子点及其他形貌材料的分散液在400w功率下超声30min,使其分散得更均匀。(5)将步骤(4)得到的分散液在13000rpm的转速下离心30min,取上清液。(6)取20ml步骤(5)得到的上清液,封于3000da的透析袋中,在磁力搅拌器上搅拌透析12h,取透析外液,即为氮化碳量子点-h2o的水溶液。图4为氮化碳量子点-h2o的荧光发射图;其中,(a)图为实施例9制备的氮化碳量子点-h2o在激发光波长分别为320nm、340nm、360nm下的荧光发射图,(b)图为实施例1、实施例7和实施例8制备的氮化碳量子点-h2o的荧光发射图;由图4可以看出,氮化碳量子点-h2o表现为带隙发光,最大发射峰位于456nm,比石墨相氮化碳cn450红移了24nm。实施例10水溶性氮化碳量子点(氮化碳量子点-h2o)的制备(1)石墨相氮化碳cn450的制备将双氰胺于坩埚中置于马弗炉中,以10℃/min的升温速度升温至450℃,保温4小时,得到淡黄色石墨相氮化碳cn450,研磨成粉备用。(2)将步骤(1)制备得到的石墨相氮化碳cn450粉末置于方舟中,将方舟置于管式炉石英管中央,拧紧法兰垫圈,法兰出气口外接30cm长的硅胶管,将硅胶管的另一端插入盛有50ml收集溶剂超纯水的100ml的广口锥形瓶中,使硅胶管口完全浸没在水中。(3)设置管式炉程序:第一阶段室温下以30l/h的流速向管式炉中通氮气1小时以排空石英管内的空气;第二阶段保持30l/h的流速通氮气,以11℃/min的升温速率升温至650℃,在650℃保温4小时以收集热剪裁产生的氮化碳量子点。(4)将步骤(3)收集到的氮化碳量子点及其他形貌材料的分散液在80w功率下超声48min,使其分散得更均匀。(5)将步骤(4)得到的分散液在5000rpm的转速下离心2h,取上清液。(6)取20ml步骤(5)得到的上清液,封于3000da的透析袋中,在磁力搅拌器上搅拌透析12h,取透析外液,即为氮化碳量子点-h2o的水溶液。表1样品收集溶剂前驱体热剪裁程序实施例1氮化碳量子点-h2o超纯水cn450680℃-(1+4)实施例2氮化碳量子点-dmfn,n-二甲基甲酰胺cn450680℃-(1+4)实施例3氮化碳纳米叶子超纯水dcda680℃-(1+4)实施例4氮化碳纳米棒超纯水cn550680℃-(1+4)实施例5氮化碳纳米纤维乙腈cn450680℃-(1+4)实施例6氮化碳纳米网络甲苯cn450680℃-(1+4)实施例7氮化碳量子点-h2o超纯水cn450680℃-(1+2)实施例8氮化碳量子点-h2o超纯水cn450680℃-(2+4)实施例9氮化碳量子点-h2o超纯水cn450710℃-(1+4)实施例10氮化碳量子点-h2o超纯水cn450650℃-(1+4)实施例11氮化碳量子点-h2o溶酶体成像应用。以实施例1制备得到的氮化碳量子点-h2o为荧光标记物,利用激光共聚焦显微镜进行氮掺杂碳荧光量子点细胞成像实验,步骤为:(1)将mcf-7细胞接种在激光共聚焦皿(直径14mm)中,接种密度为10-5个/ml,用含有10%胎牛血清和1%青霉素-链霉素溶液的dmem细胞培养基于细胞培养箱(37℃,5%co2)培养24h。(2)将步骤(1)中的激光共聚焦皿取出,弃去上层清液,用pbs缓冲溶液润洗一次,接着用配有100μl0.05mg/ml的氮化碳量子点-h2o的dmem培养液溶液在细胞培养箱中继续孵育30min。(3)将步骤(2)中的激光共聚焦皿取出,弃去上层清液,用pbs缓冲液润洗三次,除去过量的氮化碳量子点。(4)在步骤(3)中的激光共聚焦皿中加入100μllysotrackerred溶液(用dmem以1∶20000的比例稀释),在细胞培养箱中继续孵育30min。弃去上层清液,用pbs再润洗三次除去过量的lysotrackerred荧光探针。(5)将步骤(4)中的激光共聚焦皿取出,置于激光共聚焦显微镜下观察,观察物镜100×,分别在紫外光、绿光激发波长下观察。每隔30s拍照记录一次。(6)结果:在共聚焦显微镜下观察成像,如图5所示,其中a,b,c分别为激光持续照射0s,60s,120s时,全光通道下lyso-trackerred及氮化碳量子点-h2o对mcf-7细胞的成像及溶酶体共定位效果;d,e,f分别为激光持续照射0s,60s,120s时,红光及蓝光双通道下lyso-trackerred及氮化碳量子点-h2o对mcf-7细胞的成像及溶酶体共定位效果。其中,氮化碳量子点-h2o发蓝光,lyso-trackerred发红光。在图5中,图a、d显示lyso-trackerred和氮化碳量子点-h2o都在细胞中明显发光,且氮化碳量子点-h2o与商业溶酶体荧光染料表现出共定位现象,表明氮化碳量子点-h2o可以对溶酶体进行定位荧光成像。图b、e显示激光持续照射60s后lyso-trackerred的红光强度明显减弱,氮化碳量子点-h2o的蓝光无明显变化,图c、f显示激光持续照射120s后lyso-trackerred的红光几乎不可见,已无法达到成像效果,氮化碳量子点-h2o的蓝光无明显变化。由共聚焦显微镜下观察成像可知:(1)氮化碳量子点可在孵育半小时内有效地进入mcf-7细胞。(2)氮化碳量子点与用商业溶酶体标记荧光染料lyso-trackerred都对mcf-7细胞中的溶酶体具有良好的荧光标记作用。(3)在持续长时间照射下,可观察到lyso-trackerred在60秒内强烈淬灭,并且在90秒后几乎完全从双通道复合的视野中消失;相对应地,氮化碳量子点在120秒后仍表现出强烈的荧光发射,没有明显的光漂白(图5),表明与商业化溶酶体荧光染料lyso-trackerred相比,水溶性氮化碳量子点具有更强的长时间实时成像能力。实施例12氮化碳量子点-h2o信息加密应用。(1)以实施例1制备得到的氮化碳量子点-h2o(一种隐形安全墨水)和cucl2作为加密试剂,uv光和乙二胺四乙酸二钠盐作为解密试剂。加密步骤为:(1)将滤纸上溶液滴在滤纸上的特定点上以编码所需信息。干燥后,在日光下,滤纸上的字符几乎不可见(图6a)。(2)在uv光照射下,可读取代码内信息(图6b)。(3)将滤纸浸润在cu2+溶液中30s,进行二层加密,此时在日光灯及紫外灯下信息均不可见。(图6c,6d)解密步骤为:(1)将edta加载到滤纸上,进行第一层解密。(2)用紫外灯照射进行第二层解密。此时信息可读取(图6e)。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1