电石渣矿化固定CO2并制备微细碳酸钙的方法与流程
本发明涉及固废利用及碳减排领域,具体涉及一种电石渣矿化固定co2并制备微细碳酸钙的方法。
背景技术:
二氧化碳的大规模储存与固定是co2减排的主要途径,主要包括地质储存、海洋储存以及矿物碳酸化固定。其中,矿物碳酸化是将co2与钙镁等碱土金属的氧化物、盐反应,生成碳酸盐的过程。二氧化碳的矿物碳酸化固定具有稳定性高、能耗较小等优势,而被认为是二氧化碳固定利用的重要途径之一。
电石渣是电石与水反应放出乙炔气体后的残渣,主要成分是氢氧化钙,此外由于电石的组成不同,还会含有少量有机杂质、氧化镁、氧化铁、氧化铝、二氧化硅等杂质。当前一些利用电石渣开发的产品,价格比较低廉,若能将其转化为在无机盐用量中居第四位的碳酸钙产品,不仅给企业带来巨大的经济效益,而且对环境保护具有深刻的现实意义。目前,利用电石渣生产碳酸钙主要可分为煅烧法和浸取法。如cn102527225b、cn100457632c、cn109467322a等介绍了将电石渣经高温煅烧得到生石灰,再与co2或其他碳化剂(碳酸盐、碳酸氢盐等)反应得到碳酸钙。此工艺的高温煅烧过程需要消耗大量能耗。浸取法制备碳酸钙通常包括两个阶段:浸取阶段和碳酸化阶段。浸取阶段主要通过选择合适的浸取剂浸取出电石渣中的钙离子。在碳酸化阶段,上述钙离子与co2在碱性条件反应得到碳酸钙产品。浸取剂通常为酸或酸式盐,包括盐酸、氨基酸、脂肪酸、氯化铵等,如cn101264920b、cn101580257a等利用盐酸为浸取剂,通过电石渣与盐酸反应得到氯化钙溶液,然后氯化钙溶液与碳化剂(碳酸钠)或在碱性条件下与co2反应生成碳酸钙沉淀,该方法虽然过程简单,但过程中不断消耗酸碱,并产生氯化盐废液,从资源利用和环境角度不具有大规模生产的前景。cn101293663b、cn102992373a等以氨基酸、脂肪酸为浸取剂制备碳酸钙,制备的碳酸钙具有粒径小,分散性好等特点,但是使用氨基酸作为浸取剂价格较昂贵,而使用脂肪酸作为浸取剂因其酸性大于碳酸,因此无法使用co2作为碳化剂,需不断消耗碳化剂(碳酸盐、碳酸氢盐等),无法实现大规模工业应用。使用氯化铵为浸取剂浸取电石渣制备碳酸钙是比较常见的工艺,相关报道有很多,如cn102602973b(一种利用电石渣合成超细碳酸钙的方法)、cn104229852b(一种电石渣制备微细碳酸钙的表面改性方法)、cn1854069a(用电石渣制备超细碳酸钙的方法)、cn101020579a(一种由电石渣制备高纯轻质碳酸钙微粉的方法)、cn103738997a(以电石渣为原料制取纳米碳酸钙的方法)等。上述方法均以氯化铵为浸取剂,区别在于分散剂和活化剂等不尽相同。这些方法从化学原理看是可行的,但其通性问题在于整个工艺过程未注意氨气的分离和溢出问题。上述浸取法均需使用第三种酸性的浸取剂,即使浸取剂可以回收套用,也将产生浸取剂的损耗以及由此引入的其他杂质,并延长了工艺路线。
综上所述,目前已经公开的利用电石渣制备碳酸钙的方法都存在某些缺点,如煅烧法需消耗大量酸碱和碳化剂,能耗较高,产生废盐水等。浸取法需使用第三种酸性浸取剂,存在工艺路线长、浸取剂的损耗以及由此引入其他杂质等问题。
技术实现要素:
本发明的目的是提供一种新型的浸取电石渣并矿化固定co2制备微细碳酸钙的方法,该方法采用co2作为电石渣的浸取剂和碳化剂,避免了第三种酸性浸取剂的使用,也避免了氨气的使用和溢出,具有工艺简单,对设备材质要求低等优点。
本发明所提供的电石渣矿化固定co2并制备微细碳酸钙的方法,包括如下步骤:
1)采用含co2的气体与电石渣的浆液在第ⅰ反应器中进行反应,使其中的cao(或ca(oh)2)生成ca(hco3)2并溶解于水中;
2)将步骤1)反应后的体系经固液分离得到的含有ca(hco3)2的水溶液输送至第ⅱ反应器中,加热分解得到碳酸钙沉淀、co2气体和水蒸汽;
3)将步骤2)反应所得的co2气体返回至所述第ⅰ反应器中进行反应,分离出步骤2)反应后体系中的所述碳酸钙沉淀,所得清液返回至所述第ⅰ反应器,完成一个循环。
上述的方法中,步骤1)中,进行所述反应之前,将所述电石渣研磨至100~500目,然后与水混合配成浆液;
以氧化钙的质量计,所述浆液中电石渣的质量分数为1%~8%,优选地选择4%~7.5%。上述的方法中,步骤1)中,所述含co2的气体包括但不限于火力发电厂废气、煤化工废气、水泥厂废气等;
所述含co2的气体中co2的体积含量为5%~100%,优选10%~100%。
上述的方法中,步骤1)中,所述含co2的气体与所述电石渣的摩尔比为2~6:1,优选3~5:1,其中,所述电石渣的量以氧化钙计;
控制溶液的ph在4~8.4,通过所述含co2的气体的通气量进行控制。
上述的方法中,所述第ⅰ反应器包括但不限于喷淋塔、鼓泡塔、鼓泡搅拌釜、鼓泡管式反应器和气升式反应器;
所述第ⅱ反应器包括但不限于蒸发结晶器、喷雾塔、浆态床和加热反应釜。
上述的方法中,步骤2)中,所述加热分解的温度为50~100℃,优选60~95℃;
所述方法还包括在步骤2)反应后的体系中添加分散剂和改性剂对所述碳酸钙进行改性的步骤;
经所述改性后的碳酸钙产品的粒径为100~1000nm。
上述的方法中,步骤2)中,所述固液分离的方式为沉降分离、过滤和/或离心;
步骤3)中,采用沉降分离、过滤和/或离心的方式分离所述碳酸钙。
上述的方法中,将步骤2)中经固液分离后的后未溶解的固渣部分循环至所述第ⅰ反应器中,以提高钙的提取利用率,循环比(循环的质量:排出的质量)为2~6:1,优选3~5:1。
上述的方法中,将步骤1)中未反应的co2气体部分循环至所述第ⅰ反应器中,以提高co2的矿化利用率,循环比(循环的体积:排出的体积)为1:1~7,优选1:2~6。
与现有技术相比,本发明提供的电石渣矿化固定co2并制备微细碳酸钙的方法,具有如下优势:
1)避免了使用酸碱、氯化铵等浸取剂,降低了物料消耗,避免了可能引入的杂质;
2)避免了氨气的使用和溢出,对设备的密封性和材质等要求较低;
3)工艺流程短,易于放大,有利于实现大规模工业化应用。
附图说明
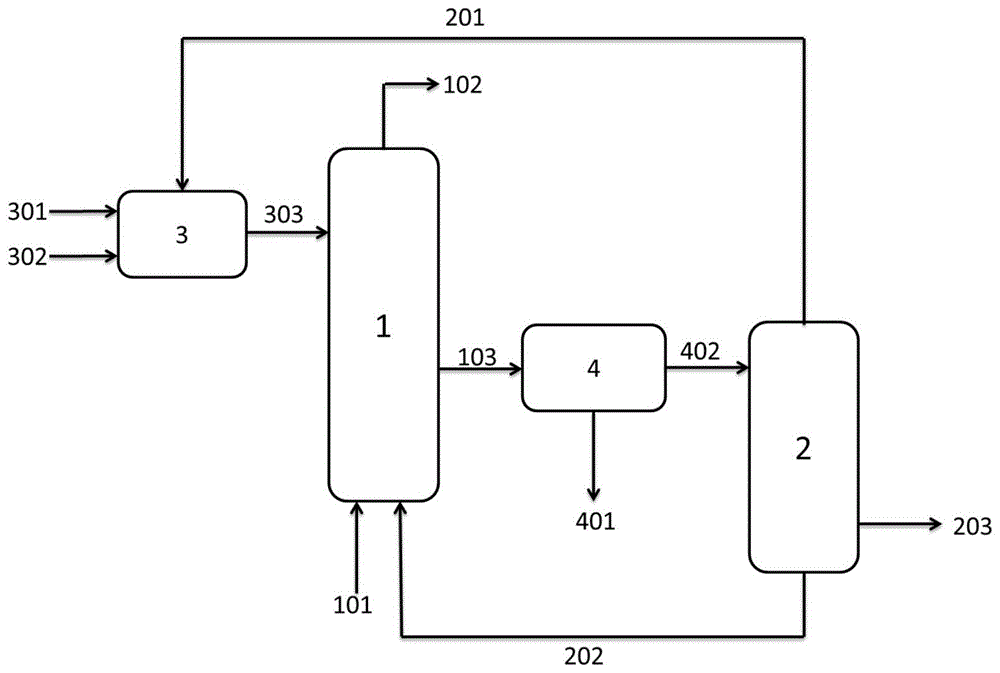
图1为本发明电石渣矿化固定co2并制备微细碳酸钙的方法第一种流程图。
图2为本发明电石渣矿化固定co2并制备微细碳酸钙的方法第二种流程图。
图3为本发明电石渣矿化固定co2并制备微细碳酸钙的方法第三种流程图。
具体实施方式
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
本发明方法涉及的化学反应如下:
1)浸取过程
在第ⅰ反应器中电石渣浆液中的氢氧化钙和过量的含二氧化碳气体发生如下反应:
ca(oh)2+2co2=ca(hco3)2
电石渣中的其他组分(如si、al、fe等)不参与反应,反应生成可溶的碳酸氢钙,将上述未反应的电石渣残渣与碳酸氢钙溶液分离,残渣部分循环至第ⅰ反应器中提高钙离子的提取利用率,未反应的二氧化碳部分循环至第ⅰ反应器中提高co2的矿化吸收率。
2)分解过程
由第ⅰ反应器得到的碳酸氢钙溶液经加热分解,得到碳酸钙沉淀和co2气体,反应方程如下:
ca(hco3)2=caco3+co2+h2o
将上述碳酸钙沉淀从溶液中分离并干燥得到微细碳酸钙产品,所生成的co2气体和水蒸气循环至第ⅰ反应器内循环使用,增加含co2气体中co2的浓度,利于形成碳酸氢钙并提高浸取反应速率。
具体步骤:
如图1所示的流程,在混合器3中,电石渣301与清液201及补加水302混合均匀制成浆液303加入到第i反应器1中,与过量的含co2气体101反应生成溶于水的碳酸氢钙,未反应的电石渣与碳酸氢钙水溶液103经固液分离装置4分离得到残渣401和碳酸氢钙溶液402,碳酸氢钙溶液402进入第ⅱ反应器2中,经加热分解生成碳酸钙沉淀203和co2气体202,co2气体202循环至第ⅰ反应器中提高气体101中co2的浓度,利于形成碳酸氢钙并提高浸取速率,分离碳酸钙沉淀后得到的清液201循环至混合器3中用于制备浆液303。
如图2所示的流程,与图1所示流程的区别在于:将固液分离得到的残渣403循环至第ⅰ反应器中继续反应,以提高钙离子的提取利用率。
如图3所示的流程,与图2所示流程的区别在于:将第ⅰ反应器中未反应的含co2气体104部分返回第1反应器中继续反应,以提高co2的矿化吸收率。
实施例1、
选用电石渣原料a为实验原料,其主要组成如表1所示,
表1电石渣原料a的主要元素组成
电石渣原料a烘干,去除其中的硫化物、有机质等易挥发组分后,研磨至100目,取500g研磨后的电石渣加7.8l水制成匀浆加入到气升式反应器(反应器直径11cm,高度95cm)内,通入模拟的火力发电厂废气,二氧化碳体积含量为12%,空塔气速为1cm/s,反应液ph降至5停止通气,沉降分离,清液泵入蒸发结晶器中,温度控制在70℃,压力0.03mpa,分解产生的co2和水蒸汽冷凝后重新通入气升式反应器中,所得碳酸钙经105℃干燥既得碳酸钙产品,经分析,所得碳酸钙为球霰型,粒径1微米,白度97.6,纯度98.5%。所得碳酸钙总量为500g,电石渣中钙离子的提取率为89.2%。
实施例2、
选用电石渣原料b作为实验原料,其主要组成如表2所示,
表2电石渣原料b主要元素组成
电石渣原料b经烘干,去除其中的硫化物、有机质等易挥发组分后,研磨至200目,电石渣(301)以0.5kg/h速率与清液(201)和补加水(302)在搅拌混合器3内混合,清液(201)和补加水(302)的加入速率分别为4.89kg/h和0.11kg/h,制成的浆液(303)通入到喷淋塔(第ⅰ反应器)内(浆液从顶部喷淋,含co2气体从塔底通入),喷淋速率5.5kg/h,通入新鲜的模拟的煤化工废气0.08l/h,二氧化碳含量为80%,未反应的co2气体(104)部分返回喷淋塔内,循环比为1:4,浆液(103)排出到沉降槽4内,浆液(103)的ph控制在5.5,排出速率为5.97kg/h,从底部排出未反应的固渣(401)的速率为0.18kg/h,其含水率控制在5%,其中部分残渣(403)返回至喷淋塔内,循环比为3:1,碳酸氢钙溶液(402)的排入加热反应釜(第2反应器)内,排出速率为5.78kg/h,控制加热釜溶液温度保持在80℃,加热反应釜分解产生的co2气体(202)和水蒸汽排出后,冷凝水蒸汽并入清液(201),co2排出速率为0.26kg/h,经加压循环至喷淋塔,上层清液(201)以4.89kg/h的速率泵入混合器3,生成的碳酸钙沉淀排出速率为0.63kg/h,含水率为5%。经分析,所得碳酸钙为文石型,粒径50nm,白度97.9,纯度98.6%。电石渣中钙离子的提取率为90%,碳酸氢钙分解率为95%,二氧化碳矿化吸收率为82%。
依照本发明的实施例如上文所述,这些实施例并没有详尽叙述所有的细节,也不限制该发明仅为所述的具体实施例。显然,根据以上描述,可作很多的修改和变化。本说明书选取并具体描述这些实施例,是为了更好地解释本发明的原理和实际应用,从而使所属技术领域技术人员能很好地利用本发明以及在本发明基础上的修改使用。
- 还没有人留言评论。精彩留言会获得点赞!