一种制备高纯硅酸的方法与流程
1.本发明属于化工领域,具体涉及一种制备高纯硅酸的方法。
背景技术:
2.化学机械抛光(cmp)是集成电路制造中获得全局平坦化得唯一可行手段,是芯片制造的必需步骤之一,硅溶胶是集成电路cmp抛光液中应用最多的磨料。半导体制造工艺的进步对抛光液中的金属杂质含量提出了越来越高的要求,因为磨料中的杂质金属离子易吸附在硅晶圆表面造成产品性能和良品率下降。
3.在众多cmp用硅溶胶制备方法中,离子交换法原料廉价、设备和工艺简单、易于操作、产品技术参数可控,因此被广泛采用。该方法以硅酸钠或水玻璃为原料,经离子交换工艺得到硅酸,后者在碱性条件下成核、生长即得硅溶胶。硅酸中间体的金属杂质含量将直接决定硅溶胶产品的纯度,研究低金属含量高纯硅酸的制备具有重要的意义。
4.高纯硅酸的制备目前已有专利涉及,例如cn 1420843a采用正硅酸酯水解法制备硅酸,由于正硅酸酯容易提纯,所以此方法获得的硅酸纯度很高,但缺点是需要使用有机溶剂,成本较高,而且后续需将溶剂蒸馏除去才可用于cmp用途。cn 1143354a采用四氯化硅水解制备硅酸,并加入氨基酸、氯化胆碱等含氮有机物作为稳定剂,该方法所使用的四氯化硅极易挥发且遇水立即水解发烟,安全性较差,大批量工业生产较困难。cn 104591192a以水玻璃为原料,先后经过阳、阳、阴离子交换,其中第二次阳离子交换前,加入有机酸或无机酸调节ph,以便将铝、铁等元素的氢氧化物转化为阳离子,随后在阳离子交换中被除去。该发明制备的硅酸可以满足制备硅晶圆cmp用硅溶胶的要求,但由于采用了三次离子交换工艺,存在酸碱消耗量大、废盐处理费用高的问题。cn 112299424a是对cn 104591192a的改进,采用酸性缓冲液代替单一强酸,使离子交换过程中的ph保持稳定,硅酸纯度有所提高,但仍需要进行三次离子交换。
技术实现要素:
5.本发明的目的是提出一种以水玻璃为原料,采用过滤除杂制备高纯硅酸的方法,利用工业水玻璃(硅酸钠的水溶液,硅酸钠化学式为na2o
·
nsio2)和强碱的加热处理,能将水玻璃中的硅酸铝和硅酸铁分解为偏铝酸盐和铁(iii)酸盐,进而在离子交换后将铝、铁杂质转化为氢氧化物,然后被过滤除去。
6.为达到上述目的,本发明采用以下技术方案:
7.一种制备高纯硅酸的方法,包括以下步骤:
8.(1)取工业水玻璃,加水稀释,再加入强碱,使sio2:m
+
达到摩尔比(0.25-0.45):1,其中m
+
为金属阳离子或有机阳离子,对得到的溶液在搅拌下加热并保温;
9.(2)待该溶液冷却后,将该溶液通过阳离子交换柱,收集ph<6的液体,得到粗硅酸;
10.(3)用折叠式滤芯对得到的粗硅酸进行过滤,滤芯的孔径为1-10μm,得到高纯硅
酸。
11.进一步地,工业水玻璃组成按照摩尔比为sio2:na2o=(1-4):1。
12.进一步地,强碱为氢氧化钾、氢氧化钠、氢氧化锂、四甲基氢氧化铵、四乙基氢氧化铵、乙醇钠、叔丁醇钾中的一种或者几种。
13.进一步地,金属阳离子为na
+
、k
+
或ca
2+
,有机阳离子为四甲基铵离子或四乙基铵离子。
14.进一步地,搅拌下加热至70-100℃,保温1-10小时。
15.进一步地,粗硅酸的ph为5.0-5.5。
16.本发明用到的工业水玻璃中含有较高的铝、铁杂质,并以相应的杂硅酸盐的形式存在。常规的离子交换工艺无法破坏杂硅酸盐中的al-o-si和fe-o-si结构,因此造成较多的铝、铁杂质被混入硅酸中。本发明在水玻璃中加入强碱,使得sio2:m
+
达到0.2-0.45(m表示金属或有机阳离子),水玻璃、强碱加热步骤可将杂质硅酸铝的al-o-si结构和硅酸铁的fe-o-si结构分解为偏铝酸盐和铁(iii)酸盐,反应式如下:
17.al-o-si+2oh-→
al-o-+si-o-+h2o;
18.fe-o-si+2oh-→
fe-o-+si-o-+h2o;
19.离子交换后,硅酸根被转化为硅酸,粗硅酸的ph约为5.0-5.5,在该ph下,偏铝酸盐和铁(iii)酸盐均被质子化,并生成氢氧化物沉淀,通过过滤将氢氧化物除去,得到高纯硅酸。
20.本发明制备的硅酸可达到以下技术指标:sio2含量1%-6%,ph=5.0-5.5,钠离子含量≤300ppb(2%sio2含量时,使用含钠的强碱),钠离子含量≤200ppb(2%sio2含量时,采用不含钠的强碱),铝离子含量≤50ppb,铁离子含量≤25ppb。
附图说明
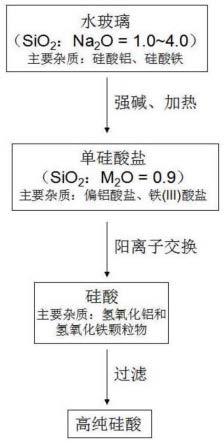
21.图1是高纯硅酸制备流程示意图。
具体实施方式
22.为使本发明的技术方案能更明显易懂,特举实施例并结合附图详细说明如下。
23.实施例一:取60kg无水硅酸钠固体(sio2质量分数49.25%,摩尔比sio2:na2o=1:1),用1000kg水溶解并充分搅匀。在强烈搅拌下缓慢加入55.26kg(985mol)氢氧化钾固体,加完后升温至80℃并保温3小时,此时sio2:m
+
为0.25:1。待溶液冷却后,将其通过阳离子交换柱,收集ph<6的液体,得到粗硅酸。用平均孔径为2μm的折叠式滤膜对上述粗硅酸进行过滤,得到高纯硅酸,表征结果见表1。
24.实施例二:取60kg液态水玻璃(sio2质量分数25%,摩尔比sio2:na2o=3.3:1),用1200kg水溶解并充分搅匀。在强烈搅拌下缓慢加入16.16kg(404mol)氢氧化钠固体(强烈放热!),加完后加热至100℃沸腾并保温1小时,此时sio2:m
+
为0.45:1。待溶液冷却后,将其通过阳离子交换柱,收集ph<6的液体,得到粗硅酸。用平均孔径为10μm的折叠式滤膜对上述粗硅酸进行过滤,得到高纯硅酸,表征结果见表1。
25.实施例三:取60kg液态水玻璃(sio2质量分数15%,摩尔比sio2:na2o=4:1),用140kg水溶解并充分搅匀。于通风良好的场所,在强烈搅拌下缓慢加入136.7kg四甲基氢氧
化铵水溶液(质量分数25%,含四甲基氢氧化铵375mol),加完后加热至100℃沸腾并保温1小时,此时sio2:m
+
为0.33:1。待溶液冷却后,将其通过阳离子交换柱,收集ph<6的液体,得到粗硅酸。用平均孔径为5μm的折叠式滤膜对上述粗硅酸进行过滤,得到高纯硅酸,表征结果见表1。
26.实施例四:取60kg九水合硅酸钠(sio2质量分数21.14%,摩尔比sio2:na2o=1:1),用210kg水溶解并充分搅匀。在搅拌下,缓慢加入43.16kg(634.2mol)乙醇钠粉末,30分钟左右加完,加完后再搅拌30分钟,此时sio2:m
+
为0.25:1。将混合物加热70℃并保温10小时,此过程中蒸出100kg液体,使大部分反应生成的乙醇与水共沸蒸出。随后冷却至室温,进行阳离子交换,收集ph<6的液体,再用平均孔径为1μm的折叠式滤膜对上述粗硅酸进行过滤,得到含有微量乙醇的高纯硅酸,表征结果见表1。
27.以下对比例采用常规方法制备硅酸,即去掉强碱加热和过滤步骤。
28.对比例:取60kg水玻璃(sio2质量分数25%,摩尔比sio2:na2o=3.3:1),加340kg水稀释。将稀释液进行阳离子交换即得硅酸,表征结果见表1。
29.表1各实施例中高纯硅酸表征结果
[0030] sio2含量钠含量/ppb铝含量/ppb铁含量/ppb实施例一2.65%1874219实施例二1.03%124239实施例三2.50%2095629实施例四5.83%80110256对比例4.61%6281986505
[0031]
表1表明:本发明的强碱加热和过滤措施能将硅酸中的铁、铝含量降低一个数量级以上。铁、铝是水玻璃中含量最高的金属杂质,一般以硅酸盐的形式存在。常规离子交换法不能破坏al-o-si和fe-o-si结构,造成铁、铝元素进入到硅酸中。本发明的强碱加热步骤可使上述硅酸盐分解,铁和铝都被转化为氢氧化物,然后被过滤除去,最后得到金属含量更低的高纯硅酸。
[0032]
以上实施例仅用以说明本发明的技术方案而非对其进行限制,本领域的普通技术人员可以对本发明的技术方案进行修改或者等同替换,本发明的保护范围以权利要求所述为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1