用于治疗一氧化碳中毒的RCOM蛋白基一氧化碳清除剂和制剂
用于治疗一氧化碳中毒的rcom蛋白基一氧化碳清除剂和制剂
1.相关申请的交叉引用
2.本技术要求于2020年5月11日提交的美国临时申请号63/022,821的权益,该申请通过引用整体并入本文。
技术领域
3.本公开涉及重组一氧化碳代谢调节因子(rcom)蛋白及其药物组合物。本公开进一步涉及重组rcom蛋白和组合物用于治疗一氧化碳(co)中毒、氰化物中毒和硫化氢中毒以及作为血液替代品的用途。
4.关于政府支持的声明
5.本发明是在国立卫生研究院授予的基金号hl098032、hl125886、hl136857、hl103455、hl110849和hl007563的政府支持下完成的。政府对本发明享有一定权利。
背景技术:
6.吸入暴露于一氧化碳是环境中毒的主要原因。个体可能在各种不同的情况下暴露于空气中的一氧化碳,诸如房屋火灾、发电机或室内使用的露天烧烤架,或者试图在封闭空间内自杀。一氧化碳与细胞中的血红蛋白和血红素蛋白结合,特别是与呼吸转运链的酶结合。与血红蛋白及其他血红素蛋白结合的一氧化碳的积累有损于氧的输送和氧化磷酸化的氧利用。这最终导致大脑和心脏等重要器官严重缺氧和缺血性损伤。在血液中积累超过5-10%碳碳氧血红蛋白的个体存在脑损伤和神经认知功能障碍的风险。碳氧血红蛋白水平非常高的患者通常会遭受不可逆的脑损伤、呼吸衰竭和/或心血管虚脱。
7.尽管存在利用标准的动脉和静脉血气分析和血氧饱和度测定来快速地诊断一氧化碳中毒的方法,并且尽管了解一氧化碳中毒的危险因素,但对于这种有毒暴露尚无可用的解毒剂。目前的治疗方法是通过面罩给予100%氧气,并在可能的情况下让患者暴露于高压氧。高压氧疗法增加一氧化碳从血红蛋白释放的速率并加速一氧化碳的自然清除。然而,这种疗法对一氧化碳清除率仅具有较小作用,并且基于高压氧设施的复杂性,该疗法在现场是不可用的。此外,高压氧疗法通常与显著的治疗延误和运输成本相关。因此,需要一种有效、快速和容易获得的疗法来治疗一氧化碳中毒,也称为碳氧血红蛋白血症。
技术实现要素:
8.本公开描述了对co具有高亲和力的重组一氧化碳代谢调节因子(rcom)蛋白及其作为co清除剂的用途。所公开的rcom蛋白能够从结合co的血红蛋白、肌红蛋白和细胞色素c氧化酶(在线粒体中)中去除co,因而可用于治疗碳氧血红蛋白血症的方法并作为血液替代品。
9.本文提供了重组rcom蛋白。在一些实施方案中,重组rcom蛋白包括血红素结合结构域(hbd),其氨基酸序列与seq id no:2具有至少90%的同一性。在一些实例中,hbd的氨基酸序列与seq id no:2具有至少90%的同一性并且在h74、c94、m104、m105、c127和c130中
的一个或更多个处包括氨基酸取代。在另一些实例中,hbd具有野生型氨基酸序列。重组rcom蛋白可以是全长rcom(诸如seq id no:1的rcom),或者可以是截短的rcom,诸如由hbd组成或基本上由hbd组成的rcom。在一些特定实例中,重组rcom蛋白在n-端或c-端包括亲和标签,诸如可切割的亲和标签。
10.进一步提供了包含本文公开的重组rcom蛋白的药物组合物。在一些实施方案中,药物组合物还包含还原剂或氧化剂。
11.本文还提供了一种从血液或动物组织中的血红蛋白、肌红蛋白或线粒体(细胞色素c氧化酶)中去除一氧化碳的体外方法。在一些实施方案中,该方法包括使血液或动物组织与有效量的本文公开的重组rcom蛋白接触。
12.进一步提供了治疗对象的碳氧血红蛋白血症的方法。在一些实施方案中,该方法包括向对象施用治疗有效量的本文公开的重组rcom蛋白或药物组合物。在一些实例中,重组rcom蛋白作为包含还原剂的药物组合物施用。
13.还提供了治疗对象的氰化物中毒的方法。在一些实施方案中,该方法包括向对象施用治疗有效量的本文公开的重组rcom蛋白或药物组合物。在一些实例中,rcom蛋白处于其氧化形式。
14.进一步提供了治疗对象的硫化氢(h2s)中毒的方法。在一些实施方案中,该方法包括向对象施用治疗有效量的本文公开的重组rcom蛋白或药物组合物。在一些实例中,rcom蛋白处于其还原形式。
15.进一步提供了置换对象中的血液的方法。在一些实施方案中,该方法包括向对象施用治疗有效量的本文公开的重组rcom蛋白或药物组合物。
16.本公开的前述及其他目的和特征将从参照附图进行的如下详细描述而变得更明显。
附图说明
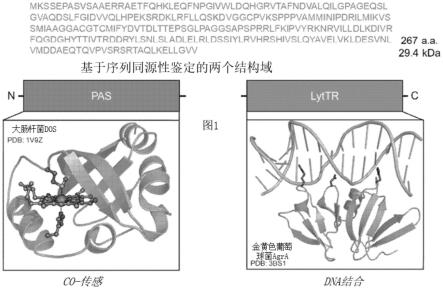
17.图1:示出来自p.xenovorans的rcom-1直系同源物的氨基酸序列(seq id no:1)。rcom-1含有pas结构域(seq id no:1的第1-154位残基)和lyttr结构域(seq idno:1的第155-267位残基)。还示出了来自其他细菌的同源pas和lyttr结构域的晶体结构。pas结构域结构来自大肠杆菌(e.coli)中的直接氧传感(dos)蛋白(kurokawa et al.,j biol chem 279(19):20186-20193,2004),lyttr结构域结构来自金黄色葡萄球菌(s.aureus)中的转录因子agra(sidote et al.,structure 16(5):727-735,2008)。
18.图2:来自p.xenovorans的rcom-1的氨基酸序列被截短为仅包括pas co结合结构域并且没有n端甲硫氨酸(seq id no:2的第2-154位残基)。血红素结合残基以粗体显示。还示出了rcom-1中血红素配位环境的示意图。
19.图3:来自p.xenovorans的rcom-1的氨基酸序列被进一步截短为仅包括pas co结合结构域的关键区域(seq id no:3)。血红素结合残基以粗体显示(h74、c75和m104,参考seq id no:1编号)。还示出了来自大肠杆菌dos蛋白的pas结构域与使用i-tasser在线建模服务器得到的rcom-1pas结构域的同源模型的结构比对。破折号表示建议的截短位点的位置。血红素结合残基显示为虚线。
20.图4:在37℃的有氧条件、wt全长rcom-1的存在下,使用停流uv-vis光谱法测量的
hbd(图12d)中rcom血红素结合结构域(hbd)截短物的电子吸收(uv-vis)光谱比较。示出了三价铁(fe(iii))、脱氧亚铁(fe(ii))、和亚铁-co物质(fe(ii)-co)以及氧化亚铁(fe(ii)-o2)的光谱。
29.图13a-13c:met104变体cc m104a(图13a)和cc m104h(图13b)中rcom hbd截短物质的电子吸收(uv-vis)光谱比较,均携带cys94。示出了三价铁(fe(iii)、脱氧亚铁(fe(ii))、和亚铁-co物质(fe(ii)-co)以及氧化亚铁(fe(ii)-o2)的光谱。(图13c)rcom的蛋白质来源的配体转换机制的示意图,突出了这些变体中的配位层变化。
30.图14a-14d:met104变体ccc m104a(图14a)、ccc m104l(图14b)和ccc m104h(图14c)中的rcom hbd截短物质的电子吸收(uv-vis)光谱比较,均具有cys94
→
ser取代。示出了三价铁(fe(iii)、脱氧亚铁(fe(ii))、和亚铁-co物质(fe(ii)-co)以及氧化亚铁(fe(ii)-o2)的光谱。(图14d)rcom的蛋白质来源的配体转换机制的示意图,突出了这些变体中的配位层变化。
31.图15a-15d:rcom hbd截短物中氧结合亲和力(p
50
)的量化。使用配备有光学比色皿的眼压计设备,采用uv-vis光谱法测量与氧结合的血红蛋白的分数作为氧分压的函数。(图15a)cc hbd rcom变体的uv-vis特征的代表性光谱变化作为氧分压(p
o2
)的函数。cc hbd(图15b)、c94s hbd(图15c)和ccc hbd(图15d)的氧结合曲线,以无氧(脱氧)血红蛋白和氧结合(氧+fe(iii))血红蛋白的分数绘制。低氧张力下的自氧化可能是形成一些铁血红素的原因。将曲线拟合至非线性单位点结合模型以量化p
50
。
32.图16a-16d:co结合(k
on
,co)rcom wt hbd(图16a)和hbd截短物cc hbd(图16b)、c94s(图16c)和ccc hbd(图16d)的二级速率常数的测定。使用停流uv-vis光谱测量每个co浓度下的co结合速率并拟合至单指数。每个数据点代表这些速率的2至3次重复测量的平均值。对每条曲线应用线性回归,并将二阶速率常数估计为斜率。
33.图17a-17c:wt hbd rcom截短物的自氧化速率(k
oxid
)的代表性测定。(图17a)fe(iii)和fe(ii)-o2蛋白的参考光谱。(图17b)fe(ii)-o2wt hbd的uv-vis特征的光谱变化。(图17c)将542nm和573nm处的光谱变化拟合至单指数以确定k
oxid
。
34.图18:wt rcom和rcom hbd变体c94s、cc hbd和ccc hbd的配体结合参数和血红素稳定性特性的总结。
35.图19a-19b:在37℃于尿素的存在下fe(iii)ccc hbd rcom的代表性解折叠。(图19a)通过在415nm血红素索雷最大值处的吸光度变化监测解折叠。在记录每个uv-vis光谱之前,使样品平衡10分钟。(图19b)将解折叠数据拟合至s形曲线以确定一半蛋白质样品解折叠时的变性剂浓度([d]
50
)。
[0036]
图20a-20d:rcom hbd截短物与过氧化氢之间缺乏反应性。在ph 7.4、25℃下用500μm过氧化氢孵育fe(iii)wt hbd(图20a)和变体ccc hbd(图20b)、ccc m104ahbd(图20c)和ccc m104h hbd(图20d),并在30分钟内每2分钟通过uv-vis光谱进行监测。每个变体都观察到最小的光谱变化,这表明过氧化氢不与rcom hbd截短物的fe(iii)血红素中心反应以产生高度氧化的物质。
[0037]
图21a-21c:全长和hbd截短rcom变体的亚硝酸盐还原数据总结。在37℃、2.5mm连二亚硫酸钠的存在下用1-5mm亚硝酸钠孵育亚铁蛋白(10-15μm)。(图21a)采用uv-vis光谱监测fe(ii)血红素向fe(ii)-no的转化。(图21b-21c)将562nm和578nm处的光谱特征变化拟
合至单指数曲线以确定观察到的亚硝酸盐还原速率。将观察到的速率绘制为亚硝酸盐浓度的函数,将线性回归应用于每幅图,将二阶速率常数估计为斜率。
[0038]
图22a-22d:在37℃、有氧条件下,体外co从血红蛋白(hb)转移到wt rcom hbd(图22a)和rcom hbd变体cc hbd(图22b)、c94s hbd(图22c)和ccc hbd(图22d)的代表性动力学轨迹。将结合co的hb(20μm)与等摩尔含氧铁rcom一起孵育,并利用uv-vis光谱监测从hb到rcom的co转移。使用光谱反卷积确定每种co结合血红蛋白的分数,并将相应的动力学轨迹拟合至单指数或双指数方程。示出了每种与co结合的物质的半衰期,其中对于拟合至双指数的曲线示出了快速的物质半衰期和振幅。
[0039]
图23a-23b:在37℃、有氧条件下监测从红细胞(rbc)包裹的hbco到细胞外rcom hbd截短物的co转移的动力学轨迹。在等摩尔浓度(50-100μm)下孵育血红蛋白,并在每个时间点通过离心从细胞外rcom中分离rbc。采用uv-vis光谱监测从hb到wt hbd rcom(图23a)和c94s hbd rcom(图23b)的co转移。使用光谱反卷积确定每种co结合血红蛋白的分数,并将相应的动力学轨迹拟合至单指数方程。数据点代表3次试验的平均值
±
sem,并示出了每个实验中cohb的半衰期。
[0040]
图24:c94s和ccc hbd rcom变体在体内致死co中毒模型中从hbco中清除co。小鼠严重co中毒体内模型示意图(上图)。将经麻醉、机械通气的小鼠暴露于空气中3,000ppm co 4.5分钟,然后以10μl/g体重的注射体积静脉内输注fe(ii)-o
2 ccc hbd rcom(表中列出的血红蛋白浓度,下图)。在输注之前和之后立即抽取血液样品(15μl),以及在co暴露后25分钟抽取血液样品。在每个时间点,通过离心从血浆中分离rbc,立即将分离的rbc沉淀和血浆样品在-80℃冷冻。随后,使用光谱反卷积确定来自rbc的co结合血红蛋白的分数(%hbco)和co结合rcom的分数(%rcom-co)。与输注pbs相比,输注rcom导致co结合hb的分数(δ%hbco)下降更大。
[0041]
序列表
[0042]
随附序列表中列出的核酸和氨基酸序列使用标准字母缩写表示核苷酸碱基,使用三字母代码表示氨基酸,如37c.f.r.1.822中所定义的那样。仅示出了每个核酸序列的一条链,但应当理解互补链包括在对所示链的任何引用中。序列表创建于2021年5月3日,以ascii文本文件提交,大小为18.7kb,该序列表通过引用并入本文。在随附的序列表中:
[0043]
seq id no:1是来自p.xenovorans的全长wt rcom-1的氨基酸序列。
[0044]
seq id no:2是没有lyttr结构域的截短rcom-1(hbd16)的氨基酸序列。
[0045]
seq id no:3是没有lyttr结构域和部分pas结构域的截短rcom-1(hbd12)的氨基酸序列。
[0046]
seq id no:4是来自h.crassostreae的wt rcom的氨基酸序列。
[0047]
seq id no:5是来自烟草蚀纹病毒(tev)的切割位点的氨基酸序列。
[0048]
seq id no:6是来自凝血酶的切割位点的氨基酸序列。
[0049]
seq id no:7是rcom变体c94s hbd的氨基酸序列。
[0050]
seq id no:8是rcom变体c127s/c130s hbd的氨基酸序列。
[0051]
seq id no:9是rcom变体ccc hbd的氨基酸序列。
[0052]
seq id no:10是rcom变体cc m104a hbd的氨基酸序列。
[0053]
seq id no:11是rcom变体cc m104h hbd的氨基酸序列。
[0054]
seq id no:12是rcom变体ccc m104a hbd的氨基酸序列
[0055]
seq id no:13是rcom变体ccc m104h hbd的氨基酸序列。
[0056]
seq id no:14是rcom变体ccc m104l hbd的氨基酸序列。
[0057]
发明详述
[0058]
i.缩略语
[0059]
co
ꢀꢀꢀꢀꢀꢀꢀ
一氧化碳
[0060]
h2s
ꢀꢀꢀꢀꢀꢀ
硫化氢
[0061]
hb
ꢀꢀꢀꢀꢀꢀꢀ
血红蛋白
[0062]
hb-co
ꢀꢀꢀꢀ
碳氧血红蛋白
[0063]
hboc
ꢀꢀꢀꢀꢀ
血红蛋白基氧载体
[0064]
hbd
ꢀꢀꢀꢀꢀꢀ
血红素结合结构域
[0065]
no
ꢀꢀꢀꢀꢀꢀꢀ
一氧化氮
[0066]
rcom
ꢀꢀꢀꢀꢀ
一氧化碳代谢调节因子
[0067]
tev
ꢀꢀꢀꢀꢀꢀ
烟草蚀纹病毒
[0068]
wt
ꢀꢀꢀꢀꢀꢀꢀ
野生型
[0069]
ii、术语和方法
[0070]
除非另有说明,否则按照常规用法使用技术术语。分子生物学中常用术语的定义可见于benjamin lewin,genes x,2009,由jones&bartlett publishers出版;和meyers等人(编著),the encyclopedia of cell biology and molecular medicine,第16卷,2008,由wiley-vch出版;以及其他相似的参考资料。
[0071]
如本文所用,单数形式“一”、“一个/种”和“所述/该”指单数和复数两者,上下文另有明确说明除外。例如,术语“一种抗原”包括单个或多个抗原并且可以被认为等同于短语“至少一种抗原”。如本文所用,术语“包含”是指“包括”。还应当理解,对于核酸或多肽给出的任何和所有碱基大小或氨基酸大小,以及所有分子量或分子质量值都是近似的,并且提供用于描述目的,另有说明除外。尽管可以使用与本文描述的那些相似或等效的许多方法和材料,但本文对特别合适的方法和材料进行了描述。如有矛盾,以本说明书(包括术语解释)为准。此外,材料、方法和实施例仅是说明性的而无意于限制。
[0072]
为了便于查阅各种实施方案,提供了如下术语解释:
[0073]
施用:通过任何有效途径向对象提供或给予药剂,诸如治疗剂(例如重组rcom蛋白)。示例性施用途径包括但不限于注射或输注(诸如皮下、肌内、皮内、腹膜内、鞘内、静脉内、脑室内、纹状体内、颅内和进入脊髓)、口服、导管内、舌下、直肠、经皮、鼻内、阴道和吸入途径。
[0074]
亲和标签:添加到重组蛋白或多肽中的肽序列,以辅助使用基于亲和力的纯化技术(诸如亲和层析)进行纯化。亲和标签的实例包括但不限于白蛋白结合蛋白、碱性磷酸酶、au1表位、au5表位、噬菌体t7表位、噬菌体v5表位、生物素-羧基载体蛋白、蓝舌病毒标签、钙调蛋白结合肽、氯霉素乙酰基转移酶、纤维素结合结构域、几丁质结合结构域、胆碱结合结构域、二氢叶酸还原酶、e2表位、flag表位、半乳糖结合蛋白、绿色荧光结合蛋白、glu-glu(e-e标签)、谷胱甘肽s-转移酶、流感血凝素、halo组氨酸亲和标签、辣根过氧化物酶、hsv表位、酮类固醇异构酶、kt3表位、lacz、萤光素酶、麦芽糖结合蛋白、myc表位、nusa、
pdz结构域、pdz配体、聚精氨酸、聚天冬氨酸、聚半胱氨酸、聚组氨酸、聚苯丙氨酸、profinitye xact、蛋白c、s1-标签、s标签、葡萄球菌蛋白a(蛋白a)、葡萄球菌蛋白g(蛋白g)、strep-标签、链霉亲和素、小泛素样修饰剂(sumo)、硫氧还蛋白、trpe、泛素和vsv-g(参见例如kimple et al.,curr protoc protein sci 73:9.9.1-.9.9.23,2013,doi:10.1002/0471140864.ps0909s73)。
[0075]
贫血:缺乏红细胞和/或血红蛋白。贫血是最常见的血液疾患,其导致血液向组织输送氧的能力降低。由于所有人类细胞的生存都依赖于氧,因此不同程度的贫血会产生广泛的临床后果。贫血主要的三种类型包括失血过多(急性失血诸如出血或因低容量失血而导致的慢性失血)、血细胞破坏过度(溶血)或红细胞生成不足(无效造血)。
[0076]
术语“贫血”是指所有类型的临床贫血,包括但不限于:小红细胞性贫血、缺铁性贫血、血红蛋白病、血红素合成缺陷、珠蛋白合成缺陷、铁粒幼细胞缺陷、正常红细胞性贫血、慢性病性贫血、再生障碍性贫血、溶血性贫血、大细胞性贫血、巨幼细胞性贫血、恶性贫血、二形性贫血、早产儿贫血、范可尼贫血、遗传性球形红细胞增多症、镰状细胞性贫血、温性自身免疫性溶血性贫血、冷凝集素溶血性贫血。
[0077]
在严重的贫血或持续失血的情况下,可能需要输血。医生可以使用许多临床上接受的标准中的任何一个来确定输血对于治疗患有贫血的对象而言是必要的。例如,目前接受的用于脓毒症早期目标导向疗法的rivers方案要求将血细胞比容保持在30以上。
[0078]
缺氧:身体作为一个整体或身体区域完全缺乏氧供应的一种病理状态。
[0079]
解毒剂:中和或抵消有毒物(诸如一氧化碳)的作用的药剂。
[0080]
出血性疾患:导致血液凝固不良和持续出血的各种医学问题的总称。医生还利用诸如凝血病、异常出血和凝血障碍等术语来指示出血性疾患。出血性疾患包括导致异常(或病理性)出血的任何先天性、获得性或诱导性缺陷。实例包括但不限于凝血或止血不足的疾患,诸如血友病a(缺乏因子viii)、血友病b(缺乏因子ix)、血友病c(缺乏因子xi)、其他凝血因子缺乏症(诸如因子vii或因子xiii)、凝血因子抑制剂水平异常、血小板疾患、血小板减少症、维生素k缺乏症和维勒布兰德氏病(von willebrand’s disease)。
[0081]
出血发作:指发生不受控制的、过度的和/或病理性出血。出血发作可以由例如药物引起的出血(诸如由非甾体抗炎药或华法林引起的出血)、抗凝剂过量或中毒、动脉瘤、血管破裂、手术和外伤(包括例如擦伤、挫伤、撕裂伤、切口或枪伤)导致。出血发作也可能由癌症、胃肠道溃疡等疾病或由感染引起。
[0082]
血液置换品或血液替代品:用于在心血管系统中填充流体体积和/或携带氧及其他血气的组合物。血液替代品包括例如扩容剂(用于增加血容量)和氧治疗剂(用于输送血液中的氧)。氧疗法包括例如基于血红蛋白的氧载体(hboc)和全氟化碳(pfc)。优选的血液替代品模拟血红蛋白的携氧能力、不需要交叉匹配或相容性测试、保质期长、表现出血管内半衰期长(经数天和数周)且无副作用和病原体。
[0083]
一氧化碳(co):一种无色、无臭、无味的气体,其在浓度足够高时对人类和动物有毒。在正常动物新陈代谢过程中也会产生低水平的co。
[0084]
碳氧血红蛋白(hbco):一氧化碳(co)和血红蛋白(hb)的稳定络合物,在正常代谢过程中吸入或产生co时在红细胞中形成。
[0085]
碳氧血红蛋白血症或一氧化碳中毒:由于血液中存在过量的一氧化碳而导致的病
症。通常,暴露于百万分之100份(ppm)或更高的co足以导致碳氧血红蛋白血症。轻度急性co中毒的症状包括头晕、意识错乱、头痛、眩晕和流感样反应;较大量的暴露可导致中枢神经系统和心脏的显著毒性,甚至死亡。急性中毒后,常出现长期后遗症。一氧化碳也会对孕妇的胎儿产生严重影响。长期暴露于低水平的一氧化碳可导致抑郁、意识错乱和记忆力丧失。一氧化碳主要通过在血液中与血红蛋白结合形成碳氧血红蛋白(hbco)对人体造成不良影响。这会阻止氧与血红蛋白结合,降低血液的携氧能力,导致缺氧。此外,认为肌红蛋白和线粒体细胞色素氧化酶受到不利影响。碳氧血红蛋白可以还原为血红蛋白,但该还原需要时间,因为hbco复合物相当稳定。目前治疗co中毒的方法包括施用100%氧或提供高压氧治疗。
[0086]
脑缺血或缺血性中风:当通往大脑或大脑中的动脉部分地或完全地阻塞致使组织的氧需求超过供应的氧时发生的病症。缺血性中风后缺乏氧及其他营养物质,大脑会因中风而受损。
[0087]
凝血病:身体的凝血机制缺陷的医学术语。
[0088]
接触:置于直接物理性关联;包括固体和液体两种形式。当在体内方法的上下文中使用时,“接触”还包括施用。
[0089]
氰化物中毒:由于暴露于一些形式的氰化物诸如氰化氢气体和氰化物盐而导致的一种中毒。氰化物中毒可能因吸入房屋火灾产生的烟雾、暴露于金属抛光剂、特定杀虫剂和某些种子(诸如苹果种子)而发生。氰化物中毒的早期症状包括头痛、头晕、心率加快、呼吸急促和呕吐。后期症状包括发作、心率减慢、低血压、丧失意识和心脏骤停。
[0090]
细胞色素c氧化酶:一种酶,是呼吸电子传递链的一部分。该酶见于线粒体中。
[0091]
蚕豆病:葡萄糖-6-磷酸脱氢酶(g6pd)缺乏症的俗称;一种x连锁隐性遗传病,特征为对多种病因作出反应的非免疫性溶血性贫血。
[0092]
融合蛋白:包含两种不同(异源)蛋白质的至少一部分的蛋白质。
[0093]
胃肠道出血:指胃肠道中从咽部到直肠的任何形式的出血(失血)。
[0094]
血红蛋白(hb):脊椎动物及其他动物血液的红细胞中的含铁氧转运金属蛋白。在人类中,血红蛋白分子是四个球状蛋白质亚基的集合体。每个亚基由与非蛋白质血红素基团紧密结合的蛋白质链构成。每条蛋白质链排列成一组以珠蛋白折叠排列连接在一起的α-螺旋结构片段,之所以这么称呼是因为这种排列与其他血红素/珠蛋白中使用的折叠基序相同。这种折叠图案包含紧密结合血红素基团的口袋(pocket)。
[0095]
基于血红蛋白的氧载体(hboc):一种可输注的经纯化、重组和/或修饰的血红蛋白流体,起氧载体的作用,并且可用作血液替代品。许多hboc是已知的和/或正在临床开发中。hboc的实例包括但不限于dclhb(hemassist
tm
;baxter)、mp4(hemospan
tm
;sangart)、吡氧基化hb poe
–
缀合物(php)+过氧化氢酶&sod(apex biosciences)、o-r-polyhba0(hemolink
tm
;hemosol)、polybvhb(hemopure
tm
;biopure)、polyhb(polyheme
tm
;northfield)、rhb1.1(optrotm;somatogen)、peg-血红蛋白(enzon)、oxyvita
tm
和hboc-201(greenburg and kim,crit care 8(suppl 2):s61-s64,2004;te lintel hekkert et al.,am j physiol heart circ physiol 298:h1103-h1113,2010;eisenach,anesthesiology 111:946-963,2009)。
[0096]
血友病:若干遗传性基因疾病的名称,这些疾病会损害身体控制凝血的能力。
[0097]
出血:循环系统的血液流失。出血可能发生在内部,血液从体内的血管渗漏,或者
可能发生在外部,通过阴道、口腔或直肠等天然开口,或者通过皮肤破裂。
[0098]
异源:异源蛋白质或多肽是指源自不同来源或物种的蛋白质或多肽。
[0099]
硫化氢中毒:一种由过量暴露于硫化氢(h2s)引起的中毒。h2s结合线粒体细胞色素酶中的铁并阻止细胞呼吸。暴露于较低浓度的h2s可导致眼部刺激、喉咙痛、咳嗽、恶心、气短、肺水肿、疲劳、食欲不振、头痛、易怒、记忆力差和头晕。更高水平的暴露可导致立即崩溃、无法呼吸和死亡。
[0100]
出血性休克:组织灌注减少导致细胞功能所必需的氧和营养物质输送不足的一种病症。低血容量性休克是最常见的类型,由临床病因引起的循环血容量减少导致,诸如穿透性和钝性创伤、胃肠道出血和产科出血。
[0101]
低氧血症:动脉血氧浓度异常不足。
[0102]
缺氧:身体整体(全身性缺氧)或身体部位(组织缺氧)缺乏足够的氧供应的病理性状况。
[0103]
缺血:一种血管现象,其中身体器官、组织或部位的血液供应减少是由例如一条或多条血管的收缩或阻塞引起的。缺血有时由血管收缩或血栓形成或栓塞引起。缺血可因供氧减少造成细胞死亡而导致直接缺血性损伤、组织损伤。
[0104]
缺血/再灌注损伤:除了血流剥夺期间发生的直接损伤外,缺血/再灌注损伤还涉及血流恢复后发生的组织损伤。目前的理解是,这种损伤大部分是由化学产品和释放到缺血组织中的自由基引起的。
[0105]
当组织经受缺血时,会引发一系列化学事件,最终可能导致细胞功能障碍和坏死。如果通过恢复血流来结束缺血,则继而发生第二系列的损伤性事件,从而产生额外的损伤。因此,每当对象的血流出现短暂的减少或中断时,所产生的损伤涉及两个部分—在缺血间隔期间发生的直接损伤和随后的间接或再灌注损伤。当缺血持续时间较长时,由缺氧引起的直接缺血性损伤占主导。对于持续时间较短的缺血,间接或再灌注介导的损伤变得越来越重要。在一些情况下,再灌注产生的损伤可能比缺血本身引起的损伤更严重。这种直接和间接机制造成的损伤的相对贡献模式已被证明发生在所有器官中。
[0106]
分离的:“分离的”生物成分(诸如核酸分子、蛋白质或细胞)已与生物体的细胞、血液或组织或生物体本身中的其他生物成分基本上分离或纯化,其中该成分是天然存在的,诸如其他染色体和染色体外的dna和rna、蛋白质和细胞。已“分离”的核酸分子和蛋白质包括通过标准纯化方法纯化的那些。该术语还包括通过在宿主细胞中重组表达制备的核酸分子和蛋白质以及化学合成的核酸分子和蛋白质。
[0107]
高铁血红蛋白:血红蛋白的氧化形式,其中血红素成分中的铁已从亚铁(+2)态氧化为三价铁(+3)态。这使得血红蛋白分子无法有效地将氧输送和释放到组织中。通常,高铁血红蛋白形式占总血红蛋白的约1%。
[0108]
小红细胞症:一种以血液中存在小红细胞(异常地小的红细胞)为特征的血液疾患。
[0109]
肌红蛋白:见于脊椎动物和大多数哺乳动物的肌肉组织中的一种含血红素的珠蛋白。肌红蛋白在肌肉细胞中携带和存储氧。
[0110]
氧化剂:能够从另一种物质接受电子的物质(也称为“氧化”物质)。氧化剂获得电子并在化学反应中被还原。氧化剂也称为“电子受体”。在本文的一些实施方案中,氧化剂是
醌,诸如苯醌或萘醌。在另一些实施方案中,氧化剂是含氧气体混合物、含氧液体混合物、铁氰化物盐或其任意组合。在一些实例中,电子介体(例如tmpd或结晶紫)与氧化剂组合使用以促进电子转移。在本文的一些实施方案中,rcom的氧化通过暴露于可见光来进行。
[0111]
paraburkholderia xenovorans:一种见于土壤中的变形菌。p.xenovorans是革兰氏阴性需氧菌。p.xenovorans具有9.7mb的已知最大的原核基因组之一。该细菌能够有效降解多氯联苯(pcb)。p.xenovorans也称为burkholderia xenovorans。
[0112]
肽或多肽:一种聚合物,其中单体是通过酰胺键连接在一起的氨基酸残基。当氨基酸是α-氨基酸时,可以使用l-旋光异构体或d-旋光异构体,优选l-异构体。如本文所用,术语“肽”、“多肽”或“蛋白质”旨在涵盖任何氨基酸序列并且包括经修饰的序列,包括经修饰的rcom蛋白。术语“肽”和“多肽”特别地旨在涵盖天然存在的蛋白质,以及重组地或合成地产生的蛋白质。
[0113]
保守性氨基酸取代是在进行时对原始蛋白质的性质干扰最小的那些取代,即蛋白质的结构和特别是功能是保守性的,并且不会因这样的取代而显著地改变。保守性取代的实例示于下表中。
[0114][0115]
保守性取代通常维持(a)取代区域中多肽骨架的结构,例如,作为折叠或螺旋构象,(b)分子在靶位点的电荷或疏水性,或(c)侧链的体积(bulk)。
[0116]
通常预期蛋白质性质产生最大变化的取代是非保守性的,例如如下变化:其中(a)亲水性残基例如丝氨酸或苏氨酸取代(或被取代成)疏水性残基例如亮氨酸、异亮氨酸、苯丙氨酸、缬氨酸或丙氨酸;(b)半胱氨酸或脯氨酸取代(或被取代成)任何其他残基;(c)具有正电侧链的残基例如赖氨酸、精氨酸或组氨酸取代(或被取代成)电负性残基例如谷氨酰胺或天冬氨酸;或者(d)具有大侧链的残基例如苯丙氨酸取代(被取代成)不具有侧链的残基,
例如甘氨酸。
[0117]
可药用载体:使用的可药用载体是常规的。remington:the science and practice of pharmacy,the university of the sciences in philadelphia,editor,lippincott,williams,&wilkins,philadelphia,pa,第21版(2005)描述了适用于本文公开的蛋白质及其他组合物的药物递送的组合物和制剂。一般而言,载体的性质将取决于所采用的特定施用方式。例如,肠胃外制剂通常包含可注射流体,其包括药学和生理学上可接受的流体诸如水、生理盐水、平衡盐溶液、葡萄糖水溶液、甘油等作为载剂。对于固体组合物(诸如粉末、丸剂、片剂或胶囊形式),常规的无毒固体载体可以包括例如药物级的甘露醇、乳糖、淀粉或硬脂酸镁。除了生物学中性载体之外,待施用的药物组合物可以含少量无毒辅助物质,诸如润湿剂或乳化剂、防腐剂和ph缓冲剂等,例如乙酸钠或脱水山梨糖醇单月桂酸酯。
[0118]
预防、治疗或改善疾病:“预防”疾病是指抑制疾病的全面发展。“治疗”是指在疾病或病理病症开始发展后改善其体征或症状的治疗性干预,诸如降低co中毒的对象血液中的hbco。“改善”是指降低疾病体征或症状的数量或严重程度。
[0119]
纯化的:术语纯化的不要求绝对纯度;而是其为相对术语。因此,例如,纯化的肽制剂是其中肽或蛋白质比在细胞内的其天然环境中的肽或蛋白质更富集的一种。在一个实施方案中,纯化制剂以使蛋白质或肽占制剂的总肽或蛋白质含量的至少50%。基本上纯化是指从其他蛋白质或细胞成分纯化。基本上纯化的蛋白质的纯度为至少60%、70%、80%、90%、95%或98%。因此,在一个特定的非限制性实例中,基本上纯化的蛋白质的90%不含其他蛋白质或细胞成分。
[0120]
重组:重组核酸或蛋白质是具有非天然存在的序列或具有通过人工组合两个否则分开的序列片段而产生的序列的核酸或蛋白质。这种人工组合通常通过化学合成或通过人工操作分离的核酸片段来完成,例如通过基因工程技术。术语重组包括已通过添加、取代或缺失天然核酸分子或蛋白质的一部分而改变的核酸和蛋白质。
[0121]
还原剂:在氧化还原化学反应中失去(或“贡献”)电子给另一化学物质的元素或化合物。还原剂通常处于其可能的较低氧化态之一,并且被称为电子供体。还原剂被氧化,因为它在氧化还原反应中失去电子。示例性还原剂包括但不限于连二亚硫酸钠、抗坏血酸、n-乙酰半胱氨酸、亚甲蓝、谷胱甘肽、细胞色素b5/b5-还原酶、肼苯哒嗪、土金属、甲酸和亚硫酸盐化合物。
[0122]
一氧化碳代谢调节因子(rcom):见于一些原核生物中的参与co传感和转录调节的蛋白质。rcom蛋白含n端pas结构域和结合dna的lyttr结构域。pas结构域包含六配位的b型血红素部分,其与co和一氧化氮(no)紧密结合。pas结构域的残基his74和met104用作血红素fe(ii)轴向配体,在结合co或no后met104发生置换。需氧革兰氏阴性菌paraburkholderia xenovorans(也称为burkholderia xenovorans)表达两种同源蛋白rcom-1和rcom-2,它们具有约93%的序列同一性并且对co具有非常高的亲和力。rcom-1和rcom-2用作能够调节需氧co氧化和厌氧co氧化的co传感物。p.xenovorans rcom-1的野生型氨基酸序列在本文中如seq id no:1所示。来自多种细菌物种的rcom同源物(和uniprot id)列于表3中。
[0123]
横纹肌溶解症:由于创伤性损伤,包括机械、物理或化学损伤,骨骼肌组织快速分
解。主要结果是肌酸磷酸激酶及其他细胞副产物大量释放到血液系统中,以及由于肌肉分解产物的积累导致的急性肾功能衰竭,其中一些肌肉分解产物对肾脏有害。
[0124]
序列同一性/相似性:两条或更多条核酸序列或者两条或更多条氨基酸序列之间的同一性以序列之间的同一性或相似性表示。序列同一性可以用同一性百分比来量度;百分比越高,序列同一性越高。序列相似性可以用相似性百分比来量度(考虑保守性氨基酸取代);百分比越高,序列越相似。当使用标准方法进行比对时,核酸或氨基酸序列的同源物或直向同源物具有相对高度的序列同一性/相似性。与相关性更远的物种(诸如人序列和秀丽隐杆线虫(c.elegans)序列)相比,当直系同源蛋白质或cdna源自更密切相关的物种(诸如人序列和小鼠序列)时,该同源性更显著。
[0125]
用于比较的序列比对方法在本领域中是公知的。各种程序和比对算法描述于:smith&waterman,adv.appl.math.2:482,1981;needleman&wunsch,j.mol.biol.48:443,1970;pearson&lipman,proc.natl.acad.sci.usa 85:2444,1988;higgins&sharp,gene,73:237-44,1988;higgins&sharp,cabios 5:151-3,1989;corpet et al.,nuc.acids res.16:10881-90,1988;huang et al.computer appls.in the biosciences 8,155-65,1992;和pearson et al.,meth.mol.bio.24:307-31,1994.altschul et al.,j.mol.biol.215:403-10,1990示出对序列比对方法和同源性计算的详细考虑。
[0126]
ncbi basic local alignment search tool(blast)(altschul et al.,j.mol.biol.215:403-10,1990)可从若干来源获得,包括国家生物信息中心(ncbi)和互联网,与序列分析程序blastp、blastn、blastx、tblastn和tblastx结合使用。更多信息可在ncbi网站找到。
[0127]
球形细胞增多症:一种自身溶血性贫血,其特征是产生球形而非甜甜圈形的血红细胞(或红细胞)。
[0128]
对象:活的多细胞生物,包括脊椎动物生物,这一类别包括人类和非人类哺乳动物。
[0129]
地中海贫血:一种遗传性常染色体隐性遗传血液病。在地中海贫血中,遗传缺陷导致构成血红蛋白的珠蛋白链之一的合成速率降低。珠蛋白链之一的合成减少导致形成异常的血红蛋白分子,这进而导致贫血,这是地中海贫血的特征性症状。
[0130]
治疗有效量:化合物或组合物例如分离的或重组的rcom蛋白的足以在接受治疗的对象中实现期望效果的量。例如,其可以是清除血液或组织中的一氧化碳、降低血液中的hbco水平和/或减少与一氧化碳中毒相关的一种或多种体征或症状所需的量。
[0131]
溃疡:皮肤、眼睛或粘膜的开放性疼痛,通常但不完全是由最初的擦伤引起,通常因炎症、感染和/或阻碍愈合的医学状况维持。
[0132]
血管痉挛:中风的原因之一;继发于供应大脑的血管痉挛。这种类型的中风通常发生在蛛网膜下腔动脉瘤出血后,并在出血事件后2至3周内延迟发展为血管痉挛。类似类型的中风可能会使镰状细胞病复杂化。
[0133]
iv.重组rcom蛋白
[0134]
需要一种有效、快速和容易获得的疗法来治疗碳氧血红蛋白血症。本公开提供了重组一氧化碳代谢调节因子(rcom)蛋白,其对一氧化碳表现出非常高的亲和力,因此可以用作co清除剂。所公开的rcom蛋白也可用于治疗硫化氢或氰化物中毒,或者可以用作血液
替代品。
[0135]
rcom蛋白首先被鉴定为co传感细菌转录调节因子,其将n端pas折叠结构域与c端dna结合lyttr结构域偶联(见图1)。rcom蛋白含有六配位的b型血红素部分,其与co和一氧化氮(no)紧密结合。pas结构域残基his74和met104(相对于seq id no:1)用作血红素fe(ii)轴向配体,在结合co或no时置换met104。来自p.xenovorans的两个rcom同系物(rcom-1和rcom-2)在体内具有功能,并且用作能够调节有氧co氧化和厌氧co氧化的co传感物。
[0136]
rcom对co表现出非常高的亲和力并且对co的选择性高于对氧的选择性。鉴于这些特性,所公开的rcom蛋白对于直接从结合co的血红蛋白、肌红蛋白和细胞色素c氧化酶清除co以治疗一氧化碳中毒而言是理想的。所公开的rcom蛋白也可用于治疗氰化物或h2s中毒,或者用作血液替代品。本文进一步描述了定向突变以增强rcom蛋白的稳定性、增加co亲和力和/或降低氧亲和力。
[0137]
野生型(wt)的和经修饰的rcom蛋白如下文所述。在wt氨基酸序列(seq idno:1)中,lyttr结构域(结合dna)加有下划线;该序列的其余部分是pas结构域(见图1)。本文公开的截短的rcom蛋白(seq id no:2、3和7-14)不包含lyttr结构域(参见图2和3)。在所有rcom序列(seq id no:1-3和7-14)中,粗体残基对应于h74、c94、m104、c127、c130和m105,相对于seq id no:1编号。
[0138]
来自p.xenovorans的wt rcom-1(29kda):
[0139][0140]
hbd16 rcom(16kda)截短序列:
[0141][0142]
hbd12 rcom(12kda)截短序列:
[0143][0144]
在本公开内容通篇中,除非另有说明,否则特定氨基酸残基参考seq id no:1的全长wt rcom-1编号。表1列出了seq id no:1-3中每个对应残基的位置。
[0145]
表1.wt和截短的rcom序列中的关键残基
[0146]
[0147][0148]
基于seq id no:2的hbd16产生了八个rcom hbd变体。表2列出了每个变体,以及它们各自的氨基酸取代和完整氨基酸序列(粗体残基表示取代)。
[0149]
表2.rcom hbd16变体
[0150]
[0151][0152]
本文提供了对co表现出非常高的亲和力的重组一氧化碳代谢调节因子(rcom)蛋白。在一些实施方案中,重组rcom蛋白包括血红素结合结构域(hbd),并且hbd的氨基酸序列与seq id no:2具有至少80%、至少85%、至少90%、至少95%、至少96%、至少97%、至少98%或至少99%的同一性。在一些实施方案中,hbd的氨基酸序列是野生型序列(诸如seq id no:2)。在另一些实施方案中,hbd的氨基酸序列在h74、c94、m104、m105、c127和c130中的一个或多个处包含氨基酸取代。在一些实例中,hbd的氨基酸序列与seq id no:2具有至少90%或至少95%的同一性并且包括在c94、m104、c127和c130中的一个或多个处的氨基酸取代。
[0153]
可以修饰公开的rcom蛋白,诸如通过在多个残基处进行氨基酸取代,以改变血红素配体亲和力和/或特异性,和/或增强蛋白质稳定性。在一些实施方案中,rcom蛋白包括单个氨基酸取代。在另一些实施方案中,rcom蛋白包括至少两个、至少三个、至少四个、至少5个或至少6个氨基酸取代。在一些实例中,氨基酸取代是保守性取代。
[0154]
在一些实例中,重组rcom蛋白包括h74处的取代,其为血红素配位组氨酸。在一些特定的非限制性实例中,取代选自h74s、h74t、h74m、h74w、h74a、h74l、h74i、h74v和h74g。
[0155]
在一些实例中,重组rcom蛋白包括c94处的取代,其为fe(ii)血红素配位半胱氨酸。在一些特定的非限制性实例中,取代选自c94s、c94t、c94h、c94w、c94m、c94a、c94l、
c94i、c94v和c94g。
[0156]
在一些实例中,重组rcom蛋白包括m104处的取代,其为fe(ii)血红素配位甲硫氨酸。在一些特定的非限制性实例中,取代选自m104s、m104t、m104h、m104w、m104a、m104l、m104i、m104v和m104g。
[0157]
在一些实例中,重组rcom蛋白包括m105处的取代,其为非血红素配位甲硫氨酸。在一些特定的非限制性实例中,取代选自m105s、m105t、m105h、m105w、m105a、m105l、m105i、m105v和m105g。
[0158]
在一些实例中,重组rcom蛋白包括c127处的取代,其为非血红素配位半胱氨酸。在一些特定的非限制性实例中,取代选自c127s、c127t、c127m、c127a、c127l、c127i、c127v和c127g。
[0159]
在一些实例中,重组rcom蛋白包括c130处的取代,其为非血红素配位半胱氨酸。在一些特定的非限制性实例中,取代选自c130s、c130t、c130m、c130a、c130l、c130i、c130v和c130g。
[0160]
在一些实例中,重组rcom蛋白包括:c94处的单个氨基酸取代;m104处的单个氨基酸取代;c94和m104处的两个氨基酸取代;c127和c130处的两个氨基酸取代;c94、c127和c130处的三个氨基酸取代;m104、c127和c130处的三个氨基酸取代;h74、c94和m104处的三个氨基酸取代;c94、m104、c127和c130处的四个氨基酸取代;c94、m104、m105、c127和c130处的五个氨基酸取代;h74、c94、m104、c127和c130处的五个氨基酸取代;或h74、c94、m104、m105、c127和c130处的六个氨基酸取代。在一些特定的非限制性实例中,重组rcom蛋白包括c94s取代;c127s取代和c130s取代;c94s取代、c127s取代和c130s取代;c94s取代和m104l取代;m104a取代、c127s取代和c130s取代;m104h取代、c127s取代和c130s取代;m104l取代、c127s取代和c130s取代;c94s取代、m104a取代、c127s取代和c130s取代;c94s取代、m104h取代、c127s取代和c130s取代;c94s取代、m104l取代、c127s取代和c130s取代;h74s取代、c94s取代和m104l取代;c94s取代、m104l取代、m105l取代、c127s取代和c130s取代;或h74s取代、c94s取代、m104l取代、m105l取代、c127s取代和c130s取代。
[0161]
在一些特定实例中,rcom蛋白的氨基酸序列包含如下或由如下组成:seq id no:7、seq id no:8、seq id no:9、seq id no:10、seq id no:11、seq id no:12、seq id no:13或seq id no:14。
[0162]
在一些实施方案中,rcom蛋白的氨基酸序列与seq id no:1-3中任一项具有至少80%、至少85%、至少90%、至少95%、至少96%、至少97%、至少98%或至少99%的同一性。在一些实例中,rcom蛋白包含seq id no:1-3中的任一项或由seq id no:1-3中的任一项组成。
[0163]
在一些实例中,rcom蛋白的氨基酸序列包含seq id no:1、seq id no:2或seq id no:3的氨基酸序列或者由seq id no:1、seq id no:2或seq id no:3的氨基酸序列组成,除了h74、c94、m104、c127、c130和m105中的一个或多个处的氨基酸取代。
[0164]
在特定实例中,rcom蛋白的氨基酸序列由seq id no:1组成,除了h74s取代、c94s取代、选自m104a、m104h和m104l的m104取代、m105l取代、c127s取代、c130s取代,或其任意组合。在另一些实例中,蛋白质的氨基酸序列由seq id no:2组成,除了h74s取代、c94s取代、选自m104a、m104h和m104l的m104取代、m105l取代、c127s取代、c130s取代,或其任意组
合。在另一些特定实例中,蛋白质的氨基酸序列由seq id no:3组成,除了h74s取代、c94s取代、选自m104a、m104h和m104l的m104取代、m105l取代、c127s取代、c130s取代,或其任意组合。
[0165]
使用生物信息学分析,鉴定了多种微生物中的112个rcom基因,其中44个与有氧co代谢有关。经鉴定的rcom基因之一来自嗜温微生物(hydrogenophaga crassostreae),认为其表达具有增强的热稳定性的rcom蛋白。因此,在一些实施方案中,重组rcom蛋白是来自表3种列出的物种之一并且具有所列出的uniprot id的蛋白。
[0166]
表3.具有rcom基因同源序列的微生物
[0167]
[0168][0169]
上面列出的rcom同源物的氨基酸序列如同其在2020年5月11日出现在uniprot数据库中时那样以引用方式并入本文。
[0170]
在一些实施方案中,rcom蛋白来自hydrogenophaga crassostreae。在一些实例中,rcom蛋白的氨基酸序列与seq id no:4具有至少80%、至少85%、至少90%、至少95%、至少96%、至少97%、至少98%或至少99%的同一性。在一些实例中,rcom蛋白的氨基酸序列包含seq id no:4或由seq id no:4组成。
[0171]
来自h.crassostreae的全长rcom序列
[0172]
meaevanksplyllekfevgvihldakrtvlamndfarkvlpvgekqpfdklvssfhparskpkvdflldqasscpmvsavpmtmiinipeqvllikvtrladhmgkttgfvlvfydvtqvvsqevaaseppstsvrltripmv
anhkvafvdtqdvlclesqahstriltrdgfhfcnlsigdlesrldpeqfmrihrcfivnlqgvaelgregskthvvlkgknkepvpvargdvlrlrkalgllsrh(seq id no:4)。
[0173]
在特定的非限制性实例中,rcom蛋白与seq id no:4具有至少90%的同一性并且含有如上对于来自p.xenovorans的rcom-1同源物描述的一个或多个氨基酸取代(关于比对请参见图6)。
[0174]
在一些实施方案中,重组rcom蛋白在n端、c端或两者处包括标签。在一些实例中,标签为亲和标签,诸如有助于蛋白质纯化的亲和标签。可以使用任何合适的亲和标签,诸如his6、flag、谷胱甘肽s-转移酶(gst)、流感病毒血凝素(ha)、c-myc、麦芽糖结合蛋白(mbp)、蛋白a或蛋白g中的一种或多种。在特定实例中,亲和标签是his6标签。在一些实例中,亲和标签是可切割的。在特定实例中,切割标签包括来自tev的具有氨基酸序列enlyfq[g/s](seq id no:5)的切割位点。在另一些特定实例中,切割标签包括来自凝血酶的具有氨基酸序列lvprgs(seq id no:6)的切割位点。
[0175]
在一些实施方案中,重组rcom蛋白不包括标签。
[0176]
在一些实施方案中,重组rcom蛋白为氧化形式(rcom中fe(ii)、结合co的血红素被氧化成fe(iii))。rcom的氧化可以例如通过暴露于氧化剂来实现。在一些实施方案中,氧化剂是含氧气体混合物、含氧液体混合物、铁氰化物盐或其任意组合。在另一些实施方案中,氧化剂是醌,诸如苯醌或萘醌。在一些实例中,电子介体(例如tmpd或结晶紫)与氧化剂组合使用以促进电子转移。在另一些实施方案中,rcom的氧化通过暴露于可见光来完成。例如,可以在存在空气的情况下使用强度为0.15w/cm2到140w/cm2的光纤或散热器屏幕将携带fe(ii)、结合co的血红素的rcom暴露于白光(例如通过暴露于白炽灯泡诸如卤素灯)持续约1至12小时。kerby等(j.bacteriol 190:3336-3343,2008)、bouzhir-sima等(j phys chem b 120:10686-10694,2016)和salman等(biochem 58:4028-4034,2019)中描述了类似的方法。
[0177]
v.药物组合物
[0178]
本文所述的重组rcom蛋白可以作为分离的蛋白质或作为药物组合物的一部分施用。因此,本文提供了药物组合物,其包括本文公开的重组rcom或其衍生物,和一种或多种可药用赋形剂,以及任选包括一种或多种其他活性(治疗)成分。赋形剂在与制剂的其他成分相容且对其接受者无害的意义上是“可接受的”。药物组合物的适当配制取决于若干因素,诸如所选择的施用途径。任何公知的技术和赋形剂都可以适当地并且如本领域中所理解的那样使用。本文公开的药物组合物可以本领域中已知的任何方式制备,例如通过常规的混合、溶解、制粒、糖衣丸制造、研磨、乳化、包封、包埋或压制工艺。
[0179]
在一些实施方案中,公开了药物组合物,其包括一种或多种本文公开的重组rcom蛋白,连同其一种或多种可药用载体和任选一种或多种其他治疗成分。一种或多种赋形剂/一种或多种载体必须是在与制剂的其他成分相容并且对其接受者无害的意义上“可接受的”。药物组合物的适当配制取决于所选择的施用途径。任何公知的技术和赋形剂都可以适当地并且如本领域所理解的那样使用。在一些实施方案中,组合物包括如下赋形剂的一种或多种:n-乙酰半胱氨酸、柠檬酸钠、甘氨酸、组氨酸、谷氨酸、山梨糖醇、麦芽糖、甘露醇、海藻糖、乳糖、葡萄糖、棉子糖、右旋糖、葡聚糖、蔗聚糖、明胶、羟乙基淀粉、苯扎氯铵、苄索氯铵、苯甲醇、氯丁醇、间甲酚、肉豆蔻基γ-甲代吡啶氯化物、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、2-戊氧基乙醇、硝酸苯汞、硫柳汞、丙酮亚硫酸氢钠、氩、棕榈酸抗坏血酸酯、抗坏血
酸盐(钠/酸)、亚硫酸氢钠、丁基羟基苯甲醚(bha)、丁基羟基甲苯(bht)、半胱氨酸/半胱氨酸盐酸盐、连二亚硫酸钠(亚硫酸氢钠、次硫酸钠)、龙胆酸、龙胆酸乙醇胺、谷氨酸一钠、谷胱甘肽、甲醛次硫酸钠、偏亚硫酸氢钾、偏亚硫酸氢钠、甲硫氨酸、单硫代甘油(硫代甘油)、氮、没食子酸丙酯、亚硫酸钠、生育酚α、α生育酚琥珀酸氢盐和巯基乙酸钠。本公开还涵盖其他赋形剂,包括在pramanick et al.,pharma times 45(3):65-77,2013中公开的任何赋形剂,其通过引用并入本文。
[0180]
在一些实施方案中,药物组合物的rcom蛋白是聚乙二醇化的、聚合的或交联的。
[0181]
在一些实施方案中,药物组合物进一步包含天然或重组珠蛋白分子,诸如天然或重组血红蛋白或神经球蛋白,或者包含基于血红蛋白的氧载体(hboc)。在一些实例中,hboc包括dclhb(hemassist
tm
;baxter)、mp4(hemospan
tm
;sangart)、吡哆醛化hb poe-缀合物(php)+过氧化氢酶&sod(apex biosciences)、o-r-polyhba0(hemolink
tm
;hemosol)、polybvhb(hemopure
tm
;biopure)、polyhb(polyheme
tm
;northfield)、rhb1.1(optro
tm
;somatogen)、peg-血红蛋白(enzon)、oxyvita
tm
或hboc-201,或其任意组合。
[0182]
本文公开的药物组合物可通过多种途径施用,这取决于是否需要局部或全身治疗以及取决于待治疗的区域。
[0183]
药物组合物包括适合肠胃外(包括皮下、皮内、肌内、静脉内、关节内和髓内)或腹膜内施用的那些,尽管最适合的途径可能取决于例如接受者的状况和疾患。肠胃外施用包括静脉内、动脉内、皮下、腹膜内、肌内或者注射或输注、或颅内例如鞘内或心室内施用。肠胃外施用可以是单次推注剂量的形式,或者可以是例如通过连续灌注泵。常规的药物载体、水性、粉末或油性基质、增稠剂等可能是必要的或合乎需要的。在一些实施方案中,化合物可以与可药用稀释剂、填料、崩解剂、粘合剂、润滑剂、表面活性剂、疏水载剂、水溶性载剂、乳化剂、缓冲剂、湿润剂、保湿剂、增溶剂、防腐剂等一起包含在这样的药物组合物中。技术人员可以参考各种药理学参考资料以获得指导。例如,可以参考modern pharmaceutics,第5版,banker&rhodes,crc press(2009);和goodman&gilman,the pharmaceutical basis of therapeutics,第13版,mcgraw hill,纽约(2018年)。组合物可以方便地以单位剂型存在并且可以通过药学领域中公知的任何方法制备。通常,这些方法包括将本文公开的分离的重组rcom分子或其衍生物(“活性成分”)与构成一种或多种辅助成分的载体结合的步骤。通常,通过如下所述来制备组合物:将活性成分与液体载体或细碎的固体载体或两者均匀且紧密地结合,然后如果需要的话将产品成型为合乎需要的组合物。
[0184]
可以将重组rcom蛋白配制为用于通过注射进行肠胃外施用。注射用组合物可以以单位剂型存在于例如安瓿或多剂量容器中,并添加防腐剂。药物组合物可以采用诸如在油性或水性载剂中的混悬剂、溶液剂或乳剂的形式,并且可以包含制剂诸如混悬剂、稳定剂和/或分散剂。组合物可存在于单位剂量或多剂量容器中,例如密封的安瓿和小瓶中,并且可以以粉末形式或在冷冻干燥(冻干)条件下储存,仅需要在使用前即刻添加无菌液体载体,例如生理盐水或无菌无热原水。临时注射液和混悬液可以由前述种类的无菌粉末、颗粒和片剂制备。
[0185]
用于肠胃外施用的药物组合物包括活性化合物的水性和非水性(油性)无菌注射液,其可以含有抗氧化剂、缓冲剂、抑菌剂和使组合物与预期接受者的血液等渗的溶质;水性和非水性无菌混悬液,其可包括混悬剂和增稠剂。合适的亲脂性溶剂或载剂包括脂肪油,
诸如芝麻油,或合成脂肪酸酯,诸如油酸乙酯或甘油三酯,或脂质体。水性注射混悬液可以含有增加混悬液粘度的物质,诸如羧甲基纤维素钠、山梨糖醇或葡聚糖。任选地,混悬液还可以包含合适的稳定剂或增加化合物溶解度的试剂以允许制备高度浓缩的溶液。
[0186]
应当理解,除了上文特别提及的成分之外,上述药物组合物还可以包括本领域中所讨论的药物组合物这一类型的其他常规试剂,例如适合口服施用的那些可以包括矫味剂。
[0187]
单位剂量药物组合物是含有如下文所述的有效剂量或其适当分数的活性成分的那些。术语“单位剂型”是指物理上离散的单位,适合作为人对象和其他哺乳动物的单位剂量,每个单位含有经计算产生所需治疗效果的预定量的活性物质,以及合适的药用赋形剂。
[0188]
rcom蛋白可以在很宽的剂量范围内有效并且通常可以以治疗有效量施用。然而,应当理解,实际施用的化合物的量通常由医师根据相关情况确定,包括待治疗的病症、选择的施用途径、实际施用的化合物、个体患者的年龄、体重和反应、患者症状的严重程度等。
[0189]
在一些实施方案中,所公开的重组rcom蛋白可以每天约0.01g至约1000g的治疗有效剂量施用。在一些实例中,重组rcom蛋白的剂量为约0.1g至约900g、约0.1g至约800g、约0.1g至约700g、约0.1g至约600g、约0.1g至约500g、约0.1g至约400g、约0.1g至约300g、约0.1g至约200g、约0.1g至约100g、约1g至约900、约1g至约800、约1g至约700g、约1g至约600g、约1g至约500g、约1g至约400g、约1g至约300g、约1g至约200g、约1g至约100g、约10g至约900g、约10g至约800g、约10g至约700g、约10g至约600g、约10g至约500g、约10g至约400g、约10g至约300g、约10g至约200g、或者约10g至约100g,或这些值中的任意两个之间的范围。
[0190]
与载体材料组合以产生单一剂型的活性成分的量将根据所治疗的宿主和特定的施用方式而变化。在本文公开的一些实施方案中,药物组合物包含一种或多种所公开的rcom蛋白(作为活性成分)与一种或多种可药用载体(赋形剂)的组合。
[0191]
在一些实施方案中,一种或多种重组rcom蛋白占药物组合物的约0.01%至约50%。在一些实施方案中,一种或多种rcom蛋白占约0.01%至约50%、约0.01%至约45%、约0.01%至约40%、约0.01%至约30%、约0.01%至约20%、约0.01%至约10%、约0.01%至约5%、约0.05%至约50%、约0.05%至约45%、约0.05%至约40%、约0.05%至约30%、约0.05%至约20%、约0.05%至约10%、约0.1%至约50%、约0.1%至约45%、约0.1%至约40%、约0.1%至约30%、约0.1%约20%、约0.1%至约10%、约0.1%至约5%、约0.5%至约50%、约0.5%至约45%、约0.5%至约40%、约0.5%至约30%、约0.5%至约20%、约0.5%至约10%、约0.5%至约5%、约1%至约50%、约1%至约45%、约1%至约40%、约1%至约35%、约1%至约30%、约1%至约25%、约1%至约20%、约1%至约15%、约1%至约10%、约1%至约5%、约5%至约45%、约5%至约40%、约5%至约35%、约5%至约30%、约5%至约25%、约5%至约20%、约5%至约15%、约5%至约10%、约10%至约45%、约10%至约40%、约10%至约35%、约10%至约30%、约10%至约25%、约10%至约20%、约10%至约15%或这些范围之一内的值。具体的非限制性实例包括约0.01%、约0.05%、约0.1%、约0.25%、约0.5%、约0.75%、约1%、约5%、约10%、约15%、约20%、约25%、约30%、约35%、约40%、约45%、约50%、约60%、约70%、约80%、约90%或这些值中任意两个之间的范围。以上均代表药物组合物的重量百分比。
[0192]
施用于患者的重组rcom蛋白的量将根据所施用的物质、施用的目的(诸如预防或
治疗)、患者的状态、施用方式等而变化。在治疗应用中,可以向已经患有疾病或病症的患者施用足以治愈或至少部分抑制疾病的症状及其并发症的量的组合物。
[0193]
在一些实施方案中,可以通过常规灭菌技术对药物组合物进行灭菌,或者可以进行无菌过滤。水溶液可以按原样或冻干包装使用,冻干制剂在施用前与无菌水性载体组合。在一些实施方案中,rcom蛋白制剂的ph为约3至约11、约5至约9、约5.5至约6.5、或约5.5至约7.5。应当理解,使用某些前述赋形剂、载体或稳定剂将致使形成药用盐。
[0194]
在某些实施方案中,药物组合物包含还原剂。在一些实例中,还原剂选自抗坏血酸、n-乙酰半胱氨酸、连二亚硫酸钠、亚甲蓝、谷胱甘肽、b5/b5-还原酶/nadh、三(2-羧乙基)膦、二硫苏糖醇或其组合。也可以使用具有还原含铁血红素分子特性的其他试剂。
[0195]
在另一些特定实施方案中,药物组合物包含氧化剂。在一些实例中,氧化剂选自含氧气体混合物、含氧液体混合物、铁氰化物盐或其任意组合。
[0196]
在某些实施方案中,可以通过在无氧环境中产生和维持rcom蛋白或药物组合物来使药物组合物脱氧。
[0197]
vi.治疗co、h2s和氰化物中毒的方法
[0198]
本文公开的重组rcom蛋白(参见第iv部分)对一氧化碳表现出非常高的亲和力。基于该特性,所公开的rcom蛋白可用于多种体内和体外方法,包括作为一氧化碳中毒的解毒剂。还描述了所公开的rcom蛋白用于治疗氰化物和硫化氢(h2s)中毒的用途。
[0199]
本文提供了治疗对象的碳氧血红蛋白血症(一氧化碳中毒)的方法。在一些实施方案中,该方法包括向对象施用治疗有效量的本文公开的重组rcom蛋白或含有重组rcom蛋白的药物组合物。在一些实施方案中,该方法包括在施用rcom蛋白或其药物组合物之前选择患有碳氧血红蛋白血症(一氧化碳中毒)的对象。在一些实例中,对象的血液中含有至少3%、至少5%、至少10%、至少15%、至少20%、至少30%、至少40%或至少50%的碳氧血红蛋白。在一些实施方案中,rcom蛋白处于其还原形式。在一些实例中,还原剂包括连二亚硫酸钠、抗坏血酸、n-乙酰半胱氨酸(nac)、亚甲蓝、谷胱甘肽、细胞色素b5/b5-还原酶、肼苯哒嗪、三(2-羧乙基)膦(tcep)、二硫苏糖醇(dtt)、海藻糖、还原性碳水化合物(诸如山梨糖醇或甘露糖醇)或其任意组合。
[0200]
本文进一步提供了一种通过使对象的血液或组织与本文公开的重组rcom蛋白或药物组合物接触从对象的血液或组织中的天然血红蛋白、肌红蛋白或线粒体(即从线粒体中的细胞色素c氧化酶)中去除一氧化碳的方法。在一些实施方案中,该方法包括在使对象的血液或组织与所公开的rcom蛋白或其药物组合物接触之前选择患有碳氧血红蛋白血症(一氧化碳中毒)的对象。在一些实例中,对象的血液中具有至少5%、至少10%、至少15%、至少20%、至少30%、至少40%或至少50%的碳氧血红蛋白。在一些实施方案中,rcom蛋白处于其还原形式。在一些实例中,还原剂包括连二亚硫酸钠、抗坏血酸、n-乙酰半胱氨酸(nac)、亚甲蓝、谷胱甘肽、细胞色素b5/b5-还原酶、肼苯哒嗪、三(2-羧乙基)膦(tcep)、二硫苏糖醇(dtt)、海藻糖、还原性碳水化合物(诸如山梨糖醇或甘露糖醇)或其任意组合。
[0201]
本文还提供了一种通过使对象的血液或组织与本文公开的重组rcom蛋白或药物组合物接触从对象的血液或组织中的天然血红蛋白、肌红蛋白或线粒体(诸如从线粒体中的细胞色素c氧化酶)中去除硫化氢的方法。在一些实例中,该方法进一步包括在使对象的血液或组织与rcom蛋白或药物组合物接触之前选择患有硫化氢中毒的对象的步骤。进一步
提供了通过向对象施用治疗有效量的本文公开的重组rcom蛋白或药物组合物来治疗对象的硫化氢中毒的方法。在一些实例中,该方法进一步包括在施用rcom蛋白或药物组合物之前选择患有硫化氢中毒的对象的步骤。在这些方法的一些实施方案中,rcom蛋白处于其还原形式。包括在药物组合物中的还原剂的实例包括但不限于连二亚硫酸钠、抗坏血酸、n-乙酰半胱氨酸(nac)、亚甲蓝、谷胱甘肽、细胞色素b5/b5-还原酶、肼苯哒嗪、三(2-羧乙基)膦(tcep)、二硫苏糖醇(dtt)、海藻糖、还原性碳水化合物(诸如山梨糖醇或甘露糖醇)或其任意组合。
[0202]
本文进一步提供了通过使对象的血液或组织与本文公开的重组rcom蛋白或药物组合物接触从对象的血液或组织中的天然血红蛋白、肌红蛋白或线粒体(诸如从线粒体中的细胞色素c氧化酶)中去除氰化物的方法。在一些实例中,该方法进一步包括在使对象的血液或组织与rcom蛋白或药物组合物接触之前选择患有氰化物中毒的对象的步骤。还提供了通过向对象施用治疗有效量的本文公开的重组rcom蛋白或药物组合物来治疗对象的氰化物中毒的方法。在一些实例中,该方法进一步包括在施用rcom蛋白或药物组合物之前选择患有氰化物中毒的对象的步骤。在这些方法的一些实施方案中,rcom蛋白处于其氧化形式。在一些实例中,氧化剂包括含氧气体混合物、含氧液体混合物、铁氰化物盐或其任意组合。
[0203]
在本文公开的体内方法的一些实施方案中,rcom蛋白或药物组合物通过静脉内或肌内施用。在一些实例中,rcom蛋白或药物组合物通过静脉输注、腹膜内注射或肌内注射施用。
[0204]
在一些实施方案中,rcom蛋白单独或作为药物组合物的一部分以每天约0.1至约300g的剂量施用。其他剂量范围在上文第v节中描述。
[0205]
本文还提供了从血液或动物组织中的血红蛋白、肌红蛋白或线粒体(例如从线粒体中的细胞色素c氧化酶)去除一氧化碳的体外方法,包括使血液或动物组织与有效量的本文所公开的重组rcom蛋白接触。在一些实施方案中,rcom蛋白处于其还原形式。
[0206]
本文进一步提供了从血液或动物组织中的血红蛋白、肌红蛋白或线粒体(例如从线粒体中的细胞色素c氧化酶)中去除硫化氢的体外方法,包括使血液或动物组织与有效量的本文所公开的重组rcom蛋白接触。在一些实施方案中,rcom蛋白处于其还原形式。
[0207]
本文还提供了从血液或动物组织中的血红蛋白、肌红蛋白或线粒体(例如从线粒体中的细胞色素c氧化酶)中去除氰化物的体外方法,包括使血液或动物组织与有效量的本文公开的重组rcom蛋白接触。在一些实施方案中,重组rcom蛋白处于其氧化形式。
[0208]
在所公开方法的一些实施方案中,重组rcom蛋白是聚乙二醇化的、聚合的或交联的。
[0209]
vii.重组rcom作为血液替代品
[0210]
本文公开的重组rcom蛋白能够结合和携带氧(参见图8和15a-15d;实施例3和4)。因此,预期使用所公开的rcom蛋白作为血液替代品。
[0211]
本文提供了一种替代血液和/或增加向对象组织的氧输送的方法。在一些实施方案中,该方法包括向对象施用治疗有效量的本文公开的重组rcom蛋白或药物组合物,从而替代血液和/或增加对象中的氧输送。
[0212]
例如,待治疗的对象是需要增加血液容量或增加向组织的氧输送的任意对象。在
一些实施方案中,对象患有与缺乏红细胞和/或血红蛋白相关或与向组织的氧输送减少相关的疾病、疾患或损伤,或存在患与缺乏红细胞和/或血红蛋白相关或与向组织的氧输送减少相关的疾病、疾患或损伤的风险。在一些实例中,所述疾病、疾患或损伤包括出血疾患、出血发作、贫血、休克、缺血、低氧、缺氧、低氧血症、烧伤、溃疡、异位妊娠、小红细胞症、横纹肌溶解症、血红蛋白病、球形细胞增多症、溶血性尿毒症综合征、地中海贫血、弥散性血管内凝血、中风或黄热病。
[0213]
在一些实施方案中,待用重组rcom蛋白治疗的对象的出血发作由抗凝剂过量、动脉瘤、血管破裂、手术、外伤、胃肠道出血、妊娠、出血或感染引起。
[0214]
在一些实施方案中,待用重组rcom蛋白治疗的对象中的出血性疾患包括血友病a、血友病b、血友病c、因子vii缺乏症、因子xiii缺乏症、血小板疾患、凝血病、蚕豆病、血小板减少症、维生素k缺乏症或维勒布兰德氏病。
[0215]
在一些实施方案中,待治疗的对象的贫血包括小红细胞性贫血、缺铁性贫血、血红素合成缺陷、珠蛋白合成缺陷、铁粒幼细胞缺陷、正常红细胞性贫血、慢性病性贫血、再生障碍性贫血、溶血性贫血、大红细胞性贫血、巨幼红细胞性贫血、恶性贫血、二形性贫血、早产儿贫血、范可尼氏贫血、遗传性球形细胞增多症、镰状细胞性贫血、温性自身免疫性溶血性贫血或冷凝集素溶血性贫血。
[0216]
在一些实施方案中,待治疗的对象的休克包括感染性休克、出血性休克或低血容量性休克。
[0217]
在一些实施方案中,待治疗的对象患有与血流减少相关的疾病或病症或有患与血流减少相关的疾病或病症的风险,使得增加的氧输送有利于对象的治疗。可以使用所公开的方法治疗的疾病或病症的实例包括但不限于缺血、心肌梗塞、中风、缺血-再灌注损伤、血压升高、肺动脉高压(包括新生儿肺动脉高压、原发性肺动脉高压和继发性肺动脉高压)、全身性高血压、皮肤溃疡、急性肾功能衰竭、慢性肾功能衰竭、血管内血栓形成、缺血性中枢神经系统事件、血管痉挛(诸如脑动脉血管痉挛)、溶血性病症、外周血管疾病、外伤、心脏骤停、普通外科或器官移植。
[0218]
在一些实施方案中,将重组rcom蛋白经静脉内施用于对象。
[0219]
在一些实施方案中,该方法还包括向对象施用第二血液替代品、血液产品或全血。在一些实例中,第二血液替代品包含基于血红蛋白的氧载体、人造红细胞或释氧化合物。在一些实例中,血液产品包括压积的红细胞、血浆或血清。
[0220]
在一些实例中,对象是人。在另一些实例中,对象是非人类动物。
[0221]
还提供了包含所公开的rcom蛋白和氧载体诸如天然或重组珠蛋白分子(诸如天然或重组血红蛋白或神经球蛋白)或基于血红蛋白的氧载体(hboc)的组合物。在一些实施方案中,所述组合物还包含可药用载体或赋形剂,或两者。在一些实例中,组合物中的rcom蛋白是聚乙二醇化的、聚合的或交联的。
[0222]
viii.实施方案
[0223]
实施方案1.重组一氧化碳代谢调节因子(rcom)蛋白,其中所述重组rcom蛋白包含血红素结合结构域(hbd),并且其中所述hbd的氨基酸序列与seq id no:2具有至少90%的同一性并且在h74、c94、m104、m105、c127和c130中的一个或多个处包含氨基酸取代。
[0224]
实施方案2.实施方案1所述的重组rcom蛋白,其中:
[0225]
h74处的取代选自h74s、h74t、h74m、h74w、h74a、h74l、h74i、h74v和h74g;
[0226]
c94处的取代选自c94s、c94t、c94h、c94w、c94m、c94a、c94l、c94i、c94v和c94g;
[0227]
m104处的取代选自m104s、m104t、m104h、m104w、m104a、m104l、m104i、m104v和m104g;
[0228]
m105处的取代选自m105s、m105t、m105h、m105w、m105a、m105l、m105i、m105v和m105g;
[0229]
c127处的取代选自c127s、c127t、c127m、c127a、c127l、c127i、c127v和c127g;和/或
[0230]
c130处的取代选自c130s、c130t、c130m、c130a、c130l、c130i、c130v和c130g。
[0231]
实施方案3.如实施方案1或实施方案2所述的重组rcom蛋白,其中所述hbd的氨基酸序列与seq id no:2具有至少95%的同一性并且在c94、m104、c127和c130中的一个或多个处包含氨基酸取代。
[0232]
实施方案4.如实施方案1至4中任一项所述的重组rcom蛋白,其中所述hbd包含:
[0233]
c94s取代;
[0234]
c127s取代和c130s取代;
[0235]
c94s取代、c127s取代和c130s取代;
[0236]
m104a取代、c127s取代和c130s取代;
[0237]
m104h取代、c127s取代和c130s取代;
[0238]
m104l取代、c127s取代和c130s取代;
[0239]
c94s取代、m104a取代、c127s取代和c130s取代;
[0240]
c94s取代、m104h取代、c127s取代和c130s取代;或者
[0241]
c94s取代、m104l取代、c127s取代和c130s取代。
[0242]
实施方案5.如实施方案1至4中任一项所述的重组rcom蛋白,其中:
[0243]
rcom蛋白的氨基酸序列包含如下或者由如下组成:seq id no:7、seq id no:8、seq id no:9、seq id no:10、seq id no:11、seq id no:12、seq id no:no:13或seq id no:14;或者
[0244]
rcom蛋白的氨基酸序列包含seq id no:1或seq id no:2或者由seq id no:1或seq id no:2组成,除了在h74、c94、m104、c127、c130和m105中的一个或多个处的氨基酸取代。
[0245]
实施方案6.如实施方案1至5中任一项所述的重组rcom蛋白,其中所述rcom蛋白包含n端标签或c端标签。
[0246]
实施方案7.如实施方案6所述的重组rcom蛋白,其中所述标签是亲和标签。
[0247]
实施方案8.如实施方案7所述的重组rcom蛋白,其中所述亲和标签是his6、flag、谷胱甘肽s-转移酶(gst)、流感病毒血凝素(ha)、c-myc、麦芽糖结合蛋白(mbp)、蛋白a或蛋白g。
[0248]
实施方案9.如实施方案6至8中任一项所述的重组rcom蛋白,其中所述标签是可切割的。
[0249]
实施方案10.一种从血液或动物组织中的血红蛋白、肌红蛋白或线粒体去除一氧化碳的体外方法,包括使血液或动物组织与有效量的实施方案1至9中任一项的重组rcom蛋
白接触,从而从血液或动物组织中的血红蛋白去除一氧化碳。
[0250]
实施方案11.一种治疗对象的碳氧血红蛋白血症的方法,包括向对象施用治疗有效量的实施方案1至9中任一项的rcom蛋白。
[0251]
实施方案12.如实施方案11所述的方法,进一步包括在施用所述重组rcom蛋白之前选择患有碳氧血红蛋白血症的对象。
[0252]
实施方案13.如实施方案11或实施方案12所述的方法,其中所述对象在其血液中具有至少5%、至少10%、至少15%、至少20%、至少30%、至少40%或至少50%的碳氧血红蛋白。
[0253]
实施方案14.如实施方案11至13中任一项所述的方法,其中所述重组rcom蛋白通过静脉内输注、腹膜内注射或肌内注射施用。
[0254]
实施方案15.如实施方案11至14中任一项所述的方法,其中所述重组rcom蛋白以每天约0.1g至约300g的剂量施用。
[0255]
实施方案16.如实施方案11至15中任一项所述的方法,其中所述重组rcom蛋白作为包含还原剂的药物组合物施用。
[0256]
实施方案17.如实施方案16所述的方法,其中所述还原剂包括连二亚硫酸钠、抗坏血酸、n-乙酰半胱氨酸(nac)、亚甲蓝、谷胱甘肽、细胞色素b5/b5-还原酶、肼苯哒嗪、三(2-羧乙基)膦(tcep)、二硫苏糖醇(dtt)或其任意组合。
[0257]
实施方案18.一种治疗对象的氰化物中毒的方法,包括向对象施用治疗有效量的实施方案1至9中任一项的重组rcom蛋白,其中所述rcom蛋白处于其氧化形式,从而治疗对象的氰化物中毒。
[0258]
实施方案19.如实施方案18所述的方法,进一步包括在施用所述重组rcom蛋白之前选择患有氰化物中毒的对象。
[0259]
实施方案20.如实施方案18或实施方案19所述的方法,其中所述重组rcom蛋白作为包含氧化剂的药物组合物施用。
[0260]
实施方案21.如实施方案20所述的方法,其中所述氧化剂包括含氧气体混合物、含氧液体混合物、铁氰化物盐或其任意组合。
[0261]
实施方案22.一种治疗对象的硫化氢(h2s)中毒的方法,包括向对象施用治疗有效量的实施方案1至9中任一项的重组rcom蛋白,其中所述rcom蛋白处于其还原形式,从而治疗对象的h2s中毒。
[0262]
实施方案23.如实施方案22所述的方法,进一步包括在施用重组rcom蛋白之前选择患有h2s中毒的对象。
[0263]
实施方案24.如实施方案22或实施方案23所述的方法,其中重组rcom蛋白作为包含还原剂的药物组合物施用。
[0264]
实施方案25.如实施方案24所述的方法,其中所述还原剂包括连二亚硫酸钠、抗坏血酸、n-乙酰半胱氨酸(nac)、亚甲蓝、谷胱甘肽、细胞色素b5/b5-还原酶、肼苯哒嗪、三(2-羧乙基)膦(tcep)、海藻糖、二硫苏糖醇(dtt)或其任意组合。
[0265]
实施方案26.一种置换对象血液的方法,包括向对象施用治疗有效量的实施方案1至9中任一项的重组rcom蛋白,从而置换对象的血液。
[0266]
实施方案27.如实施方案26所述的方法,其中所述对象患有与红细胞和/或血红蛋
白缺乏相关或与向组织的氧输送减少相关的疾病、疾患或损伤或者存在患与红细胞和/或血红蛋白缺乏相关或与向组织的氧输送减少相关的疾病、疾患或损伤的风险。
[0267]
实施方案28.如实施方案27所述的方法,其中所述疾病、疾患或损伤包括出血疾患、出血发作、贫血、休克、缺血、低氧、缺氧、低氧血症、烧伤、溃疡、异位妊娠、小红细胞症、横纹肌溶解症、血红蛋白病、球形细胞增多症、溶血性尿毒症综合征、地中海贫血、弥散性血管内凝血、中风或黄热病。
[0268]
实施方案29.如实施方案28所述的方法,其中:
[0269]
所述出血发作由抗凝剂过量、动脉瘤、血管破裂、手术、外伤、胃肠道出血、怀孕、出血或感染引起;
[0270]
所述出血性疾患包括血友病a、血友病b、血友病c、因子vii缺乏症、因子xiii缺乏症、血小板疾患、凝血病、蚕豆病、血小板减少症、维生素k缺乏症或维勒布兰德氏病;
[0271]
所述贫血包括小红细胞性贫血、缺铁性贫血、血红素合成缺陷、珠蛋白合成缺陷、铁粒幼细胞缺陷、正常红细胞性贫血、慢性病性贫血、再生障碍性贫血、溶血性贫血、大红细胞性贫血、巨幼红细胞性贫血、恶性贫血、二形性贫血、早产儿贫血、范可尼贫血、遗传性球形细胞增多症、镰状细胞性贫血、温性自身免疫性溶血性贫血或冷凝集素溶血性贫血;或者
[0272]
休克包括感染性休克、出血性休克或低血容量性休克。
[0273]
实施方案30.如实施方案26所述的方法,其中所述对象患有心肌梗塞、中风、缺血-再灌注损伤、肺动脉高压或血管痉挛或者存在患有心肌梗塞、中风、缺血-再灌注损伤、肺动脉高压或血管痉挛的风险。
[0274]
实施方案31.如实施方案26至30中任一项所述的方法,其中将所述重组rcom蛋白经静脉内施用于对象。
[0275]
实施方案32.如权利要求26至31中任一项所述的实施方案,其中所述重组rcom蛋白是聚乙二醇化的、聚合的或交联的。
[0276]
实施方案33.如实施方案26至32中任一项所述的方法,还包括向所述对象施用第二血液替代品、血液产品或全血。
[0277]
实施方案34.如实施方案33所述的方法,其中所述第二血液替代品包含基于血红蛋白的氧载体、人造红细胞或释氧化合物。
[0278]
实施方案35.如实施方案33所述的方法,其中所述血液产品包括压积的红细胞、血浆或血清。
[0279]
实施方案36.如实施方案11至35中任一项所述的方法,其中所述对象是人。
[0280]
实施方案37.如实施方案11至35中任一项所述的方法,其中所述对象是非人类动物。
[0281]
实施方案38.一种药物组合物,其包含实施方案1至9中任一项的重组rcom蛋白和可药用载体。
[0282]
实施方案39.如实施方案38所述的药物组合物,进一步包含还原剂或氧化剂。
[0283]
实施方案40.如实施方案39所述的药物组合物,其中所述还原剂包括连二亚硫酸钠、抗坏血酸、n-乙酰半胱氨酸(nac)、亚甲蓝、谷胱甘肽、细胞色素b5/b5-还原酶、肼苯哒嗪、三(2-羧乙基)膦(tcep)、二硫苏糖醇(dtt)或其任意组合。
[0284]
实施方案41.如实施方案39所述的药物组合物,其中所述氧化剂包括含氧气体混
合物、含氧液体混合物、铁氰化物盐、醌或其任意组合。
[0285]
实施方案42.如实施方案38至41中任一项所述的药物组合物,其中所述重组rcom蛋白是聚乙二醇化的、聚合的或交联的。
实施例
[0286]
实施例1:在有氧环境中将co从hbco转移到rcom-1
[0287]
在37℃有氧条件下,在wt、全长rcom-1(seq id no:1)的存在下评估血红蛋白-co(hb-co)转移动力学,并使用停流uv-vis光谱和基于rcom-1和血红蛋白的不同配体结合物质的消光系数的标准反卷积方法进行测量。hb-co和fe(ii)rcom-1的浓度为20μm,实验以一式三份进行。血红蛋白-co损失的数据拟合至双指数曲线,显示出1.4秒的慢相半衰期(t
1/2
)。fe(ii)-co rcom增加的数据拟合单一指数曲线,显示出半衰期为0.93秒。结果示于图4中。该数据表明,rcom对co具有同样高的亲和力,并允许将co从hb快速有效地转移到rcom。
[0288]
实施例2:在厌氧环境中将co从hb-co转移到rcom-1
[0289]
使用uv-vis光谱测量在37℃厌氧条件下、在wt、全长rcom-1(seq id no:1)的存在下血红蛋白-co转移动力学。hb-co和fe(ii)rcom-1的浓度分别为15μm和15.8μm。在530、562和583nm处的吸光度变化跟踪从fe(ii)到fe(ii)-co rcom的转变,拟合单指数曲线,表现出半衰期为50秒。结果示于图5中。这些结果表明,rcom-1能够从hb-co物质清除co,因此可以在体内用作co清除剂。
[0290]
实施例3:用c94c取代(hbd c94s)表征截短的rcom
[0291]
本实施例描述了表征缺少pas结构域并具有c94s取代(seq id no:7)的经修饰rcom蛋白的研究。这些研究的结果表明,改变血红素结合残基可以改变rcom的气体结合特性。
[0292]
稳定性
[0293]
hbd c94s突变体比wt rcom-1稳定得多。这种突变形式的rcom可以以比wt rcom更高的浓度储存(~480mm血红素,相比之下,wt rcom为~130mm)。hbd c94s也可以在不存在稳定还原剂(例如dtt、tcep)的情况下使用连二亚硫酸盐还原。此外,当在4℃储存超过1周时,氧化和还原形式的rcom对聚集而言是稳定的。研究表明,fe(iii)rcom-1hbd c94s的tm为90℃(在隔膜密封比色皿中于厌氧条件下以7μm的rcom浓度记录)。在相同条件下,wt rcom-1在约40℃时不可逆地解折叠。
[0294]
uv-vis光谱的比较
[0295]
评估了全长野生型rcom-1和hbd c94s rcom的光谱。测定了铁(fe(iii)、脱氧亚铁(fe(ii))和亚铁-co物质(fe(ii)-co)的光谱。计算了每种物质的最大峰值波长(nm),以及每个峰值的估计摩尔吸收率(mm-1
cm-1
)。结果示于图7中。正如预期的,wt和hbd c94s rcom蛋白之间的fe(ii)和fe(ii)-co光谱非常相似。然而,fe(iii)光谱看起来非常不同,这表明fe(iii)血红素配位环境由于c94s取代而发生了变化。
[0296]
另一项研究提供了hbd c94s中稳定的o2加合物的证据。hbd c94s被过量的连二亚硫酸盐还原,产生亚铁fe(ii)物质。然后将还原的hbd c94s脱盐并在微需氧条件下制备uv-vis样品。在微需氧条件下记录uv-vis光谱后,取下比色杯盖以引入空气,重新记录光谱,显
示氧结合物质(rcom浓度=8μm)。图8示出在还原剂存在下亚铁(fe(ii))物质、脱盐后的fe(ii)物质、暴露于空气后的fe(ii)物质和再氧化的fe(iii)物质的可见光谱。
[0297]
hbd c94s rcom-co结合和解离速率
[0298]
通过停流技术测定hbd c94s rcom的亚铁血红素结合结构域(hbd)与一氧化碳(co)的反应动力学(图9)。该研究在10μm的rcom浓度、55-287μm的co浓度和37℃的温度下进行。计算不同co浓度下的速率得到1.2
×
105m-1
s-1
的反应结合速率(k
on
)。野生型全长蛋白质也获得了相似的值。因而,co结合速率不受c94s取代的影响。
[0299]
使用10μm的rcom浓度、2mm的一氧化氮(no)浓度(使用1mm prolinonoate生成)和37℃的温度测定hbd c94s的co解离速率。随着亚铁-co络合物在no的存在下解离,通过吸光度变化监测反应。当co解离时,no与血红素结合,导致吸收光谱发生变化。过量的no会阻止co重新结合血红素。吸光度变化的时间过程允许确定解离速率为4.9
×
10-2
s-1
(图10)。
[0300]
hbd c94s的热解折叠
[0301]
通过420nm血红素索雷最大值处的吸光度变化监测解折叠(图11)。在记录每个uv-vis光谱之前,使样品在每个温度平衡5分钟。在20℃至75℃之间观察到的索雷强度的小幅损失可能是由于血红素配位数的变化。索雷强度在75℃至98℃之间的损失归因于热解折叠导致蛋白质中血红素的损失。在20℃至98℃之间的每个温度记录携带c94s突变的fe(iii)hbd rcom-1的uv-vis光谱。hbd c94s的tm确定为91℃。
[0302]
实施例4:rcom血红素结合结构域(hbd)变体
[0303]
本实施例描述了若干截短的rcom hbd变体的生成和表征。
[0304]
生成了八个rcom变体。表4中列出的变体已成功克隆、在大肠杆菌中表达并纯化至同质。这些变体涵盖来自paraburkholderia xenovorans的rcom-1的血红素结合结构域(hbd)并具有各种突变(在残基c94、m104、c127和c130中的一个或多个处)以增强溶解度、稳定性和co清除特性。表达的变体还包括c端6-his标签。具有6-his标签,变体为17kda。
[0305]
表4.rcom hdb16变体
[0306]
[0307][0308]
rcom hbd wt和变体的电子吸收(uv-vis)光谱示于图12a-12d、13a-13b和14a-14c。图13c示出rcom的蛋白质来源配体转换机制的示意图,其突出了m104变体中的配位层变化。图14d示出rcom的蛋白质来源配体转换机制的示意图,其突出了ccc m104变体的配位层变化。
[0309]
rcom hbd截短物中氧结合亲和力(p
50
)的定量示于图15a-15d。使用配备有光学比色皿的眼压计设备,采用uv-vis光谱测量与氧结合的血红蛋白的分数作为氧分压的函数。cc hbd rcom变体的uv-vis特征的代表性光谱变化作为氧分压(p
o2
)的函数示于图15a中。cc hbd、c94s hbd和ccc hbd的氧结合曲线示于图15b-15d中。测定了co与rcom wt hbd和hbd变体cc hbd、c94s hbd和ccc hbd结合的二级速率常数(k
on
,co)(图16a-16d)。采用停流uv-vis光谱测量每个co浓度下的co结合速率并拟合至单指数。对每条曲线应用线性回归,并将二阶速率常数估计为斜率。结果如下:
[0310]
rcom变体k
on,co
wt hbd4.0x104m-1
s-1
cc hbd4.4x104m-1
s-1
c94s hbd2.8x104m-1
s-1
ccc hbd4.1x104m-1
s-1
[0311]
wt hbd rcom的自氧化速率(k
oxid
)确定为0.87h-1
。图17a示出fe(iii)和fe(ii)-o2蛋白的参考光谱。fe(ii)-o
2 wt hbd的uv-vis特征的光谱变化示于图17b中。将542nm和573nm处的光谱变化拟合至单指数以确定k
oxid
(图17c)。图18示出提供wt rcom和rcom hbd变体c94s、cc hbd和ccc hbd的配体结合参数和血红素稳定性特性的总结的表格。
[0312]
评估了在尿素(0m、4m和8m尿素)存在下fe(iii)ccc hbd rcom的解折叠。通过在415nm血红素索雷最大值处的吸光度变化监测解折叠。在记录每个uv-vis光谱之前使样品平衡10分钟(图19a)。解折叠数据拟合s形曲线以确定一半蛋白质样品解折叠时的变性剂浓度([d]
50
)(图19b)。ccc hbd的[d]
50
为4.6m。
[0313]
还评估了rcom hbd变体与过氧化氢之间的反应性。在ph 7.4、25℃,用500μm过氧化氢孵育fe(iii)wt hbd和变体ccc hbd、ccc m104a hbd和ccc m104hhbd,并在30分钟内每2分钟通过uv-vis光谱监测(图20a-20d)。每个变体都观察到最小的光谱变化,这表明过氧化氢不会与rcom hbd截短物的fe(iii)血红素中心反应以产生高度氧化的物质。
[0314]
对全长和hbd截短rcom变体的亚硝酸盐减少进行评估。在37℃于2.5mm连二亚硫酸钠存在下用1-5mm亚硝酸钠孵育亚铁蛋白(10-15μm)。uv-vis光谱用于监测fe(ii)血红素向fe(ii)-no的转化(图21a)。将562nm和578nm处的光谱特征变化拟合到单指数曲线以确定观察到的亚硝酸盐还原速率。将观察到的速率作为亚硝酸盐浓度的函数作图,对每个图应用
线性回归,将二阶速率常数估计为斜率(图21b-21c)。
[0315]
进行了额外的研究以评估rcom的co清除能力。在37℃有氧条件下,开发了用于在体外使co从血红蛋白(hb)转移到wt rcom hbd和rcom hbd变体cc hbd、c94s hbd和ccc hbd的动力学轨迹。将结合co的hb(20μm)与等摩尔含氧铁rcom一起孵育,并使用uv-vis光谱监测从hb到rcom的co转移。使用光谱反卷积确定每种co结合血红蛋白的分数,并将相应的动力学轨迹拟合至单指数或双指数方程。每种结合co的物质的半衰期示于图22a-22d中,拟合至双指数的曲线显示出快速的物质半衰期和幅度。图23a-23b示出在37℃有氧条件下监测co从红细胞(rbc)包裹的hbco转移到细胞外rcom hbd截短物的动力学轨迹。以等摩尔浓度(50-100μm)孵育血红蛋白,并在每个时间点通过离心将rbc从细胞外rcom中分离出来。使用uv-vis光谱监测从hb到wt hbd rcom(图23a)和c94s hbd rcom(图23b)的co转移。使用光谱反卷积确定每种结合co的血红蛋白的分数,并将相应的动力学轨迹拟合至单指数方程。在wt hbd和c94s hbd的存在下,cohb的半衰期分别为24
±
6秒和23
±
5秒。
[0316]
这些结果表明,rcom hbd变体在有氧条件下从rbc包裹的hb中快速清除co,这与急性co中毒期间可能在体内发生的情况相似。rcom hbd变体对co的选择性高于氧气,因为在有氧条件下从hbco转移co。
[0317]
实施例5:在小鼠中rcom hbd变体的毒性筛选
[0318]
将重组表达的rcom截短物经尾静脉导管以1mm或10mm的浓度和10μl/g体重的注射体积引入健康小鼠。在48小时内监测行为(包括筑巢),随后处死并采集血液进行毒理学评估。结果示于表5。用rcom截短物处理的所有小鼠的肝功能(ast和alt)和肾功能(bun和肌酐)的血液化学结果与给予磷酸盐缓冲盐水(pbs)的对照小鼠的结果相当。这些结果表明,静脉输注rcom截短物不会在小鼠中引起器官特异性毒性。
[0319]
表5.毒性筛选结果
[0320][0321][0322]
实施例6:体内rcom co清除
[0323]
在致死的co中毒小鼠模型中评估了c94s和ccc hbd rcom变体从hbco中清除co的能力。将经麻醉、机械通气的小鼠暴露于空气中3,000ppm co,持续4.5分钟,然后以10μl/g
体重的注射体积静脉内输注fe(ii)-o
2 ccc hbd rcom(血红蛋白浓度如图24所示)。在输注之前和之后立即抽取血液样品(15μl),以及在co暴露后25分钟抽取血液样品(15μl)。在每个时间点,通过离心将rbc与血浆分离,分离的rbc沉淀和血浆样品立即在-80℃冷冻。随后,使用光谱反卷积确定来自rbc的结合co的血红蛋白的分数(%hbco)和结合co的rcom的分数(%rcom-co)。与输注pbs相比,输注rcom导致结合co的hb的分数的更大降低(δ%hbco)(图24),表明rcom能够在体内清除co。
[0324]
鉴于可以应用所公开主题的原理的许多可能的实施方案,应当认识到所示实施方案仅是本公开的实例并且不应当被视为限制本公开的范围。而是,本公开的范围由如下权利要求限定。因此,我们要求保护落入所附权利要求范围和精神内的全部内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1