钠离子电池用高首效硬碳负极
1.本发明涉及一种钠离子电池的电极材料。
背景技术:
2.由于丰富的钠储量、钠元素的均匀分布、低廉的成本等优势使得钠离子电池成为后锂离子电池时代最具有商业化前景的电化学储能技术,在大规模电网储能、日常3c电子产品、电动汽车等领域具有广泛的应用前景。但是,目前商业化的石墨负极材料在钠离子电池中无法应用,其储钠容量太低,能量密度与现有商业化锂离子电池相差甚远,因此需要开发新型碳负极材料。硬碳材料,由于具有丰富的缺陷位点、发达的孔结构、较大的层间距等优势,作为钠离子电池表现出更加优异的储钠容量。但是,硬碳材料中丰富的孔隙、活性缺陷导致电解液的持续消耗,形成了固态电解质界面膜,使得硬碳负极的首周库仑效率(首效)下降。低首效将导致硬碳负极在匹配全电池时会损失正极材料提供的钠离子,使得全电池的能量密度和循环稳定性下降。
3.目前针对提高硬碳负极首效的方法主要包括预钠化、碳材料表面包覆、电解液优化等手段,但是目前这些方法仍然存在局限。表面包覆一般需要通过原子层沉积技术在碳表面沉积惰性层或者碳层以降低表面活性,但是该方法需要复杂的操作过程和设备;电解液调控,目前发现醚类电解液具备较高的首效,但是循环稳定性较差;目前的预钠化方法基本上是使用金属钠通过先进行半电池组装实现预钠化,或者将有机钠分子溶解于有机溶剂中并浸泡金属钠形成可预钠化溶液,再将碳材料浸泡在预钠化溶液实现预钠化。但是,上述方法较危险、工艺较为繁琐且耗时长,而且无法抑制电解液在碳表面的副反应,不利于钠离子电池的循环稳定性和商业化的生产。因此,仍然需要开发绿色、简单、有效、可控的方法来提高硬碳材料的首效。
技术实现要素:
4.本发明目的是提供一种高首效硬碳电极材料,其能避免或改善背景技术部分所提及的相关缺陷。
5.根据本发明的第一方面,提供了一种硬碳电极材料制备方法,包括:
6.提供有机钠盐,其选自海藻酸钠、羧甲基纤维素钠、葡萄糖酸钠、谷氨酸钠、植酸钠、柠檬酸钠以及乳酸钠中的至少一种;
7.提供有机酸,其选自依替磷酸、己二胺四甲叉膦酸、聚天冬氨酸、氨基三甲叉膦酸、2-羟基膦酰基乙酸、二乙烯三胺五甲叉膦酸中的至少一种;
8.将所述有机钠盐和所述有机酸溶解于去离子水中形成混合溶液,所述有机钠盐与所述有机酸的质量比为1:0~1:5;
9.将上述混合溶液置入封闭反应釜中进行水热聚合反应,反应温度控制在160~200℃,反应时间控制在12~24小时;
10.分离水热聚合反应产物并干燥后得到粉末物;以及将所得粉末物在保护气氛下碳
化形成硬碳材料,碳化温度设定在800~1200℃,升温速率控制在3~5℃/min,碳化时间为2~4小时。
11.本发明通过选择合适的富钠碳源(有机钠盐)与特定的杂原子前体(有机酸)进行水热聚合反应并碳化形成碳球粉末,所得到的预钠化碳材料表现出优异的首效,与其他复杂、有毒、对设备要求较高的预钠化或者表面包覆方法来提高首效明显不同,本发明的策略更加绿色、环境友好、简单有效。
12.本发明的有机钠盐作为富钠分子前驱体同时提供了理想的碳源与预钠化来源。本发明的有机酸作为杂原子分子前驱体可提供多种杂原子,并且具备与富钠分子前驱体螯合组装并协同促进交联聚合的能力。
13.根据本发明,富钠分子前驱体优选采用海藻酸钠(sa)。
14.根据本发明,杂原子分子前驱体优选采用依替磷酸(hdep)。
15.根据本发明,富钠分子前驱体与杂原子分子前驱体的质量比优选为1:2左右。
16.根据本发明,碳化温度优选为900~1100℃,更优选为1000℃。另外,升温速率优选可以为4℃/min,碳化时间优选可以为3小时。
17.根据本发明,水热反应的温度优选可以为180℃,时间优选可以为16小时。
18.根据本发明,分离出水热聚合反应产物可以采用离心沉淀去除水分,之后的干燥温度可以为65~75℃,更优选为70℃。
19.根据本发明的第二方面,还提供了一种钠离子电池负极,由根据上述方法所制备的硬碳电极材料形成。
20.根据本发明的第三方面,还提供了一种上述负极的制备方法,包括将硬碳电极材料与导电碳黑和粘结剂混合后形成浆料,并将浆料涂覆在集流体上干燥后制得。
21.根据本发明的其它方面,还提供了具有上述负极的钠离子电池。
22.本发明具有如下优点:
23.1、本发明的制备过程简单有效,避免了多种上述提高首效方法的缺陷,操作简单、无毒、无危险性,尤其是不需要预先使用金属钠或者复杂的操作设备。
24.2、本发明所用到的原料成本低廉、储量丰富,所选用的生物质衍生小分子前驱体符合绿色可持续发展的理念。
25.3、本发明所用的杂原子掺杂剂原料不仅成本低廉,而且能够提供多种原子掺杂,比如氮、磷、氧等元素同时掺杂。
26.4、本发明所设计的两种原料之间存在螯合自组装的相互协同作用,这种基于分子工程化的设计过程有利于材料的功能性设计,比如通过调控分子原料的基团以及相互作用,实现对碳材料组分与孔结构的优化。
27.5、本发明的设计理念具有良好的开放性,可预期用于制备其他多元素掺杂的碳材料,或者制备复合型碳材料,比如与金属基活性材料复合形成金属碳复合电极材料。
附图说明
28.图1是根据实施例1得到的硬碳材料的微观形貌sem图。
29.图2是根据实施例1得到的硬碳材料的孔结构信息数据。
30.图3是根据实施例1得到的硬碳负极组装的钠离子电池的循环性能。图4是根据实
施例1得到的硬碳负极组装的钠离子电池首圈充放电曲线。
31.图5是根据对比例1得到的碳负极组装的钠离子电池的循环性能。
具体实施方式
32.以下结合附图,通过具体实例详细说明本发明。
33.实施例1
34.步骤(1):称取1g海藻酸钠溶解于50ml去离子水中,不断搅拌直至完全溶解;
35.步骤(2):称取2g依替磷酸滴加进上述液体中,海藻酸钠与依替磷酸逐渐发生自组装过程,形成絮状物,并继续搅拌12小时;
36.步骤(3):将上述混合液体倒入100ml的聚四氟内胆并封闭在反应釜中,置于烘箱中水热反应,反应温度为180℃,反应时间为16小时;
37.步骤(4):将冷却后的水热反应的产物通过离心沉淀、烘干等步骤将水分排除,离心转速设定7000r/min,每次转3min,烘干温度设定70℃;
38.步骤(5):将烘干的粉末在惰性气氛下置于管式炉中碳化,升温速率设定4℃/min,碳化温度为1000℃,碳化时间为3小时。
39.将上述得到的硬碳材料作为电极的活性物质,与导电碳黑、cmc粘结剂以8:1:1的比例搅拌混匀形成浆料,并刮涂至铜箔集流体上,并在80℃下真空烘干24小时得到电极片,最后裁成一定尺寸的圆片,以钠为对电极,1m napf6的醚类为电解液,组装扣式电池。
40.图1为根据该实施例制得的硬碳样品的电镜图;图2为其n2吸脱附曲线以及孔径分布曲线;图3为根据该实施例组装的电池0.05a/g电流密度下的循环曲线;图4为该电池首周充放电曲线。
41.实施例2-6
42.将实施例1步骤(2)中的依替磷酸加入量分别改成0g、1g、3g、4g和5g,从而依次进行了实施例2-6,其他均不变。
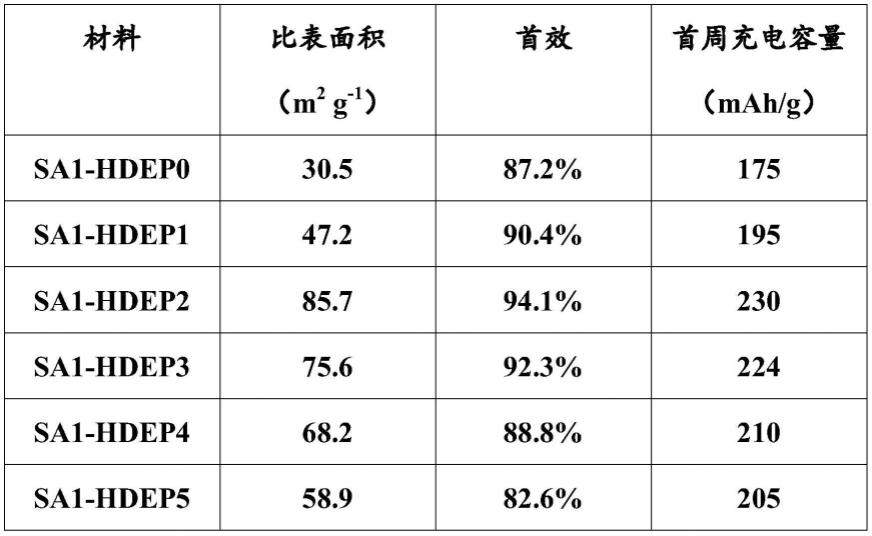
43.表1给出了实施例1-6制得的硬碳材料的比表面积以及钠离子电池性能。
44.表1
[0045][0046]
实施例7-12
[0047]
将实施例1的步骤(1)中的海藻酸钠依次换成羧甲基纤维素钠(cmc-na)、葡萄糖酸钠(gl-na)、谷氨酸钠(mg-na)、植酸钠(pa-na)、柠檬酸钠(ca-na)、乳酸钠(sl-na),其他均不变,从而依次进行了实施例7-12。
[0048]
表2给出了实施例7-12制得的硬碳材料的比表面积以及钠离子电池性能。
[0049]
表2
[0050][0051]
实施例13-17
[0052]
将实施例1步骤(2)中的依替磷酸依次换成为己二胺四甲叉膦酸(hdtmpa)、聚天冬氨酸(pasp)、氨基三甲叉膦酸(atmp)、2-羟基膦酰基乙酸(hpaa)、二乙烯三胺五甲叉膦酸
(detpmp),其他不变,从而依次进行了实施例13-17。
[0053]
表3给出了实施例13-17制得的硬碳材料的比表面积以及钠离子电池性能。
[0054]
表3
[0055][0056]
对比例1
[0057]
其它同实施例1,不同的是步骤(1)中的海藻酸钠改变成木质素磺酸钠(ln-na),实施了对比例1。
[0058]
表4给出了对比例1和实施例1制得硬碳材料的钠离子电池性能。
[0059]
表4
[0060][0061]
对比例2-4
[0062]
其它同实施例1,不同的是步骤(5)中碳化温度分别改为800、1200、1400℃。
[0063]
表5给出了对比例2-4制得的硬碳材料的钠离子电池性能。
[0064]
表5
[0065][0066]
结果分析:
[0067]
电镜图1表明实施例1制备得到的硬碳材料是微米级大尺寸的碳球颗粒,从图中可以看出碳球呈现规则的均匀分布。碳球有助于减低碳材料的比表面积,减少表面能,因此有助于缓解电解液的分解,从而提高首效。
[0068]
图2是实施例1得到的碳球的氮气吸脱附曲线,从中可以看出该碳球比表面积较小,只有85.7m
2 g-1
,而在较高的相对压力处表现出明显的大孔结构信息,从孔径分布曲线也能看到该碳球存在明显的介孔信息,说明虽然形成了碳球,但是内部仍然存在大量丰富的介孔通道,有利于电解液的浸润。
[0069]
图3是实施例1的硬碳负极组装的钠离子电池在电流密度0.05a/g下的循环曲线,图4是该过程的首周充放电曲线。从中可以看出,该硬碳负极的首效达到了94.1%,首周放电容量为244.4mah/g,充电容量为230mah/g。随着循环进行,电池容量逐渐上升,65圈循环后接近300mah/g。这些说明该电池具备良好的可逆性和稳定性。
[0070]
图5是对比例1的硬碳负极的循环性能,虽然该电池首周容量也达到了200mah/g,但是呈现明显的性能下降趋势,60圈循环后容量下降至接近50mah/g,说明该体系可逆性和稳定性都比较差。通过对比例1和实施例1的比较,说明富钠原料当中的有机骨架对碳化后的钠离子的可逆性有重要的影响,因此说明原料的选取对于实现高首效和高可逆性的硬碳负极至关重要。
[0071]
实施例2-6结果表明,随着hdep量逐渐增加,比表面积、首效、首周容量均表现先提升后下降的趋势,其中sa与hdep比例为1:2时具备最优异的性能。由于hdep与sa通过氢键组装并水热交联形成原料,hdep富含杂原子,因此对原料碳化过程的孔结构与表面组分起到了调控作用。
[0072]
实施例7-12以及实施例13-17的结果表明本发明设计理念的普适性,该实施例的硬碳负极均表现出较高的首效,但是由于不同分子中有机骨架的差异、杂原子掺杂量的差异,该系列硬碳发首效和首周容量并无明显规律。
[0073]
对比例2-4结果表明1000℃是最优的碳化温度,随着温度升高首效和首周充电容量均表现出先增加后下降的趋势。温度升高有助于提高碳材料的石墨化程度,同时能够损耗一部分不稳定且不可逆的表面官能团,因此提升电子导电性和降低活性,能够提高首效。同时温度升高有助于部分微孔的消失,提升介孔占比,也有利于提高首效。但是过高的温度
导致层间距下降、表面活性下降,碳材料的储钠容量下降。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1