一种利用数字PCR检测圆环病毒2型病毒含量的方法与流程
本发明涉及生物基因领域,涉及一种病毒核酸定量的方法,特别涉及一种利用数字PCR检测圆环病毒2型核酸含量的方法。
背景技术:
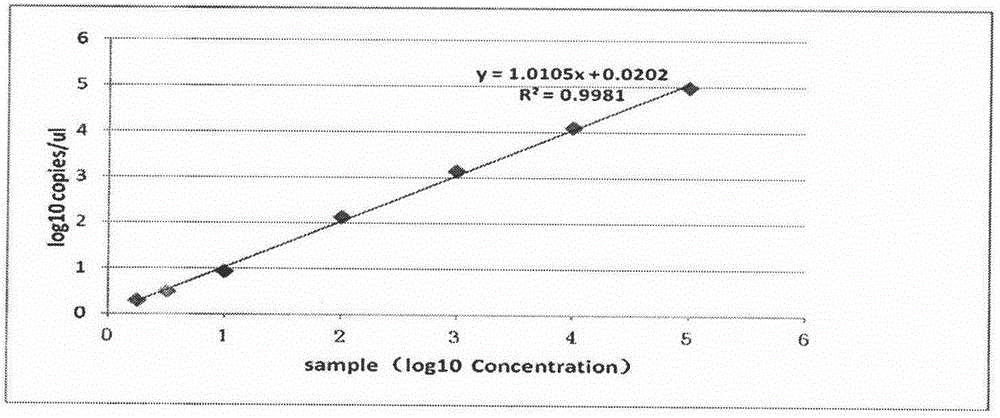
:猪圆环病毒病是由猪圆环病毒(PCV)引起的猪的一种多系统功能障碍性疾病,临床上以新生仔猪先天震颤和断奶仔猪多系统衰弱综合症为主要症状。猪圆环病毒(porcinecircovirus,PCV)在分类学上属圆环病毒科圆环病毒属,是最小的动物病毒之一。现已知PCV有两个血清型,即PCV1和PCV2。PCV1为非致病性的病毒,PCV2为致病性的病毒。针对PCV2的鉴定和检测已经有许多方法,如电镜观察、ELISA、IFA、PCR、荧光定量PCR(qPCR)等,在上述方法中qPCR技术具有快速、灵敏、高特异性等特点,因此被越来越多的应用于各种病毒的检测。但是,qPCR的定量只是“相对定量”,其准确度和重现性依然不能够满足分子生物学定量分析的要求。数字PCR(PCR(digitalpolymerasechainreaction,dPCR)是一项检测和定量核酸的新技术。20世纪末,Vogelstein等提出dPCR的概念,通过将一个样本分成几十到几万份,分配到不同的反应单元,每个单元包含一个或多个拷贝的目标分子(DNA模板),在每个反应单元中分别对目标分子进行PCR扩增,扩增结束后对各个反应单元的荧光信号进行统计学分析。与qPCR不同的是,dPCR不依赖于CT值,因此不受扩增效率影响,扩增结束后通过直接计数或泊松分布公式来计算每个反应单元的平均浓度(含量)能够将误差控制在5%以内,dPCR可以不需要对照标准样品和标准曲线来实现绝对定量分析。由于dPCR是一项具有可重复性的定量微量DNA分子的优良技术.其操作方便、检测通量高、特异性强、灵敏度高、定量准确等优点使其成为了分子生物学研究中的重要工具,并已经应用于单细胞分析、癌症早期诊断和产前诊断、疫病检测等研究领域。将dPCR技术用于PCV2的检测,可以快速、准确的对PCV2核酸进行绝对定量。技术实现要素::本发明的目是提供一种利用数字PCR检测样品中PCV2核酸浓度的试剂盒及方法。数字PCR方法在动物疫病检测、疫苗生产质量控制中的应用也属于本发明的保护范围。本发明是一种高灵敏度的检测圆环病毒2型的方法,步骤包括:(1)样品中病毒DNA的提取,获得PCR扩增模板;(2)数字PCR反应体系的配置,进行dPCR反应;所述PCR反应体系中含有步骤(1)获得的PCR扩增模板、PCV2特异引物对、探针、dNTP和DNA聚合酶;(3)根据步骤(2)dPCR反应产生的荧光信号,计算得到所述待测样品中的PCV2拷贝数;在上述方法中,所述待测样品可以为组织病料、也可以是病毒细胞培养物。在本发明的实施例中,所述待测样品为组织病料,具体为猪淋巴结、脾和肾脏;(4)当所述待检样品为组织病料时,上述方法的步骤(1)中,所述“病毒DNA的提取”可为将所述待测样品(组织病料)进行研磨匀浆,冻融3次。将所述待测样品(组织病料)8000~14000g离心1~5min,温度可为4℃。取上清液,采用商品化病毒DNA提取试剂盒进行核酸提取。当上述样品为血液、组织液、尿液等液体样品时,上述方法步骤(1)中,所述“病毒DNA的提取”可为8000~14000g离心1~5min,采用商品化病毒DNA提取试剂盒进行核酸提取。在上述的检测方法的步骤(2)中,进行所述数字PCR反应时的退火温度可为53℃。进一步,在本发明中,进行所述数字PCR反应时的反应程序为:95℃10min;94℃30s,53℃60s,40个循环;98℃10min。PCR仪升降温速度设定为≤2.5℃。在上述的检测方法的步骤(2)中,所述最佳反应体系为2×ddPCRsupermixforprobe10uL,上下游引物各100-900nmol/L,探针100-900nmol/L,模板DNA(cDNA)小于200ng,补灭菌水至总体积20uL;在上述的检测方法的步骤(2)中,所述PCV2引物具体为由序列表中序列1和序列2所示的两条单链DNA分子引物对,探针为序列表中序列3所示的1条单链DNA分子。在上述方法中,所述的探针的荧光基团选自6-羧基荧光素(FAM)、六氯-6-羧基荧光数(HEX),Cy5(美国LifeTechnologies)、Cy3(美国LifeTechnologies)、VIC(美国LifeTechnologies),荧光淬灭基团选自6-羧基四甲基若丹明(TAMARA)、BHQ1(美国LifeTechnologies)、BHQ2(美国LifeTechnologies)或MGB(美国LifeTechnologies)。在上述方法中,进行所述数字PCR反应,并根据产生的荧光信号计算所述待测样品中PCV2核酸拷贝数。首先,利用数字PCR系统的微滴发生器将配置好的反应体系进行分液处理,生成10000~20000个油包水的反应液滴,使每个微滴的PCR扩增模板数少于或者等于1个;其次,进行PCR循环扩增并进行结果判断:对PCR扩增反应后的产物进行信号收集,根据液滴中有荧光信号的液滴数量确定PCV2DNA模板的数量。可用QuantaSoft(Bio-Rad)软件进行数据分析,计算样品中病毒的核酸拷贝数。通过上述方法,可以检测PCV2的病毒核酸拷贝数。本发明的有益效果在于:本发明采用数字PCR技术检测PCV2病毒,其检测的灵敏度略高于荧光定量PCR技术;而且本方法不用设置标准曲线,根据检测结果可以直接判读样品中PCV2的核酸拷贝数,极大的简化了操作步骤。附图说明为了使本发明的目的、技术方案和优点更加清楚,下面将结合附图对本发明作进一步的详细描述,其中:图1dPCR退火温度优化结果(A~H依次为61℃~51℃)图2dPCR各浓度梯度检测结果。标准品浓度为4.85×103copy/ul、4.85×102copy/ul、4.85×101copy/ul、4.85×10-1copy/ul、2.43×10-1copy/ul、1.21×10-1copy/ul、6.06×10-2copy/ul。图3dPCR各浓度梯度检测结果线性关系图。具体实施方式:下面结合附图和具体实例对本发明做进一步说明,但不作为对本发明的限定。1.主要试验仪器CFX96荧光定量PCR仪(Bio-Rad公司);水平电泳及凝胶成像分析系统(Bio-Rad公司);梯度PCR扩增仪(Bio-Rad公司);超微量分光光度计;QX-i00微滴式数字PCR仪(Bio-Rad公司);Thermo核酸提取仪;培养箱;低温冰箱;恒温循环水浴槽;高速冷冻离心机;常温离心机;2试验材料和试剂病毒DNA/RNA磁珠法提取试剂盒(成都拓洋科技有限公司);2×PremixExTaqProbeqPCR(TakaRa公司);2×SsoFastTMProbesSupermix(美国伯乐公司);DNA分子量标准、琼脂糖(宝生物工程(大连)有限公司);其他试剂均为国产分析纯。圆环病毒疫苗株由四川华派生物技术公司提供。引物和探针送上海基康生物科技有限公司合成,见下表。名称序列长度bpSeq1CGCTGGAGAAGGAAAAATGG20Seq2CTTGACAGTATATCCGAAGGT21Seq3FAM-TTCAACACCCGCCTCTCCCG-BHQ203病毒DNA模板的制备病毒DNA提取采用成都拓洋科技有限公司的病毒DNA/RNA核酸提取试剂盒按操作说明书进行操作。病毒DNA溶于100μl灭菌蒸馏水中,立即使用或-20℃。4微滴式数字PCR的检测程序4.1反应液的配置采用2×ddPCRsupermixforprobe(Bio-Rad)试剂推荐的20uL体系,以2uL步骤3获取的模板,加入10uL2×ddPCRsupermixforprobe,加入上下游引物各2uL(终浓度为900nmol/L),加入探针2uL (终浓度为250nmol/L),不灭菌水至总体积20uL。4.2反应液的处理将20uL样品反应体系加入DG8cartridge中间一排的8个孔内,避免引入气泡,在DG8cartridge最底下的8个孔中各加入70uL微滴生成油(DGoil),盖上胶垫,将以上holder放入微滴生成仪,生成微滴。用排枪将生成的微滴缓慢转入96孔板相应位置,封膜。4.3PCR扩增将封好膜的96孔板转入梯度PCR仪中进行PCR扩增。反应程序为95℃,10min;94℃,30s;52℃,60s,40个循环;98℃,10min)。4.4荧光信号的读取PCR结束后将96孔板放入数字PCR微滴荧光检测仪进行荧光收集,根据每管反应体系中发出荧光的微滴数量,根据泊松定律计算出反应体系中的PCV2核酸拷贝数。试验同时以实时荧光PCR技术,采用标准曲线方法,对PCV2进行相对定量。计算样品中PCV2核酸拷贝数。试验重复三次,结果取平均值。检测结果见下表:当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1