对淋巴细胞中抑制途径的中和的制作方法
相关申请的引证
本申请要求于2014年9月16日提交的美国临时申请号62/050,948、2014年11月25日提交的美国临时申请号62/083,929、和2014年12月17日提交的美国临时申请号62/093,141的权益,将所有这些申请通过引用以其全文(包括任何附图)结合在此。
序列表的引用
本申请是连同电子格式的序列表提交的。序列表被提供为题为“nkg2a-pd1_st25”的文件,创建于2015年9月15日,大小是38kb。将在电子格式的序列表中的信息通过引用以其全文结合在此。
本发明涉及nkg2a中和剂和pd-1中和剂用于治疗癌症的联合用途。
背景技术:
nk细胞活性受包括激活信号和抑制信号两者的复合机制的调节。已经鉴定出若干种不同的nk特异性受体,这些受体在nk细胞介导的hlai类缺陷靶细胞的识别和杀灭中发挥重要作用。自然细胞毒性受体(ncr)是指一类活化受体蛋白质和表达它们的基因(其在nk细胞中特异性表达)。ncr的实例包括nkp30、nkp44、和nkp46(参见,例如,拉尼尔(lanier)(2001)自然免疫学(natimmunol)2:23-27,彭德(pende)等人(1999)实验医学杂志(jexpmed.)190:1505-1516,坎托尼(cantoni)等人(1999)实验医学杂志189:787-796,西沃里(sivori)等人(1997)实验医学杂志186:1129-1136,派西诺(pessino)等人(1998)实验医学杂志188(5):953-60;曼德博伊姆(mandelboim)等人(2001)自然(nature)409:1055-1060,将其全部披露的内容通过引用结合在此)。这些受体是ig超家族的成员,并且它们的交联(由特异性mab诱导)导致强的nk细胞活化,从而导致增加的细胞内ca++水平,引发细胞毒性和淋巴因子再释放、以及活化针对许多类型靶细胞的nk细胞毒性。
cd94/nkg2a是在淋巴细胞亚群上发现的抑制性受体。cd94/nkg2a限制某些淋巴细胞对表达cd94/nkg2a-配体hla-e的细胞的细胞因子释放和细胞毒性反应(参见,例如,wo99/28748)。还发现某些肿瘤细胞(德尔(derre)等人,免疫学杂志(jimmunol)2006;177:3100-7)和活化的内皮细胞(库佩尔(coupel)等人,血液(blood)2007;109:2806-14)以可溶形式分泌hla-e。抑制cd94/nkg2a信号传导的抗体可增加淋巴细胞针对hla-e阳性靶细胞的细胞因子释放和细胞溶解活性,例如cd94/nkg2a阳性nk细胞针对表达hla-e的肿瘤细胞或病毒感染细胞的反应。因此,抑制cd94/nkg2a但不引起杀死表达cd94/nkg2a的细胞的治疗性抗体(即,非耗竭性抗体)可诱导对癌症患者中的肿瘤生长的控制。
pd-1是cd28家族受体的抑制性成员,该家族还包括cd28、ctla-4、icos和btla。pd-1在活化的b细胞、t细胞和骨髓细胞上表达(冈崎(okazaki)等人(2002)当前免疫学观点(curr.opin.immunol.)14:391779-82;班尼特(bennett)等人(2003)免疫学杂志(jimmunol)170:711-8)。已经鉴定了pd-1的两种配体(pd-l1和pd-l2),这两种配体已经显示在结合至pd-1后下调t细胞活化(弗里曼(freeman)等人(2000)实验医学杂志192:1027-34;莱切曼(latchman)等人(2001)自然免疫学(natimmunol)2:261-8;卡特(carter)等人(2002)欧洲免疫学杂志(eurjimmunol)32:634-43)。多种人类癌症中存在大量的pd-l1(董(dong)等人(2002)自然医学(nat.med.)8:787-9)。pd-1和pd-l1之间的相互作用导致肿瘤浸润淋巴细胞的减少、t细胞受体介导的增殖的减少、以及癌细性胞的免疫逃避。通过抑制pd-1与pd-l1的局部相互作用,可以逆转免疫抑制,并且当pd-1与pd-l2的相互作用也被阻断时,该效果是累加的。
pd-1阻断已在许多临床试验中产生了令人印象深刻的抗肿瘤反应。然而,并非所有患者都对抗肿瘤反应的治疗有反应,并且此外一些患者患有在治疗后复发的癌症。因此,在本领域中存在着对于用pd-1轴线抑制剂治疗的患者的改进益处的需要。
技术实现要素:
本发明提供了通过抑制性受体nkg2a和pd-1的组合中和(例如,通过使用抗体)来增强抗肿瘤免疫应答的改进方法。尽管cd8t细胞和nk细胞(在外周)不表达nkg2a和pd-1,但已经发现介导消除肿瘤细胞的肿瘤浸润淋巴细胞能够表达抑制性受体pd-1和抑制性受体nkg2a两者。此外,用抗pd1的治疗可以引起肿瘤浸润淋巴细胞上的nkg2a受体的上调,这样使得nkg2a可以限制阻断pd1轴线的试剂的疗效。由于这些受体都可以限制肿瘤浸润淋巴细胞的细胞毒性活性,因此这两种受体的抑制性活性的中和通过抗体使得nkg2a+pd1+淋巴细胞有效地消除癌细胞。在一个实施例中,nkg2a+pd1+淋巴细胞是细胞毒性淋巴细胞,任选地是cd8+t细胞或nk细胞。
抑制或中和pd-1的抑制性活性可以有利地涉及多肽(例如抗体、与fc结构域融合的多肽、免疫粘附素等)的使用,该多肽例如通过阻断与其天然配体pd-l1的相互作用(并且任选地进一步阻断pd-1和pd-l2之间的相互作用)来防止pd-l1诱导的pd-1信号传导。在一方面中,该多肽是结合pd-1的抗体(抗pd-1抗体);这样的抗体可以阻断pd-1和pd-l1之间和/或pd-1和pd-l2之间的相互作用。在另一方面中,该多肽是结合pd-l1(抗pd-l1抗体)并阻断pd-1和pd-l1之间的相互作用的抗体。
因此,在一个实施例中,提供了用于治疗或预防个体中的癌症的方法,该方法包括向个体给予:(a)治疗活性量的抑制人nkg2a多肽的化合物,和(b)治疗活性量的抑制人pd-1多肽的化合物。在一个实施例中,该癌症是实体瘤。在一个实施例中,抑制人nkg2a多肽的化合物是中和nkg2a的抑制性活性的抗体。在一个实施例中,抑制人pd-1多肽的化合物是中和pd-1的抑制性活性的抗pd-1或抗pdl-1抗体。该个体可被指定为人类。
在一个实施例中,提供了激活或增强个体中的cd8+肿瘤浸润t细胞的活性的方法,该方法包括向个体给予:(a)治疗活性量的抑制人nkg2a多肽的化合物,和(b)治疗活性量的抑制人pd-1多肽的化合物。在一个实施例中,提供了激活或增强个体中的肿瘤浸润nk细胞的活性的方法,该方法包括向个体给予:(a)治疗活性量的抑制人nkg2a多肽的化合物,和(b)治疗活性量的抑制人pd-1多肽的化合物。
在一方面中,提供了治疗,该治疗包括给予中和nkg2a的抑制性活性的抗体与中和pd-1的抑制性活性的抗体的组合。
在一方面中,提供了组合物,该组合物包含抑制人nkg2a多肽的抗体和抑制人pd-1多肽的抗体。在一方面中,该组合物用于在治疗或预防癌症(任选地是实体瘤(任选地是血液恶性病))中使用。
在一个实施例中,以导致人类患者(体内)中人cd94/nkg2a的抑制性活性发生中和的量(例如以导致人cd94/nkg2a对人类患者中cd8t细胞和nk细胞的抑制性活性进行中和的量)给予该抗nkg2a抗体。在一个实施例中,导致人类患者中人cd94/nkg2a的抑制性活性发生中和的量为使nkg2a受体在nkg2a+细胞表面上基本上饱和所需的最小浓度(例如,在结合测定中,其中在pbmc上滴定抗体)的至少10倍(例如,10-20倍、10-50倍、10-100倍、20-50倍、20-100倍、30-100倍、50-100倍),任选地至少50倍、60倍、80倍或100倍。在一个实施例中,该抗nkg2a抗体与hla-e竞争结合人nkg2a。
在一个实施例中,该抗nkg2a抗体被给予至少一个给予周期,该给予周期包含该抗nkg2a抗体的至少第一次和第二次(和任选地第3次、第4次、第5次、第6次、第7次和/或第8次或更多次)给予,其中在第一次和第二次(和任选地更多次)给予之间以有效实现至少为10μg/ml(或任选地至少20μg/ml、30μg/ml、40μg/ml或50μg/ml)的抗nkg2a抗体的连续(最小)血液浓度的量给予该抗nkg2a抗体。实现或维持指定的连续血液浓度意味着,在指定时间段的持续时间内(例如在抗体的两次给予之间,数周),血液浓度基本上不下降到指定的血液浓度以下,即尽管血液浓度在指定时间段期间可以变化,但指定的血液浓度仍表示最小或“谷”浓度。
在一个实施例中,以在给药后(例如在给予的1或2天内)有效实现约或至少约50、60、70或80μg/ml(任选地至少约100μg/ml)的峰血液浓度的量给予该抗nkg2a抗体。
在一个实施例中,以有效实现约或至少约10、20、30、40、50、60、70或80μg/ml(任选地至少约100μg/ml)的抗nkg2a抗体的连续(最小)血液浓度的量给予该抗nkg2a抗体持续至少一周或至少两周,随后给予该抗体。
在一个实施例中,在两次连续给予之间以有效实现约或至少约50、60、70或80μg/ml(任选地至少约100μg/ml)的抗nkg2a抗体的连续(最小)血液浓度的量给予该抗nkg2a抗体。在一个实施例中,第一次和第二次给予在时间上间隔约两周,任选地约一周。
可以任选地以有效的量,并且根据达到如给予周期的整个持续时间中所指定的连续(最小)血液浓度的频率来给予该抗nkg2a抗体。
在一个实施例中,该抗nkg2a抗体与中和人pd-1多肽的抗体组合给予,用于治疗个体中的实体瘤,其中给予周期包括至少两次给予该抗nkg2a抗体,其中在两次连续给予之间以有效实现血管外组织(例如,在肿瘤环境中)中为至少4μg/ml(任选至少10μg/ml)的连续(最小)浓度的量给予该抗nkg2a抗体。任选地,以有效实现血管外组织(例如,在肿瘤环境中)中为至少4μg/ml(任选至少10μg/ml)的连续(最小)浓度的量给予该抗nkg2a抗体,保持给予周期的整个持续时间。在一个实施例中,在两个连续给予之间或给予周期的持续时间内,以有效实现为至少40μg/ml(任选至少100μg/ml)的抗nkg2a抗体的连续(最小)血液浓度的量给予该抗nkg2a抗体。
在一个实施例中,以导致人类患者(体内)中人pd-1的抑制性活性发生中和的量(例如以导致人pd-1对人类患者中cd8t细胞和nk细胞的抑制性活性进行中和的量)给予中和人pd-1多肽的抗体。在一方面中,根据特定的临床剂量方案,尤其是以特定的剂量并根据具体的给药方案,给予该组合(或用于给予)。
在一方面中,中和nkg2a的抗体是非耗竭性抗体(例如,不杀死、消除、裂解或诱导这样的杀伤、消除或裂解的抗体),以便负面影响样品或受试者中存在的表达nkg2a的细胞的数量。在一方面中,中和pd-1的抗体是非耗竭性抗体。非耗竭性抗体可以例如缺少fc结构域或具有对一个或多个fcγ受体(例如cd16)具有最小结合或无结合的fc结构域。实例包括具有来自人igg4同种型抗体的恒定区的抗体、具有经修饰以降低或消除与一个或多个fcγ受体(例如cd16)的结合的恒定区的任何同种型(例如igg1、igg2、igg3)的抗体。
在一个实施例中,该癌症是晚期和/或难治性实体瘤。在一个非限制性实施例中,该癌症(例如晚期难治性实体瘤)选自下组,该组由以下各项组成:非小细胞肺癌(nsclc)、肾癌、胰腺癌或食管腺癌、乳腺癌、肾细胞癌(rcc)、黑色素瘤、结肠直肠癌、以及卵巢癌。
抑制nkg2a多肽的化合物(抗nkg2a试剂)是提高表达nkg2a的nk和/或t细胞引起表达hla-e的细胞死亡的能力的化合物。任选地,该抑制nkg2a多肽的化合物是多肽,任选地是结合nkg2a多肽的抗体(例如单克隆抗体)。
在一个实施例中,该抗nkg2a试剂通过阻断其配体hla-e的结合来降低nkg2a的抑制性活性,即该抗nkg2a试剂通过hla-e干扰nkg2a的结合。具有seqidno:4-8中任一个的重链和seqidno:9的轻链的抗体是此类抗体的实例。在一个实施例中,该抗nkg2a试剂降低nkg2a的抑制活性而不阻断其配体hla-e的结合,即该抗nkg2a试剂是非竞争性拮抗剂并且不通过hla-e干扰nkg2a的结合。具有seqidno:10和11的重链和轻链可变区的抗体分别是此类抗体的实例。
在一个实施例中,该抗nkg2a试剂是以比与一种或多种活化nkg2受体显著更高的亲和力与nkg2a结合的抗体。例如,在一个实施例中,该试剂是以比与nkg2c显著更高的亲和力与nkg2a结合的抗体。在另外的或可替代的实施例中,该试剂是以比与nkg2e显著更高的亲和力与nkg2a结合的抗体。在另外的或可替代的实施例中,该试剂是以比与nkg2h显著更高的亲和力与nkg2a结合的抗体。
在一个实施例中,该抗nkg2a试剂与分别具有seqidno:4-8和9的重链和轻链的抗体或分别具有seqidno:10和11的重链和轻链可变区的抗体竞争与cd94/nkg2a的结合。该试剂可以是例如人或人源化抗nkg2a抗体。
在一个实施例中,该抗nkg2a抗体是分别具有seqidno:4-8中任一个的任意重链的重链cdr和seqidno:9的轻链的轻链cdr的人源化抗体。在一个实施例中,该抗nkg2a抗体是分别具有seqidno:4-8中任一个的任意重链的重链可变区和seqidno:9的轻链的轻链可变区的人源化抗体。提供了具有改进的性质(如,例如较低的免疫原性、改善的抗原结合或其他功能性质)、和/或改善的物理化学性质(如,例如更好的稳定性)的这类人源化抗体的框架区(fr)中的示例性互补决定区(cdr)残基或序列和/或氨基酸取代位点。
在某些任选方面中,可以通过评估nkg2a配体(任选地进一步是pd-1的配体)在肿瘤样品(例如,肿瘤组织和/或肿瘤邻近组织)中的存在来鉴定用抗nkg2a试剂和pd1中和剂治疗的患者。在本文的任何治疗用途或者癌症治疗或预防方法的一个实施例中,个体中癌症的治疗或预防包括:
a)确定该患有癌症的个体内的恶性细胞的hla-e多肽状态,并且
b)在确定hla-e多肽由恶性细胞(例如肿瘤细胞)(例如在其表面上)显著表达后,向该个体给予中和人nkg2a多肽的抑制性活性的化合物以及抑制人pd-1多肽的试剂。
在本文的任何治疗用途或者癌症治疗或预防方法的一个实施例中,个体中癌症的治疗或预防包括:
a)确定该患有癌症的个体内的恶性细胞(例如肿瘤细胞)的hla-e多肽状态和pd-l1多肽状态,并且
b)在确定hla-e和pd-l1多肽在恶性细胞的表面上显著表达后,向该个体给予中和人nkg2a多肽的抑制性活性的化合物以及抑制人pd-1多肽的试剂。
在一个实施例中,确定生物样品(例如,包含肿瘤细胞、肿瘤组织和/或肿瘤相邻组织的样品)显著表达hla-e核酸或多肽表明了,个体患有癌症,该癌症可用抑制nkg2a的试剂与抑制人pd-1多肽的试剂组合进行治疗。
在任何方法的一个实施例中,在步骤(a)中测定hla-e多肽状态或测定表达水平包括测定生物样品中恶性细胞的hla-e核酸或多肽的表达水平,并且将该水平与参考水平(例如,值、弱或强的细胞表面染色等)进行比较。该参考水平可以例如对应于健康个体,对应于从用抗nkg2a抗体(任选地与抑制人pd-1多肽的试剂组合)的治疗中未得到/得到低临床益处的个体,或对应于从用抗nkg2a抗体(任选地与抑制人pd-1多肽的试剂组合)的治疗中得到实质性临床益处的个体。确定生物样品以增加的水平(例如,高值、强表面染色,与从用抗nkg2a抗体的治疗中得到实质性临床益处的个体的水平相应的水平,高于从用抗nkg2a抗体的治疗中未得到/得到低临床益处的个体的水平相应的水平等)表达hla-e核酸或多肽表明了,该个体患有癌症,该癌症可用抗nkg2a抗体与抑制人pd-1多肽的试剂组合进行治疗,例如根据本文所述的治疗方法。
在一个实施例中,提供了用于鉴定抑制nkg2a的表达pd-1的淋巴细胞的方法,该方法包括:
a)测定生物样品中nk和/或cd8t淋巴细胞的nkg2a和pd-1多肽状态,并且
b)其中确定nkg2a和pd-1多肽在显著比例的淋巴细胞表面上表达表明了,这些淋巴细胞是抑制nkg2a的表达pd-1的淋巴细胞。任选地,这些淋巴细胞是肿瘤浸润淋巴细胞。任选地,该生物样品是包含肿瘤组织和/或肿瘤相邻组织的样品。
在一个实施例中,提供了用于鉴定患有癌症的个体的方法,用抗nkg2a试剂治疗该个体是适合的,该方法包括:
a)确定来自该个体的肿瘤浸润淋巴细胞的nkg2a和pd-1多肽状态,并且
b)其中确定nkg2a和pd-1多肽在来自该个体的显著比例的肿瘤浸润淋巴细胞(任选地预定义的亚群(例如cd8t细胞、nk细胞)的til)的表面上表达表明了,用中和人nkg2a多肽的抑制性活性的化合物和抑制人pd-1多肽的试剂的治疗适合于该个体。
在一个实施例中,提供了用于治疗或预防个体中癌症的方法,该方法包括:
a)确定来自该个体的肿瘤浸润淋巴细胞的nkg2a和pd-1多肽状态,并且
b)在测定nkg2a和pd-1多肽在来自该个体的显著比例的肿瘤浸润淋巴细胞(任选地预定义的亚群(例如cd8t细胞、nk细胞)的til)的表面上表达之后,向该个体给予治疗方案,该治疗方案包括中和人nkg2a多肽的抑制性活性的化合物和抑制人pd-1多肽的试剂。
在一个实施例中,肿瘤浸润淋巴细胞是cd8t细胞。在一个实施例中,肿瘤浸润淋巴细胞是nk细胞。在一个实施例中,至少10%、15%、20%、25%的cd8t细胞是nkg2a+pd+。在一个实施例中,至少10%、15%、20%或25%的cd8t细胞是nkg2a+pd-1+。在一个实施例中,至少20%、25%、30%或35%的nk细胞是nkg2a+pd-1+。
在其他实施例中,提供了药物组合物和试剂盒、以及使用它们的方法。在一个实施例中,提供了药物组合物,该药物组合物包含中和人nkg2a多肽的抑制性活性的化合物和抑制人pd-1多肽的试剂。在一个实施例中,提供了试剂盒,该试剂盒包含中和人nkg2a多肽的抑制性活性的化合物和抑制人pd-1多肽的试剂。
将这些方面更全面地描述于在此提供的本发明的说明书中,并且另外的方面、特征和优点将从该说明书中显而易见。
附图说明
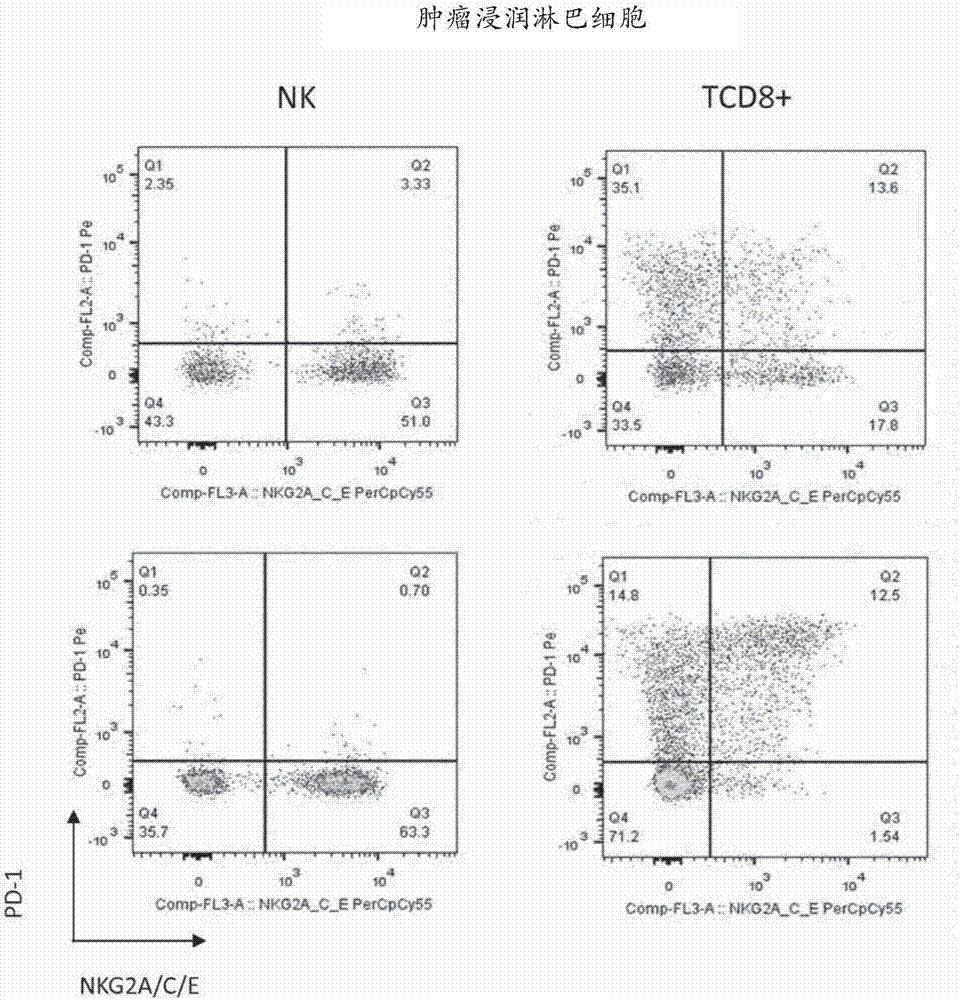
图1a和图1b示出pd-l1+qa-1+rma-sqa-1qdmb2m和a20肿瘤细胞被表达nkg2a的nk细胞和表达nkg2a和/或pd-1的cd8t细胞浸润。当肿瘤体积为约500mm3时,处死rma-sqa-1qdmb2m(顶行)和a20(底行)荷瘤小鼠。通过流式细胞术分别针对肿瘤细胞的qa-1和pdl-1的表达以及til的nkg2a/c/e和pd-1的表达来分析肿瘤细胞(图1a)和肿瘤浸润淋巴细胞-til-(图1b)。mfl荧光强度的中位数。
图2示出小鼠中nkg2a和pd-1在nk细胞和t细胞亚群上的分布。淋巴细胞取自脾、肿瘤引流淋巴结、以及实体瘤块内。在来自脾和淋巴结的所有细胞亚群中pd-1表达不频繁或不存在,然而在肿瘤浸润淋巴细胞(til)中,所有细胞亚群具有相对高百分比的表达pd-1的细胞。另一方面,nkg2a在nk细胞上发现,但未在脾和淋巴结中的t细胞亚群上发现,但在显著百分比的til中发现肿瘤,平均超过30%的nk细胞和超过19%的cd8t细胞对nkg2a和pd-1是双阳性的。
图3a和图3b示出在荷瘤小鼠中的nkg2a和pd-1表达。当其肿瘤体积分别达到500mm3、2000mm3和800mm3时,处死rmarae1(顶行)、mc38(中行)和rma(底行)荷瘤小鼠。通过流式细胞术在脾、肿瘤引流淋巴结(ln)和肿瘤中针对nkg2a/c/e和pd-1表达来分析nk细胞(图3a)和cd8t细胞(图3b)。
图4示出用抗pd-1mab治疗小鼠增加了mc38肿瘤中表达nkg2a的tcd8细胞的频率。在细胞移植后第11天、第14天和第17天,用200μg的大鼠igg2a同种型对照(ic)或抗小鼠pd-1抗体处理mc38荷瘤小鼠。在第31天处死小鼠,并通过流式细胞术在脾、肿瘤引流淋巴结(ln)和肿瘤中表征cd8t细胞。
图5示出在第11天、第14天和第18天用同种型对照、抗小鼠nkg2amab(200μg,静脉)、抗小鼠pd-l1mab(200μg,腹腔)或抗mnkg2a/mpdl-1组合处理的小鼠中随时间推移的肿瘤体积中位数。虽然与该模型中的同种型对照相比,抗nkg2a仅产生适度的抗肿瘤效应,并且抗pd-l1产生实质性抗肿瘤效应但肿瘤体积随着接近第28天而增加,用抗nkg2a和抗pd-l1组合治疗完全消除肿瘤生长,在第28天观察到肿瘤体积没有显著生长。
具体实施方式
定义
如在该说明书中所使用的,“一种/一个(a/an)”可以意指一种/一个或多于一种/一个。如在权利要求中使用的,当与词“包括(comprising)”结合使用时,这些词“一种/一个(a/an)”可以意指一种/一个或多于一种/一个。如在此所使用的,“另一个”可以意指至少第二个或更多个。
当使用“包括”时,这可以任选地被“基本上由......组成”或通过“由......组成”代替。
nkg2a(omim161555,将其全部公开内容通过引用结合在此)是nkg2转录物组的成员(霍施因斯(houchins)等人(1991)实验医学杂志173:1017-1020)。nkg2a由跨越25kb的7个外显子编码,显示出一些差别剪接。nkg2a与cd94一起形成在nk细胞、α/βt细胞、γ/δt细胞、和nkt细胞的亚群的表面上发现的异源二聚体抑制性受体cd94/nkg2a。与抑制性kir受体类似,nkg2a在其胞质域中具有itim。如本文所使用的,“nkg2a”是指nkg2a基因或编码的蛋白的任何变体、衍生物或同种型。人nkg2a在3个结构域中包含233个氨基酸,其中是包含残基1-70的胞质域,包含残基71-93的跨膜区,以及包含残基94-233的胞外区,该人nkg2a具有以下序列:
mdnqgviysdlnlppnpkrqqrkpkgnkssilateqeityaelnlqkasqdfqgnd-ktyhckdlpsapeklivgilgiiclilmasvvtivvipstliqrhnnsslntrtqkarhcghcpeewitysnscyyigkerrtweesllactsknssllsidneeemkflsiispsswigvfrnsshhpwvtmnglafkheikdsdnaelncavlqvnrlksaqcgssiiyhckhkl(seqidno:1).
nkg2c(omim602891,将其全部公开内容通过引用并入本文)和nkg2e(omim602892,将其全部内容通过引用并入本文)是nkg2转录物组的另外两个成员(吉尔恩科(gilenke)等人,(1998)免疫遗传学(immunogenetics)48:163-173)。cd94/nkg2c和cd94/nkg2e受体是在淋巴细胞(例如nk细胞和t细胞)的亚群的表面上发现的活化受体。
hla-e(omim143010,将其全部公开内容通过引用并入本文)是在细胞表面上表达并受肽的结合调节的非经典mhc分子,例如衍生自其他mhci类分子的信号序列的片段。还已经鉴定了hla-e的可溶性形式。除了它的t细胞受体结合特性,hla-e通过特异性结合cd94/nkg2a、cd94/nkg2b和cd94/nkg2c(参见,例如,布劳德(braud)等人,(1998)自然(nature)391:795-799,其全部公开内容通过引用并入本文)而结合自然杀伤(nk)细胞、自然杀伤t细胞(nkt)和t细胞(α/β和γ/δ)的亚群。hla-e的表面表达保护靶细胞免受cd94/nkg2a+nk、t、或nkt细胞克隆的裂解。如本文所使用的,“hla-e”是指hla-e基因或编码的蛋白的任何变体、衍生物或同种型。
在本发明的上下文中,“nkg2a”或“cd94/nkg2a阳性淋巴细胞”是指在细胞表面上表达cd94/nkg2a的淋巴谱系(例如nk细胞、nkt细胞和t细胞)的细胞,这些细胞可以通过例如使用抗体的流式细胞术来检测,这些抗体特异性识别cd94和nkg2a上的组合表位或单独nkg2a上的表位。“nkg2a阳性淋巴细胞”还包括淋巴起源的无限增殖细胞系(例如nkl、nk-92)。
在本发明的上下文中,“降低nkg2a的抑制性活性”、“中和nkg2a”或“中和nkg2a的抑制性活性”是指如下过程,其中cd94/nkg2a在其负面影响导致淋巴细胞反应(如,细胞因子释放和细胞毒性反应)的细胞内过程的能力方面受到抑制。这可以例如在基于nk细胞或t细胞的细胞毒性测定中进行测量,其中测量治疗性化合物用于刺激cd94/nkg2a阳性淋巴细胞杀死hla-e阳性细胞的能力。在一个实施例中,抗体制剂引起cd94/nkg2a限制性淋巴细胞的细胞毒性增加至少10%,任选地淋巴细胞细胞毒性增加至少40%或50%,任选地nk细胞毒性增加至少70%,并且涉及所述的细胞毒性测定。如果抗nkg2a抗体减少或阻断cd94/nkg2a与hla-e的相互作用,则它可以增加cd94/nkg2a限制性淋巴细胞的细胞毒性。这可以例如在标准的4小时体外细胞毒性测定中,使用例如表达cd94/nkg2a的nk细胞和表达hla-e的靶细胞进行评价。这类nk细胞不能有效地杀死表达hla-e的靶标,因为cd94/nkg2a识别hla-e,从而导致阻止淋巴细胞介导的细胞溶解的抑制性信号传导的启动和传播。此类体外细胞毒性测定可以通过本领域熟知的标准方法进行,如例如在科里根(coligan)等人编辑,当代免疫学指南(currentprotocolsinimmunology),格林出版联盟和威力跨学科(greenepublishingassoc.andwileyinterscience),纽约(1992,1993)中所描述的。用以评估抗体刺激淋巴细胞杀死靶细胞(例如p815、k562细胞或适合的肿瘤细胞)的能力的铬释放和/或其他参数也披露于西沃里(sivori)等人,实验医学杂志1997;186:1129-1136;瓦伊塔尔(vitale)等人,实验医学杂志1998;187:2065-2072;派西诺(pessino)等人,实验医学杂志1998;188:953-960;内里(neri)等人,临床与诊断实验室免疫学(clin.diag.lab.immun.)2001;8:1131-1135;彭德(pende)等人,实验医学杂志1999;190:1505-1516中;将其各自全部披露的内容通过引用结合在此。在添加nk细胞之前,用51cr标记这些靶细胞,并且然后作为杀伤结果,据估计杀伤与从细胞释放到培养基的51cr成比例。添加防止cd94/nkg2a与hla-e结合的抗体导致防止经cd94/nkg2a的抑制性信号传导的启动和传播。因此,添加这类试剂导致淋巴细胞介导的靶细胞杀伤的增加。该步骤由此鉴定通过例如阻断配体结合来阻止cd94/nkg2a诱导的负信号传导的试剂。在特定的释放51cr的细胞毒性测定中,表达cd94/nkg2a的nk效应细胞可以杀死hla-e阴性lcl721.221靶细胞,但是不能很好地杀死表达hla-e的lcl721.221-cw3对照细胞。相比之下,缺乏cd94/nkg2a的yts效应细胞能有效地杀死这两种细胞系。因此,由于hla-e诱导的经cd94/nkg2a的抑制性信号传导,nk效应细胞较低效地杀死hla-e+lcl721.221-cw3细胞。当在这种释放51cr的细胞毒性测定中将nk细胞与根据本发明的封闭的抗cd94/nkg2a抗体进行预孵育时,以抗体浓度依赖性方式更有效地杀死表达hla-e的lcl721.221-cw3细胞。抗nkg2a抗体的抑制性活性(即细胞毒性增强潜力)也可以按许多其他方式中的任一种来评估,例如通过其对细胞内游离钙的影响,例如在西沃里等人,实验医学杂志1997;186:1129-1136中所述,将其披露的内容通过引用并入本文。nk细胞细胞毒性的活化可以是例如通过测量细胞因子产生(例如ifn-γ产生)或细胞毒性标记物(例如cd107或cd137转移)的增加来评价的。在一个示例性方案中,通过细胞表面和细胞质内染色以及通过流式细胞术在培养4天后的分析来评估来自pbmc的ifn-γ产生。简言之,在培养的最后4小时以5μg/ml的终浓度添加布雷菲德菌素a(西格玛-奥德里奇公司(sigmaaldrich))。然后在透化(intrapreptm;贝克曼库尔特公司(beckmancoulter))并且用pe-抗ifn-γ或pe-igg1(pharmingen公司)染色之前用抗cd3和抗cd56mab孵育这些细胞。使用elisa(gm-csf:duosetelisa,r&d系统公司,明尼阿波里斯(minneapolis),明尼苏达州,ifn-γ:opteia设置,pharmingen公司)在上清液中测量来自多克隆活化的nk细胞的gm-csf和ifn-γ产生。
如本文所使用的,术语“pd-1”是指蛋白质程序性死亡1(pd-1)(也称为“程序性细胞死亡1”),cd28受体家族(还包括cd28、ctla-4、icos和btla)的抑制性成员。完整的人pd-1序列可以在基因库登录号u64863下找到,如下所示:
mqipqapwpvvwavlqlgwrpgwfldspdrpwnpptffpallvvtegd-natftcsfsntsesfvlnwyrmspsnqtdklaafpedrsqpgqdcrfrvtqlpngrd-fhmsvvrarrndsgtylcgaislapkaqikeslraelrvterraevptahp-spsprpagqfqtlvvgvvggllgslvllvwvlavicsraargtigarrtgqplkedpsav-pvfsvdygeldfqwrektpeppvpcvpeqteyativfpsgmgtssparrg-sadgprsaqplrpedghcswpl(seqidno:2).
“pd-1”还包括pd-1基因或编码的蛋白的任何变体、衍生物、或同种型。pd-1在活化的b细胞、t细胞和骨髓细胞上表达(冈崎(okazaki)等人(2002)当前免疫学观点(curr.opin.immunol.)14:391779-82;班尼特(bennett)等人(2003)免疫学杂志(jimmunol)170:711-8)。通过添加单克隆抗体后增强t细胞增殖方面的功能效应,发现了该家族的初始成员cd28和icos(胡特洛夫(hutloff)等人(1999)自然397:263-266;汉森(hansen)等人(1980)免疫原(immunogenics)10:247-260)。已经鉴定了pd-1的两种配体(pd-l1和pd-l2),这两种配体已经显示在结合至pd-1后下调t细胞活化(弗里曼(freeman)等人(2000)实验医学杂志192:1027-34;莱切曼(latchman)等人(2001)自然免疫学(natimmunol)2:261-8;卡特(carter)等人(2002)欧洲免疫学杂志(eurjimmunol)32:634-43)。pd-l1和pd-l2都是结合pd-1但不结合其他cd28家族成员的b7同源物。
完整的人pd-l1序列可以在uniprotkb/swiss-prot、标识符q9nzq7-1下找到,如下所示:
多种人类癌症中存在大量的pd-l1(董(dong)等人(2002)自然医学(nat.med.)8:787-9)。pd-1和pd-l1之间的相互作用导致肿瘤浸润淋巴细胞的减少、t细胞受体介导的增殖的减少、以及癌性细胞的免疫逃避(董(dong)等人(2003)分子医学杂志(j.mol.med.)81:281-7;布兰克(blank)等人(2005)癌症免疫学免疫治疗(cancerimmunol.immunother.)54:307-314;小西(konishi)等人(2004)临床癌症研究(clin.cancerres.)10:5094-100)。通过抑制pd-1与pd-l1的局部相互作用,可以逆转免疫抑制,并且当pd-1与pd-l2的相互作用也被阻断时,该效果是累加的。
在本发明的上下文中,“降低人pd-1的抑制性活性”、“中和pd-1”或“中和人pd-1的抑制性活性”是指如下过程,其中pd-1在其由pd-1与其一种或多种结合配偶体(例如pd-l1或pd-l2)的相互作用产生的信号转导能力方面受到抑制。中和pd-1的抑制性活性的试剂降低、阻断、抑制、消除或干扰由pd-1与其一种或多种结合配偶体(例如pd-l1、pd-l2)的相互作用产生的信号转导。因此,此类试剂可以减少通过或经由t淋巴细胞上表达的细胞表面蛋白介导的阴性共刺激信号,以便增强t细胞效应子功能(例如增殖、细胞因子产生和/或细胞毒性)。
关于抗nkg2a和抗pd-1或抗pd-l1结合剂(例如抗体),每当在这整个说明书内提到“治疗癌症”或类似物,包括:(a)治疗癌症的方法,所述方法包括以下步骤:以允许治疗癌症的剂量(治疗有效量),任选地以如本文所指定的剂量(量)给予(例如,至少一次治疗)nkg2a和抗pd-1或抗pd-l1结合剂(例如,一起或各自独立地在药学上可接受的载体材料中)至需要这种治疗的个体、哺乳动物,尤其是人类;(b)抗nkg2a和抗pd-1或抗pd-l1结合剂用于治疗癌症的用途,或使用抗nkg2a结合剂用于所述治疗(尤其在人类中)中;(c)抗nkg2a和抗pd-1或抗pd-l1结合剂用于制造用于治疗癌症的药物制剂的用途,使用抗nkg2a和抗pd-1或抗pd-l1结合剂用于制造用于治疗癌症的药物制剂的方法,该方法包括混合抗nkg2a和抗pd-1或抗pd-l1结合剂与药学上可接受的载体,或包含有效剂量的适合于治疗癌症的抗nkg2a和抗pd-1或抗pd-l1结合剂的药物制剂;或(d)a)、b)、以及c)的任何组合,这是根据本主题,本主题允许在提交本申请的国家取得专利权。
如在此所使用的术语“活检样品”被定义为去除组织用于检查例如以建立诊断的目的。活检样品类型的实例包括通过施加抽吸,例如通过附加至注射器的针头;通过仪器去除组织的片段;通过用适当的仪器通过内窥镜去除;通过手术切除例如整个病损;等等。
如在此所使用,术语“抗体”是指多克隆和单克隆抗体。根据重链恒定区的类型,可将抗体归入以下五种主要类别之一:iga、igd、ige、igg和igm。将这些类别中的几种进一步分为亚类或同种型,例如igg1、igg2、igg3和igg4等。示例性免疫球蛋白(抗体)结构单元包括四聚体。每个四聚体由两对相同的多肽链构成,每对包括一条“轻”链(约25kda)和一条“重”链(约50-70kda)。每条链的n末端限定具有约100个至110个或更多个氨基酸的可变区,主要负责抗原识别。术语可变轻链(vl)和可变重链(vh)分别指这些轻链和重链。对应于不同类别免疫球蛋白的重链恒定区分别命名为“α”、“δ”、“ε”、“γ”和“μ”。不同类别的免疫球蛋白的亚基结构和三维构型是熟知的。igg是在此使用的示例性抗体类别,因为它们是生理状况下最常见的抗体且在实验室条件下最容易制备。任选地,该抗体是单克隆抗体。抗体的具体实例是人源化的、嵌合的、人的或其他适合人的抗体。“抗体”还包括在此描述的任一抗体的任一片段或衍生物。
术语“特异地结合到”是指优选地在竞争性结合测定法中抗体可以结合到结合配偶体上(例如nkg2a、pd-1、pd-l1),正如使用重组体形式的蛋白、其中的表位、或存在于分离的靶细胞的表面上的天然蛋白所评估的。用于确定特异性结合的竞争性结合测定法以及其他方法在本领域内是熟知的。例如,可以经由放射性标记、物理方法(如质谱法)、或使用例如细胞荧光分析(例如facscan)检测的直接或间接荧光标记来检测结合。结合高于用对照所看到的量,非特异性试剂指示出试剂结合至靶标。特异性结合nkg2a的试剂可以单独地结合nkg2a或作为与cd94的二聚体结合nkg2a。
当抗体被称为与具体的单克隆抗体“竞争”时,它意指在使用重组分子(例如,nkg2a、pd-1、pd-l1)或表面表达的分子(例如,nkg2a、pd-1、pd-l1)的结合测定中,该抗体与该单克隆抗体竞争。例如,如果测试抗体在结合测定中降低具有seqidno:4-8中任一个的重链和seqidno:9的轻链的抗体与nkg2a多肽或表达nkg2a的细胞的结合,则该抗体被称为分别与这类抗体“竞争”。
如在此使用的术语“亲和力”意指抗体与表位结合的强度。抗体的亲和力是由解离常数kd给出的,该kd定义为[ab]x[ag]/[ab-ag],其中[ab-ag]是抗体-抗原复合物的摩尔浓度,[ab]是未结合抗体的摩尔浓度并且[ag]是未结合抗原的摩尔浓度。亲和力常数ka被定义为1/kd。用于确定mab的亲和力的方法可以发现于哈洛(harlow)等人,《抗体:实验室手册》(antibodies:alaboratorymanual),冷泉港实验室出版社(coldspringharborlaboratorypress),冷泉港实验室(coldspringharbor),纽约(n.y.),1988),科尔根(coligan)等人编著,《当代免疫学实验手册》(currentprotocolsinimmunology),格林出版联盟和威力跨学科(greenepublishingassoc.andwileyinterscience),纽约,(1992,1993),以及马勒(muller),《酶学方法》(meth.enzymol.)92:589-601(1983),将这些文献通过引用完全结合在此。本领域中熟知的用于确定mab亲和力的一种标准的方法是使用表面等离子体共振(spr)筛选(例如通过用biacoretmspr分析装置分析)。
在此处的上下文中,“决定簇”指明多肽上相互作用或结合的位点。
术语“表位”是指抗原决定簇,并且是在抗原上与抗体结合的面积或区域。蛋白质表位可以包括直接参与结合的氨基酸残基连同通过特异性抗原结合的抗体或肽被有效地阻断的氨基酸残基,即,抗体“足迹”内的氨基酸残基。它是可以与例如抗体或受体组合的复杂抗原分子上的最简单形式或最小结构区域。表位可以是直链或构象性的/结构性的。术语“直链的表位”被定义为由多个氨基酸残基组成的表位,这些氨基酸残基在氨基酸的线性顺序上(一级结构)是连续的。术语“构象性表位或结构性表位”被定义为由氨基酸残基构成的表位,这些氨基酸残基不全是连续性的,并且因此表示了通过分子折叠(二级、三级和/或四级结构)而彼此邻近的氨基酸线性序列的分离的部分。构象性表位取决于三维结构。因此,术语‘构象性’通常与‘结构性’可互换地使用。
在此使用术语“试剂”来表示化合物、化合物混合物、生物大分子、或由生物学材料制备的提取物。术语“治疗剂”是指具有生物活性的试剂。
出于本文的目的,“人源化的”或“人类的”抗体是指一种抗体,其中一种或多种人类免疫球蛋白的恒定和可变框架区与动物免疫球蛋白的结合区(例如,cdr)相融合。这类抗体被设计成保持衍生出这些结合区的非人类抗体的结合特异性,但是却要避免对抗非人类抗体的免疫反应。这类抗体可以从转基因小鼠或其他动物体内得到,这些小鼠或动物已经被“工程化”从而产生响应于抗原激发的特异性人类抗体((参见,例如,格林(green)等人(1994)自然遗传学(naturegenet)7:13;朗伯格(lonberg)等人(1994)自然368:856;泰勒(taylor)等人(1994)国际免疫学(intimmun)6:579,将其全部传授内容通过引用结合在此)。完全的人抗体也可通过基因或染色体转染法以及噬菌体展示技术而构建,所有这些技术在本领域中已知(参见,例如麦卡菲蒂(mccafferty)等人(1990)自然348:552-553)。人抗体还可以通过体外激活的b细胞生成(参见,例如,美国专利号5,567,610和5,229,275,将其全部内容通过引用结合在此)。
“嵌合抗体”是抗体分子,其中(a)对恒定区或其一部分进行改变、置换或交换,从而将抗体结合位点(可变区)被连接于类别、效应器功能和/或种属不同(或已改变的)的恒定区,或是完全不同的分子,该分子对该嵌合抗体赋予新的属性,例如酶、毒素、激素、生长因子、药物等;或者(b)将该可变区或其一部分用具有不同或已经改变的抗原特异性的可变区进行改变、置换或交换。
术语“fc结构域”、“fc部分”、以及“fc区”是指抗体重链的c末端片段,例如从约氨基酸(aa)230至约aa450的人类γ重链或其在其他类型的抗体重链(例如针对人类抗体的α、δ、ε以及μ)中的对应物序列、或其天然存在的同种异型。除非另外指明,贯穿本披露使用普遍接受的免疫球蛋白卡巴特氨基酸编号(参见卡巴特(kabat)等人(1991)《免疫学上感兴趣的蛋白的序列》(sequencesofproteinofimmunologicalinterest),第5版,美国公共卫生署(unitedstatespublichealthservice),美国国立卫生研究院(nationalinstituteofhealth),贝塞斯达,马里兰州)。
术语“分离的”、“纯化的”或“生物学纯的”是指实质上或基本上不含在天然状态下发现的通常伴随其的组分的物质。纯度和均质性典型地是使用分析化学技术(例如聚丙烯酰胺凝胶电泳或高效液相色谱法)来确定的。制剂中存在的主要种类的蛋白实质上是纯化的。
术语“多肽”、“肽”以及“蛋白”在此可互换地使用,是指氨基酸残基的聚合物。这些术语应用到氨基酸聚合物上,其中一个或多个氨基酸残基是对应的天然发生氨基酸的人工化学模拟物,并且应用到天然发生的氨基酸聚合物以及非天然发生的氨基酸聚合物上。
当提及例如细胞或核酸、蛋白或载体时使用术语“重组”是指该细胞、核酸、蛋白或载体已经通过引入异源性核酸或蛋白或通过改变天然核酸或蛋白而被修饰,或者表示该细胞来源于如此修饰的细胞。因此,例如,重组细胞表达在天然(非重组)形式的细胞内部找不到的基因,或表达天然基因然而却异常表达、低表达或根本不表达。
在此上下文中,“结合”多肽的或表位的术语抗体指定结合所述具有特异性和/或亲和性决定簇的抗体。
术语“一致性”或“一致的”当用于两种或更多种多肽的序列之间的关系时,是指多肽之间的序列关联程度,如通过两个或更多个氨基酸残基链之间匹配的数目来确定的。“一致性”使用由具体数学模型或计算机程序(即,“算法”)解决的空位比对(如果有的话)测量两种或更多种序列中较短序列之间的一致匹配的百分比。相关多肽的一致性可以通过已知方法容易地计算出。这些方法包括但不限于以下文献所描述的那些:计算分子生物学(computationalmolecularbiology),莱斯克a.m.(lesk,a.m.)编辑,牛津大学出版社(oxforduniversitypress),纽约,1988;生物计算:信息学与基因组计划(biocomputing:informaticsandgenomeprojects),史密斯d.w.(smith,d.w.)编辑,学术出版社(academicpress),纽约,1993;序列数据的计算机分析(computeranalysisofsequencedata),第1部分,格里芬a.m.(griffin,a.m.)和格里芬h.g.(griffin,h.g.)编辑,胡马纳出版社(humanapress),新泽西州,1994;分子生物学中的序列分析(sequenceanalysisinmolecularbiology),冯·海因切g.(vonheinje,g.)编辑,学术出版社,1987;序列分析初级读本(sequenceanalysisprimer),哥博斯科夫m.(gribskov,m.)和德弗罗j.(devereux,j.)编辑,斯托克顿出版社(m.stocktonpress),纽约,1991;以及卡里略(carillo)等人,工业和应用数学学会应用数学杂志(siamj.appliedmath.)48,1073(1988)。
用于确定一致性的方法被设计为在测试的序列之间给出最大的匹配。确定一致性的方法描述于可公开获得的计算机程序中。用于确定在两个序列之间的一致性的计算机程序方法包括gcg程序包,包括gap(德弗罗(devereux)等人,《核酸研究》(nucl.acid.res.)12,387(1984);遗传学电脑集团(geneticscomputergroup),威斯康辛大学(universityofwisconsi),麦迪逊(madison),威斯康辛(wis.))、blastp、blastn、以及fasta(阿特休尔(altschul)等人,《分子生物学杂志》(j.mol.biol),215,403-410(1990))。blastx程序可以公开地从美国国家生物技术信息中心(ncbi)以及其他来源(blast手册,阿尔丘尔(altschul)等人ncb/nlm/nih贝塞斯达(bethesda),马里兰州20894;阿尔丘尔等人,同上)得到。熟知的史密斯-沃特曼算法(smithwatermanalgorithm)也可以用来确定一致性。
nkg2a中和治疗剂
抗nkg2a试剂结合人cd94/nkg2a受体的细胞外部分,并降低在cd94/nkg2a阳性淋巴细胞表面上表达的人cd94/nkg2a受体的抑制性活性。在一个实施例中,该试剂与hla-e竞争结合cd94/nkg2a,即该试剂阻断cd94/nkg2a与其配体hla-e之间的相互作用。在另一个实施例中,该试剂不与hla-e竞争结合cd94/nkg2a;即该试剂能够与hla-e同时结合cd94/nkg2a。该抗体可以结合cd94和nkg2a上的组合表位或单独结合nkg2a上的表位。
在一方面中,该抗nkg2a试剂是选自完全人抗体、人源化抗体、和嵌合抗体的抗体。在一方面中,该试剂包含来源于人igg1、igg2、igg3或igg4抗体的恒定结构域。在一方面中,该试剂是选自iga、igd、igg、ige和igm抗体的抗体的片段。在一方面中,该试剂是选自以下各项的抗体片段:fab片段、fab'片段、fab'-sh片段、f(ab)2片段、f(ab')2片段、fv片段、重链ig(美洲驼或骆驼ig)、vhh片段、单结构域fv、以及单链抗体片段。在一方面中,该试剂是选自以下各项的合成的或半合成的抗体衍生的分子:scfv、dsfv、微小抗体、双抗体、三抗体、κ体、ignar、以及多特异性抗体。
任选地,这些抗nkg2a抗体不显示与fcγ受体(例如cd16)的实质特异性结合。这类抗体可以包含已知不结合fc受体的各种重链的恒定区。一个这样的实例是人igg4恒定区。在一个实施例中,该igg4抗体包含修饰以防止体内半抗体(fab臂交换)形成,例如,抗体包含igg4重链,该igg4重链包含残基241(对应于根据eu指数的位置228)中的丝氨酸至脯氨酸突变(卡巴特(kabat)等人,“免疫学上感兴趣的蛋白的序列(sequencesofproteinsofimmunologicalinterest)”,第5版,nih,贝塞斯达(bethesda),ml,1991)。如此修饰的igg4抗体将会在体内保持完整并且保持与nkg2a结合的二价(高亲和力),与将在体内经历fab臂交换的天然igg4相反,使得它们以可以改变结合亲和力的单价方式来结合nkg2a。可替代地,不包含恒定区的抗体片段(例如fab或f(ab')2片段)可用于避免fc受体结合。可以根据本领域已知的方法来评估fc受体结合,包括例如在biacore测定中测试抗体与fc受体蛋白的结合。还可以使用任何人抗体类型(例如igg1、igg2、igg3或igg4),其中fc部分被修饰以最小化或消除与fc受体的结合(参见,例如wo03101485,将其披露的内容通过引用并入本文)。用于评估fc受体结合的测定(如,例如基于细胞的测定)是本领域熟知的,并且描述于例如wo03101485中。
因此,本发明涉及结合nkg2a的抗体或其他试剂。在一方面中,该抗体以低于与人nkg2c和/或nkg2e至少100倍的kd结合nkg2a。
在本发明的一方面中,该试剂通过干扰cd94/nkg2a信号传导(例如通过干扰nkg2a与hla-e的结合、阻止或诱导cd94/nkg2a受体的构像变化、和/或影响cd94/nkg2a受体的二聚化和/或聚集)来降低cd94/nkg2a介导的对表达cd94/nkg2a的淋巴细胞的抑制。
在本发明的一方面中,该试剂以比与nkg2c低至少100倍的kd结合nkg2a的细胞外部分。在另一个优选的方面中,该试剂以比与nkg2c低至少150、200、300、400、或10,000倍的kd结合nkg2a的细胞外部分。在本发明的另一方面中,该试剂以比与nkg2c、nkg2e和/或nkg2h分子低至少100倍的kd结合nkg2a的细胞外部分。在另一个优选的方面中,该试剂以比与nkg2c、nkg2c和/或nkg2h分子低至少150、200、300、400、或10,000倍的kd结合nkg2a的细胞外部分。这可以例如在biacore实验中进行测量,其中测量试剂结合固定化的cd94/nkg2a的细胞外部分(例如,从表达cd94/nkg2的细胞中纯化的或在生物系统中产生的)的能力,并与在相同测定中试剂与类似产生的cd94/nkg2c和/或其他cd94/nkg2变体的结合进行比较。可替代地,可以测量试剂与天然表达或过表达(例如在瞬时转染或稳定转染后)cd94/nkg2a的细胞的结合,并与表达cd94/nkg2c和/或其他cd94/nkg2变体的细胞的结合进行比较。抗nkg2a抗体可任选地结合nkg2b,该nkg2b是与cd94一起形成抑制性受体的nkg2a剪接变体。在一个实施例中,可以使用美国专利号8,206,709中披露的方法测量亲和力,例如通过如美国专利号8,206,709的实例8所示的biacore来评估与共价固定的nkg2a-cd94-fc融合蛋白的结合,将其披露的内容通过引用并入本文。
抗nkg2a抗体可以是人源化抗体,例如包含来自选自例如vh1_18、vh5_a、vh5_51、vh1_f、和vh1_46的人受体序列的vh人受体框架,和jh6j-区段,或其他本领域中已知的人类种系vh框架序列。vl区人受体序列可以是例如vki_o2/jk4。
在一个实施例中,该抗体是基于抗体z270的人源化抗体。不同的人源化z270vh链示于seqidno:4-8中(加下划线的是可变区结构域氨基酸)。humz270vh6(seqidno:4)是基于vh5_51的;humz270vh1(seqidno:5)是基于vh1_18的;humz270vh5(seqidno:6)是基于vh5_a的;humz270vh7(seqidno:7)是基于vh1_f的;并且humz270vh8(seqidno:8)是基于vh1_46的;都具有jh6j-区段。这些抗体中的每一种都保持与nkg2a结合的高亲和力,对抗该抗体的宿主免疫应答的可能性低,因为每个人源化构建体的卡巴特(kabat)cdr-h2的6个c-末端氨基酸残基与人受体框架是相同的。使用比对程序vectornti,获得humz270vh1和humz270vh5、humz270vh6、humz270vh7、和humz270vh8之间的以下序列一致性:78.2%(vh1vs.vh5)、79.0%(vh1vs.vh6)、88.7%(vh1vs.vh7)、和96.0%(vh1vs.vh8)。
在一方面中,该试剂包括(i)seqidno:4-8中任一个的重链可变区,或与其至少50%、60%、70%、80%、90%、95%、98%或99%一致的氨基酸序列,和(ii)seqidno:9的轻链可变区,或与其至少50%、60%、70%、80%、90%、95%、98%或99%一致的氨基酸序列。在一方面中,该试剂包括(i)包含seqidno:4-8中任一个的氨基酸序列的重链,或与其至少50%、60%、70%、80%、90%、95%、98%或99%一致的氨基酸序列,和(ii)包含seqidno:9的氨基酸序列的轻链,或与其至少50%、60%、70%、80%、90%、95%、98%或99%一致的氨基酸序列。具有seqidno:4-8中任一个的重链和seqidno:9的轻链的抗体中和nkg2a的抑制性活性,但基本上不结合活化受体nkg2c、nkge或nkg2h。此外,该抗体与hla-e竞争结合细胞表面上的nkg2a。在一方面中,该试剂包含hcdr1、hcdr2和/或hcdr3序列,这些序列来源于具有seqidno:4-8中任一个的氨基酸序列的重链。在本发明的一方面中,该试剂包含lcdr1、lcdr2和/或lcdr3序列,这些序列来源于具有seqidno:9的氨基酸序列的轻链。
重链
vh6:
evqlvqsgaevkkpgeslkisckgsgysftsywmnwvrqmpgkglewmgridpyd-sethyspsfqgqvtisadksistaylqwsslkasdtamyycarggydfdvgtly-wffdvwgqgttvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkp-sntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmis-rtpevtcvvvdvsqedpevqfnwyvdgvevhnak-tkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiek-tiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpen-nykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seqidno:4)
vh1:
qvqlvqsgaevkkpgasvkvsckasgytftsywmnwvrqapgqglewmgridpydsethya-qklqgrvtmttdtststaymelrslrsddtavyycarggydfdvgtlywffdvwgqgttvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglys-lssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seqidno:5)
vh5:
evqlvqsgaevkkpgeslrisckgsgysftsywmnwvrqmpgkglewmgridpyd-sethyspsfqghvtisadksistaylqwsslkasdtamyycarggydfdvgtly-wffdvwgqgttvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkp-sntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmis-rtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seqidno:6)
vh7:
evqlvqsgaevkkpgatvkisckvsgytftsywmnwvqqapgkglewmgridpydsethyaekfqgrvtitadtstdtaymelsslrsedtavyycatggydfdvgtly-wffdvwgqgttvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkp-sntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmis-rtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seqidno:7)
vh8:
qvqlvqsgaevkkpgasvkvsckasgytftsywmnwvrqapgqglewmgridpydsethyaqkfqgrvtmtrdtststvymelsslrsedtavyycarggydfdvgtlywffdvwgqgttvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvht-fpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpape-flggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnak-tkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiek-tiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpen-nykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seqidno:8)
轻链
diqmtqspsslsasvgdrvtitcraseniysylawyqqkpgkapklliynaktlaegvpsrfsgsgsgtdftltisslqpedfatyycqhhygtprtfgggtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seqidno:9)
在一方面中,该抗nkg2a抗体是包含以下各项的抗体:对应于seqidno:4-8的残基31-35的cdr-h1,对应于seqidno:4-8的残基50-60(任选地是50-66,当包括人类来源的氨基酸时)的cdr-h2,以及对应于seqidno:4-8的残基99-114(根据kabat的95-102)的cdr-h3。在一个实施例中,该cdr-h2对应于seqidno:4-8的残基50-66。任选地,cdr可包含一个、两个、三个、四个、或更多个氨基酸取代。
在一方面中,该抗nkg2a抗体是包含以下各项的抗体:对应于seqidno:9的残基24-34的cdr-l1,对应于seqidno:9的残基50-56的cdr-l2,以及对应于seqidno:9的残基89-97的cdr-l3。任选地,cdr可包含一个、两个、三个、四个、或更多个氨基酸取代。
在一方面中,该抗nkg2a抗体是包含以下各项的抗体:对应于seqidno:4-8的残基31-35的cdr-h1,对应于seqidno:4-8的残基50-60(任选地是50-66)的cdr-h2,以及对应于seqidno:4-8的残基99-114(根据kabat的95-102)的cdr-h3,对应于seqidno:9的残基24-34的cdr-l1,对应于seqidno:9的残基50-56的cdr-l2,以及对应于seqidno:9的残基89-97的cdr-l3。
在一方面中,该试剂包含hcdr1、hcdr2和/或hcdr3序列,这些序列来源于具有seqidno:10的氨基酸序列的vh。在本发明的一方面中,该试剂包含lcdr1、lcdr2和/或lcdr3序列,这些序列来源于具有seqidno:11的氨基酸序列的vl。在一方面中,该试剂包含源自具有seqidno:10的氨基酸序列的vh的hcdr1、hcdr2和/或hcdr3序列,以及源自具有氨基酸序列seqidno:11的vl的lcdr1、lcdr2和/或lcdr3序列。具有seqidno:10的重链和seqidno:11的轻链的抗体中和nkg2a的抑制性活性,并且还结合活化受体nkg2c、nkg2e或nkg2h。该抗体不与hla-e竞争结合细胞表面上的nkg2a(即它是nkg2a的非竞争性拮抗剂)。
evqlvesggglvkpggslklscaasgftfssyamswvrqspekrlewvaeissggsytyypdtvtgrftisrdnakntlyleisslrsedtamyyctrhgdyprffdvwgagttvtvss(seqidno:10)
qivltqspalmsaspgekvtmtcsasssvsyiywyqqkprsspkpwiyltsnlasgvparfsgsgsgtsysltissmeaedaatyycqqwsgnpytfgggtkleikr(seqidno:11)
在一方面中,该试剂包含可变重链(vh)结构域(seqidno:10)的氨基酸残基31-35、50-60、62、64、66、和99-108以及可变轻链(vl)结构域(seqidno:11)的氨基酸残基24-33、49-55、和88-96,任选地具有一个、两个、三个、四个、或更多个氨基酸取代。
在一方面中,该试剂是针对任何上述抗体结合的cd94/nkg2a表位而产生的完全人抗体。
应当理解,尽管可以使用上述抗体,但是其他抗体可以识别nkg2a多肽的任何部分并且针对nkg2a多肽的任何部分而产生,只要所述抗体引起nkg2a的抑制性活性的中和。例如,nkg2a(优选地是但不专一地是人nkg2a)的任何片段,或nkg2a片段的任何组合,可以用作免疫原以产生抗体,并且这些抗体可以识别在nkg2a多肽内的任何位置的表位,只要它们能在如此处描述的表达nkg2a的nk细胞上这样做。任选地,该表位是由具有seqidno:4-8的重链和seqidno:9的轻链的抗体特异性识别的表位。
在一方面中,该试剂与美国专利号8,206,709(将其披露的内容通过引用并入本文)中披露的humz270抗体竞争结合人cd94/nkg2a受体的细胞外部分。竞争性结合可以例如在biacore实验中进行测量,其中测量试剂结合固定化的用humz270饱和的cd94/nkg2a受体的细胞外部分(例如从表达cd94/nkg2的细胞纯化的,或在生物系统中产生的)的能力。可替代地,测量试剂与天然表达或过表达(例如在瞬时转染或稳定转染后)cd94/nkg2a受体并且已经用饱和剂量的z270预孵育的细胞的结合。在一个实施例中,可以使用美国专利号8,206,709中披露的方法测量竞争性结合,例如通过如美国专利号8,206,709的实例15所示的流式细胞术来评估与ba/f3-cd94-nkg2a细胞的结合,将其披露的内容通过引用并入本文。
pd-1中和治疗剂
目前在市场上或在临床评价中存在至少六种阻断pd-1/pd-l1途径的试剂。一种试剂是bms-936558(纳武单抗(nivolumab)/ono-4538,百时美施贵宝公司(bristol-myerssquibb);以前是mdx-1106)。纳武单抗(商品名
mk-3475(来自默克公司(merck)的人igg4抗pd1mab),也称为拉立珠单抗(lambrolizumab)或派姆单抗(pembrolizumab)(商品名
mpdl3280a/rg7446(来自罗氏公司(roche)/基因泰克公司(genentech)的抗pd-l1)是包含工程改造的fc结构域的人抗pd-l1mab,该fc结构域经设计通过最小化fcγr结合和随之产生的抗体依赖性细胞毒性(adcc)而优化功效和安全性。每3周给予≤1、10、15和25mg/kgmpdl3280a的剂量长达1年。在第3期试验中,在nsclc中每三周通过静脉内输注以1200mg给予mpdl3280a。
amp-224(阿帕里免疫公司(amplimmune)和gsk公司)是包含与fc结构域融合的pd-l2细胞外结构域的免疫粘附素。中和pd-1的试剂的其他实例可以包括结合pd-l2(抗pd-l2抗体)并阻断pd-1和pd-l2之间的相互作用的抗体。
皮立珠单抗(pidilizumab)(ct-011;curetech)(来自cu-retech/teva的人源化igg1抗pd1mab),皮立珠单抗(ct-011;curetech)(参见,例如wo2009/101611),用3mg/kg静脉内的ct-011每4周进行4次输注,与每周375mg/m2的利妥昔单抗联合治疗30名患有利妥昔单抗(rituximab)敏感的复发性fl的患者4周,开始于第一次输注ct-011后的2周。
另外已知的pd-1抗体和其他pd-1抑制剂包括:amp-224(gsk许可的b7-dc/igg1融合蛋白),描述于wo2012/145493中的amp-514,描述于wo2011/066389和us2013/034559中的抗体medi-4736(由阿斯利康公司(astrazeneca)/医学免疫公司(medimmune)研发的抗pd-l1),描述于wo2010/077634中的抗体yw243.55.s70(抗pd-l1),mdx-1105(也称作bms-936559,由百时美施贵宝公司(bristol-myerssquibb)研发并描述于wo2007/005874中的抗pd-l1抗体),以及描述于wo2006/121168、wo2009/014708、wo2009/114335和wo2013/019906中的抗体和抑制剂,将其披露的内容通过引用并入本文。抗pd1抗体的另外的实例披露于wo2015/085847(上海恒瑞药业有限公司(shanghaihengruipharmaceuticalco.ltd.))中,例如分别具有seqidno:6、seqidno:7和/或seqidno:8的轻链可变结构域cdr1、cdr2和cdr3的抗体,以及分别具有seqidno:3、seqidno:4或seqidno:5的重链可变结构域cdr1、cdr2和cdr3的抗体,其中seqidno参照是根据wo2015/085847进行编号的,将其披露的内容通过引用并入本文。也可以使用与这些抗体中的任一种竞争结合pd-1或pd-l1的抗体。
示例性抗pd-1抗体是派姆单抗(pembrolizumab)(参见,例如wo2009/114335,将其披露的内容通过引用并入本文)。抗pd-1抗体可以是wo2008/156712中的抗体h409ai1,其包含由在atcc中作为081469_spd-h保藏的dna编码的重链可变区和由在atcc中作为0801470_spd-l-i1保藏的dna编码的轻链可变区。在其他实施例中,该抗体包含重链和轻链cdr或派姆单抗(pembrolizumab)的可变区。因此,在一个实施例中,该抗体包含由在atcc中作为081469_spd-h保藏的dna编码的派姆单抗的vh的cdr1、cdr2、和cdr3结构域,以及由在atcc中作为0801470_spd-l-i1保藏的dna编码的派姆单抗的vl的cdr1、cdr2和cdr3结构域。
在一些实施例中,该pd-1中和剂是抑制pd-l1与pd-1结合的抗pd-l1mab。在一些实施例中,该pd-1中和剂是抑制pd-1与pd-l1结合的抗pd1mab。在一些实施例中,该pd-1中和剂是免疫粘附素(例如,包含与恒定区(例如,免疫球蛋白序列的fc区)融合的pd-l1或pd-l2的细胞外结合部分或pd-1结合部分的免疫粘附素)。
另一个示例性抗pd-1抗体是包含具有seqidno:12和13所示的各自序列或者具有与其至少50%、60%、70%、80%、90%、95%,98%或99%一致的各自氨基酸序列的重链和轻链的纳武单抗,或其抗原结合片段以及变体。在其他实施例中,该抗体包含纳武单抗的重链和轻链cdr或可变区。因此,在一个实施例中,该抗体包含具有seqidno:12所示序列的纳武单抗的重链的cdr1、cdr2、和cdr3结构域,以及具有seqidno:13所示序列的纳武单抗的轻链的cdr1、cdr2和cdr3结构域。
qvqlvesgggwqpgrslrldckasgitfsnsgmhwvrqapgkglewvavrwydgskryyadsvkgrftisrdnskntlflqmnslraedtavyycatnddywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgttytcnvdhkpsntkvdrvesygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcwvdvsqedpevqfnwyydgvevhnatkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskagqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpeknykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seqidno:12).
eivltqspatlslspgeratlscrasqsvssylawyqqpgqaprlliydasnratgiparfsgsgsgtdftltisslepedfavyycqqssnwprtfgqgtkveirtvaapsvfifppsdeqlsgtasvvcllnnfypreavqwkvdnalqsgnsqesvteqdsdstyslsstllskadyekhkvyacevthqglsspvtsfnrgec(seqidno:13).
示例性抗pd-l1抗体包含具有seqidno:14和15所示的各自序列或者具有与其至少50%、60%、70%、80%、90%、95%,98%或99%一致的各自氨基酸序列的重链和轻链可变区,或其抗原结合片段以及变体。在其他实施例中,该抗体包含mpdl3280a的重链和轻链cdr或可变区。因此,在一个实施例中,该抗体包含具有seqidno:14所示序列的重链的cdr1、cdr2、和cdr3结构域,以及具有seqidno:15所示序列的轻链的cdr1、cdr2和cdr3结构域。
evqlvesggglvqpggslrlscaasgftfsdswihwvrqapgkglewvawispyggsty-yadsvkgrftisadtskntaylqnslraedtavyycarrhwpggfdywgqgtlvtvss(seqidno:14)
diqmtqspsslsasvgdrvtitcrasqdvstavawyqqpgkapklliysasflysgvpsrfsgsgsgtdftltisslqpedfatyycqqylyhpatfgqgtkveikr(seqidno:15)
抗pd-1或抗pd-l1抗体可以选自完全人抗体、人源化抗体、和嵌合抗体。在本发明的一方面中,该试剂包含来源于人igg1、igg2、igg3或igg4抗体的恒定结构域。在本发明的一方面中,该试剂是选自iga、igd、igg、ige和igm抗体的抗体的片段。在本发明的一方面中,该试剂是选自以下的抗体片段:fab片段、fab′片段、fab′-sh片段、f(ab)2片段、f(ab′)2片段、fv片段、重链ig(美洲驼或骆驼ig)、vhh片段、单结构域fv、以及单链抗体片段。在本发明的一方面中,该试剂是选自以下各项的合成的或半合成的抗体衍生的分子:scfv、dsfv、微小抗体、双抗体、三抗体、κ体、ignar、以及多特异性抗体。
该抗pd-1或抗pd-l1抗体可以缺少与fcγ受体(例如,cd16)的实质特异性结合。这样的抗体可以包含已知不结合fc受体的各种重链的恒定区。一个这样的实例是igg4恒定区。可替代地,不包含恒定区的igg4抗体片段(例如fab或f(ab′)2片段)可用于避免fc受体结合。可以根据本领域已知的方法来评估fc受体结合,包括例如在biacore测定中测试抗体与fc受体蛋白的结合。还可以使用任何人抗体类型(例如igg1、igg2、igg3或igg4),其中fc部分被修饰以最小化或消除与fcγ受体的结合。因此,该抗pd-1或抗pdl1抗体,所述抗体通常具有降低的或最小的效应子功能。在一方面中,最小效应子功能源自原核细胞中的产生。在一方面中,最小效应子功能源自“效应子减少的fc突变”或无糖基化。在另一个实施例中,效应子减少的fc突变是恒定区中的n297a或d265a/n297a取代。
配制品
可以将抗nkg2a或抗pd-1或抗pd-l1试剂(如抗体)掺入药物配制品中,该药物配制品包含浓度从1mg/ml至500mg/ml,其中所述配制品具有从2.0至10.0的ph。该配制品可以进一步包含缓冲体系、一种或多种防腐剂、一种或多种张度剂、一种或多种螯合剂、稳定剂和表面活性剂。在一个实施例中,该药物配制品是水性配制品,即包含水的配制品。这种配制品通常是溶液或悬浮液。在另一个实施例中,该药物配制品是水性溶液。术语“水性配制品”被定义为包含至少50%w/w水的配制品。同样地,术语“水性溶液”被定义为包含至少50%w/w水的溶液,并且术语“水性悬浮液”被定义为包含至少50%w/w水的悬浮液。
在另一个实施例中,该药物配制品是冷冻干燥的配制品,医生或患者在使用前向其中添加溶剂和/或稀释剂。
在另一个实施例中,该药物配制品是立即可用而不需任何预先溶解的干燥配制品(例如冷冻干燥的或喷雾干燥的)。
在另一方面中,该药物配制品包含此类抗体的水性溶液、和缓冲液,其中该抗体以从1mg/ml或以上的浓度存在,并且其中所述配制品具有从约2.0至约10.0的ph。
在另一个实施例中,该配制品的ph是在选自以下列表的范围内,该列表由以下各项组成:从约2.0至约10.0、约3.0至约9.0、约4.0至约8.5、约5.0至约8.0、以及约5.5至约7.5。
在另一个实施例中,所述缓冲剂选自下组,该组由以下各项组成:乙酸钠、碳酸钠、柠檬酸盐、甘氨酰甘氨酸、组氨酸、甘氨酸、赖氨酸、精氨酸、磷酸二氢钠、磷酸氢二钠、磷酸钠、以及三(羟甲基)-氨基甲烷、二甘氨酸、曲辛、苹果酸、琥珀酸、马来酸、富马酸、酒石酸、天冬氨酸或其混合物。这些特定缓冲剂中的每一种构成本发明的可替代实施例。
在另一个实施例中,该配制品进一步包含药学上可接受的防腐剂。在另一个实施例中,该配制品进一步包含等渗剂。在另一个实施例中,该配制品进一步包含螯合剂。在本发明的另一个实施例中,该配制品进一步包含稳定剂。在另一个实施例中,该配制品进一步包含表面活性剂。为了方便,参考《雷明顿:药物科学与实践》(remington:thescienceandpracticeofpharmacy),第19版,1995。
其他成分可以存在于本发明的肽药物配制品中是可能的。这些另外的成分可以包括润湿剂、乳化剂、抗氧化剂、膨胀剂、张度调节剂、螯合剂、金属离子、油质运载体、蛋白质(例如人血清白蛋白、明胶或蛋白质)以及两性离子(例如氨基酸,如甜菜碱、牛磺酸、精氨酸、甘氨酸、赖氨酸和组氨酸)。当然,这些另外的成分不应不利地影响本发明的药物配制品的总体稳定性。
根据本发明的药物组合物的给药可以通过若干种给药途径(例如静脉内给药)。还可以通过检查其他已经研发的治疗性单克隆抗体的经验来确定适合的抗体配制品。已经证实数种单克隆抗体在临床情形中比较有效,例如利妥昔(rituxan)(利妥昔单抗)、赫赛汀(曲妥单抗)、xolair(奥马佐单抗)、bexxar(托西莫单抗)、坎帕斯(阿仑单抗)、泽娃灵(zevalin)、oncolym,并且类似的配制品可以与本发明的抗体一起使用。例如,可以在100mg(10ml)或500mg(50ml)单次使用的小瓶中以10mg/ml的浓度提供单克隆抗体,以9.0mg/ml氯化钠、7.35mg/ml柠檬酸钠二水合物、0.7mg/ml聚山梨醇酯80、以及注射用无菌水配制该单克隆抗体用于iv给药。将ph调节到6.5。在另一个实施例中,在包含约20mm柠檬酸钠、约150mmnacl、约6.0的ph下的配制品中提供该抗体。
还提供了包括适应用于上述方法的治疗有效量的一种药物组合物的试剂盒,该药物组合物含有抗nkg2a抗体、和抗pd-1或抗pd-l1抗体、以及药学上可接受的载体。这些试剂盒还可以任选地包括说明书,例如,包括给药计划,以允许专业人员(例如,医师、护士或患者)将其中含有的组合物给予患有癌症(例如,实体瘤)的患者。所述试剂盒还可以包括注射器。
任选地,这些试剂盒包括单剂量药物组合物的多个包装,每种药物组合物含有用于根据上文提供的方法单次给药的有效量的抗nkg2a、抗pd-1或抗pd-l1抗体。给予该一种或多种药物组合物所必要的仪器或装置也可以被包括在这些试剂盒中。例如,试剂盒可以提供一个或多个预填充的注射器,这些注射器包含一定量的抗nkg2a、抗pd-1或抗pd-l1抗体。
在一个实施例中,本发明提供了用于治疗人类患者的癌症的试剂盒,该试剂盒包括:
(a)抗nkg2a抗体的剂量,该抗nkg2a抗体包含具有seqidno:4-8中任一个所示的序列的重链的cdr1、cdr2和cdr3结构域,以及具有seqidno:9所示的序列的轻链的cdr1、cdr2和cdr3结构域;
(b)抗pd-1抗体或抗pd-l1抗体的剂量;以及
(c)任选地,在本文所述的任何方法中使用抗nkg2a抗体和抗pd-1抗体的说明书。
恶性肿瘤的诊断、预后、以及治疗
描述了用于个体中癌症的诊断、预后、监测、治疗和预防的方法。尽管本文所述的治疗方案和方法对于治疗实体瘤特别有用,但本文所述的治疗方案和方法还可用于多种血液癌症以及感染性疾病、以及炎症和自身免疫障碍。本发明的这些方法和组合物例如用于治疗多种癌症和其他增殖性疾病,这些疾病包括但不限于:癌症,包括膀胱、乳房、结肠、肾、肝、肺、卵巢、前列腺、胰、胃、宫颈、甲状腺、以及皮肤的癌症;淋巴系统的造血肿瘤、包括白血病、急性淋巴细胞性白血病、急性淋巴细胞白血病、急性成淋巴细胞白血病、b细胞淋巴瘤、t细胞淋巴瘤、何杰金淋巴瘤、非何杰金淋巴瘤、毛细胞淋巴瘤以及伯基特淋巴瘤、以及多发行骨髓瘤;骨髓系统的造血细胞肿瘤,包括急性和慢性髓细胞白血病、前髓细胞白血病、以及骨髓增生异常综合症;间质来源的肿瘤,包括纤维肉瘤以及横纹肌肉瘤;其他肿瘤,包括黑色素瘤、精原细胞瘤、畸胎癌、成神经细胞瘤以及神经胶质瘤;中央以及外周神经系统肿瘤,包括星形胶质细胞瘤、成神经细胞瘤、神经胶质瘤、以及神经鞘瘤;间质来源的肿瘤,包括纤维肉瘤、横纹肌肉瘤、以及骨肉瘤;以及其他的肿瘤,包括黑色素瘤、着色性干皮病、角化棘皮瘤、精原细胞瘤、以及甲状腺滤泡性癌。
用于治疗本文提供的癌症的组合疗法包括施用中和抗nkg2a抗体和pd-1中和剂(例如,中和抗pd-1或抗pd-l1抗体)以治疗患有癌症(例如晚期难治性实体瘤)的受试者。在一个实施例中,本发明提供抗nkg2a抗体和抗pd-1抗体组合用于治疗患有实体瘤(例如实体瘤、晚期难治性实体瘤)或患有血液肿瘤的受试者。在一个具体的实施例中,该抗nkg2a抗体包含seqidno:4-8中任一个的重链和seqidno:9的轻链。在一个实施例中,中和pd-1的抑制性活性的抗体选自下组,该组由以下各项组成:派姆单抗、纳武单抗、amp-514、medi-4736、ct-011和mpdl3280a。
如在此所使用,辅助或联合给药(共同给药)包括呈相同或不同剂量形式的化合物的同时给药,或化合物的分开给药(例如,顺序给药)。因此,抗nkg2a和抗pd-1或抗pd-l1抗体可以在单一配制品中同时施用。可替代地,抗nkg2a和抗pd-1或抗pd-l1抗体可以配制用于单独施用,以及同时地或顺序地施用。
在一个实施例中,用本文所披露的方法治疗的癌症是表达hla-e的癌症。在一个实施例中,该癌症选自下组,该组由以下各项组成:肺癌(例如非小细胞肺癌(nsclc))、肾细胞癌(rcc)、黑色素瘤、结肠直肠癌、以及卵巢癌。
可以在有或没有预先检测步骤的情况下用抗nkg2a试剂治疗患有癌症的患者,以评估hla-e在肿瘤细胞表面上的表达。有利地,这些治疗方法可以包括以下步骤:在来自个体的肿瘤的生物样品(例如在肿瘤细胞上)中检测hla-e核酸或多肽。生物样品的实例包括任何适合的生物学流体(例如血清、淋巴液、血液)、细胞样品、或组织样品。例如,组织样品可以是肿瘤组织或肿瘤相邻组织的样品。任选地,在恶性细胞的表面上检测hla-e多肽。确定生物样品表达hla-e(例如突出表达;与参考相比,以高水平表达hla-e,用抗hla-e抗体进行高强度染色)表明了,该个体患有癌症,该癌症可以受到抑制nkg2a的试剂的治疗的强烈益处。在一个实施例中,该方法包括在生物样品中确定hla-e核酸或多肽的表达水平并且将该水平与对应于健康个体的参考水平(例如值、弱的细胞表面染色等)进行比较。确定生物样品以增加(与参考水平相比)的水平表达hla-e核酸或多肽表明了,个体患有癌症,该癌症可用抑制nkg2a的试剂进行治疗。
在一个实施例中,确定生物样品(例如,包含肿瘤细胞、肿瘤组织和/或肿瘤相邻组织的样品)显著表达hla-e核酸或多肽表明了,个体患有癌症,该癌症可用抑制nkg2a的试剂进行治疗。当提及hla-e多肽时,“显著表达”是指hla-e多肽在取自给定个体的相当多的肿瘤细胞中表达。然而术语“显著表达”的定义不限于精确的百分率值,在一些实例中,称为“显著表达”的受体将存在于至少30%、40%、50%、60%、70%、80%或更多的取自患者(样品中的)的肿瘤细胞上。
确定个体是否具有表达hla-e多肽的癌细胞可以例如包括:从包含癌细胞的个体获得生物样品(例如通过进行活检),使所述细胞与结合hla-e多肽的抗体接触,并检测这些细胞在其表面上是否表达hla-e。任选地,确定个体是否具有表达hla-e的癌细胞包括进行免疫组织化学测定。任选地,确定个体是否具有表达hla-e的癌细胞包括进行流式细胞术测定。
在这些治疗方法中,抗nkg2a抗体和抗pd-1或抗pd-l1抗体可以单独地、一起或顺序地,或以组合物给予。在一些实施例中,在给予该抗pd-1或抗pd-l1抗体之前给予该结合抗原的化合物。例如,可以在给予该抗pd-1或抗pd-l1抗体之前约0至30天给予该抗nkg2a抗体。在一些实施例中,在给予该抗pd-1或抗pd-l1抗体之前从大约30分钟至大约2周、从大约30分钟至大约1周、从大约1小时至大约2小时、从大约2小时至大约4小时、从大约4小时至大约6小时、从大约6小时至大约8小时、从大约8小时至1天、或从大约1天至5天给予抗nkg2a抗体。在一些实施例中,与给予该抗pd-1或抗pd-l1抗体同时给予抗nkg2a抗体。在一些实施例中,在给予该抗pd-1或抗pd-l1抗体之后给予抗nkg2a抗体。例如,可以在给予该抗pd-1或抗pd-l1抗体之后约0至30天给予抗nkg2a抗体。在一些实施例中,在给予该抗pd-1或抗pd-l1抗体之后从大约30分钟至大约2周、从大约30分钟至大约1周、从大约1小时至大约2小时、从大约2小时至大约4小时、从大约4小时至大约6小时、从大约6小时至大约8小时、从大约8小时至1天、或从大约1天至5天给予抗nkg2a抗体。
用于治疗患有癌症的人的适合的治疗方案包括例如向患者给予有效量的每种抑制nkg2a的抗体与中和人pd-1的抑制性活性的抗体,其中该方法包括至少一个给予周期,其中以1-10mg/kg体重的剂量给予至少一个剂量的抗nkg2a抗体,并且以1-20mg/kg体重的剂量给予至少一个剂量的抗pd-1或抗pd-l1抗体。在一个实施例中,该给予周期在2周和8周之间。
在一个实施例中,该方法包括至少一个给予周期,其中该周期为8周或更短的时期,其中对于所述至少一个周期中的每一个,以1-10mg/kg体重的剂量给予两个、三个或四个剂量的抗nkg2a抗体,并且以1-20mg/kg体重的剂量给予两个、三个或四个剂量的抗pd-1或抗pd-l1抗体。
该抗nkg2a抗体可有利地以实现循环中浓度高于基本上完全(例如90%、95%)受体饱和所需浓度(如通过在表达nkg2a的细胞(例如在pbmc中)上滴定抗nkg2a抗体所评估的)至少10倍、20倍或30倍的量给予,或任选地以实现在血管外组织(例如肿瘤组织或环境)中的浓度高于基本上完全受体饱和所需浓度(如通过在表达nkg2a的细胞(例如在pbmc中)上滴定抗nkg2a抗体所评估的)至少10倍、20倍或30倍的量给予。
可以使用表达nkg2a的nk细胞对表达hla-e的靶细胞的细胞毒活性的适合测定来评估nkg2a+nk细胞应答。实例包括基于nk细胞活化的标记物的测定,例如cd107或cd137表达。本文实例中使用的阻断抗nkg2a抗体humz270(例如,具有seqidno:4-8中任一个的重链和seqidno:9的轻链)的nkg2a+nk细胞应答的ec50(例如,如在cd107转移测定中所评估的)为约4g/ml,并且ec100为约10μg/ml。因此,给予一定量的抗nkg2a抗体以维持至少4μg/ml的连续(最小)血液浓度。有利地,可给予一定量的抗nkg2a抗体以达到和/或维持至少10μg/ml的连续(最小)血液浓度。例如,要达到和/或维持的血液浓度可以在10-12μg/ml、10-15μg/ml、10-20μg/ml、10-30μg/ml、10-40μg/ml、10-50μg/ml、10-70μg/ml、10-100μg/ml、10-150μg/ml或10-200μg/ml之间。当脉管系统的外部组织被靶向(例如在实体瘤的治疗中)时,给予一定量的抗nkg2a抗体以达到和/或维持至少10μg/ml的组织浓度;例如,给予一定量的抗nkg2a抗体以达到至少100μg/ml的血液浓度,据预期达到至少10μg/ml的组织浓度。例如,为了在组织中达到/维持10μg/ml,所要达到和/或维持的血液浓度可以在100-110μg/ml、100-120μg/ml、100-130μg/ml、100-140μg/ml、100-150μg/ml、100-200μg/ml、100-250μg/ml或100-300μg/ml之间。
在一些实施例中,给予一定量的抗nkg2a抗体以获得对应于至少nkg2a+淋巴细胞应答(例如,nkg2a+nk细胞应答)的ec50的(任选地约为或至少约为)ec100在血液(例如,血清)中的浓度。关于nkg2a+细胞应答(例如nk细胞应答),“ec50”(或“ec100”)是指抗nkg2a抗体的有效浓度,其关于这种nkg2a+细胞应答(例如,nk细胞应答)产生其最大应答或效应的50%(或100%,当提及ec100时)。在一些实施例中,特别是为了治疗实体瘤,设计达到的浓度以导致组织中(在脉管系统外部,例如在肿瘤环境中)的浓度,该组织中的浓度对应于nkg2a+nk细胞应答的至少ec50(任选地约为或至少约为)、nkg2a+nk细胞应答的ec100。
针对本文实例中使用的具有约10μg/ml的nkg2a+nk细胞应答的ec100的抗nkg2a抗体(如humz270)的适合治疗方案包括至少一个给予周期,其中至少一个剂量的抗nkg2a抗体以以下剂量给予:2-10mg/kg、任选地4-10mg/kg、任选地6-10mg/kg、任选地2-6mg/kg、任选地2-8mg/kg、或任选地2-4mg/kg体重。任选地,给予至少2、3、4、5、6、7或8个剂量的抗nkg2a抗体。在一个实施例中,该给予周期在2周和8周之间。在一个实施例中,该给予周期是8周。在一个实施例中,该给予周期是8周,并且包括每两周给予一个剂量的抗nkg2a抗体(即,总共四个剂量)。
在本文的任何实施例的一个方面中,约每两周给予一次该抗nkg2a抗体。
与抗nkg2a抗体一起使用,特别是用于治疗造血系统肿瘤的适合的治疗方案包括例如,以有效维持抗nkg2a抗体的连续血液浓度为至少10μg/ml的量每月两次向患者给予抗nkg2a抗体,至少两次连续给予抗nkg2a抗体之间的连续血液浓度为2-10mg/kg、任选地2-8mg/kg、任选地2-6mg/kg、任选地2-4mg/kg、任选地约4mg/kg体重之间。可以任选地给予这些剂量,以便在整个治疗周期中提供至少10μg/ml的抗nkg2a抗体的连续血液浓度。达到10μg/ml的抗nkg2a抗体的血液浓度对应于抗体(如人源化z270)的ec100。
与抗nkg2a抗体一起使用,特别是用于治疗实体瘤(其中在血管外组织中(例如,在肿瘤或肿瘤环境中)寻求抗nkg2a抗体ec50浓度)的适合的治疗方案包括例如,以有效维持抗nkg2a抗体的连续血液浓度为至少40μg/ml的量每月两次向患者给予抗nkg2a抗体,至少两次连续给予抗nkg2a抗体之间的连续血液浓度为2-10mg/kg、任选地2-6mg/kg、任选地2-4mg/kg、任选地约4mg/kg体重之间。可以任选地给予这些剂量,以便在整个治疗周期中提供至少40μg/ml的抗nkg2a抗体的连续血液浓度。达到40μg/ml的抗nkg2a抗体的血液浓度被预期提供约4μg/ml的组织(例如,血管外组织、肿瘤环境)浓度,进而对应于抗体(如,人源化z270)的ec50。
与抗nkg2a抗体一起使用,特别是用于治疗实体瘤(其中在血管外组织中(例如,在肿瘤或肿瘤环境中)寻求抗nkg2a抗体ec50浓度)的适合的治疗方案包括例如向患者给予有效量的抗nkg2a抗体,其中每月两次并且以有效维持抗nkg2a抗体的连续血液浓度为至少100μg/ml的量给予该抗体,至少两次连续给予抗nkg2a抗体之间的连续血液浓度为4-10mg/kg、任选地4-6mg/kg、任选地4-8mg/kg、任选地约4mg/kg、任选地约6mg/kg、、任选地约8mg/kg、或任选地约10mg/kg之间。可以任选地给予这些剂量,以便在整个治疗周期中提供至少100μg/ml的抗nkg2a抗体的连续血液浓度。达到100μg/ml的抗nkg2a抗体的血液浓度被预期提供约10μg/ml的组织(例如,血管外组织、肿瘤环境)浓度,进而对应于抗体(如,人源化z270)的ec100。
与抗nkg2a抗体一起使用的另外的适合的治疗方案包括采用具有更高剂量的负荷期、然后是维持期的方案。例如,负荷期可以包括向患者给予有效量的抗nkg2a抗体,其中以有效维持抗nkg2a抗体的连续血液浓度为至少100μg/ml的量给予一次或多次该抗体直到在维持方案中第一次给予抗nkg2a抗体。例如,当给予一次时,可以给予抗nkg2a抗体的10mg/kg的负荷剂量,其中在维持方案内第一次给予抗nkg2a抗体在负荷剂量后的约两周(或更短)时发生。然后该维持方案可以采用给予的较低剂量和/或较低频率,以便在维持方案内的连续给予之间维持抗nkg2a抗体的连续血液浓度为至少100μg/ml。例如,维持方案可以包括每两周以以下剂量给予抗nkg2a抗体:2-10mg/kg、任选地4-10mg/kg、任选地2-4mg/kg、任选地4-6mg/kg、任选地4-8mg/kg、任选地约4mg/kg、任选地约6mg/kg、任选地约8mg/kg。
在某些实施例中,以4mg/kg、6mg/kg、8mg/kg或10mg/kg给予该抗nkg2a抗体的剂量(例如每个剂量)。在某些实施例中,以1-20mg/kg,任选地以10mg/kg给予抗pd-1抗体的剂量(例如每个剂量)。在某些实施例中,以10mg/kg、15mg/kg、20mg/kg或25mg/kg,任选地以1200mg总剂量给予抗pd-l1抗体的剂量(例如每个剂量)。在某些实施例中,联合治疗允许以较低剂量给予抗pd-1或pd-l1抗体;在一个实施例中,以2mg/kg或3mg/kg给予每剂量的抗pd-1抗体。
在一个实施例中,以下列剂量给予该抗nkg2a抗体和抗pd-1或抗pd-l1抗体:
(a)1-10mg/kg抗nkg2a抗体,和(i)1-10mg/kg的抗pd-1抗体,或(ii)1-20mg/kg的抗pd-l1抗体;
(b)4mg/kg、6mg/kg、8mg/kg或10mg/kg抗nkg2a抗体和10mg/kg的抗pd-1或抗pd-l1抗体;
(c)4mg/kg、6mg/kg、8mg/kg或10mg/kg抗nkg2a抗体和3mg/kg的抗pd-1抗体;或者
(d)4mg/kg、6mg/kg、8mg/kg或10mg/kg抗nkg2a抗体和2mg/kg的抗pd-1抗体。
在本文任何实施例的一方面中,约每两周给予一次该抗nkg2a抗体。在本文任何实施例的一方面中,约每三周给予一次该抗pd-1或抗pd-l1抗体。在本文任何实施例的一方面中,约每两周给予一次该抗pd-1或抗pd-l1抗体。在本文任何实施例的一方面中,约每四周给予一次该抗pd-1或抗pd-l1抗体。
在一个实施例中,通过静脉内给予该抗pd-1或抗pd-l1抗体以及抗nkg2a抗体。在一个实施例中,在同一天、任选地进一步约每两周一次、任选地进一步通过静脉内给予该抗pd-1或抗pd-l1抗体以及抗nkg2a抗体。
在其他方面中,提供了用于鉴定nkg2a+pd1+nk细胞和/或t细胞的方法。评估nkg2a和pd-1在nk细胞和/或t细胞上的共表达可用于诊断的或预后的方法中。例如,可以从个体(例如来自从癌症患者获得的癌组织或癌相邻组织)获得生物样品,并分析nkg2a+pd1+nk和/或t细胞的存在。nkg2a和pd-1两者在这些细胞上的表达可以例如用于鉴定具有肿瘤浸润性nk和/或t细胞的个体,这些肿瘤浸润性nk和/或t细胞被nkg2a和pd1多肽两者抑制。该方法可以例如用作针对用中和nkg2a的试剂治疗的响应的预后,用作针对用中和pd1的试剂治疗的响应的预后,或用作针对用中和nkg2a的试剂与中和pd1的试剂组合治疗的响应的预后。
在一个实施例中,提供了用于评估个体是否适于用抑制nkg2a的试剂与中和人pd-1的抑制性活性的试剂治疗的方法,该方法包括在来自个体的生物样品中检测表达nkg2a核酸或多肽以及pd-1核酸或多肽两者的淋巴细胞群(例如,cd8+t细胞)。确定个体具有表达nkg2a核酸或多肽以及pd-1核酸或多肽两者的淋巴细胞群表明了,患者患有癌症,该癌症可以用抑制nkg2a的试剂组合中和人pd-1的抑制性活性的试剂进行治疗。
在其他方面中,提供了用于鉴定nkg2a+pd1+nk细胞和/或t细胞的方法。肿瘤浸润效应淋巴细胞可以表达抑制性受体nkg2a和pd-1两者的发现产生了改进的治疗方法以及检测可用于诊断和预后的这些双重限制/抑制的效应细胞的方法。
例如,可以从个体(例如来自从癌症患者获得的肿瘤或肿瘤相邻组织)获得生物样品,并分析nkg2a+pd1+nk和/或t细胞的存在。nkg2a和pd-1两者在这些细胞上的表达可以例如用于鉴定具有肿瘤浸润性nk和/或t细胞的个体,这些肿瘤浸润性nk和/或t细胞被nkg2a和pd1多肽两者抑制。该方法可以例如用作针对用中和nkg2a的试剂治疗的响应的预后,用作针对用中和pd1的试剂治疗的响应的预后,或用作针对用中和nkg2a的试剂与中和pd1的试剂组合治疗的响应的预后。
检测生物样品内的nkg2a限制性和pd-1限制性nk和/或cd8t细胞可以更普遍地具有用于研究、评估、诊断、预后和/或病理学预测的优势,其中nk和/或cd8t细胞的表征是感兴趣的。例如,可以通过评估肿瘤或肿瘤相邻组织是否通过表达nkg2a和pd-1两者的浸润性nk和/或cd8t细胞来表征而做出有利或不利的癌症预后。
例如,可以使用抗nkg2a和抗pd1抗体来表征或评估患者中的癌症,以评估肿瘤浸润nk和/或cd8t细胞是否是nkg2a+pd1+,包括这些nk和/或cd8t细胞是否存在于肿瘤外周(在肿瘤相邻组织中)。这些方法可用于确定患者是否具有由nk和/或cd8t细胞表征的病理学,所述病理学可以适于通过直接作用于这样的nk和/或cd8t细胞(例如通过结合nkg2a和/或pd-1、或它们各自的配体hla-e或pd-l1)或间接作用于这样的nk和/或cd8t细胞(例如,通过产生可调节nk和/或cd8t细胞活性的细胞因子或其他信号分子)的治疗剂调节。任选地,在任何实施例中,已经用中和pd-1的试剂治疗该患者。本文所述的方法可任选地进一步包括:如果确定个体具有可以适于通过作用于肿瘤浸润nk和/或cd8t细胞的治疗剂调节的病理学,则向个体给予此类治疗剂。
在一方面中,诸位发明人提供了用于检测nkg2a+pd-1+淋巴细胞(任选地nk或cd8+t细胞)的体外方法,该方法包括提供包含肿瘤浸润淋巴细胞的生物样品,并确定这些淋巴细胞是否表达nkg2a和pd-1。
在一方面中,诸位发明人提供了在来自人类个体的样品内检测表达nkg2a和pd-1的(即,双阳性)cd8t细胞或nk细胞的体外方法,所述方法包括提供来自个体的样品,使用特异性结合人nkg2a多肽的单克隆抗体和特异性结合样品中的人pd-1多肽的单克隆抗体使所述样品中的细胞进行接触,并检测抗体与细胞的结合。在一个实施例中,这些细胞是cd8t细胞和/或nk细胞。
在一方面中,诸位发明人提供了在来自人类个体的样品内检测被nkg2a和pd-1二者抑制的组织浸润人cd8t细胞和/或nk细胞的体外方法,所述方法包括提供来自个体的样品,并且使用特异性结合人nkg2a多肽的单克隆抗体和特异性结合样品中人pd-1多肽的单克隆抗体检测所述样品中的组织浸润cd8t细胞和/或nk细胞,其中nkg2a和pd-1多肽的检测表明了nkg2a和pd-1抑制的组织浸润cd8t细胞和/或nk细胞的存在。任选地,在任何实施例中,已经用中和pd-1的试剂治疗该患者。在一个实施例中,该样品包括肿瘤细胞、肿瘤组织或肿瘤相邻组织。在一个实施例中,使用免疫组织化学方法鉴定cd8t细胞和/或nk细胞。在一个实施例中,该样品是石蜡包埋的样品;任选地将石蜡包埋的样品固定,包埋在石蜡中,切片,脱蜡,并在与单克隆抗体接触之前转移到载玻片上。在一个实施例中,使用流式细胞术方法鉴定cd8t细胞和/或nk细胞。
实例
实例1-rma-s和a20肿瘤细胞被表达nkg2a的nk细胞和表达nkg2a和/或pd-1的cd8t细胞浸润
通常发现淋巴细胞不共表达nkg2a和pd-1。为了研究这些受体在肿瘤浸润淋巴细胞上的表达,研究了nkg2a和pd-1在来自小鼠的肿瘤中的nk和t细胞亚群上的分布。淋巴细胞取自脾、肿瘤引流淋巴结、以及实体瘤内。
将c57/bl6小鼠用pdl-1+qa-1+rma-s细胞(qa-1,qdm,b2m)或用a20肿瘤细胞进行移植(sc)。当肿瘤体积为约500mm3时,处死rma-sqa-1qdmb2m(顶行)和a20(底行)荷瘤小鼠。
结果示于图1a和图1b中。通过流式细胞术分别针对肿瘤细胞的qa-1和pdl-1的表达以及til的nkg2a和pd-1的表达来分析肿瘤细胞(图1a)和肿瘤浸润淋巴细胞-til-(图1b)。示出了3只中的一只代表性小鼠。mfl荧光强度的中位数。
来自两种肿瘤类型的超过一半的浸润性nk细胞表达nkg2a,这表明肿瘤浸润nk细胞被nkg2a抑制。nkg2a+nk细胞通常不表达显著量的pd-1。然而,发现了对于nkg2a和pd-1都是阳性的cd8t细胞,这表明cd8t细胞可能受到抑制性受体nkg2a和pd-1两者的限制。
实施例2-来自荷有rma-rae1肿瘤的小鼠的nk和t细胞亚群能够共表达nkg2a和pd-1
为了进一步研究受体nkg2a和pd-1的表达,研究了nkg2a和pd-1在小鼠中的nk和t细胞亚群上的分布。淋巴细胞取自脾、肿瘤引流淋巴结、以及实体瘤内。
将c57/bl6小鼠用rma-rae克隆6(200万个细胞)进行抑移植(sc)。这些肿瘤细胞表达cd94/nkg2a配体(qa-1)。在第12天处死小鼠,平均肿瘤体积:723mm3,sd:161mm3,n=4。在从脾、ln和肿瘤制备细胞悬浮液后,将细胞如下进行染色:cd3epercpcy5.5,nkp46alexa647,nkg2a/c/efitc,pd1pe,cd8太平洋蓝(pacificblue)。
结果示于图2和表1-3中。
在nk细胞亚群中,引流淋巴结和脾两者中的细胞约为一半nkg2a阳性和一半nkg2a阴性,然而在这两种情况下均没有pd1的显著表达。来自淋巴结的nk细胞是nkg2a+pd-1-(49.2%)和nkg2a-pd-1-(49.5%),并且小于1%(平均值)的nk细胞是nkg2a+pd-1+。来自脾的nk细胞是nkg2a+pd-1-(44.1%)和nkg2a-pd-1-(55.7%),并且平均0.1%(平均值)的nk细胞是nkg2a+pd-1+。
在t细胞亚群中,大多数细胞是nkg2a阴性的(淋巴结中仅1.1%和脾中4.7%是nkg2a+),并且一小部分细胞是pd-1+(淋巴结中3.5%和脾中10%是pd-1+nkg2a-),没有显著的双阳性nkg2apd-1细胞。淋巴结中的仅0.1%(平均值)的t细胞是nkg2a+pd-1+,并且脾中的仅0.4%(平均值)的t细胞是nkg2a+pd-1+。来自淋巴结的95.1%的t细胞是双阴性的并且来自脾的85.6%的t细胞是双阴性的。
在cd8t细胞亚群中,大多数细胞是nkg2a阴性的(淋巴结中仅1.6%和脾中3.9%是nkg2a+),并且一小部分细胞是pd-1+(淋巴结中1.1%和脾中2.5%是pd-1+nkg2a-),没有显著的双阳性nkg2apd-1细胞。淋巴结中的仅0.2%(平均值)的t细胞是nkg2a+pd-1+,并且脾中的仅0.3%(平均值)的t细胞是nkg2a+pd-1+。来自淋巴结的97.3%的t细胞是双阴性的并且来自脾的93.6%的t细胞是双阴性的。
然而,在肿瘤浸润淋巴细胞(til)中,所有细胞亚群具有表达pd-1的细胞。在肿瘤中观察到以前在表达pd-1的显著百分比中未曾发现的nk细胞是pd-1阳性的,包括在nkg2a+亚群内,31.8%(平均值)的nk细胞是nkg2a+pd-1+。尽管肿瘤外几乎无cd8t细胞具有nkg2a表达,但表达pd-1的cd8t细胞在肿瘤中是常见的(肿瘤浸润cd8t细胞亚群具有26.3%nkg2a+阳性细胞的平均值)。此外,在该nkg2a阳性cd8t细胞亚群中,大多数细胞是nkg2a+pd-1+(19.4%(平均值))。然而,在cd8-t细胞亚群中,在til和脾或淋巴结细胞之间观察到的nkg2a表达几乎没有差异,因为肿瘤中仅有5.1%的t细胞表达nkg2a,并且仅3.6%的t细胞是双阳性nkg2apd-1。
表1:脾
表2:肿瘤引流淋巴结
表3:肿瘤浸润淋巴细胞
实例3-荷瘤小鼠中的nkg2a和pd-1表达
为了进一步研究荷瘤小鼠中的nkg2a和pd-1表达,用不同的肿瘤细胞(rma-rae1、mc38或rma细胞系)移植c57/bl6小鼠。为了评价肿瘤体积的影响,当小鼠的肿瘤分别达到500mm3、2000mm3和800mm3的体积时处死小鼠。
结果示于图3a和图3b中,其中rmarae1(顶行),mc38(中行)和rma(底行)。通过流式细胞术在脾、肿瘤引流淋巴结(ln)和肿瘤中针对nkg2a和pd-1表达来分析nk细胞(图3a)和cd8t细胞(图3b)。示出了2至4只中的一只代表性小鼠。
在nk细胞亚群中,肿瘤、淋巴结和脾中的细胞为约一半nkg2a阳性和一半nkg2a阴性。来自引流淋巴结或脾的nk细胞(不管他们的nkg2a表达)都不显示pd1的任何显著表达。然而,来自rma-rae1和rma的肿瘤浸润nk细胞表达了显著水平的nkg2a和pd1两者。特别大体积(2000mm3)下被处死的来自肿瘤系mc38的肿瘤浸润nk细胞表达nkg2a(50%)但不显著表达pd1(3%)。
与在大约一半群体中表达nkg2a的nk细胞不同,来自脾和淋巴结的cd8t细胞通常既不表达nkg2a也不表达pd1。然而,在肿瘤中,大比例的cd8t细胞表达nkg2a和pd1两者(rma-rae1中28%、mc38的43%和rma的40%是双阳性的)。结果再次表明,肿瘤浸润cd8t细胞以及nk细胞可以能够受抑制性受体nkg2a和pd1两者的限制,进一步受跨不同类型的肿瘤细胞的限制。
实例4-用抗pd-1mab的治疗增加了肿瘤中表达nkg2a的cd8t细胞的频率
为了评价用抗pd1抗体的治疗对cd8t细胞的影响,在细胞植入后的第11天、第14天和第17天用200μg的大鼠igg2a同种型对照(ic)或中和抗小鼠pd-1的单克隆抗体处理mc38荷瘤小鼠。在第31天处死小鼠(n=3/组),并通过流式细胞术在脾、肿瘤引流淋巴结(ln)和肿瘤中表征cd8t细胞。表示了cd8t细胞中cd8nkg2a+的百分比的平均值+/-sd(n=3)。p<0.005(***),p<0.0005(****),用双向anova进行统计分析,然后进行tukey多重比较检验。
结果示于图4中。类似于在其他实验中观察到的,来自脾或淋巴结的cd8t细胞不显著表达nkg2a。给予抗pd1抗体不引起脾或淋巴结t细胞中nkg2a表达水平的任何变化。然而,在肿瘤浸润cd8t细胞群中,给予抗pd1抗体导致表达nkg2a的cd8t细胞增加超过50%。结果表明,在用抗pd1抗体治疗时,nkg2a受体可以对于cd8t细胞应答对体内肿瘤的抑制具有增加的贡献。因此,nkg2a的中和可用于逆转对用中和pd-1轴线的试剂(例如抗pd1或抗pdl1抗体)处理的个体中的nkg2a限制性t细胞的抑制。
实例5-组合的抗nkg2a/抗pd1阻断抑制肿瘤生长
为了评价用中和抗pd1的抗体与中和抗nkg2a的抗体的联合治疗的效果,用rma-sqa-1qdmb2m肿瘤细胞移植(sc)c57bl/6小鼠,并用中和抗pd1试剂(中和抗pd-l1的抗体)与中和抗nkg2a的抗体处理。
简言之,在第11天,当rma-sqa-1qdmb2m肿瘤体积为约85mm3(n=8只小鼠/组)时,将c57bl/6小鼠进行随机试验,并在第11天、第14天和第18天用同种型对照、抗小鼠nkg2amab(200μg,静脉)、抗小鼠pd-l1mab(200μg,腹腔)或抗mnkg2a/mpdl-1组合进行处理。每周用卡尺测量肿瘤体积两次。当肿瘤变大(体积>2000mm3)时,将动物进行安乐死,溃烂或坏死。数据表示每次实验的肿瘤体积中位数。
肿瘤体积中位数随时间的发展如图5所示。虽然与该模型中的同种型对照相比,抗nkg2a仅产生适度的抗肿瘤效应,并且抗pd-l1产生实质性抗肿瘤效应但肿瘤体积随着接近第28天而增加,用抗nkg2a和抗pd-l1组合治疗完全消除肿瘤生长,在第28天观察到肿瘤体积没有显著生长。
在此所引用的所有文献(包括出版物、专利申请、以及专利)均通过引用以其全部内容特此结合,并且引用的程度如同每个文献被个别地并且明确地指示通过引用结合并且以其全部内容在此阐述(至法律允许的最大程度),而不考虑在此其他地方做出的特定文件的任何单独提供的结合。
除非在此另外指示或与上下文明显矛盾,否则在描述本发明的上下文中,术语“一个/种”和“该”以及类似指称对象的使用应解释为包括单数和复数二者。
除非另有说明,所有在此提供的精确值均代表相应的近似值(例如,所有精确的示例值是相对于具体因子提供的,或者测量可以视为还包括提供相应的近似测量,在适当时由“大约”修饰)。其中“约”与数字结合使用,这可以被指定为包括对应于指定数字的+/-10%的值。
除非另外陈述或与上下文明显矛盾,否则在此对于使用了涉及一种或多种要素的术语如“包含”、“具有”、“包括”或“含有”的本发明的任何方面或实施例的描述,旨在提供对“由那一种或多种特定要素组成”、“基本上由那一种或多种特定要素组成”或“基本上包含那一种或多种特定要素”的本发明的类似方面或实施例的支持(例如,除非另外陈述或与上下文明显矛盾,否则在此所述的包含特定要素的组合物应理解为也描述由那个要素组成的组合物)。
本文提供的任何和所有实例或示例性语言(例如“如”)的应用仅旨在更好地说明本发明,而不对另外要求保护的本发明范围做出限制。说明书中的语言不应当被解释为指示任何未要求保护的要素为实践本发明所必需的。
序列表
<110>依奈特制药公司
<120>对淋巴细胞中抑制途径的中和
<130>nkg2a-pd1
<150>us62/050,948
<151>2014-09-16
<150>us62/083,929
<151>2014-11-25
<150>us62/093,141
<151>2014-12-17
<160>15
<170>patentin3.5版本
<210>1
<211>233
<212>prt
<213>智人
<400>1
metaspasnglnglyvaliletyrseraspleuasnleuproproasn
151015
prolysargglnglnarglysprolysglyasnlysserserileleu
202530
alathrgluglngluilethrtyralagluleuasnleuglnlysala
354045
serglnasppheglnglyasnasplysthrtyrhiscyslysaspleu
505560
proseralaproglulysleuilevalglyileleuglyileilecys
65707580
leuileleumetalaservalvalthrilevalvalileproserthr
859095
leuileglnarghisasnasnserserleuasnthrargthrglnlys
100105110
alaarghiscysglyhiscysprogluglutrpilethrtyrserasn
115120125
sercystyrtyrileglylysgluargargthrtrpglugluserleu
130135140
leualacysthrserlysasnserserleuleuserileaspasnglu
145150155160
gluglumetlyspheleuserileileserprosersertrpilegly
165170175
valpheargasnserserhishisprotrpvalthrmetasnglyleu
180185190
alaphelyshisgluilelysaspseraspasnalagluleuasncys
195200205
alavalleuglnvalasnargleulysseralaglncysglyserser
210215220
ileiletyrhiscyslyshislysleu
225230
<210>2
<211>288
<212>prt
<213>智人
<400>2
metglnileproglnalaprotrpprovalvaltrpalavalleugln
151015
leuglytrpargproglytrppheleuaspserproaspargprotrp
202530
asnproprothrphepheproalaleuleuvalvalthrgluglyasp
354045
asnalathrphethrcysserpheserasnthrsergluserpheval
505560
leuasntrptyrargmetserproserasnglnthrasplysleuala
65707580
alapheprogluaspargserglnproglyglnaspcysargphearg
859095
valthrglnleuproasnglyargaspphehismetservalvalarg
100105110
alaargargasnaspserglythrtyrleucysglyalaileserleu
115120125
alaprolysalaglnilelysgluserleuargalagluleuargval
130135140
thrgluargargalagluvalprothralahisproserproserpro
145150155160
argproalaglyglnpheglnthrleuvalvalglyvalvalglygly
165170175
leuleuglyserleuvalleuleuvaltrpvalleualavalilecys
180185190
serargalaalaargglythrileglyalaargargthrglyglnpro
195200205
leulysgluaspproseralavalprovalpheservalasptyrgly
210215220
gluleuasppheglntrpargglulysthrprogluproprovalpro
225230235240
cysvalprogluglnthrglutyralathrilevalpheprosergly
245250255
metglythrserserproalaargargglyseralaaspglyproarg
260265270
seralaglnproleuargprogluaspglyhiscyssertrpproleu
275280285
<210>3
<211>290
<212>prt
<213>智人
<400>3
metargilephealavalpheilephemetthrtyrtrphisleuleu
151015
asnalaphethrvalthrvalprolysaspleutyrvalvalglutyr
202530
glyserasnmetthrileglucyslyspheprovalglulysglnleu
354045
aspleualaalaleuilevaltyrtrpglumetgluasplysasnile
505560
ileglnphevalhisglyglugluaspleulysvalglnhisserser
65707580
tyrargglnargalaargleuleulysaspglnleuserleuglyasn
859095
alaalaleuglnilethraspvallysleuglnaspalaglyvaltyr
100105110
argcysmetilesertyrglyglyalaasptyrlysargilethrval
115120125
lysvalasnalaprotyrasnlysileasnglnargileleuvalval
130135140
aspprovalthrsergluhisgluleuthrcysglnalagluglytyr
145150155160
prolysalagluvaliletrpthrserserasphisglnvalleuser
165170175
glylysthrthrthrthrasnserlysarggluglulysleupheasn
180185190
valthrserthrleuargileasnthrthrthrasngluilephetyr
195200205
cysthrpheargargleuaspproglugluasnhisthralagluleu
210215220
valileprogluleuproleualahisproproasngluargthrhis
225230235240
leuvalileleuglyalaileleuleucysleuglyvalalaleuthr
245250255
pheilepheargleuarglysglyargmetmetaspvallyslyscys
260265270
glyileglnaspthrasnserlyslysglnseraspthrhisleuglu
275280285
gluthr
290
<210>4
<211>452
<212>prt
<213>人工的
<220>
<223>人-鼠嵌合体
<400>4
gluvalglnleuvalglnserglyalagluvallyslysproglyglu
151015
serleulysilesercyslysglyserglytyrserphethrsertyr
202530
trpmetasntrpvalargglnmetproglylysglyleuglutrpmet
354045
glyargileaspprotyraspsergluthrhistyrserproserphe
505560
glnglyglnvalthrileseralaasplysserileserthralatyr
65707580
leuglntrpserserleulysalaseraspthralamettyrtyrcys
859095
alaargglyglytyrasppheaspvalglythrleutyrtrpphephe
100105110
aspvaltrpglyglnglythrthrvalthrvalserseralaserthr
115120125
lysglyproservalpheproleualaprocysserargserthrser
130135140
gluserthralaalaleuglycysleuvallysasptyrpheproglu
145150155160
provalthrvalsertrpasnserglyalaleuthrserglyvalhis
165170175
thrpheproalavalleuglnserserglyleutyrserleuserser
180185190
valvalthrvalproserserserleuglythrlysthrtyrthrcys
195200205
asnvalasphislysproserasnthrlysvalasplysargvalglu
210215220
serlystyrglyproprocysproprocysproalaproglupheleu
225230235240
glyglyproservalpheleupheproprolysprolysaspthrleu
245250255
metileserargthrprogluvalthrcysvalvalvalaspvalser
260265270
glngluaspprogluvalglnpheasntrptyrvalaspglyvalglu
275280285
valhisasnalalysthrlysproargglugluglnpheasnserthr
290295300
tyrargvalvalservalleuthrvalleuhisglnasptrpleuasn
305310315320
glylysglutyrlyscyslysvalserasnlysglyleuproserser
325330335
ileglulysthrileserlysalalysglyglnproarggluprogln
340345350
valtyrthrleuproproserglngluglumetthrlysasnglnval
355360365
serleuthrcysleuvallysglyphetyrproseraspilealaval
370375380
glutrpgluserasnglyglnprogluasnasntyrlysthrthrpro
385390395400
provalleuaspseraspglyserphepheleutyrserargleuthr
405410415
valasplysserargtrpglngluglyasnvalphesercysserval
420425430
methisglualaleuhisasnhistyrthrglnlysserleuserleu
435440445
serleuglylys
450
<210>5
<211>452
<212>prt
<213>人工的
<220>
<223>人-鼠嵌合体
<400>5
glnvalglnleuvalglnserglyalagluvallyslysproglyala
151015
servallysvalsercyslysalaserglytyrthrphethrsertyr
202530
trpmetasntrpvalargglnalaproglyglnglyleuglutrpmet
354045
glyargileaspprotyraspsergluthrhistyralaglnlysleu
505560
glnglyargvalthrmetthrthraspthrserthrserthralatyr
65707580
metgluleuargserleuargseraspaspthralavaltyrtyrcys
859095
alaargglyglytyrasppheaspvalglythrleutyrtrpphephe
100105110
aspvaltrpglyglnglythrthrvalthrvalserseralaserthr
115120125
lysglyproservalpheproleualaprocysserargserthrser
130135140
gluserthralaalaleuglycysleuvallysasptyrpheproglu
145150155160
provalthrvalsertrpasnserglyalaleuthrserglyvalhis
165170175
thrpheproalavalleuglnserserglyleutyrserleuserser
180185190
valvalthrvalproserserserleuglythrlysthrtyrthrcys
195200205
asnvalasphislysproserasnthrlysvalasplysargvalglu
210215220
serlystyrglyproprocysproprocysproalaproglupheleu
225230235240
glyglyproservalpheleupheproprolysprolysaspthrleu
245250255
metileserargthrprogluvalthrcysvalvalvalaspvalser
260265270
glngluaspprogluvalglnpheasntrptyrvalaspglyvalglu
275280285
valhisasnalalysthrlysproargglugluglnpheasnserthr
290295300
tyrargvalvalservalleuthrvalleuhisglnasptrpleuasn
305310315320
glylysglutyrlyscyslysvalserasnlysglyleuproserser
325330335
ileglulysthrileserlysalalysglyglnproarggluprogln
340345350
valtyrthrleuproproserglngluglumetthrlysasnglnval
355360365
serleuthrcysleuvallysglyphetyrproseraspilealaval
370375380
glutrpgluserasnglyglnprogluasnasntyrlysthrthrpro
385390395400
provalleuaspseraspglyserphepheleutyrserargleuthr
405410415
valasplysserargtrpglngluglyasnvalphesercysserval
420425430
methisglualaleuhisasnhistyrthrglnlysserleuserleu
435440445
serleuglylys
450
<210>6
<211>452
<212>prt
<213>人工的
<220>
<223>人-鼠嵌合体
<400>6
gluvalglnleuvalglnserglyalagluvallyslysproglyglu
151015
serleuargilesercyslysglyserglytyrserphethrsertyr
202530
trpmetasntrpvalargglnmetproglylysglyleuglutrpmet
354045
glyargileaspprotyraspsergluthrhistyrserproserphe
505560
glnglyhisvalthrileseralaasplysserileserthralatyr
65707580
leuglntrpserserleulysalaseraspthralamettyrtyrcys
859095
alaargglyglytyrasppheaspvalglythrleutyrtrpphephe
100105110
aspvaltrpglyglnglythrthrvalthrvalserseralaserthr
115120125
lysglyproservalpheproleualaprocysserargserthrser
130135140
gluserthralaalaleuglycysleuvallysasptyrpheproglu
145150155160
provalthrvalsertrpasnserglyalaleuthrserglyvalhis
165170175
thrpheproalavalleuglnserserglyleutyrserleuserser
180185190
valvalthrvalproserserserleuglythrlysthrtyrthrcys
195200205
asnvalasphislysproserasnthrlysvalasplysargvalglu
210215220
serlystyrglyproprocysproprocysproalaproglupheleu
225230235240
glyglyproservalpheleupheproprolysprolysaspthrleu
245250255
metileserargthrprogluvalthrcysvalvalvalaspvalser
260265270
glngluaspprogluvalglnpheasntrptyrvalaspglyvalglu
275280285
valhisasnalalysthrlysproargglugluglnpheasnserthr
290295300
tyrargvalvalservalleuthrvalleuhisglnasptrpleuasn
305310315320
glylysglutyrlyscyslysvalserasnlysglyleuproserser
325330335
ileglulysthrileserlysalalysglyglnproarggluprogln
340345350
valtyrthrleuproproserglngluglumetthrlysasnglnval
355360365
serleuthrcysleuvallysglyphetyrproseraspilealaval
370375380
glutrpgluserasnglyglnprogluasnasntyrlysthrthrpro
385390395400
provalleuaspseraspglyserphepheleutyrserargleuthr
405410415
valasplysserargtrpglngluglyasnvalphesercysserval
420425430
methisglualaleuhisasnhistyrthrglnlysserleuserleu
435440445
serleuglylys
450
<210>7
<211>452
<212>prt
<213>人工的
<220>
<223>人-鼠嵌合体
<400>7
gluvalglnleuvalglnserglyalagluvallyslysproglyala
151015
thrvallysilesercyslysvalserglytyrthrphethrsertyr
202530
trpmetasntrpvalglnglnalaproglylysglyleuglutrpmet
354045
glyargileaspprotyraspsergluthrhistyralaglulysphe
505560
glnglyargvalthrilethralaaspthrserthraspthralatyr
65707580
metgluleuserserleuargsergluaspthralavaltyrtyrcys
859095
alathrglyglytyrasppheaspvalglythrleutyrtrpphephe
100105110
aspvaltrpglyglnglythrthrvalthrvalserseralaserthr
115120125
lysglyproservalpheproleualaprocysserargserthrser
130135140
gluserthralaalaleuglycysleuvallysasptyrpheproglu
145150155160
provalthrvalsertrpasnserglyalaleuthrserglyvalhis
165170175
thrpheproalavalleuglnserserglyleutyrserleuserser
180185190
valvalthrvalproserserserleuglythrlysthrtyrthrcys
195200205
asnvalasphislysproserasnthrlysvalasplysargvalglu
210215220
serlystyrglyproprocysproprocysproalaproglupheleu
225230235240
glyglyproservalpheleupheproprolysprolysaspthrleu
245250255
metileserargthrprogluvalthrcysvalvalvalaspvalser
260265270
glngluaspprogluvalglnpheasntrptyrvalaspglyvalglu
275280285
valhisasnalalysthrlysproargglugluglnpheasnserthr
290295300
tyrargvalvalservalleuthrvalleuhisglnasptrpleuasn
305310315320
glylysglutyrlyscyslysvalserasnlysglyleuproserser
325330335
ileglulysthrileserlysalalysglyglnproarggluprogln
340345350
valtyrthrleuproproserglngluglumetthrlysasnglnval
355360365
serleuthrcysleuvallysglyphetyrproseraspilealaval
370375380
glutrpgluserasnglyglnprogluasnasntyrlysthrthrpro
385390395400
provalleuaspseraspglyserphepheleutyrserargleuthr
405410415
valasplysserargtrpglngluglyasnvalphesercysserval
420425430
methisglualaleuhisasnhistyrthrglnlysserleuserleu
435440445
serleuglylys
450
<210>8
<211>452
<212>prt
<213>人工的
<220>
<223>人-鼠嵌合体
<400>8
glnvalglnleuvalglnserglyalagluvallyslysproglyala
151015
servallysvalsercyslysalaserglytyrthrphethrsertyr
202530
trpmetasntrpvalargglnalaproglyglnglyleuglutrpmet
354045
glyargileaspprotyraspsergluthrhistyralaglnlysphe
505560
glnglyargvalthrmetthrargaspthrserthrserthrvaltyr
65707580
metgluleuserserleuargsergluaspthralavaltyrtyrcys
859095
alaargglyglytyrasppheaspvalglythrleutyrtrpphephe
100105110
aspvaltrpglyglnglythrthrvalthrvalserseralaserthr
115120125
lysglyproservalpheproleualaprocysserargserthrser
130135140
gluserthralaalaleuglycysleuvallysasptyrpheproglu
145150155160
provalthrvalsertrpasnserglyalaleuthrserglyvalhis
165170175
thrpheproalavalleuglnserserglyleutyrserleuserser
180185190
valvalthrvalproserserserleuglythrlysthrtyrthrcys
195200205
asnvalasphislysproserasnthrlysvalasplysargvalglu
210215220
serlystyrglyproprocysproprocysproalaproglupheleu
225230235240
glyglyproservalpheleupheproprolysprolysaspthrleu
245250255
metileserargthrprogluvalthrcysvalvalvalaspvalser
260265270
glngluaspprogluvalglnpheasntrptyrvalaspglyvalglu
275280285
valhisasnalalysthrlysproargglugluglnpheasnserthr
290295300
tyrargvalvalservalleuthrvalleuhisglnasptrpleuasn
305310315320
glylysglutyrlyscyslysvalserasnlysglyleuproserser
325330335
ileglulysthrileserlysalalysglyglnproarggluprogln
340345350
valtyrthrleuproproserglngluglumetthrlysasnglnval
355360365
serleuthrcysleuvallysglyphetyrproseraspilealaval
370375380
glutrpgluserasnglyglnprogluasnasntyrlysthrthrpro
385390395400
provalleuaspseraspglyserphepheleutyrserargleuthr
405410415
valasplysserargtrpglngluglyasnvalphesercysserval
420425430
methisglualaleuhisasnhistyrthrglnlysserleuserleu
435440445
serleuglylys
450
<210>9
<211>214
<212>prt
<213>人工的
<220>
<223>人-鼠嵌合体
<400>9
aspileglnmetthrglnserproserserleuseralaservalgly
151015
aspargvalthrilethrcysargalasergluasniletyrsertyr
202530
leualatrptyrglnglnlysproglylysalaprolysleuleuile
354045
tyrasnalalysthrleualagluglyvalproserargphesergly
505560
serglyserglythraspphethrleuthrileserserleuglnpro
65707580
gluaspphealathrtyrtyrcysglnhishistyrglythrproarg
859095
thrpheglyglyglythrlysvalgluilelysargthrvalalaala
100105110
proservalpheilepheproproseraspgluglnleulyssergly
115120125
thralaservalvalcysleuleuasnasnphetyrproarggluala
130135140
lysvalglntrplysvalaspasnalaleuglnserglyasnsergln
145150155160
gluservalthrgluglnaspserlysaspserthrtyrserleuser
165170175
serthrleuthrleuserlysalaasptyrglulyshislysvaltyr
180185190
alacysgluvalthrhisglnglyleuserserprovalthrlysser
195200205
pheasnargglyglucys
210
<210>10
<211>119
<212>prt
<213>人工的
<220>
<223>人-鼠嵌合体
<400>10
gluvalglnleuvalgluserglyglyglyleuvallysproglygly
151015
serleulysleusercysalaalaserglyphethrphesersertyr
202530
alametsertrpvalargglnserproglulysargleuglutrpval
354045
alagluileserserglyglysertyrthrtyrtyrproaspthrval
505560
thrglyargphethrileserargaspasnalalysasnthrleutyr
65707580
leugluileserserleuargsergluaspthralamettyrtyrcys
859095
thrarghisglyasptyrproargphepheaspvaltrpglyalagly
100105110
thrthrvalthrvalserser
115
<210>11
<211>107
<212>prt
<213>人工的
<220>
<223>人-鼠嵌合体
<400>11
glnilevalleuthrglnserproalaleumetseralaserprogly
151015
glulysvalthrmetthrcysseralaserserservalsertyrile
202530
tyrtrptyrglnglnlysproargserserprolysprotrpiletyr
354045
leuthrserasnleualaserglyvalproalaargpheserglyser
505560
glyserglythrsertyrserleuthrilesersermetglualaglu
65707580
aspalaalathrtyrtyrcysglnglntrpserglyasnprotyrthr
859095
pheglyglyglythrlysleugluilelysarg
100105
<210>12
<211>432
<212>prt
<213>智人
<400>12
glnvalglnleuvalgluserglyglyglytrpglnproglyargser
151015
leuargleuaspcyslysalaserglyilethrpheserasnsergly
202530
methistrpvalargglnalaproglylysglyleuglutrpvalala
354045
valargtrptyraspglyserlysargtyrtyralaaspservallys
505560
glyargphethrileserargaspasnserlysasnthrleupheleu
65707580
glnmetasnserleuargalagluaspthralavaltyrtyrcysala
859095
thrasnaspasptyrtrpglyglnglythrleuvalthrvalserser
100105110
alaserthrlysglyproservalpheproleualaprocysserarg
115120125
serthrsergluserthralaalaleuglycysleuvalasptyrphe
130135140
progluprovalthrvalsertrpasnserglyalaleuthrsergly
145150155160
valhisthrpheproalavalleuglnserserglyleutyrserleu
165170175
serservalvalthrvalproserserserleuglythrthrtyrthr
180185190
cysasnvalasphislysproserasnthrlysvalaspargvalglu
195200205
sertyrglyproprocysproprocysproalaproglupheleugly
210215220
glyproservalpheleupheproprolysprolysaspthrleumet
225230235240
ileserargthrprogluvalthrcystrpvalaspvalserglnglu
245250255
aspprogluvalglnpheasntrptyrtyraspglyvalgluvalhis
260265270
asnalathrlysproargglugluglnpheasnserthrtyrargval
275280285
valservalleuthrvalleuhisglnasptrpleuasnglylysglu
290295300
tyrlyscyslysvalserasnlysglyleuproserserileglulys
305310315320
thrileserlysalaglyglnproarggluproglnvaltyrthrleu
325330335
proproserglngluglumetthrlysasnglnvalserleuthrcys
340345350
leuvallysglyphetyrproseraspilealavalglutrpgluser
355360365
asnglyglnproglulysasntyrlysthrthrproprovalleuasp
370375380
seraspglyserphepheleutyrserargleuthrvalasplysser
385390395400
argtrpglngluglyasnvalphesercysservalmethisgluala
405410415
leuhisasnhistyrthrglnlysserleuserleuserleuglylys
420425430
<210>13
<211>207
<212>prt
<213>智人
<400>13
gluilevalleuthrglnserproalathrleuserleuserprogly
151015
gluargalathrleusercysargalaserglnservalsersertyr
202530
leualatrptyrglnglnproglyglnalaproargleuleuiletyr
354045
aspalaserasnargalathrglyileproalaargpheserglyser
505560
glyserglythraspphethrleuthrileserserleugluproglu
65707580
aspphealavaltyrtyrcysglnglnserserasntrpproargthr
859095
pheglyglnglythrlysvalgluileargthrvalalaalaproser
100105110
valpheilepheproproseraspgluglnleuserglythralaser
115120125
valvalcysleuleuasnasnphetyrproargglualavalglntrp
130135140
lysvalaspasnalaleuglnserglyasnserglngluservalthr
145150155160
gluglnaspseraspserthrtyrserleuserserthrleuleuser
165170175
lysalaasptyrglulyshislysvaltyralacysgluvalthrhis
180185190
glnglyleuserserprovalthrserpheasnargglyglucys
195200205
<210>14
<211>117
<212>prt
<213>智人
<400>14
gluvalglnleuvalgluserglyglyglyleuvalglnproglygly
151015
serleuargleusercysalaalaserglyphethrpheseraspser
202530
trpilehistrpvalargglnalaproglylysglyleuglutrpval
354045
alatrpileserprotyrglyglyserthrtyrtyralaaspserval
505560
lysglyargphethrileseralaaspthrserlysasnthralatyr
65707580
leuglnasnserleuargalagluaspthralavaltyrtyrcysala
859095
argarghistrpproglyglypheasptyrtrpglyglnglythrleu
100105110
valthrvalserser
115
<210>15
<211>107
<212>prt
<213>智人
<400>15
aspileglnmetthrglnserproserserleuseralaservalgly
151015
aspargvalthrilethrcysargalaserglnaspvalserthrala
202530
valalatrptyrglnglnproglylysalaprolysleuleuiletyr
354045
seralaserpheleutyrserglyvalproserargpheserglyser
505560
glyserglythraspphethrleuthrileserserleuglnproglu
65707580
aspphealathrtyrtyrcysglnglntyrleutyrhisproalathr
859095
pheglyglnglythrlysvalgluilelysarg
100105
- 还没有人留言评论。精彩留言会获得点赞!