一种完全必需氨基酸的分离制备方法与流程
本发明涉及完全氨基酸分离制备的生产技术领域,尤其是涉及一种完全必需氨基酸的分离制备方法。
背景技术:
氨基酸是蛋白质的组成成分,在人体营养和生理上占有重要地位,人们对蛋白质的需求实际上就是对氨基酸的需要。我们每天从食物中摄取的蛋白质,在胃肠道中,经过胃蛋白酶、胰蛋白酶、糜蛋白酶和羧肽酶等酶的作用,最终被分解为氨基酸,然后经小肠粘膜的上皮细胞被吸收。其作用主要表现在以下5个方面:
一是合成或修补组织蛋白质,以补充人体新陈代谢中被分解掉的同类蛋白质;
二是合成或转变为其它氨基酸,如苯丙氨酸可转变为酪氨酸、蛋氨酸可合成为半胱氨酸等;
三是进入氨基酸的分解代谢过程,其含氮部分通常转变成尿素;
四是被合成蛋白质以外的含氮化合物,如嘌呤、肌酸等;
五是作为生热营养素,在代谢过程中释放出能量,供机体需要。
在构成人体蛋白质的20多种氨基酸中,大多数是可以在人体内直接合成或由其它氨基酸转变而来,少数人体是不能合成或合成速度较慢,满足不了人体新陈代谢的需要,必须由食物蛋白质供给,这类氨基酸在营养学上通常称为必需氨基酸。必需氨基酸通常有8种,即异亮氨酸、亮氨酸、赖氨酸、蛋氨酸、苯丙氨酸、苏氨酸、缬氨酸、色氨酸。此外,组氨酸对婴儿来讲也是必需氨基酸。
必需氨基酸及其代谢产物在维持肠黏膜完整性和肠道功能方面发挥着重要的作用。不仅如此,必需氨基酸的肠道代谢对整个机体健康也有重要意义。由于肠道组织在解剖结构上处于优先利用摄入氨基酸的地位,肠道组织内氨基酸代谢可影响到食物氨基酸进入门脉循环的模式,从而影响整个机体对食物中必需氨基酸的利用和氨基酸功能的发挥。人体内的必需氨基酸在维持正常代谢,机体稳态上以及整个机体的健康上都有重要意义。由于必需氨基酸的特点和作用,使得必需氨基酸的生产和应用成为一个很有前景的研究领域,开发利用这些必需氨基酸作为新的营养制剂、功能食品和饲料添加剂大有可为。
氨基酸生产方法分为四种:生物资源提取法(蛋白质水解法)、化学合成法、发酵法(分直接发酵法和前体添加发酵法)、酶法。提取法和化学合成法由于原料来源受限制、生产成本较高、污染环境,难以实现大规模工业化生产。酶法是利用生物酶催化的立体专一性反应,从底物生产光学活性的氨基酸。反应大多在水溶液中进行,条件温和,选择性高,底物浓度高,转化率高,副产物少,生产工艺简单,分离精制容易。微生物发酵法具有原料成本低、反应条件温和、容易实现大规模生产等优点,是目前生产L-氨基酸最主要的方法。发酵主要是利用微生物在生长过程中产酶,使底物中蛋白质等大分子物质降解来提高产品的营养价值。与非发酵制品相比,原料中的蛋白质微生物酶水解为氨基酸提高了产品的营养价值和消化性能,游离必需氨基酸含量与游离总氨基酸的含量均显著增加。
凝胶过滤色谱是利用具有网状结构的凝胶分子筛作用,根据被分离物分子大小不同进行分离。与其他分离技术相比,凝胶过滤色谱具有一些较为突出的优势,包括:凝胶色谱介质不带电荷,具有良好稳定性,在很宽的范围内呈化学惰性,不与待分离物质发生反应,分离条件温和,回收率高,重现性好;通常情况下,溶液中存在的各种离子、小分子、去污剂、表面活性剂、蛋白质变性剂等不会对 分离产生影响,色谱还能在不同pH、温度下进行;应用范围广,能分离的物质相对分子质量的覆盖面宽;设备相对简单、易于操作;分离周期短、连续分离时色谱介质不需要再生即可反复使用。
相对分子质量较大的物质由于直径大于凝胶网孔被完全排阻在孔外,只能现在凝胶颗粒外的空间下流动,因此流程较短,流动速度快,所以首先流出;
相对分子质量较小的物质由于直径小于凝胶网孔,可完全渗透进去入凝胶颗粒的网孔,在向下移动的过程中,因此流程较长,移动速率慢,所以最后流出;
中等大小的分子,它们在凝胶颗粒内外部分渗透,渗透的程度取决于它们的大小,所以它们流出的时间介于二者之间,这样分子大的组分先流出,分子小的组分后流出。这样样品经过凝胶层析后,各个组分便按分子从大到小的顺序依次流出,从而达到了分离的目的。
技术实现要素:
本发明的目的旨在提供一种完全必需氨基酸的分离制备方法,提高氨基酸的提取率,并将必需氨基酸从复合氨基酸中分离,得到完全必需氨基酸。
本发明通过将大豆蛋白经富含蛋白酶的枯草芽孢杆菌发酵处理后,利用蛋白酶将大豆蛋白水解成游离氨基酸;烘干粉碎后即获得完全氨基酸原料。
本发明通过将选用的大豆蛋白经富含蛋白酶的枯草芽孢杆菌发酵处理后,游离总氨基酸的含量由0.267g/100g增加至8.726g/100g,增加了31.68倍。游离必需氨基酸的含量由0.063g/100g增加至3.616g/100g,增加了56.40倍,显著提高了游离总氨基酸和游离必需氨基酸的含量。
本发明通过单因素试验、正交试验对总游离游离氨基酸的提取工艺进行了优选,确定了最优的提取条件为提取时间为2.5h、提取温度为45℃、料液比为45倍、乙醇浓度为55%。按照最优提取工艺,总游离氨基酸的浸出量达48.31mg/g;按确定的提取条件进行了验证试验,RSD=0.15%,结果表明稳定性好。
本发明通过利用最优的提取条件提取的总游离氨基酸的浸出量为48.31mg/g,产率达总游离氨基酸含量的55.36%。
本发明通过利用相似相溶法、等电点沉淀法、凝胶过滤色谱法等方法,将完全必需游离氨基酸成功的从提取出来的总游离氨基酸中分离。实验最后可得到包括8种必需氨基酸和一种非必需氨基酸脯氨酸在内的高纯度完全必需游离氨基酸溶液。
以下是发明人为实现本发明的目的,采取的实验方案:一种完全必需氨基酸的分离制备方法,包括以下步骤:
1材料与方法
1.1实验试剂与原料准备
1.1.1实验试剂
水合茚三酮(分析纯),磷酸二氢钾(分析纯),氢氧化钠(分析纯),甘氨酸(层析纯),乙醇(95%,分析纯)
1.1.2原料准备将大豆蛋白经富含蛋白酶的植物乳杆菌和枯草芽孢杆菌发酵处理后,利用蛋白酶将大豆蛋白酶水解成氨基酸;烘干粉碎后即获得完全氨基酸原料。
1.2实验仪器设备
日本岛津公司LC-6A高效液相(HPLC)色谱仪,RF-530荧光检测器,SIC-6A自动进样器,CR-3A数据处理系统,HH数显恒温水浴锅(金坛市金城国胜实验仪器厂),精密电子天平(天津天马衡基仪器有限公司),SHZ-D(Ⅲ)循环水式真 空泵(巩义市予华仪器有限责任公司),Spectrumlab 22pc可见分光光度计(上海棱光技术有限公司),500克密封型摇摆式粉碎机(广州市旭朗机械设备有限公司)
2实验方法
2.1实验试剂的配制
2.1.1茚三酮溶液的配制精密称取水合茚三酮2.0000g至100mL容量瓶中,用少量95%乙醇溶解并定容至刻度。
2.1.2磷酸盐缓冲液的配制(pH=6.8)精密称取磷酸二氢钾3.4022g,氢氧化钠0.4720g混合加蒸馏水使其溶解,蒸馏水加至500ml。
2.1.3甘氨酸对照品溶液的配制(0.1mg/ml)精密称取甘氨酸0.0100g,加蒸馏水溶解完全后定容至100ml。
2.2测量波长的选择
分别取甘氨酸对照品溶液、蒸馏水各1ml于2个容量瓶中,分别加茚三酮溶液2ml和磷酸盐缓冲液1ml,摇匀,水浴加热15min,取出,冷却,用蒸馏水定容至25ml。在可见分光光度计中进行波长扫描,结果显示分光光度计最大吸收波长在570nm处。因此,确定本试验的最佳测定波长为570nm。
2.3标准曲线的绘制
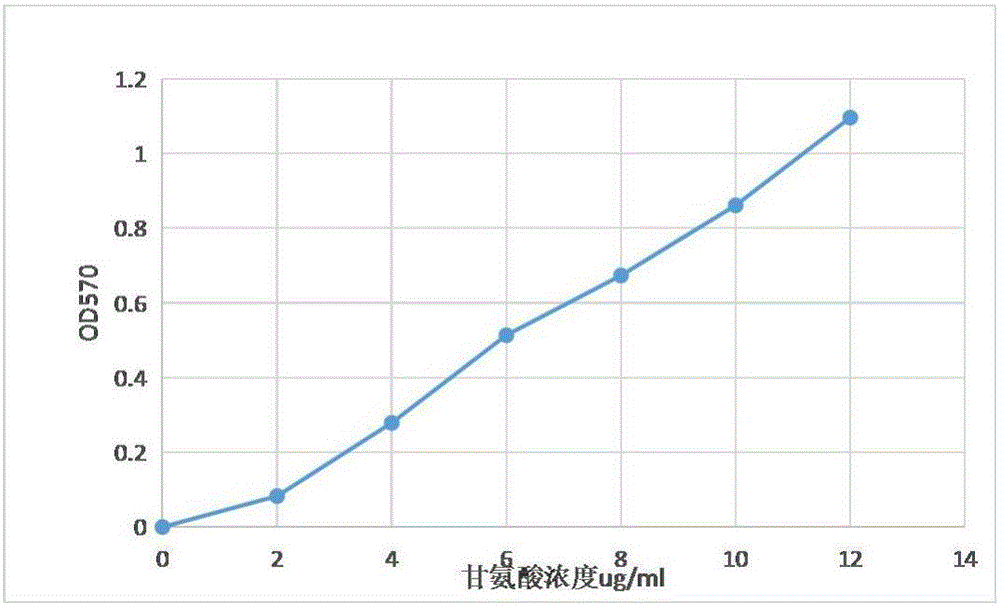
精取0.1mg/ml甘氨酸对照液0.00、0.50、1.00、1.50、2.00、2.50、3.00,各加2%茚三酮溶液2ml,缓冲液1ml,沸水浴加热15min,取出,冷却,用蒸馏水定容至25ml,在570nm处测吸光度。以甘氨酸浓度(μg/ml)为横坐标,吸光度为纵坐标,绘制标准曲线。求得其回归方程为Y=0.09364x-0.06057;R2=0.9914。
表1甘氨酸标准曲线
2.4蛋白酶制备
将大豆蛋白经富含蛋白酶的植物乳杆菌和枯草芽孢杆菌发酵处理后,利用蛋白酶将大豆蛋白酶水解成氨基酸,通过比较总游离氨基酸的含量及增加倍值来确定植物乳杆菌和枯草芽孢杆菌蛋白酶活性的大小。氨基酸的测定方法采用HPLC-RF法。
2.5氨基酸提取率的测定方法
将每次实验的提取液定容至250mL,移取1ml至25ml容量瓶中,加入2%茚三酮溶液2ml,缓冲液1ml,沸水浴加热15min,取出,冷却,定容,在分光光度计上以相应试剂为空白,于570nm处测定吸光度。
2.6工艺优化
采用浸提法提取完全氨基酸,并考察提取溶剂及溶剂浓度、提取时间、料液比、提取温度对氨基酸提取效果的影响。测定提取液中氨基酸含量作为实验条件讨论参考根据。提取液中氨基酸浓度的测定采用茚三酮显色分光光度法。
2.7正交试验设计
为了进一步确定各因素综合效果,可通过单因素试验对每个因素的适宜范围,以提取溶剂及溶剂浓度、提取时间、料液比、提取温度为影响因素,做正交优化试验。
2.8完全必需氨基酸的分离
通过利用相似相溶法、等电点沉淀法、凝胶过滤色谱法等方法,将完全必需 游离氨基酸成功地从提取出来的总游离氨基酸中分离。
3结果及分析
3.1植物乳杆菌和枯草芽孢杆菌蛋白酶活性的比较
将大豆蛋白经富含蛋白酶的植物乳杆菌和枯草芽孢杆菌发酵处理后,利用蛋白酶将大豆蛋白酶水解成氨基酸,酶解得到游离总氨基酸的数据如下表。
表2游离总氨基酸含量
表3游离必需氨基酸含量
由表2和表3可以看出,大豆蛋白经富含蛋白酶的植物乳杆菌和枯草芽孢杆菌发酵处理后,游离总氨基酸的含量分别由0.267g/100g增加至7.988g/100g和8.726g/100g,分别增加了28.92倍和31.68倍。游离必需氨基酸的含量分别由0.063g/100g增加至3.242g/100g和3.616g/100g,分别增加了50.46倍和56.40倍。这表明大豆蛋白经富含蛋白酶的植物乳杆菌和枯草芽孢杆菌发酵处理后,显著提高了游离总氨基酸和游离必需氨基酸的含量,且枯草芽孢杆菌处理后游离总氨基 酸和游离必需氨基酸含量与增加倍值都明显高于植物乳杆菌,因此,本实验选用的菌种是富含蛋白酶的枯草芽孢杆菌。
3.2工艺优化结果
3.2.1提取溶剂及溶剂浓度的选择
在常规植物材料的游离氨基酸测定中,常用水或一定浓度乙醇溶液作为提取剂。精密称取过80目筛原料粉2.5g置三角瓶中,分别加入30倍的水、60%、70%、80%、90%的乙醇,于80℃提取4h,趁热过滤,残渣用热水洗涤,洗液并入滤液中,置冷后,滤液与洗涤液定容至250ml,按3.3项下测定,在570nm处测定其吸光度。
表4不同提取剂及浓度提取总游离氨基酸的结果
由表4和图2可以看出,以60%、70%、80%乙醇为提取溶剂,总游离氨基酸的浸出量要高于以水为提取溶剂,其中,以60%乙醇为提取溶剂,总游离氨基酸的浸出量较大,因此,总游离氨基酸的提取的最适提取剂为乙醇,浓度为60%。
3.2.2提取时间的选择
精密称取过80目筛原料粉2.5g置三角瓶中,加入30倍最适浓度的乙醇,,于80℃提取1.0、2.0、3.0、4.0、5.0h,趁热过滤,残渣用热水洗涤,洗液并入滤液中,置冷后,滤液与洗涤液定容至250ml,按3.3项下测定,在570nm处测定其吸光度。
表5提取时间对总游离氨基酸浸出量的影响
由表5和图3可知,3h之前,总游离氨基酸的浸出量随着时间的延长开始增加,提取3h总游离氨基酸的浸出量相对较高;3h之后总游离氨基酸的浸出量开始下降,提取5h总游离氨基酸的浸出量有回升的趋势,但仍小于3h。因此,确定提取时间为3h。
3.2.3料液比的选择
精密称取过80目筛原料粉2.5g置三角瓶中,分别加入1:20、1:30、1:40、1:50、1:60最适浓度的乙醇,于80℃提取确定的最适时间,趁热过滤,残渣用热水洗涤,洗液并入滤液中,置冷后,滤液与洗涤液定容至250ml,按
3.3项下测定,在570nm处测定其吸光度。
表6料液比对总游离氨基酸浸出量的影响
由表6和图4可以看出,1:50、1:60的料液比对总游离氨基酸的浸出量最高,考虑节约提取剂和节约成本方面考虑,选择料液比为1:50。
3.2.4提取温度的选择
精密称取过80目筛原料粉2.5g置三角瓶中,加入最适料液比的提取溶剂, 分别于40、50、60、70、80、90℃水浴浸提最适时间,趁热过滤,残渣用热水洗涤,洗液并入滤液中,置冷后,滤液与洗涤液定容至250ml,按3.3项下测定,在570nm处测定其吸光度。
表7提取温度对总游离氨基酸浸出量的影响
由表7和图5可以看出,随着温度的增加,总游离氨基酸的浸出量有下降的趋势,50℃时浸出量较大。因此,提取温度确定为50℃。
3.3正交试验结果与分析
在单因素试验的基础上,选用正交试验设计进行条件的优化,同时对试验结果进行分析,并验证单因素试验中各因素对氨基酸提取率的影响程度,选用因素水平见表。准确称取2.5g原料,,以总游离氨基酸的浸出量为考察指标,进行正交试验,结果见表8和表9。
表8总游离氨基酸提取工艺正交试验因素水平表
表9正交试验结果
表10方差分析结果
F0.05(2,2)=19
根据表9和表10可知,影响总游离氨基酸浸出量的因素中,以提取温度的影响最大,其后依次是乙醇浓度、料液比、提取时间,其中提取温度对提取效果有显著差异,而乙醇浓度、料液比及提取时间都没有显著影响,水平以A2B1C1D3为最佳。考虑A因素、C因素和D因素对结果影响较小,从生产成本方面看,选择A1B1C1D1为提取条件,即提取时间为2.5h、提取温度为45℃、料液比为45倍、乙醇浓度为55%。
3.4验证试验
准确称取原料2.5g,平行3份,按最佳工艺提取,总游离氨基酸的浸出量见表,RSD=0.15%,表明该提取工艺稳定可行。
表11验证试验结果
3.5完全必需氨基酸的分离
3.5.1极性氨基酸与非极性氨基酸的分离
取30ml氯仿倒入洁净的分液漏斗中。提取得到的复合氨基酸溶液浓缩至30ml后,浓缩液调节pH至7.0,将复合氨基酸浓缩液倒入分液漏斗,摇匀后,静置分层。
静置10分钟后开始分层,上层为氯仿浸提的非极性氨基酸,从上边倒出;下层浸提的则为极性氨基酸,从下端放出,并分别用洁净的三角瓶收集。
3.5.2苏氨酸和赖氨酸的分离
将浸提的极性氨基酸溶液调节pH至6.18,摇匀后,静置15分钟,于8000r/min离心15分钟,沉淀即为苏氨酸。分别收集沉淀与上清液,再将上清液的pH调节至9.74,摇匀后,静置15分钟,于8000r/min离心15分钟,沉淀即为赖氨酸,收集沉淀。
3.5.3非极性氨基酸中甘氨酸和丙氨酸的去除
本次实验选用的凝胶是Bio-Gel P-2聚丙烯酰胺凝胶,其分级范围为(相对分子质量)100-1800。可用来分离非极性氨基酸中的甘氨酸(相对分子质量为75)和丙氨酸(相对分子质量为89)与其他的非极性氨基酸(相对分子质量均大于110)。
(1)装柱关闭出口,向柱内加入洗脱液(0.1mol/L pH6.8磷酸缓冲液)约1cm高,将凝胶缓慢地倾入柱中,使之自然沉降,凝胶沉降约1cm高度后打开 出水口,继续加入凝胶,直到凝胶沉积至一定高度即可。
(2)平衡将洗脱液与恒流泵相连,恒流泵出口端与层析柱入口相连,用2~3倍柱床体积的洗脱液平衡,流速为8cm/h。
(3)加样与洗脱将柱中多余的液体放掉,使液面刚好盖过凝胶,关闭出口,将样品沿层析柱管壁小心加入,加完后打开低端出口,使液面降至与凝胶相平时关闭出口,加洗脱液至液层4cm左右,接上恒流泵,开始洗脱(8cm/h)。用部分收集器收集洗脱液。最后流出的即为甘氨酸和丙氨酸。
综上所述,实验最后可得到包括8种必需氨基酸和一种非必需氨基(脯氨酸)在内的高纯度完全必需游离氨基酸溶液。
附图说明
图1是是本发明实施例提供的一种完全必需氨基酸的分离制备方法实验的甘氨酸标准曲线图;
图2是本发明实施例提供的一种完全必需氨基酸的分离制备方法实验的不同提取剂及浓度提取总游离氨基酸的结果图;
图3是本发明实施例提供的一种完全必需氨基酸的分离制备方法实验的提取时间对总游离氨基酸浸出量的影响图;
图4是本发明实施例提供的一种完全必需氨基酸的分离制备方法实验的料液比对总游离氨基酸浸出量的影响图;
图5是本发明实施例提供的一种完全必需氨基酸的分离制备方法实验的提取温度对总游离氨基酸浸出量的影响图。
- 还没有人留言评论。精彩留言会获得点赞!