一类汞离子荧光探针及其制备方法和应用与流程
本发明属于环境分析、生物分析检测的荧光探针技术领域,具体涉及一类高选择性的、能够对样品中汞离子含量进行定量检测的汞离子荧光探针及其制备方法和用。
背景技术:
汞是一种重金属,俗称水银。溶解态的Hg2+具有较高的化学活性,是汞污染物的主要存在形式,在浓度很低时对生物体就具有极强的生理毒性。无机汞通过各种途径进入环境后,通过沉积物中微生物的作用转变为甲基汞,威胁水体生物的生存,造成大量鱼类中毒或者死亡。汞的毒性可以通过食物链的生物富集作用,最终传输到食物链顶端的人类体内,人类无法通过自身代谢作用将汞排出体外,进而引发多种心脑血管疾病和内分泌系统疾病,严重危害人类的身体健康。因此,对生物体和环境中汞的分析检测一直是人们非常关注的问题,建立快速、高效的汞离子检测方法在生命科学、医学和环境保护等领域具有重大意义。
近几十年里,已经报道了多种检测汞离子的方法。例如紫外分光光度法、原子吸收/发射法、生物传感器法、电感耦合等离子体质谱法和电化学法(伏安法和极谱法)等,上述几种传统的检测方法虽然可以完成对不同体系样品的汞含量检测,但它们对仪器的设备要求很高,价格昂贵,并要求有大量的待测样品,而且不允许连续检测,这些方法的自身局限性制约着对各种待测样品特别是生物体内的即时检测与痕量分析。
荧光分析法具有选择性好、灵敏度高、检测限低和消耗样品量少等优点,在汞的痕量检测中发挥着极大的作用,而且荧光分子可以穿透细胞壁,对活细胞和生物体内的金属离子进行显影示踪检测,这是上述传统分析方法所不可代替的。目前,荧光分析法中应用最为广泛的是荧光分子探针。荧光分子探针分为络合型和反应型两种,络合型荧光探针基于非共价键的超分子相互作用,主要是配位键和氢键作用;反应型荧光探针的识别过程不同于络合型,它是探针与检测对象发生化学反应,生成不同结构的光活性化合物,使荧光分子探针的光谱性质(主要是颜色)发生变化,从而实现光学传感。反应型荧光分子探针利用选择反应的优势识别特定物质,具有专一性和不可逆性等优点,并且可以长久保留检测信号,近年来受到越来越多的关注。基于罗丹明类、香豆素类、花青染料和荧光素等荧光母体的反应型荧光分子探针在重金属离子的检测方面发展迅速。
罗丹明B具有光稳定性好和荧光量子产率高等优越的光物理性能使其成为一类较好的荧光探针母体,具有很高的实际应用价值,其光性能受外界条件如光照、温度和取代基的影响较大,在氢离子或某些金属阳离子作用下可以开环,荧光显著增强且伴随着颜色的变化。常见报道的罗丹明B类荧光探针种类很多,大致分为络合-螺环开环型以及开环-环化反应型。其中基于罗丹明螺环“off-on”机理的反应型金属离子荧光探针是近年来研究的重点与热点,由于Hg2+具有亲硫性,它可以促进硫羰基化合物发生脱硫反应,生成相应的羰基化合物,例如Hg2+诱导硫脲类衍生物脱硫化生成胍。设计含硫羰基结构的罗丹明类荧光分子探针可以很好地识别Hg2+,反应后的Hg2+以HgS沉淀的形式存在。研究机理表明,罗丹明特定的螺环结构中由于含有N、O和S等原子,使Hg2+首先与罗丹明结合,并促进螺环打开形成第一个平衡,进一步生成具有强荧光性质的罗丹明类衍生物。利用反应前后荧光物质光物理性质不同,可实现对Hg2+的检测。另外,选择性实验证明这类反应型荧光探针对Hg2+表现出高度专一性,在化学和生物检测方面具有重要意义。
技术实现要素:
本发明解决的技术问题是提供了一类汞离子荧光探针及其制备方法和用,该汞离子荧光探针采用将罗丹明B底环酯基胺解重新成环的方法,合成具有特异性响应的汞离子荧光探针分子,用于汞离子的选择性荧光快速检测。
本发明为解决上述技术问题采用如下技术方案,一类汞离子荧光探针,其特征在于是罗丹明B的底环修饰衍生物,结构式为,其中取代基F位于苯环上的邻位、间位或对位。
本发明所述的汞离子荧光探针的制备方法,其特征在于具体步骤:
步骤(1),在反应容器中将罗丹明B溶于乙醇中,再加入水合肼水溶液,于85℃的油浴中回流反应,TLC监控原料反应完全后加入蒸馏水淬灭反应,用乙酸乙酯萃取反应体系,收集有机相后减压蒸馏得到罗丹明B酰肼化合物;
步骤(2),在反应容器中加入氟基取代苯异硫氰酸酯类化合物和步骤(1)得到的罗丹明B酰肼化合物,再加入异丙醇,于85 ℃的油浴中搅拌回流反应,TLC监控原料反应完全后降至室温,减压蒸馏除去溶剂并加入中性氧化铝对其干法拌样,使用中性氧化铝作为固定相进行柱层析分离纯化得到氟基取代荧光探针。
进一步优选,步骤(1)中所述水合肼水溶液的质量浓度为80%,水合肼与罗丹明B的摩尔比为20:3。
进一步优选,步骤(2)中所述氟基取代苯异硫氰酸酯类化合物与罗丹明B酰肼化合物的摩尔比为1.5:1。
本发明所述的汞离子荧光探针在检测水环境体系、药物或生物细胞体系中汞离子含量中的应用,其特征在于具体过程为:(1)将汞离子荧光探针溶于二甲基亚砜溶液中,配成摩尔浓度为0.1 mmol/L的汞离子荧光探针标准溶液,用N-(2-羟乙基)哌嗪-N'-2-乙烷磺酸的缓冲溶液配制不同浓度的汞离子储备液,取30 μL汞离子荧光探针标准溶液分别与3 mL不同浓度的汞离子储备液混合,室温下静置10 min,分别测混合液在波长589 nm处的荧光发射强度,以汞离子的浓度为横坐标,以荧光强度为纵坐标绘制标准曲线,或再拟合得到标准直线方程;(2)将摩尔浓度为0.1 mmol/L的汞离子荧光探针的二甲基亚砜溶液30 μL加入到3 mL待测样品溶液中,室温下静置10 min,测定被检测溶液在波长589 nm处的荧光发射强度,再与标准曲线对比或代入标准直线方程计算,得到待测样品溶液中汞离子的浓度。
本发明与现有技术相比具有以下有益效果:本发明提供的罗丹明B的底环修饰衍生物,合成步骤简单,反应时间短,易于提纯且收率较高,该化合物是汞离子的荧光增强型探针,对汞离子具有高度专一性,可在生理环境条件下工作,具有应用于生物荧光成像的前景。
附图说明
图1是pH对荧光探针RFS和RFS+Hg2+荧光光谱的影响曲线;
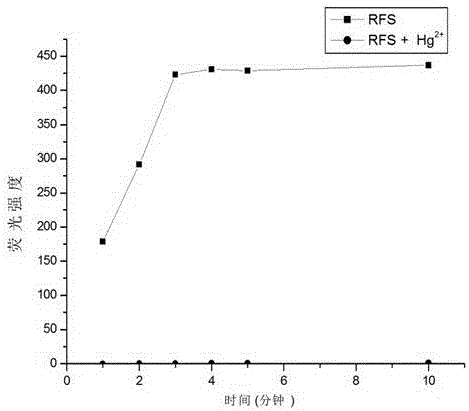
图2是配位时间对荧光探针RFS和RFS+Hg2+荧光光谱的影响曲线;
图3是荧光探针RFS对不同金属离子的选择性识别曲线;
图4是荧光探针RFSP对不同金属离子的选择性识别曲线;
图5是荧光探针RFSM对不同金属离子的选择性识别曲线;
图6是共存离子对荧光探针RFS检测汞离子的影响图;
图7是共存离子对荧光探针RFSP检测汞离子的影响图;
图8是共存离子对荧光探针RFSM检测汞离子的影响图;
图9是荧光探针RFS对汞离子的荧光测试曲线;
图10是荧光探针RFSP对汞离子的荧光测试曲线;
图11是荧光探针RFSM对汞离子的荧光测试曲线;
图12是荧光探针RFS对汞离子络合的工作曲线;
图13是荧光探针RFSP对汞离子络合的工作曲线;
图14是荧光探针RFSM对汞离子络合的工作曲线;
图15是荧光探针RFS对汞离子在细胞体内进行的荧光成像实验,其中荧光探针RFS的摩尔浓度为5 μM,Hg2+的摩尔浓度为10 μM。
具体实施方式
以下通过实施例对本发明的上述内容做进一步详细说明,但不应该将此理解为本发明上述主题的范围仅限于以下的实施例,凡基于本发明上述内容实现的技术均属于本发明的范围。
实施例1
罗丹明B酰肼化合物的合成
取罗丹明B 1.443 g(3 mmol)移入100 mL的圆底烧瓶内,用50 mL乙醇溶解,然后用移液枪移取水合肼水溶液3 mL(80wt%,20 mmol),此时反应体系呈深酒红色,于85℃的油浴中进行回流反应,薄层色谱检测法(TLC)监测反应进度,展开剂为体积比1:1的石油醚与乙酸乙酯混合溶液,反应6 h后点板发现薄层板上原料点基本消失,比移值在约0.5位置出现罗丹明酰肼产物点,微热后产物点呈玫红色,此时反应体系由深酒红色变为土黄色,加100 mL蒸馏水淬灭反应,用乙酸乙酯萃取体系,收集有机相后减压蒸馏得罗丹明酰肼化合物1.2537 g,收率91%。
实施例2
邻氟基罗丹明探针RFS的合成
取2-氟苯异硫氰酸酯0.1238 g(0.75 mmol)和罗丹明酰肼化合物0.2292 g(0.5 mmol)并转移至25 mL的圆底烧瓶内,然后加入5 mL干燥的异丙醇,于85℃的油浴中磁力搅拌回流反应,反应5 min后对其进行TLC监测反应,展开剂为体积比为1:1的石油醚与乙酸乙酯混合溶液,10 h后原料点消失,停止反应,体系降至室温后,减压蒸馏除去溶剂并加入中性氧化铝对其干法拌样,使用中性氧化铝作为固定相进行柱层析(石油醚:乙酸乙酯=10:2,v/v)分离纯化,产品为白色蓬松状粉末邻氟基罗丹明探针RFS(收率82%)。
实施例3
间氟基罗丹明探针RFSM的合成
取3-氟苯异硫氰酸酯0.1238 g(0.75 mmol)和罗丹明酰肼化合物0.2292 g(0.5 mmol)并转移至25 mL的圆底烧瓶内,然后加入5 mL干燥的异丙醇,于85℃的油浴中磁力搅拌回流反应,反应5 min后对其进行TLC监测反应,展开剂为体积比为1:1的石油醚与乙酸乙酯混合溶液,10 h后原料点消失,停止反应,体系降至室温后,减压蒸馏除去溶剂并加入中性氧化铝对其干法拌样,使用中性氧化铝作为固定相进行柱层析(石油醚:乙酸乙酯=10:2,v/v)分离纯化,产品为白色蓬松状粉末间氟基罗丹明探针RFSM(收率74%)。
实施例4
对氟基罗丹明探针RFSP的合成
取4-氟苯异硫氰酸酯0.1238 g(0.75 mmol)和罗丹明酰肼化合物0.2292 g(0.5 mmol)并转移至25 mL的圆底烧瓶内,然后加入5 mL干燥的异丙醇,于85℃的油浴中磁力搅拌回流反应,反应5 min后对其进行TLC监测反应,展开剂为体积比为1:1的石油醚与乙酸乙酯混合溶液,10 h后原料点消失,停止反应,体系降至室温后,减压蒸馏除去溶剂并加入中性氧化铝对其干法拌样,使用中性氧化铝作为固定相进行柱层析(石油醚:乙酸乙酯=10:2,v/v)分离纯化,产品为白色蓬松状粉末对氟基罗丹明探针RFSP(收率80%)。
实施例5
1、荧光光谱测定条件
激发狭缝宽度5.0 nm,发射狭缝宽度3.0 nm,激发波长λex为566 nm或568 nm,响应时间1 s,波长范围500-700 nm,灵敏度为medium,样品池选择1 cm×1 cm×4 cm的四通石英比色皿。
准确称取0.0122 g邻氟基罗丹明探针RFS、间氟基罗丹明探针RFSM和对氟基罗丹明探针RFSP,分别用二甲亚砜溶液(DMSO)溶解于10 mL容量瓶中并定容,摩尔浓度均为2×10-3 mol/L,取0.5 mL母液于另一支10 mL容量瓶中用DMSO定容,此时荧光探针的摩尔浓度均为1×10-4 mol/L,再用HEPES缓冲溶液配制1×10-3 mol/L的多种金属盐溶液,同样稀释至1×10-4 mol/L。
其中荧光探针RFS和荧光探针RFSP的测试条件为Ex=5 nm,Em=3 nm,荧光探针RFSM的测试条件为Ex=3 nm,Em=3 nm,测试条件的区别表明间位氟基取代的荧光探针RFSM相对荧光强度较弱。
2、荧光测试条件的筛选
(1)pH对荧光探针RFS和RFS+Hg2+荧光光谱的影响
通常情况下,罗丹明衍生物的内酰胺环在酸性介质中是开环的,有很强的荧光发射,为了将荧光探针RFS更好地应用于有机体或者环境等复杂体系中,配制不同的缓冲体系如HAc-NaAc、HEPES(N-(2-羟乙基)哌嗪-N'-2-乙烷磺酸)、NaHCO3-Na2CO3等调整不同的pH值,测定了不同pH值对荧光探针RFS以及RFS+Hg2+在其最大发射波长(589 nm)处荧光强度的影响,如图1所示,在pH为7左右的范围内,荧光探针RFS的荧光强度几乎不变,主要以内酰胺的结构稳定存在。在pH为6-8的范围内,RFS+Hg2+的荧光强度几乎不变。因此,在pH为6-8的范围内,荧光探针RFS对Hg2+的检测不受pH的影响,有利于其在活细胞及生物体内Hg2+的检测。所以实验选择生理条件的HEPES缓冲体系(pH=7.20)作为测定介质的缓冲溶液。
(2)配位时间和稳定性
实验结果表明,图2空白体系的荧光强度随时间缓慢增加,但加入汞离子以后,其荧光强度迅速增强,在3 min后即趋于稳定,5-10 min时荧光强度基本不变。故选择在试剂混合作用10 min后进行测定。
3、苯基异硫氰酸酯上氟取代基位置不同对汞离子的选择性识别的影响
(1)荧光探针对不同金属离子的选择性识别
为了测定三种荧光探针对不同金属离子的识别性能,分别选择过渡金属(Fe3+、Cr3+、Co2+、Mn2+、Ni2+、Fe2+、Zn2+、Cu2+、Hg2+、Cd2+、Ag+、)、碱金属(K+、Na+)和碱土金属(Ba2+、Ca2+、Mg2+)和Hg2+为识别对象。如图3-5所示,除细胞内摩尔浓度较大的Na+、Mg2+、Ca2+的摩尔浓度为20 μM外,其余离子及荧光探针的浓度均为1 μM。结果显示,在分别加入空白荧光探针溶液以及K+、Na+、Ag+、Mg2+、Ca2+、Ba2+、Cd2+、Co2+、Cr3+、Cu2+、Mn2+、Ni2+、Zn2+、Fe2+、Fe3+离子时,体系在最大发射波长589 nm处几乎没有荧光,溶液无色,说明此时荧光探针主要以螺环的形式存在;而在加入Hg2+后,体系在最大发射波长589 nm处荧光明显增强,溶液颜色由无色变为桃红色,说明Hg2+诱导荧光探针中电子发生转移从而导致螺环结构打开。实验结果表明,三种荧光探针RFS、RFSM和RFSP均对Hg2+具有较高的专一识别能力。
(2)共存离子对三种荧光探针检测汞离子的影响
进一步考察了其它金属离子和Hg2+共存时对Hg2+测定的干扰,令三种荧光探针的摩尔浓度为10 μM,除Ca2+、Mg2+、Na+的摩尔浓度为0.50 mM(50 equiv)外,其它金属离子的摩尔浓度均为0.1 mM(10 equiv),如图6-8所示,黑色柱状图表示在荧光探针分子与不同的竞争离子分别共存情况下的荧光强度,灰色柱状图表示分别加入1 equiv Hg2+后各体系内的荧光强度。从图表数据可以看出,在共存离子(尤其是Ca2+、Mg2+、Na+的浓度为Hg2+浓度的50倍)存在的条件下,三种荧光探针RFS、RFSM和RFSP对其它金属离子均表现出较强的抗干扰能力。因此,荧光探针RFS、RFSM和RFSP都是对Hg2+有较高选择性的荧光增强型探针。
(3)三种荧光探针检测限的测定
由公式LOD=3σ/K(σ为标准方差,n=6)算出对应的检测限依次为0.6x10-7 mol/L、2.7x10-7 mol/L和1.2x10-7mol/L,由此可知,苯环上取代基位置为间位时荧光探针对汞离子识别的灵敏度较差,苯环上取代基为邻、对位取代基时荧光探针对汞离子识别的灵敏度较好,其中邻位取代基灵敏度要略高于对位。
4、荧光探针与Hg2+的作用机理探讨
室温下将荧光探针RFS(0.2 mmol)与HgCl2(0.2 mmol)在甲醇中搅拌20 min,有黑色不溶固体析出,抽滤后旋干溶剂得到化合物RFS与Hg2+反应后产物RFR, 1H NMR (400 MHz, CDCl3) δ 9.55 (s, 1H), 8.26 (d, J = 7.8 Hz, 1H), 7.84 (t, J = 7.2 Hz, 1H), 7.70 (t, J = 7.7 Hz, 1H), 7.63 (t, J = 7.5 Hz, 1H), 7.25 (d, J = 7.4 Hz, 1H), 7.08 (d, J = 9.4 Hz, 2H), 6.97 (d, J = 7.8 Hz, 1H), 6.93 (d, J = 5.5 Hz, 1H), 6.89 (d, J = 7.3 Hz, 1H), 6.77 (d, J = 9.4 Hz, 2H), 6.68 (s, 2H), 3.53 (q, J = 6.9 Hz, 8H), 1.24 (t, J = 6.9 Hz, 12H)。
5、活细胞内荧光探针RFS检测Hg 2+
为了研究探针RFS在癌细胞内的检测Hg 2+的能力,首先将Hela细胞用磷酸盐缓冲溶液(DPBS)润洗后用5 μM 的RFS(含有1% DMSO的HEPES缓冲溶液)在37 ℃下培养30 分钟,再用PBS缓冲溶液清洗3次,最后再将Hela细胞分别用10 μM 的HgCl2的HEPES缓冲溶液37 ℃下培养30 分钟,再次用PBS缓冲溶液清洗3次。此时用Olympus FV 1000激光共焦显微镜观察共焦荧光成像。
以上实施例描述了本发明的基本原理、主要特征及优点,本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明原理的范围下,本发明还会有各种变化和改进,这些变化和改进均落入本发明保护的范围内。
- 还没有人留言评论。精彩留言会获得点赞!