一种用于惰性表面固载的季铵盐型卤胺抗菌前体、制备及应用方法与流程
本发明属于功能分子合成、功能材料制备领域,具体涉及一种可用于惰性表面固载的季铵型卤胺抗菌前体的制备及应用方法。
背景技术:
卤胺类抗菌剂是近年来研究较多的一种有机类抗菌剂,由于具有抗菌活性高、活性可再生、抗菌作用广谱等优点而受到广泛的关注并在医疗卫生、日用品等各个领域被广泛应用。卤胺前体活化后分子中N-H转化为N-Cl,在水溶液中溶解度与分散性能降低,尤其当卤胺分子大量固载于材料表面之后,材料亲水性受到影响。有研究(Adv.Healthcare Mater.2012,1,609-620)表明将季铵盐基团引入卤胺抗菌剂分子中显著提高了其水溶性,同时大大提高了卤胺结构的杀菌效率。研究推测这是由于季铵盐基团与呈负电性的细菌膜之间的静电作用促进了细菌与抗菌分子之间的接触,进而显著提高了卤胺基团的杀菌效率。
然而,一方面有机小分子抗菌剂的大量使用往往会引起二次污染,且难以重复回收使用,所以非溶出型抗菌材料受到人们越来越多的重视;另一方面,医用材料表面的细菌污染是导致细菌感染及交叉感染的主要途径之一,有些致病细菌甚至可以在材料表面存活数月之久。因此,将卤胺抗菌分子固载到高分子材料表面制备非溶出型抗菌材料可以重复利用材料表面卤胺分子,近年来成为医用材料领域的研究热点。目前卤胺抗菌前体在惰性材料表面的共价固载方法主要有亲电/亲核反应以及自由基引发的表面接枝聚合反应。
(1)通过与材料表面活性基团进行亲电/亲核反应可实现卤胺抗菌剂的固载。Sun等人(Ind.Eng.Chem.Res.1994,33,168-170)通过傅克反应在商品化聚苯乙烯材料表面引入乙酰基团,之后利用“Bucherer-Berg's”反应在该位置生成海因基团,成功制备了卤胺改性高分子抗菌剂。Lin等人(J.Appl.Polym.Sci.2001,81,943-947)利用甲醛对尼龙材料进行预处理后,以羟基作为偶联基团将乙内酰脲、恶唑烷酮和咪唑啉酮等卤胺前体固载到改性的尼龙材料表面上,通过该方法制备的抗菌材料具有较高的稳定性和抗菌再生性能。但该方法需要先利用甲醛及强碱对材料进行预处理再进行卤胺前体的固载,工艺相对较为复杂且易造成环境污染。Li等人(Adv.Healthcare Mater.2012,1,609-620)通过“click”反应将5,5-二甲基海因分子接枝到聚对苯甲酸乙二醇酯膜表面,然而该方法需要预先在材料表面引入炔基基团,并且反应当中用到的铜离子催化剂对生物体尤其是水生生物具有一定的生物毒性。
(2)首先制备可聚合单体,之后在材料表面进行表面接枝聚合反应,可将卤胺或卤胺前体基团引入到材料表面形成具有抗菌活性的功能材料。如Sun等人(J.Appl.Polym.Sci.2001,81,617–624)制备了以3-烯丙基-5,5-二甲基海因为代表的烯丙基可聚合单体衍生物,经表面接枝聚合后可将DMH固载到聚对苯甲酸乙二醇酯(PET)和聚丙烯(PP)等惰性材料表面。然而表面接枝聚合反应比较复杂,接枝效率及接枝物形态易受单体及引发剂的种类、浓度等影响,并且丙烯基团存在自阻聚的问题,往往需要与其他单体共聚才能有效完成表面接枝聚合反应。全氟苯基叠氮类化合物由于具有制备简单、稳定性好等优点而成为近年来应用较多的偶联剂之一,该化合物中苯基叠氮基团在254nm波长激发下能够产生高活性的单线态氮卡宾并在材料表面进行C=C双键加成或C-H、N-H键插入反应,能够实现目标分子与惰性材料表面之间的键合偶联。Yan M等人(J.Am.Chem.Soc.1993,115,814-816)以PFPA作为偶联基团在材料表面成功接枝NHS(N-羟基琥珀酰亚胺),之后通过NHS与氨基反应将荧光蛋白固载到具有一定图案的聚合物聚苯乙烯膜上。Pastine等人(J.Am.Chem.Soc.2008,130,4238-4239)将亲水性羟丙基链和疏水性氟代烷基链分别固载到碳纳米管表面极大地改变了碳纳米管的亲水/疏水性能。因此本专利申请设计利用全氟苯基叠氮基团作为偶联基团实现季铵盐型卤胺前体在惰性材料表面的固载。
技术实现要素:
本发明针对传统卤胺抗菌剂在惰性材料表面较难有效实现共价固载的问题,提出了一种可用于惰性表面固载的季铵盐型卤胺抗菌前体制备及应用方法,该卤胺抗菌剂前体能够实现在惰性材料表面的共价键固载并能赋予修饰后材料优异的抗菌活性。
本发明的技术方案:
一种可用于惰性表面固载的季铵盐型卤胺抗菌前体,其结构如下:
其中,n是0、2或4。
一种可用于惰性表面固载的季铵盐型卤胺抗菌前体的制备与应用方法,步骤如下:
(1)将N,N-二甲氨基氯丙烷盐酸盐与5,5-二甲基海因溶解在溶剂A中,再加入KOH,回流反应4~16小时,除溶剂后硅胶柱层析分离,得到3-(N,N-二甲氨基氯丙烷基)-5,5-二甲基海因;其中,KOH、N,N-二甲氨基氯丙烷盐酸盐与5,5-二甲基海因的摩尔比为1:1~8:2~10,5,5-二甲基海因在溶剂A中的浓度w/v为2~10%;所述的溶剂A选自丙酮或无水乙醇。
(2)将五氟苯甲酸与溴乙醇、4-氯-1-丁醇、6-氯-1-己醇中的三者中的一个溶解在溶剂B中,在催化剂条件下反应6~24小时,硅胶柱层析分离,得到五氟苯甲酸氯代烷烃酯或五氟苯甲酸溴代烷烃酯;其中,五氟苯甲酸与溴乙醇、4-氯-1-丁醇或6-氯-1-己醇的摩尔比为1:1~5,五氟苯甲酸在溶剂B中的浓度w/v为2~20%;所述的催化剂为浓硫酸;所述的溶剂B选自四氯化碳或二氯甲烷。
(3)将五氟苯甲酸氯丁酯或五氟苯甲酸氯己酯中的一种与碘化钠溶解在溶剂C中,回流反应6~24小时,除溶剂后硅胶柱层析分离,得五氟苯甲酸碘丁酯或五氟苯甲酸碘己酯;其中五氟苯甲酸氯丁酯或五氟苯甲酸氯己酯与碘化钠的摩尔比为1:1~5,五氟苯甲酸氯丁酯或五氟苯甲酸氯己酯在溶剂C中的浓度w/v为2~20%;所述的溶剂C为丙酮或丁酮。
(4)五氟苯甲酸溴乙醇酯、五氟苯甲酸碘丁酯、五氟苯甲酸碘己酯中一种与3-(N,N-二甲氨基氯丙烷基)-5,5-二甲基海因以摩尔比1~5:1溶解在乙腈中,回流反应6~24小时,除溶剂后硅胶柱层析分离,得到相应的季铵盐溴盐或季铵盐碘盐;3-(N,N-二甲氨基氯丙烷基)-5,5-二甲基海因在乙腈中的浓度w/v为2~20%。
(5)将步骤(4)中得到的季铵盐溴盐或季铵盐碘盐配制成浓度w/v为60~80%的水溶液,然后缓慢通过氯型阴离子交换树脂,除水后得到季铵盐型卤胺前体氯盐。
(6)将步骤(5)中得到的季铵盐型卤胺前体氯盐与叠氮化钠溶解在体积比为3:1的丙酮与水的混合溶剂中,回流反应6~24小时,除溶剂后硅胶柱层析分离,得可固载的季铵盐型卤胺抗菌前体;其中,季铵盐型卤胺前体氯盐与叠氮化钠的摩尔比为1:1~1.3,季铵盐型卤胺前体氯盐在混合溶剂中的浓度w/v为10~20%。
(7)将步骤(6)中得到的可固载的季铵盐型卤胺前体配制成浓度为1~7mg/mL的可固载型含季铵盐卤胺前体的甲醇溶液,然后滴涂在膜上,在室温条件下避光放置自然晾干;随后将膜置于254nm紫外灯下光照1~10min,膜表面照射的紫外光总量为0.202~2.02J/cm2;最后用95%乙醇溶液将表面未固载的小分子冲洗干净,自然晾干。
(8)将步骤(7)中修饰的聚氨酯膜在的商品化漂白水溶液中活化;其中漂白水溶液的浓度为1-15%,活化时间为0.5-3h。
所述的膜选自聚氨酯、聚对苯二甲酸乙二醇酯、聚苯乙烯和聚丙烯膜材料。
本发明的有益效果:
(1)本发明提供的季铵盐型卤胺前体能够提高固载后的聚氨酯膜材料的抗菌活性与亲水性。
(2)全氟苯基叠氮基团作为偶联基团,能够在254nm波长下实现卤胺前体在多种惰性材料表面的固载偶联,对材料表面的活性基团没有要求。
(3)制备工艺简单,原料易得,能够在多种材料表面实现功能改性。
附图说明
图1是发明实施例1技术实施方案制备的可固载的季铵盐型卤胺前体的核磁共振氢谱。
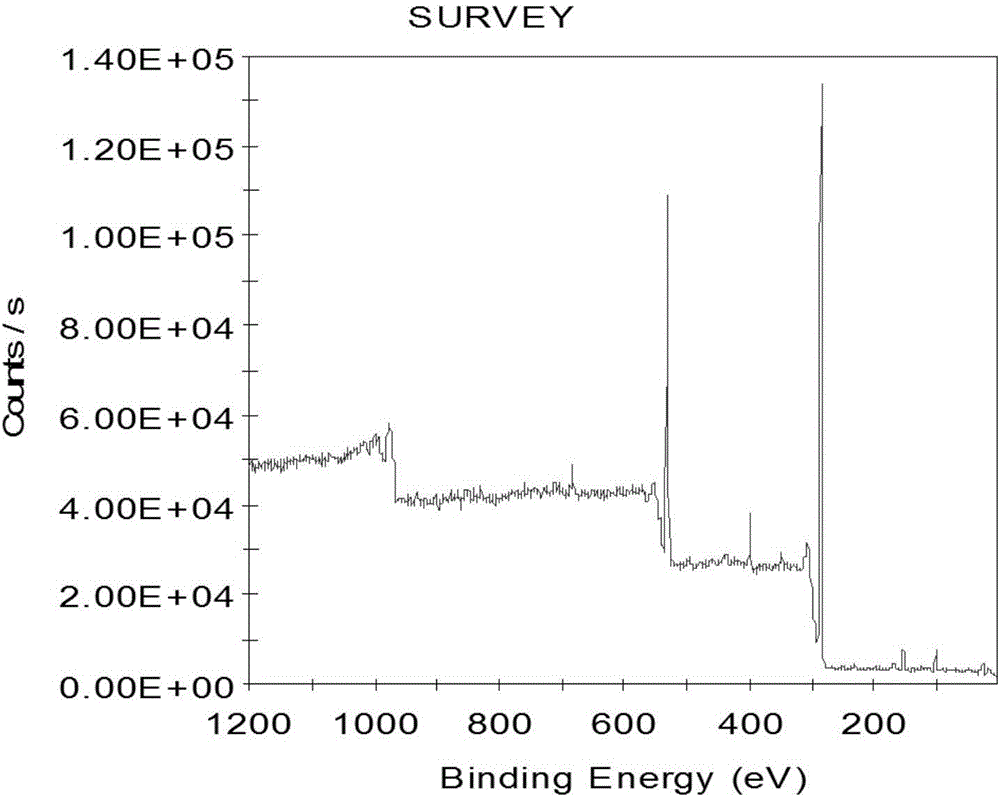
图2是发明实施例1技术实施方案制备的可固载的季铵盐型卤胺前体改性后聚氨酯膜的XPS表征。
图3是发明实施例1技术实施方案制备的卤胺前体所修饰聚氨酯膜的接触角测试结果;其中(a)实施案例1中卤胺前体修饰的聚氨酯膜;(b)未处理的的聚氨酯膜。
具体实施方式
以下结合附图和技术方案,进一步说明本发明的具体实施方式。
实施例1:
将5,5二甲基海因(5.12g,40mmol)、KOH(6.73g,120mmol)与N,N-二甲基氯丙胺盐酸盐(9.42g,80mmol)溶解在50mL无水乙醇中,回流反应24h。反应结束后过滤除去盐,浓缩之后硅胶柱层析分离,得到黄色油状液体产物3-(N,N-二甲氨基氯丙烷基)-5,5-二甲基海因(3.45g,41.6%)。
将五氟苯甲酸(2.12g,10mmol)与溴乙醇(1.87g,0.74mL,15mmol)溶解在100mL二氯甲烷中,然后加入二环己基碳二亚胺(2.06g,10mmol)与4-二甲氨基吡啶(0.05g,0.41mol)催化反应进行,室温下反应20h后过滤除去固体杂质,浓缩后硅胶柱层析分离,以乙酸乙酯/石油醚(v:v=1:9)为洗脱剂,得到五氟苯甲酸溴乙醇酯(2.65g,83.1%)。
将五氟苯甲酸溴乙醇酯(1.75g,5.5mmol)与3-(N,N-二甲氨基氯丙烷基)-5,5-二甲基海因(1.07g,5mmol)溶解在30mL乙腈中,反应回流24h,浓缩后硅胶柱层析分离,以甲醇/二氯甲烷(v:v=1:9)为洗脱剂得到季铵盐卤胺溴盐(2.34g,88.0%)。
将季铵盐卤胺溴盐溶解于约2mL的去离子水中,缓慢通过氯型阴离子交换树脂。除去水,得到季铵盐卤胺氯盐。
将季铵盐卤胺氯盐(2.34g,4.47mmol)与叠氮化钠(DDN)(0.31g,4.71mmol)溶于30mL丙酮与5mL水中,回流反应24h,浓缩后硅胶柱层析分离,以甲醇/二氯甲烷(v:v=3:7)为洗脱剂,得到可固载型季铵盐型卤胺前体(2.42g,91.4%)。
参照附图1,它是本实施案例技术方案制备的季铵盐型卤胺抗菌剂前体(n=0)的核磁共振氢谱。
1H NMR(500MHz,Deuterium Oxide)δ4.76(dd,J=5.8,2.8Hz,1H),3.83-3.76(m,1H),3.55-3.44(m,1H),3.44-3.32(m,1H),3.26(s,2H),3.13(s,2H),2.08(dq,J=13.8,6.9Hz,1H),1.36-1.27(m,3H).
实施例2:
将五氟苯甲酸(4.24g,20mmol)与4-氯-1-丁醇(3.26g,0.03mol)溶解在20mL CCl4中,加入6滴浓硫酸,回流反应20小时。反应结束后依次用20mL 5%NaHCO3溶液、20mL饱和NaCl溶液洗涤,加入无水MgSO4干燥。溶液浓缩硅胶柱层析分离,以乙酸乙酯/石油醚(v:v=1:9)为洗脱剂,得五氟苯甲酸氯丁醇酯(4.31g,71.2%)。
将五氟苯甲酸-4-氯-1-丁酯(4.31g,14mmol)与NaI(6.30g,42mmol)溶解在60mL丙酮中,反应回流过夜。过滤除去NaCl固体,柱层析分离,以乙酸乙酯/石油醚(v:v=1:9)为洗脱剂,得五氟苯甲酸碘丁醇酯(5.14g,93.2%)。
将五氟苯甲酸碘丁醇酯(1.28g,3.25mmol)与3-(N,N-二甲氨基氯丙烷基)-5,5-二甲基海因(0.46g,2.16mmol)溶解在30mL乙腈中,反应回流24h,浓缩后硅胶柱层析分离,以甲醇/二氯甲烷(v:v=1:9)为洗脱剂,得到季铵盐卤胺前体碘盐(0.99g,95.3%)。
将季铵盐卤胺前体碘盐溶解于约2mL的去离子水中,缓慢通过氯型阴离子交换树脂。除去水,得到季铵盐卤胺前体氯盐。
将季铵盐卤胺前体氯盐(0.99g,1.76mmol)与叠氮化钠(DDN)(0.12g,1.87mmol)溶于15mL丙酮与5mL水中,回流反应12h,除掉大部分丙酮之后加入水,用CH2Cl2萃取三次之后将溶液用无水MgSO4干燥,除去溶剂,得可固载型季铵盐型卤胺前体(1.93g,95.2%)。
1H NMR(D2O,500MHz,δ)4.38(t,J=5.6Hz,2H),3.50(t,J=6.6Hz,2H),3.34-3.26(m,4H),3.03(s,6H),2.04-2.01(m,2H),1.84-1.79(m,4H),1.32(s,6H).13C NMR(126MHz,CDCl3)δ180.6,158.61,157.0,146.67,144.52,142.45,138.66,136.72,108.41,67.36,60.74,59.12,50.85,24.54,23.36,21.71,21,17.
实施例3:将五氟苯甲酸(4.24g,20mmol)与6-氯-1-己醇(4.10g,30mmol)溶解在20mL CCl4中,加入6滴浓硫酸,反应回流过夜。反应结束后依次用20mL 5%NaHCO3溶液、20mL饱和NaCl溶液洗涤,加入无水MgSO4干燥。溶液浓缩硅胶柱层析分离,以乙酸乙酯/石油醚(v:v=1:9)为洗脱剂,得五氟苯甲酸氯己醇酯(5.97g,90.3%)。
将五氟苯甲酸-6-氯己酯(5.97g,18mmol)与NaI(8.09g,54mmol)溶解在60mL丙酮中,反应回流过夜。过滤除去NaCl固体,柱层析分离,以乙酸乙酯/石油醚(v:v=1:9)为洗脱剂,得到五氟苯甲酸碘己醇酯(7.41g,97.5%)。
将五氟苯甲酸碘己醇酯(2.25g,5.33mmol)与3-(N,N-二甲氨基氯丙烷基)-5,5-二甲基海因(0.70g,3.29mmol)溶解在30mL乙腈中,反应回流24h,浓缩后硅胶柱层析分离,以甲醇/二氯甲烷(v:v=1:9)为洗脱剂,得季铵盐卤胺前体碘盐(2.01g,96.1%)。
将季铵盐卤胺前体碘盐溶解于约2mL的去离子水中,缓慢通过氯型阴离子交换树脂。除去水,得到季铵盐卤胺前体氯盐。
将季铵盐卤胺前体氯盐(1.84g,3.6mmol)与叠氮化钠(DDN)(0.26g,4.0mmol)溶于15mL丙酮与5mL水中,回流反应12h,除掉大部分丙酮之后加入水,用CH2Cl2萃取三次之后将溶液用无水MgSO4干燥,除去溶剂,得可固载型季铵盐型卤胺前体(1.80g,94.2%)。
1H NMR(500MHz,Deuterium Oxide)δ4.34(t,J=6.3Hz,1H),3.50(td,J=6.8,3.2Hz,1H),3.26(s,7H),2.99(s,3H),2.01(s,1H),1.75–1.61(m,2H),1.41(td,J=14.0,6.7Hz,1H),1.35(d,J=6.9Hz,1H),1.32(s,3H).13C NMR(126MHz,Deuterium Oxide)δ180.6,158.61,157.0,146.67,144.52,142.45,138.66,136.72,108.41,66.12,63.39,61.05,59.12,50.79,35.35,24.52,23.36,21.22,18.92.
实施例4:
抗菌剂前体在聚氨酯膜上的固载
(1)将聚氨酯膜用水与乙醇分别洗涤三次,之后室温条件下晾干。
(2)配制7mg/mL的可固载型含季铵盐卤胺前体溶液,然后滴涂在聚氨酯膜上,然后在室温条件下避光放置自然晾干。将膜置于254nm紫外灯下光照10min,膜表面照射的紫外光总量为2.02J/cm2。
(3)用95%乙醇溶液将表面未固载的小分子冲洗干净,自然晾干。
实施例5:
改性聚氨酯膜的活化
用氯浓度为5%的家用漂白水配制体积比为1:10的漂白水溶液,并调节其pH至7。将季铵盐型卤胺前体固载后的聚氨酯膜置于次氯酸钠溶液之中,持续振荡120min。将氯化后的聚氨酯膜样品取出并用去离子水洗涤3次,然后放置在空气中自然晾干,之后进行表征并测定其抗菌活性。
实施例6:
改性聚氨酯膜的抗菌活性测定
以大肠杆菌(ATCC 25922)与金黄色葡萄球菌(ATCC 25923)为被测试菌种,利用“Sandwich test”方法对改性后的PU膜进行抗菌性能测试。将被测试细菌菌种加入LB培养基中培养24h。将菌液离心分离后得到被测试细菌,以PBS溶液配制成浓度约为106-107CFU(Colony-Forming Unit,菌落形成单位)的菌液。待测试样品与空白对照样品裁剪成3cm×3cm大小自然晾干保存待用。
将待测样品放在玻璃板上,滴加25μL的菌液到样品之上,之后以“Sandwich”形态覆盖一块同样的测试样品,在样品之上放置玻璃作为重物保证样品与菌液充分接触。接触作用15min后,将被测试样品与整体放入10mL 1.0%硫代硫酸钠溶液中充分振荡。硫代硫酸钠中和活性氯,将杀菌过程终止。利用平板计数法测定细菌浓度取出100μL进行逐级稀释,然后取出100μL菌液涂覆于固体LB培养基上,将LB培养基置于37℃环境下培养24h后通过数菌落的个数来计算存活的细菌数量。以未处理的聚氨酯膜作为空白对照,进行同样的操作。样品的抗菌活性以如下公式(1)进行计算:
细菌减少百分数(%)=(A-B)/A×100
Log减少值=log A-log B;如果B=0则log B为0 (1)
其中,A为空白对照样品中洗脱的菌液浓度(CFU/mL),B为被测试样品中洗脱的细菌浓度(CFU/mL)。
表1是发明实施例1技术实施方案制备的可固载型季铵盐型卤胺改性聚氨酯膜对大肠杆菌与金黄色葡萄球菌的抗菌活性测试结果。
表1
注:a):大肠杆菌浓度为2.50×106,b):金黄色葡萄球菌浓度为2.75×107。
- 还没有人留言评论。精彩留言会获得点赞!