一种从工业大麻花叶中提取大麻二酚的方法与流程
本发明涉及一种从工业大麻中提取大麻二酚的方法,特别涉及一种从工业大麻花叶中提取大麻二酚的方法。
背景技术:
大麻(学名:Cannabis sativa L.)大麻科、大麻属植物,又名麻、汉麻、火麻、山丝苗、黄麻,具有重要的农用及药用价值。大麻中含有一种毒性成分THC(四氢大麻酚)可使人致幻成瘾,可作毒品,曾在相当长时期内禁种。
由于大麻的经济、药用价值极高,专供工业用途的原料大麻简称为“工业大麻”,其生长期大麻花叶中的四氢大麻酚(THC)含量小于千分之三,不具备提取毒性成分四氢大麻酚的价值或直接作为毒品吸食,可以合法进行规模化种植与工业化开发利用。
目前,人们已从大麻植株中分离出了500余种物质,其中大麻酚类化合物至少有86种。大麻酚类化合物是大麻植株中特有的一类物质,是大麻植物中主要的活性成分,有关它的研究一直是大麻研究的热点。大麻植株中主要的大麻酚类化合物有四氢大麻酚(THC)、大麻酚(CBN)、大麻二酚(CBD)、大麻萜酚(CBG)、大麻环萜酚(CBC)等,其中前三者占大麻酚类化合物的90%以上。
近年来,通过对大麻活性成分的研究发现,大麻二酚(cannabidiol)不具有神经毒性,药用价值明显。相关的药理研究表明,其能阻碍四氢大麻酚对人体神经系统的影响,并具有抗痉挛、抗风湿性关节炎、抗焦虑等药理活性,具有巨大产业开发价值。
目前,公开信息中有一些关于从工业大麻中提取大麻二酚的方法的报道,其中与本发明最为接近的现有技术为:发明专利“从工业大麻中提取二氢大麻酚(CBD)工艺”(专利申请号:201410052776.8)。
通过对比研究,现有技术中所提及的从工业大麻中提取大麻二酚的方法,主要存在以下问题:
1)因原植物中大麻酚类成分复杂,极性相似成分较多,采用传统方法提取、精制后,最终产品中大麻二酚纯度不高。
2)提取纯化后,仍可检出精神毒性成分四氢大麻酚,产品安全性不能得到保证,产品流通受限,影响工业化生产和应用。
3)因大麻二酚在有机溶剂中的溶解度高于在乙醇中,故,为了提高大麻二酚的产率,行业中通常在提取、萃取、纯化等工艺步骤中采用石油醚、正己烷、二氯甲烷等有毒有机溶剂。但此类有机溶剂的使用会对环境产生危害,而且终产品中溶剂残留不能除尽,对产品安全性也有影响。
因此,目前亟需提供一种制备高纯度且无四氢大麻酚的大麻二酚的方法,并且无不良有机溶剂残留,该制备方法还应满足节能环保,经济适用的产业化发展需求。
技术实现要素:
本发明旨在提供一种从工业大麻花叶中提取大麻二酚的方法,以解决现有技术中提取大麻二酚纯度不高、精神毒性成分四氢大麻酚残留的问题。
为了实现上述目的,本发明提供了一种从工业大麻花叶中提取大麻二酚的方法。该方法包括以下步骤:1)将工业大麻的花叶粉碎、烘干,得到药材粉末;2)将药材粉末采用30-100v%的乙醇提取,得到提取液;3)将提取液浓缩,得到浸膏;4)将浸膏进行水沉,去除杂质,得到水沉液;5)将水沉液离心,在离心获得的沉淀中加入10-100v%乙醇溶解,得到沉淀物的醇溶液;6)将沉淀物的醇溶液进行柱层析;7)浓缩上述步骤6)得到的洗脱液,加入乙醇过饱和溶解,获得结晶物;8)将结晶物,加入纯化水或乙醇洗涤,得到初品;9)将步骤8)初品用纯化水混匀,干燥,即得大麻二酚。
进一步地,步骤1)中工业大麻花叶粉碎后烘干,包括在60-200℃温度条件下,烘干0.5-3h,至水分5%以下。
进一步地,步骤1)中工业大麻花叶粉碎至10-80目。
进一步地,步骤2)的提取方式包括回流提取、超声提取和/或浸泡提取,具体如下:
回流提取:采用2-8倍药材量的乙醇进行回流提取1-3次,每次0.5-3h;
超声提取:采用2-8倍药材量的乙醇进行超声提取1-3次,每次0.1-1h;
浸泡提取:采用2-8倍药材量的乙醇进行浸泡提取1-3次,每次0.5-5h。
进一步地,步骤3)具体包括:将提取液浓缩至50℃时测量,相对密度1.05-1.35。
进一步地,步骤4)具体包括:采用1-10倍药材量的纯化水,在0-20℃的温度条件下,水沉1-48h。
进一步地,步骤6)中将沉淀物的醇溶液进行柱层析的步骤包括:采用洗脱溶剂对层析柱进行梯度洗脱,优选洗脱溶剂为乙醇和水,更优选梯度洗脱的步骤包括:先用0-30v%的乙醇除杂,再用40-80v%的乙醇洗脱获得目标产物部分,最后用90-95v%的乙醇洗脱以使层析柱再生。
进一步地,步骤6)中柱层析所用的层析柱的填料包括大孔树脂、MCI树脂、十八烷基硅烷键合硅胶中的一种或多种。
进一步地,大孔树脂包括AB-8、D-101、XDA-8、LSA-7、D-941、DM-130、ADS-17、SP-825和HPD-600中的一种或多种。
进一步地,步骤7)中,还包括对洗脱液中乙醇的回收步骤。
进一步地,步骤7),包括在10-80℃温度条件下,用60-100v%乙醇过饱和溶解,获得结晶物。
进一步地,步骤8),具体为:0-24℃温度条件下,加纯化水或5-40v%乙醇洗涤,得到初品。
进一步地,步骤9)中,干燥的方式包括喷雾干燥、真空干燥、冷冻干燥、近红外干燥、微波干燥中的一种或几种,干燥温度不超过65℃。
进一步地,步骤9)后,进一步包括将获得的大麻二酚粉碎成粉的步骤,优选粉碎的方式包括汽流粉碎、和/或冷冻粉碎,进一步优选粉碎时物料温度不超过65℃。
应用本发明的技术方案从工业大麻花叶中提取大麻二酚,通过摈弃现有技术中对大麻二酚(CBD)溶解度较高的石油醚、正己烷、二氯甲烷等溶剂,而采用溶解度相对低的乙醇作为提取溶剂,并结合改进的提取工艺从而不仅提高了大麻二酚的纯度,去除了成品中精神毒性成分四氢大麻酚,使产品安全性得到保障;而且使用的试剂为乙醇和水,减少了对环境、操作人员、产品溶剂残留的影响,减少柱层析过程中造成的环境污染,对人员造成的伤害。此外,层析柱的填料可重复利用,使总体生产成本降低,且降低填料废弃物对环境造成的污染。
附图说明
构成本申请的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
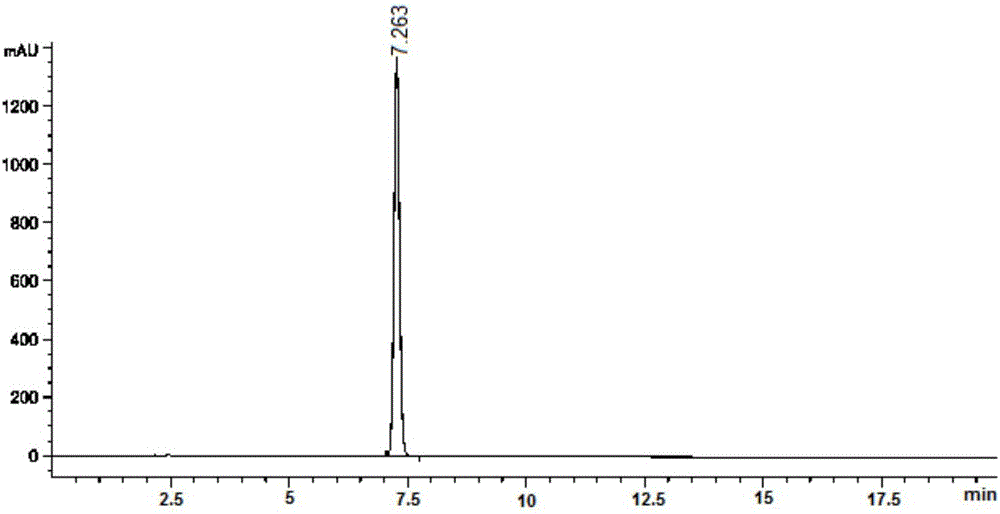
图1示出了产物1的色谱图;
图2示出了产物2的色谱图;
图3示出了产物3的色谱图;
图4示出了产物4的色谱图;
图5A、5B和5C分别示出了产物5-1、产物5-2和产物5-3的色谱图;
图6A、6B和6C分别示出了产物6-1、产物6-2和产物6-3的色谱图;
图7A、7B和7C分别示出了产物7-1、产物7-2和产物7-3的色谱图;
图8示出了对比产物1的色谱图;以及
图9示出了对比产物2的色谱图。
具体实施方式
需要说明的是,在不冲突的情况下,本申请中的实施例及实施例中的特征可以相互组合。下面将参考附图并结合实施例来详细说明本发明。
需要说明的是,本申请中的“2-8倍药材量”或“1-10倍药材量”等描述,是指采用的溶剂如乙醇或水的体积是药材质量的2-8倍或1-10倍,比如,药材粉末为1g,提取溶剂乙醇的用量为2ml-8ml。
现有技术中大麻二酚的生产纯化工艺存在大麻二酚纯度不高且含有精神毒性成分四氢大麻酚等问题。针对上述技术问题,本发明的发明人提出了以下技术方案。
根据本发明一种典型的实施方式,提供一种从工业大麻花叶中提取大麻二酚的方法。该方法包括以下步骤:1)将工业大麻的花叶粉碎、烘干,得到药材粉末;2)将药材粉末采用30-100v%的乙醇提取,得到提取液;3)将提取液浓缩,得到浸膏;4)将浸膏进行水沉,去除杂质,得到水沉液;5)将水沉液离心,在离心获得的沉淀中加入10-100v%乙醇溶解,得到沉淀物的醇溶液;6)将沉淀物的醇溶液进行柱层析;7)浓缩上述步骤6)得到的洗脱液,加入乙醇过饱和溶解,获得结晶物;8)将结晶物,加入纯化水或乙醇洗涤,得到初品;9)将步骤8)初品用纯化水混匀,干燥,即得大麻二酚。
应用本发明的技术方案从工业大麻花叶中提取大麻二酚的方法,与现有技术的相比,提高了大麻二酚(CBD)纯度,去除了成品中精神毒性成分四氢大麻酚,使产品安全性得到保障;并且层析柱的填料可重复利用,使总体生产成本降低,降低废弃物对环境造成的污染;使用的试剂为乙醇和水,减少了对环境、操作人员、产品溶剂残留的影响,也克服了本领域关于提取溶剂的选择与产品得率间的技术偏见,产生了预料不到的技术效果。
本发明所述的方法,打破了本领域的常规认识,在工艺过程中全程使用乙醇作为提取溶剂,通过对比同样技术条件下采用现有有机溶剂进行提取的结果,不仅克服了现有技术存在的缺陷,而且出乎意料地发现大麻二酚的得率、纯度均有明显提高,且未检出精神毒性成分四氢大麻酚,有利于工业化生产。
上述方法的步骤5)中得到沉淀物的醇溶液的步骤包括:将水沉液离心,弃去上清液,获得沉淀物;采用10-100v%乙醇对沉淀物进行溶解,得到沉淀物的醇溶液。而在上述步骤7)中,浓缩步骤6)得到的洗脱液,并加入乙醇过饱和溶解洗脱液后,进行静置,从而获得结晶物。
根据本发明一种典型的实施方式,步骤1)中工业大麻花叶粉碎后烘干,包括在60-200℃温度条件下,烘干0.5-3h,至水分5%以下。在此种条件烘干效率高,干燥好,且不会破坏有效成分。优选的,步骤1)中工业大麻花叶粉碎至10-80目,从而可以使大麻二酚在后续的乙醇提取步骤中充分提取出来。
根据本发明一种典型的实施方式,步骤2)的提取方式包括回流提取、超声提取和/或浸泡提取,具体如下:回流提取:采用2-8倍药材量的乙醇进行回流提取1-3次,每次0.5-3h;超声提取:采用2-8倍药材量的乙醇进行超声提取1-3次,每次0.1-1h;浸泡提取:采用2-8倍药材量的乙醇进行浸泡提取1-3次,每次0.5-5h。
优选的,步骤3)具体包括:将提取液浓缩至50℃测量,相对密度1.05-1.35。优选的,步骤4)具体包括:采用1-10倍药材量纯化水,在0-20℃的温度条件下,水沉1-48h。
优选的,步骤6)中将沉淀物的醇溶液进行柱层析的步骤包括:采用洗脱溶剂对层析柱进行梯度洗脱;优选洗脱溶剂为乙醇和水,更优选梯度洗脱的步骤包括:先用0-30v%的乙醇除杂,再用40-80v%的乙醇洗脱获得目标产物部分,最后用90-95v%的乙醇洗脱以使层析柱再生。上述梯度洗脱的步骤不仅使得目标产物部分纯度高,而且使层析柱不断再生,可循环使用。
更优选地,上述柱层析所用的层析柱的填料为选自大孔树脂、MCI树脂、十八烷基硅烷键合硅胶中的一种或多种。
本发明中提到的MCI树脂,是最近几年日本三菱化学在Diaion和Sepabeads大孔树脂的基础上设计的新型树脂,粒径只有75-150微米,较小的颗粒有更高的色谱分离性能,用于分离天然产物有独特的效果。本发明的发明人发现其对大麻二酚(CBD)有独特的选择性吸附,其再生简单、可重复使用,减少成本,工艺重复性极佳。运用这一新的填料在大麻二酚的纯化工艺中,极大的提高了精制后CBD的含量。
根据本发明一种典型的实施方式,大孔树脂包括AB-8、D-101、XDA-8、LSA-7、D-941、DM-130、ADS-17、SP-825和HPD-600中的一种或多种。上述型号的树脂,价格便宜,再生简单,用于大麻二酚的初步纯化。
根据本发明一种典型的实施方式,步骤7)中,还包括对洗脱液中乙醇的回收步骤。
优选的,步骤7),包括在10-80℃温度条件下,用60-100%乙醇过饱和溶解,获得结晶物。优选的,步骤8),具体为:0-24℃温度条件下,加纯化水或者5-40%乙醇洗涤,得到初品。
优选的,步骤9)中,干燥的方式包括喷雾干燥、真空干燥、近红外干燥、微波干燥中的一种或几种,干燥温度不超过65℃。
优选的,步骤9)后,进一步包括将获得的大麻二酚粉碎成粉的步骤,优选粉碎的方式包括汽流粉碎和/或冷冻粉碎,进一步优选粉碎时物料温度不超过65℃。
下面将结合实施例进一步说明本发明的有益效果。
实施例1
本发明所述方法制备大麻二酚
本实验提供了采用本发明所述方法,在不同技术参数条件下,制备大麻二酚,本实验中采取的工业大麻花叶的量均为10千克。
方法1:
1)将实验用工业大麻的花叶粉碎,过80目筛,得到药材粉末。在60℃温度条件下,烘干3h,通过检测,其水分含量为4%。
2)将上述药材粉末采用2倍量、30v%的乙醇、回流提取3次,每次0.5h,得到提取液;
3)将上述提取液浓缩,浓缩至50℃时,相对密度1.05,得到浸膏;
4)将上述浸膏用1倍纯化水,在温度20℃条件下,水沉1h,得到水沉液;
5)将上述水沉液离心,转速5000转,在离心获得的沉淀中加入100v%乙醇溶解,得到沉淀物的醇溶液;
6)将沉淀物的醇溶液进行柱层析,其层析柱的填料为AB-8,脱溶剂为乙醇和水,洗脱的步骤包括:先用30v%的乙醇洗脱除杂,再用80v%的乙醇洗脱获得目标产物部分,最后用95v%的乙醇洗脱以使层析柱再生;
7)浓缩上述步骤6)得到的洗脱液,至50℃时,相对密度1.15,在温度10℃下,用100v%乙醇过饱和溶解,获得结晶物;
8)将步骤7)所述结晶物,在温度0℃条件下,加纯化水洗涤,得到初品;
9)将步骤8)所述初品真空干燥,即得大麻二酚。
10)采用汽流粉碎步骤9)所得大麻二酚,即得产物1。
方法2:
1)将实验用工业大麻的花叶粉碎,过10目筛,得到药材粉末。在200℃温度条件下,烘干0.5h,通过检测,其水分含量为2.7%。
2)将上述药材粉末采用2倍量、100v%的乙醇、超声提取1次,每次1h,得到提取液;
3)将上述提取液浓缩,浓缩至50℃时,相对密度1.35,得到浸膏;
4)将上述浸膏用10倍纯化水,在温度0℃条件下,水沉48h,得到水沉液;
5)将上述水沉液离心,转速10000转,在离心获得的沉淀中加入10v%乙醇溶解,得到沉淀物的醇溶液;
6)将沉淀物的醇溶液进行柱层析,其层析柱的填料为MCI树脂,脱溶剂为乙醇和水,洗脱的步骤包括:先用10v%的乙醇洗脱除杂,再用40v%的乙醇洗脱获得目标产物部分,最后用90v%的乙醇洗脱以使层析柱再生;
7)浓缩上述步骤6)得到的洗脱液,至50℃时,相对密度1.25,在温度80℃下,用60v%乙醇过饱和溶解,获得结晶物;
8)将步骤7)所述结晶物,然后在温度24℃条件下,加5v%乙醇洗涤,得到初品;
9)将步骤8)所述初品用纯化水混匀,冷冻干燥,即得大麻二酚。
10)采用冷冻粉碎步骤9)所得大麻二酚,即得产物2。
方法3:
1)将实验用工业大麻的花叶粉碎,过40目筛,得到药材粉末。在130℃温度条件下,烘干1.7h,通过检测,其水分含量为3.1%。
2)将上述药材粉末采用5倍量、60v%的乙醇、浸泡提取2次,每次2.5h,得到提取液;
3)将上述提取液浓缩,浓缩至50℃时,相对密度1.2,得到浸膏;
4)将上述浸膏用5倍纯化水,在温度10℃条件下,水沉24h,得到水沉液;
5)将上述水沉液离心,转速7500转,在离心获得的沉淀中加入60v%乙醇溶解,得到沉淀物的醇溶液;
6)将沉淀物的醇溶液进行柱层析,其层析柱的填料为ODS,脱溶剂为乙醇和水,洗脱的步骤包括:先用25v%的乙醇洗脱除杂,再用60v%的乙醇洗脱获得目标产物部分,最后用93v%的乙醇洗脱以使层析柱再生;
7)浓缩上述步骤6)得到的洗脱液,至50℃时,相对密度1.2,在温度45℃下,用80v%乙醇过饱和溶解,获得结晶物;
8)将步骤7)所述结晶物,然后在温度12℃条件下,加40v%乙醇洗涤,得到初品;
9)将步骤8)所述初品真空干燥,即得大麻二酚。
10)采用汽流粉碎步骤9)所得大麻二酚,即得产物3。
方法4:
1)将实验用工业大麻的花叶粉碎,过40目筛,得到药材粉末。在120℃温度条件下,烘干1h,通过检测,其水分含量为2.6%。
2)将上述药材粉末采用3倍量、70v%的乙醇、60赫兹条件下,超声提取3次,每次0.5h,得到提取液;
3)将上述提取液浓缩,浓缩至50℃时,相对密度1.1,得到浸膏;
4)将上述浸膏用5倍纯化水,在温度4℃条件下,水沉12h,得到水沉液;
5)将上述水沉液离心,转速5000转,在离心获得的沉淀中加入80v%乙醇溶解,得到沉淀物的醇溶液;
6)将沉淀物的醇溶液进行柱层析,其层析柱的填料为MCI树脂,脱溶剂为乙醇和水,洗脱的步骤包括:先用15v%的乙醇洗脱除杂,再用75v%的乙醇洗脱获得目标产物部分,最后用95v%的乙醇洗脱以使层析柱再生;
7)浓缩上述步骤6)得到的洗脱液,至50℃时,相对密度1.1,在温度70℃下,用80v%乙醇过饱和溶解,获得结晶物;
8)将步骤7)所述结晶物,然后在温度10℃条件下,加10v%乙醇洗脱,得到初品;
9)将步骤8)所述初品真空干燥,即得大麻二酚。
10)采用汽流粉碎步骤9)所得大麻二酚,即得产物4。
实施例2不同提取方法制备大麻二酚
本次实验用药材量与实施例1相同
超声提取:
1)将实验用工业大麻的花叶粉碎,过40目筛,得到药材粉末。在120℃温度条件下,烘干1h,通过检测,其水分含量为2.6%。
2)将上述药材粉末采用5倍量、80v%的乙醇、70赫兹条件下,超声提取2次,每次0.5h,得到提取液;
3)将上述提取液浓缩,浓缩至50℃时,相对密度1.1,得到浸膏;
4)将上述浸膏用5倍纯化水,在温度4℃条件下,水沉12h,得到水沉液;
5)将上述水沉液离心,转速5000转,在离心获得的沉淀中加入80v%乙醇溶解,得到沉淀物的醇溶液;
6)将沉淀物的醇溶液进行柱层析,其层析柱的填料为MCI树脂,脱溶剂为乙醇和水,洗脱的步骤包括:先用30v%的乙醇洗脱除杂,再用75v%的乙醇洗脱获得目标产物部分,最后用95v%的乙醇洗脱以使层析柱再生;
7)浓缩上述步骤6)得到的洗脱液,50℃时,相对至密度1.1,在温度70℃下,用80v%乙醇过饱和溶解,获得结晶物;
8)将步骤7)所述结晶物,然后在温度10℃条件下,加10v%乙醇洗涤,得到初品;
9)将步骤8)所述初品真空干燥,即得大麻二酚。
10)采用汽流粉碎步骤9)所得大麻二酚,即得产物。
按此方法,平行制备三批,所得产物分别命名为产物5-1,产物5-2,产物5-3。
回流提取:
1)将实验用工业大麻的花叶粉碎,过40目筛,得到药材粉末。在120℃温度条件下,烘干1h,通过检测,其水分含量为2.6%。
2)将上述药材粉末采用5倍量、80v%的乙醇、回流提取2次,每次1.5h,得到提取液;
3)将上述提取液浓缩,浓缩至50℃时,相对密度1.1,得到浸膏;
4)将上述浸膏用5倍纯化水,在温度4℃条件下,水沉12h,得到水沉液;
5)将上述水沉液离心,转速5000转,在离心获得的沉淀中加入80v%乙醇溶解,得到沉淀物的醇溶液;
6)将沉淀物的醇溶液进行柱层析,其层析柱的填料为MCI树脂,脱溶剂为乙醇和水,洗脱的步骤包括:先用30v%的乙醇洗脱除杂,再用75v%的乙醇洗脱获得目标产物部分,最后用95v%的乙醇洗脱以使层析柱再生;
7)浓缩上述步骤6)得到的洗脱液,至50℃时,相对密度1.1,在温度70℃下,用80v%乙醇过饱和溶解,获得结晶物;
8)将步骤7)所述结晶物,然后在温度10℃条件下,加10v%乙醇洗涤,得到初品;
9)将步骤8)所述初品真空干燥,即得大麻二酚。
10)采用汽流粉碎步骤9)所得大麻二酚,即得产物。
按此方法,平行制备三批,所得产物分别命名为产物6-1,产物6-2,产物6-3。
浸泡提取;
1)将实验用工业大麻的花叶粉碎,过40目筛,得到药材粉末。在120℃温度条件下,烘干1h,通过检测,其水分含量为2.6%。
2)将上述药材粉末采用5倍量、80v%的乙醇、浸泡提取2次,每次2.5h,得到提取液;
3)将上述提取液浓缩,浓缩至50℃时,相对密度1.1,得到浸膏;
4)将上述浸膏用5倍纯化水,在温度4℃条件下,水沉12h,得到水沉液;
5)将上述水沉液离心,转速5000转,在离心获得的沉淀中加入80v%乙醇溶解,得到沉淀物的醇溶液;
6)将沉淀物的醇溶液进行柱层析,其层析柱的填料为MCI树脂,脱溶剂为乙醇和水,洗脱的步骤包括:先用30v%的乙醇洗脱除杂,再用75v%的乙醇洗脱获得目标产物部分,最后用95v%的乙醇洗脱以使层析柱再生;
7)浓缩上述步骤6)得到的洗脱液,至50℃时,相对密度1.1,在温度70℃下,用80v%乙醇过饱和溶解,获得结晶物;
8)将步骤7)所述结晶物,然后在温度10℃条件下,加10v%乙醇洗脱,得到初品;
9)将步骤8)所述初品真空干燥,即得大麻二酚。
10)采用汽流粉碎步骤9)所得大麻二酚,即得产物。
按此方法,平行制备三批,所得产物分别命名为产物7-1,产物7-2,产物7-3。
对比例参照现有技术的方法制备大麻二酚
参数1:
1)采用盛花期的花叶,将其投入烘烤设备内,130℃烘干35min;
2)把烘干的花叶进行磨碎,粒径达到5-10目之间;
3)把磨好的花叶装入浸泡器内进行浸泡,浸泡溶剂采用石油醚。浸泡温度48℃,浸泡时间1h;
4)浸泡后,将花叶滤出,滤液在90℃下加热,得到浸膏;
5)层析分离:把吸附齐称量后装入层析分离器内;将浸膏均匀地放在吸附剂表面吸附CBD,吸附剂与浸膏按重量比25:1;采用石油醚进行洗脱,干燥即得对比产物1。
参数2:
1)采用盛花期的花叶,将其投入烘烤设备内,160℃烘干15min;
2)把烘干的花叶进行磨碎,粒径达到5-10目之间;
3)把磨好的花叶装入浸泡器内进行浸泡,浸泡溶剂采用正己烷。浸泡温度20℃,浸泡时间2h;
4)浸泡后,将花叶滤出,滤液在120℃下加热,得到浸膏;
5)层析分离:把吸附剂大孔树脂称量后装入层析分离器内;吸附剂与浸膏以1:1比例混匀吸附CBD;采用正己烷进行洗脱,干燥即得对比产物2。
检测1:不同制法所得产物中CBD含量及四氢大麻酚的检出情况对比
检测方法:
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以乙腈为流动相A,以水为流动相B,按A(%):B(%)=80:20进行等度洗脱;检测波长为210nm。理论板数按CBD峰计算应不低于2500。
对照品溶液的制备精密称取CBD对照品,加甲醇(1:1)制成每1ml各含0.1mg的对照品溶液,即得;精密称取四氢大麻酚对照品,加甲醇(1:1)制成每1ml各含0.01mg的对照品溶液,即得。
供试品溶液的制备取本品约25mg,精密称定,置25ml量瓶中,加乙腈-水(1:1)20ml,超声处理15分钟,加乙腈-水(1:1)稀释至刻度,摇匀,用微孔滤膜(0.45μm)滤过,取续滤液,即得。
测定法分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。
上述各产物的CBD含量及四氢大麻酚含量检测结果参见表1及附图1至附图9。
表1.不同制法所得产物其CBD含量及THC检出情况对比
由表1和图1至图9可知,通过本发明的方法制备得到的产物1、2、3、4,5-1、5-2、5-3,6-1、6-2、6-3,7-1、7-2、7-3中CBD(大麻二酚)的含量明显高于现有技术制备所得CBD(对比产物1和对比产物2)的含量;采用本发明所述的技术其产物中无THC(四氢大麻酚)检出,而采用现有技术制备所得的产物中明显检出THC。进一步说明,采用本发明提取出来的CBD含量更高,纯度更纯,更安全,符合法规对产品的相关要求。
将对比产物1和2的制备方法与本发明的制备方法相比,具体存在以下差异点:
1)烘干、粉碎顺序及条件
本发明:先粉碎,后烘干。60-200℃条件下,烘干0.5-3h,粉末水份含量5%以下
现有技术:先烘干,后粉碎。130-160℃条件下,烘干15-35min,花叶水份含量3-5%。
2)提取
本发明:采用2-8倍药材量的30-100v%乙醇提取,提取方式选自回流提取、超声提取和/或浸泡提取,具体如下:
(1)回流提取:1-3次,每次0.5-3h;
(2)超声提取:1-3次,每次0.1-1h;
(3)浸泡提取:1-3次,每次0.5-5h;
现有技术:采用石油醚、正己烷或6#溶剂油作为溶剂通过浸泡提取,浸泡温度不小于50℃,浸泡时间不少于1h。浸泡前可对加入的物料进行溶剂喷淋。
3)浓缩
本发明:50℃时,浓缩至相对密度1.05-1.35;现有技术:在90-120℃下浓缩。
4)层析分离
本发明:将浓缩后的浸膏,用1-10倍纯化水,在温度0-20℃条件下,水沉1-48h,得到水沉液;水沉液离心,在离心获得的沉淀中加入10-100v%乙醇溶解,得到乙醇溶液;
其层析柱的填料选自大孔树脂、MCI树脂、ODS(十八烷基硅烷键合硅胶填料)。
沉淀物的醇溶液进行柱层析的步骤包括:采用洗脱溶剂对层析柱进行梯度洗脱,优选洗脱溶剂为乙醇和水。优选梯度洗脱的步骤包括:先用0-30v%的乙醇除杂,再用40-80v%的乙醇洗脱获得目标产物部分,最后用90-95v%的乙醇洗脱以使所述层析柱再生。
现有技术:将浸膏用吸附剂吸附后,采用正己烷、二氯甲烷、石油醚、乙酸乙酯、乙醇、甲醇中的一种或者任意几种混合物进行洗脱;吸附剂为大孔树脂或柱层层析硅胶。
5)产物的富集及干燥方式
本发明:浓缩洗脱液后,优选在10-80℃温度条件下,用60-100%乙醇过饱和溶解,获得结晶物。在0-24℃条件下,加纯化水或者5-40%乙醇洗涤,得到初品。干燥方式选包括真空干燥、冷冻干燥、近红外干燥、微波干燥中的一种或多种,干燥温度不超过65℃。
干燥获得大麻二酚后,可采用包括汽流粉碎、冷冻粉碎等方式粉碎,获得大麻二酚成品,粉碎时物料温度不超过去65℃。
现有技术:未明显体现具体方式。
从上述制备方法的比较也可以看出,本发明通过全程采用乙醇为主要试剂进行制备,相较于采用对CBD溶解度高的有机溶剂进行提取的制备方法,不仅能大幅提高CBD的产量,而且打破了传统科研的思维,带来了“去除神经毒性成分四氢大麻酚,提高CBD纯度”的意想不到的有益技术效果。
检测2:不同提取方法对CBD提取率影响的比较
(1)原花叶药材含量检测方法
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以乙腈为流动相A,以水为流动相B,按A(%):B(%)=80:20进行等度洗脱;检测波长为210nm。理论板数按CBD峰计算应不低于2500。
对照品溶液的制备精密称取CBD对照品,加甲醇(1:1)制成每1ml各含0.1mg的对照品溶液,即得;精密称取四氢大麻酚对照品,加甲醇(1:1)制成每1ml各含0.01mg的对照品溶液,即得。
供试品溶液的制备取本品约1g,精密称定,加甲醇25ml,超声处理15分钟,过滤,再加甲醇25ml,超声处理15分钟,合并滤液,定容至50ml,摇匀,用微孔滤膜(0.45μm)滤过,取续滤液,即得。
测定法分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。
(2)提取液含量检测方法
色谱条件与系统适用性试验以十八烷基硅烷键合硅胶为填充剂;以乙腈为流动相A,以水为流动相B,按A(%):B(%)=80:20进行等度洗脱;检测波长为210nm。理论板数按CBD峰计算应不低于2500。
对照品溶液的制备精密称取CBD对照品,加甲醇(1:1)制成每1ml各含0.1mg的对照品溶液,即得;精密称取四氢大麻酚对照品,加甲醇(1:1)制成每1ml各含0.01mg的对照品溶液,即得。
供试品溶液的制备提取液1ml,定容至25ml,用微孔滤膜(0.45μm)滤过,取续滤液,即得。
测定法分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,即得。
上述三种提取方法采用实施例2中的三种方法:1)浸泡提取;2)回流提取;3)超声提取。具体提取率的实验结果见下表2。
表2.三种提取方法提取率试验(以CBD含量为指标)
由上表2可知,三种提取方法提取效率相当,提取方法的改变对提取率没有影响。在其它技术参数相同的条件下,利用浸泡提取所得产物7-1、7-2、7-3中CBD(大麻二酚)的含量与利用超声提取所得产物5-1、5-2、5-3中CBD(大麻二酚)的含量无明显差别。进一步说明,本发明的有益效果并非是由于仅是引入了超声提取这一工艺技术导致的。
检测3:采用稳定性试验方法检测不同制法所得产物的稳定性
主要仪器:
药品稳定性试验箱(长期):SHH-250SD,重庆永生实验仪器厂;
药品稳定性试验箱(加速):SHH-250SD,重庆永生实验仪器厂;
高效液相色谱仪:Agilent1200;
分析天平:MS-105DU,瑞士梅特勒-托利多;
紫外可见分光光度计:UV-2550,日本岛津;
薄层色谱成像仪:TLC Visualizer,瑞士卡玛;
试验样品:
将按照上述各实施例和对比例的方法制备的15批样品,进行加速稳定性试验。检测具体数据参见表3至表17。
其中,
产物1,批号:11030801;产物2,批号:11030802;产物3,批号:11030803;
产物4,批号:11030804;产物5-1,批号:11030805;产物5-2,批号:11030806;
产物5-3,批号:11030807;产物6-1,批号:11030808;产物6-2,批号:11030809;
产物6-3,批号:11030810;产物7-1,批号:11030811;产物7-2,批号:11030812;
产物7-3,批号:11030813;对比产物1,批号:11030814;对比产物2,批号:11030815。
上述15批样品中,每批批量为10kg(以药材投料量计),由汉义生物科技(北京)有限公司生产,产品用玻璃料瓶密封包装,每瓶10g。
表3.产物1稳定性试验
表4.产物2稳定性试验
表5.产物3稳定性试验
表6.产物4稳定性试验
表7.产物5-1稳定性试验
表8.产物5-2稳定性试验
表9.产物5-3稳定性试验
表10.产物6-1稳定性试验
表11.产物6-2稳定性试验
表12.产物6-3稳定性试验
表13.产物7-1稳定性试验
表14.产物7-2稳定性试验
表15.产物7-3稳定性试验
表16.对比产物1稳定性试验
表17.对比产物2稳定性试验
由表3-17可知,通过本发明的方法制备得到的产物1、2、3、4,5-1、5-2、5-3,6-1、6-2、6-3,7-1、7-2、7-3中CBD(大麻二酚)的含量经6个月加速稳定性试验放置,稳定性良好,CBD的含量变化范围仅为0.6%以内,(其中,存放3个月、2个月以及1个月后CBD含量的变化最高的也仅为0.6%)。而采用文献方法制得对比产物1和对比产物2经6个月加速稳定性试验放置后CBD(大麻二酚)的含量分别从83.1%降到73.8%(下降率为9.3%),从81.2%降到69.1%(下降率为12.1%),稳定性较差。对比产物1和对比产物2经3个月的稳定性试验中,含量下降率分别为7.1%和10.1%,同样,稳定性显著差于实施例。
从以上的描述中,可以看出,本发明上述的实施例实现了如下技术效果:1)通过增加结晶步骤,使终产品中大麻二酚(CBD)含量提高至96%以上。2)通过对工艺技术的改进,使成品中四氢大麻酚含量控制在0.3%以下(在实施例中,四氢大麻酚未检出),符合国家法律法规要求,产品安全性得到保障。3)初步精制步骤中使用大孔树脂、MCI树脂或ODS代替现有技术中的硅胶,使得填料可重复利用,使总体生产成本降低,减少废弃物硅胶对环境的污染。4)采用乙醇和水作为提取溶剂,溶剂安全,对环境、操作人员危害小,产品溶剂残留大大改善;柱层析过程中采用不同纯度乙醇洗脱树脂柱,减少对环境污染,减少人员伤害。
另外,经实验室规模实验验证和中试放大验证,按照本发明所述工艺能生产出纯度高(含量95%)以上,安全(THC含量0.3%以下)产品。
以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!