一种新的N(2)‑L‑丙氨酰‑L‑谷氨酰胺晶型及其制备方法与流程
技术领域:
:本发明属于化学医药制备
技术领域:
,具体涉及一种新的n(2)-l-丙氨酰-l-谷氨酰胺晶型及其制备方法。
背景技术:
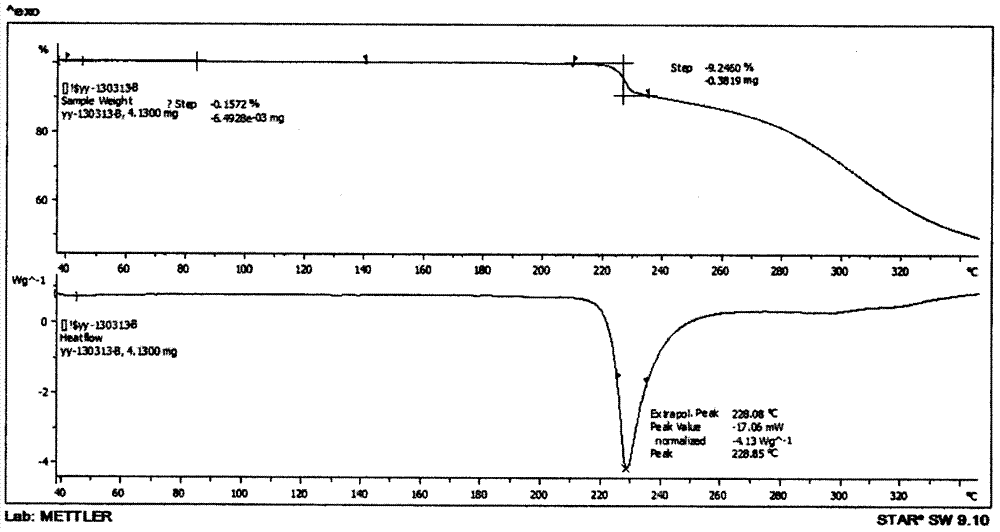
::具有式i结构的n(2)-l-丙氨酰-l-谷氨酰胺属于氨基酸的衍生物,在维持肠道机能,促进免疫功能,维持体内碱平衡及提高机体对应激的适应等方面都发挥着及其重要的作用,n(2)-l-丙氨酰-l-谷氨酰胺克服了谷氨酰胺(gln)溶解度低且不稳定,加热时可产生有毒的焦谷氨酸和氨的缺点,不仅溶解度高,而且性质稳定,在体内可迅速分解出(gln),具有与(gln)相同的生物学效应。是人体含量最丰富的氨基酸谷氨酰胺(gln)的理想替代品,临床上主要适用于需要补充谷氨酰胺的病人,包括处于分解代谢和高代谢状况的病人。目前,该产品在国内外上市剂型为注射剂,包括丙氨酰谷氨酰胺注射液和注射用丙氨酰谷氨酰胺,其中注射液规格为50ml:10g和100ml:20g。注射用无菌粉规格为10g和20g。虽然该产品临床主要供注射用,其体内吸收及生物利用度与晶型关系不大。但晶型作为该产品原料药的一种物理性质,以及其是否为溶剂化物,可以影响式i原料药的稳定性,同时不同的晶型可以对产品流动性,堆密度,澄清度造成不同程度的影响。因而深入研究式i原料药的晶型是很有必要及现实意义的。尤其是获得无结晶溶剂,流动性好,堆密度较小,适于式i无菌原料药生产及分装要求的晶型。文献报道的获得n(2)-l-丙氨酰-l-谷氨酰胺原料药的晶型的主要方式是通过采用不同的结晶溶剂,现对文献报道的有关n(2)-l-丙氨酰-l-谷氨酰胺原料药晶型研究及其干燥方法的研究报道进行总结。文献[1]_cn101519428a、[2]-cn101062938a、[3]_cn1679531a、[4]_cn102698247a、[5]_organicprocessresearch&development(2000),4(3),147-152、[6]_王如帆.l-丙氨酰-l-谷氨酰胺结晶过程研究.天津大学硕士学位论文.2007报道的n(2)-l-丙氨酰-l-谷氨酰胺原料药纯化或结晶的方法采用的溶剂为乙醇/水体系。其中文献[1]~[5]并未详细研究n(2)-l-丙氨酰-l-谷氨酰胺的晶型,同时也未提供获得何种晶型,未有晶型鉴定或表征数据。文献[6]对n(2)-l-丙氨酰-l-谷氨酰胺采用乙醇/水体系结晶,干燥进行了详细的研究。并提供了一种晶型的表征数据。但文献[6]作者对采用乙醇/水体系结晶,n(2)-l-丙氨酰-l-谷氨酰收率异常,小试与工厂放大样品(tga、dsc)数据不一致,常压干燥与真空减压干燥晶形不一致未能给出合理的解释。本发明人在重复实施以上文献报道的方法制备n(2)-l-丙氨酰-l-谷氨酰胺原料药过程中,也遇到过以上问题,制备获得的n(2)-l-丙氨酰-l-谷氨酰胺原料药产品,有机残留,澄清度,含量,晶型,等质量控制项目小试与放大产品,批与批之间差异很大,根本无法满足工业化生产对工艺稳定的要求。文献[7]_cn1683391a、[8]_李永新,覃军,赵树铭.l-丙氨酰-l-谷氨酰胺的合成及初步鉴定.第三军医大学学报。2001。23(5).571-572、[9]_ep0595345a1报道的n(2)-l-丙氨酰-l-谷氨酰胺原料药纯化或结晶的方法采用的溶剂为甲醇/水体系。文献[7]~[9]并未详细研究n(2)-l-丙氨酰-l-谷氨酰胺的晶型,同时也未提供获得何种晶型,未有晶型鉴定或表征数据。本发明人在实施文献报道的方法时发现。n(2)-l-丙氨酰-l-谷氨酰胺在甲醇/水混合体系中的溶解度与过饱和度与乙醇/水混合体系相差较大,采用甲醇/水混合体系结晶获得的结晶固体颗粒较细,堆密度较大,流动性差。同时由于甲醇毒性较大,考虑到n(2)-l-丙氨酰-l-谷氨酰胺临床主要用于注射,且使用剂量较大。过高的甲醇残留将会对患者造成极大的伤害。因而n(2)-l-丙氨酰-l-谷氨酰胺原料药最后一步采用甲醇/水结晶显然是不合适的。文献[10]_wo2000059925a1、[11]_us5032675a、[12]_cn103554218b报道的n(2)-l-丙氨酰-l-谷氨酰胺原料药纯化或结晶的方法采用的溶剂为异丙醇/水体系。其中文献[12]通过控制搅拌速度及结晶温度获得了n(2)-l-丙氨酰-l-谷氨酰胺两种晶型(分别为iv,v晶型)。同样的,本发明人在实施文献报道的方法时发现n(2)-l-丙氨酰-l-谷氨酰胺在异丙醇/水混合体系中的溶解度与过饱和度与乙醇/水混合体系相差较大,采用异丙醇/水混合体系结晶获得的结晶固体颗粒较细,堆密度较大,流动性差。且干燥过程中,异丙醇有时不容易去除。导致产品有机残留,澄清度不合格。文献[13]_cn103073617a报道的获得晶型iii的方法为采用二恶烷或n,n-二甲基甲酰胺。以上两种溶剂不但沸点较高,产品干燥时难于去除。且毒性较大。因而不适于n(2)-l-丙氨酰-l-谷氨酰胺原料药工业化生产。文献[14]_cn102698248a、[15]_cn103709228a、提及了两种工业化生产上采用的n(2)-l-丙氨酰-l-谷氨酰胺干燥方法。其中文献[14]_cn102698248a为采用喷雾干燥方法制备,采用此种干燥方法,温度较高(150~200℃),产品容易降解。且比较容易获得无定型的n(2)-l-丙氨酰-l-谷氨酰胺,产品容易吸潮,放置过程中容易出现结块。文献[15]为采用常压干燥方法,且干燥过程中加入了一定质量分数的二甲亚砜。该方法的主要缺陷主要体现在以下几个方面,一是干燥过程中,采用以上文献报道的方法结晶获得的n(2)-l-丙氨酰-l-谷氨酰胺湿品,含有大量的易燃易爆有机溶剂,常压较高温度干燥过程中,干燥箱中充满大量有机蒸汽,非常危险。二是干燥过程中加入了高沸点溶剂二甲亚砜(沸点189℃),且干燥过程中保持的蒸汽压力为正压,由于n(2)-l-丙氨酰-l-谷氨酰胺在水中溶解度极大,干燥过程中部分产品极易重新溶解,包裹二甲亚砜。造成最终产品有机残留不合格。三是采用鼓风常压干燥n(2)-l-丙氨酰-l-谷氨酰胺,需要经常人工翻料,不适于进行大规模n(2)-l-丙氨酰-l-谷氨酰胺无菌粉的生产制备。综上,使用上述方法制备获得的式i化合物的晶型,虽可以对部分参数进行优化,但工业化生产过程中,仍然无法获得有机残留,澄清度,产品流动性,堆密度等质控指标符合无菌生产及分装要求的n(2)-l-丙氨酰-l-谷氨酰胺晶型产品,尤其是需要解决产品小试与工业化生产产品,批与批之间产品的质量均一性问题。为此亟待一种新的技术方案,以提供更优的工艺条件,解决小试与工业化生产产品,批与批之间产品在有机残留,澄清度,流动性,晶型等方面的差异问题。进而使其更有利于大规模工业化生产n(2)-l-丙氨酰-l-谷氨酰胺无菌粉。技术实现要素::为克服现有技术缺陷,本发明的目的是提供一种新的n(2)-l-丙氨酰-l-谷氨酰胺晶型及其制备方法,本发明通过在干燥过程中实现晶型转换,不但可以获得有机残留量低,水分含量低,流动性好的n(2)-l-丙氨酰-l-谷氨酰胺固体晶型,且提供了一种适合于工业化生产的转晶方法。该方法非常适合于n(2)-l-丙氨酰-l-谷氨酰胺无菌原料药工业化生产。为实现上述目的,本发明的技术方案为:本发明提供了一种式i化合物的新晶型及其制备方法。所述新晶型a的晶体进行x-ray粉末衍射,以衍射峰位置2θ为光谱图特征参数,所述2θ依次为:13.76±0.2,18.72±0.2,19.67±0.2,20.74±0.2,21.38±0.2,22.53±0.2,34.85±0.2;其制备方法为:以n(2)-l-丙氨酰-l-谷氨酰胺湿品为原料,在减压条件下,先控制温度为25-80℃,压力≤-0.09mpa干燥0.5-6小时.获得晶型b,然后继续控制温度为40-100℃,-0.09mpa≤压力≤-0.07mpa,干燥3-24小时获得晶型a。所述n(2)-l-丙氨酰-l-谷氨酰胺新晶型a晶体进行x-ray粉末衍射,其特征在于,以衍射峰位置2θ为光谱图特征参数,所述2θ依次为:13.76±0.2,18.72±0.2,19.67±0.2,20.74±0.2,21.38±0.2,22.53±0.2,23.14±0.2,24.13±0.2,25.42±0.2,27.68±0.2,34.85±0.2,36.61±0.2。进一步,所述的n(2)-l-丙氨酰-l-谷氨酰胺新晶型a晶体进行x-ray粉末衍射,其x-ray粉末衍射图谱如附图1和/或3和/或5和/或7所示。进一步,所述的n(2)-l-丙氨酰-l-谷氨酰胺新晶型a的所述衍射峰位置2θ按i/io的值由大至小依次为:13.76±0.2,20.74±0.2,19.67±0.2,18.72±0.2,21.38±0.2,34.85±0.2,22.53±0.2。作为本领域技术人员,在x-ray粉末衍射图谱中,例举所述新晶型a强度位列前5-10的衍射峰具有误差范围内的相同的峰位置和峰强度,即可代表所述新晶型a的指纹。所述n(2)-l-丙氨酰-l-谷氨酰胺新晶型a晶体进行差示扫描量热测定(dsc)及热重分析(tga),差示扫描量热测定(dsc)及热重分析(tga)图谱如附图2和/或4和/或6和/或8所示。进一步,所述n(2)-l-丙氨酰-l-谷氨酰胺新晶型a不含结晶水及其它结晶溶剂。本发明要解决的技术问题还在于提供n(2)-l-丙氨酰-l-谷氨酰胺新晶型a的制备方法,工艺简单,方法稳定。为实现上述目的,本发明的技术方案为:本发明提供的新晶型a制备方法为:以n(2)-l-丙氨酰-l-谷氨酰胺湿品为原料,在减压条件下,先控制温度为25-100℃,压力≤-0.09mpa干燥0.5-10小时.获得晶型b,然后继续控制温度为40-100℃,-0.09mpa≤压力≤-0.07mpa,干燥3-24小时获得a晶型。所述n(2)-l-丙氨酰-l-谷氨酰胺湿品,为从含乙醇/水体系结晶,经过滤或离心获得。进一步,所述用于获得n(2)-l-丙氨酰-l-谷氨酰胺湿品的含乙醇/水结晶体系,包括乙醇与水,乙醇与水和/或甲醇和/或正丙醇和/或丙酮和/或异丙醇组成的混合体系。优选乙醇与水。所述n(2)-l-丙氨酰-l-谷氨酰胺湿品的干燥条件为减压,其使用的减压干燥设备,本领域技术人员可熟知,如烘箱,双锥干燥器,单锥干燥器等工业化生产可实现减压干燥条件的设备。所述n(2)-l-丙氨酰-l-谷氨酰胺湿品的减压干燥,第一阶段的干燥条件为,控制温度25-100℃,压力≤-0.09mpa,干燥0.5~10小时.进一步,所述n(2)-l-丙氨酰-l-谷氨酰胺湿品第一阶段的干燥条件可控制温度优选为40-80℃,压力≤-0.092mpa,更优选压力≤-0.095mpa。优选干燥时间为1~7小时所述n(2)-l-丙氨酰-l-谷氨酰胺湿品第一阶段干燥结束获得的固体(晶体)进行x-ray粉末衍射,x-ray粉末衍射图谱如附图9和/或11和/或13所示。以衍射峰位置2θ为光谱图特征参数,所述2θ依次为:7.62±0.2,8.64±0.2,10.64±0.2,11.58±0.2,13.34±0.2,18.38±0.2,20.77±0.2,21.38±0.2,22.01±0.2,23.32±0.2,23.9±0.2,24.48±0.2,28.05±0.2,32.3±0.2,38.29±0.2。所述n(2)-l-丙氨酰-l-谷氨酰胺湿品第一阶段干燥结束获得的固体(晶体)为b晶型,所述n(2)-l-丙氨酰-l-谷氨酰胺晶型b的所述衍射峰位置2θ按i/io的值由大至小依次为:10.64±0.2,7.62±0.2,13.34±0.2,22.01±0.2,21.38±0.2,24.48±0.2,20.77±0.2,11.58±0.2,18.38±0.2,28.05±0.2。所述n(2)-l-丙氨酰-l-谷氨酰胺湿品第一阶段干燥结束获得的固体(晶体)为b晶型,进一步,所述b晶型的晶型纯度一般大于90%,优选大于95%,更优选大于98%。所述n(2)-l-丙氨酰-l-谷氨酰胺新晶型b晶体进行差示扫描量热测定(dsc)及热重分析(tga),差示扫描量热测定(dsc)及热重分析(tga)图谱如附图10和/或12和/或14所示。所述n(2)-l-丙氨酰-l-谷氨酰胺湿品的减压干燥,第二阶段的干燥条件为,控制温度40-100℃,-0.09mpa≤压力≤-0.07mpa,干燥3~24小时.进一步,所述n(2)-l-丙氨酰-l-谷氨酰胺湿品第一阶段的干燥条件可控制温度优选为50-80℃,优选压力为-0.09mpa≤压力≤-0.08mpa,优选干燥时间为6~18小时。所述n(2)-l-丙氨酰-l-谷氨酰胺湿品的减压干燥的第二阶段,为控制减压干燥条件压力范围为-0.09mpa≤压力≤-0.07mpa,干燥过程中可以补充空气,氮气,惰性气体(氦气,氩气),水蒸气(h2o↑)中的任意一种或以上两种气体或两种以上气体以任何比例混合的混合气体。进一步,所述n(2)-l-丙氨酰-l-谷氨酰胺湿品的减压干燥的第二阶段,为降低真空度(压力)所补充的气体,可以经过净化或无菌过滤处理。以符合国家法规及生产控制要求。所述n(2)-l-丙氨酰-l-谷氨酰胺湿品的减压干燥方法,可以应用于n(2)-l-丙氨酰-l-谷氨酰胺非无菌及无菌原料药的生产制造。与现有技术相比,本发明方案的技术优点体现在以下几个方面:1、本发明的关键之一在于,采用本发明方法制备获得的n(2)-l-丙氨酰-l-谷氨酰胺晶型b及晶型a,与现有技术提供的其它晶型相比,在流动性,堆密度,吸湿性方面具有显著的优势,尤其是获得的新晶型a,可以满足n(2)-l-丙氨酰-l-谷氨酰胺无菌原料药及其注射用n(2)-l-丙氨酰-l-谷氨酰胺无菌分装的要求。2、本发明的关键之二在于,转晶使用的n(2)-l-丙氨酰-l-谷氨酰胺湿品,只需要从含乙醇/水体系中结晶获得,无需对结晶条件进行苛刻限制。本发明人意外发现,干燥过程中存在晶型转变过程,与现有技术采用不同的结晶溶剂获得不同的晶型相比,本发明可以保持乙醇/水在n(2)-l-丙氨酰-l-谷氨酰胺结晶过程中的所有优势,同时可以克服由于采用乙醇/水结晶,后续处理比较容易获得共晶,产品有机残留不合格,澄清度不合格的技术缺陷。3、本发明的关键之三在于,本发明人利用n(2)-l-丙氨酰-l-谷氨酰胺湿品在干燥过程中意外发现的转晶现象,并进一步探究了转晶的影响因素及其本质,解决了现有技术采用乙醇/水结晶,经后续干燥处理。小试与工业化生产样品,批与批之间样品在晶型,样品关键质量指标等的差异性问题。本发明的关键之四在于,本发明提供了一种n(2)-l-丙氨酰-l-谷氨酰胺湿品的干燥工艺,相比较于现有技术提供的常压干燥,喷雾干燥等干燥工艺存在的干燥温度过高,需添加高沸点溶剂,需要手工翻料,易燃易爆等问题。本发明提供的干燥工艺工艺简单,温度较低,安全性好,无需人工翻料,工艺可控,重复性好,非常适于工业化自动化生产。以下具体实施例是为进一步阐述本发明,不应当被理解为是对本发明的限制。实施例中所涉及的x-ray粉末衍射和差示扫描量热测定及热重分析测试的仪器型号及测试条件中,涉及x-ray粉末衍射仪器型号及测试条件如下:实验仪器名称:荷兰帕纳科公司锐影x射线衍射仪(empyrean);x射线管:cu靶,ni滤波单色标识;x射线波长:测试样品形状:粉末;测试温度:室温;测试角度:5-50度;扫描速度:4°/min;扫描模式:选theta/2theta联动即可;扫描方式:continue;管压:40kv;管电流:16ma。涉及差示扫描量热测定(dsc)及热重分析(tg)仪器型号及测试条件如下:实验仪器名称:mettlertoledo1100lf测试条件:上限温度350℃;下限温度20℃;升温速率10℃/min。附图说明图1、3、5、7分别为实施例一至实施例四制备获得的n(2)-l-丙氨酰-l-谷氨酰胺晶型a的x-ray粉末衍射图谱图2、4、6、8分别为实施例一至实施例四制备获得的n(2)-l-丙氨酰-l-谷氨酰胺晶型a的差示扫描量热测定及热重分析图谱图9、11、13分别为实施例二至实施例四制备获得的n(2)-l-丙氨酰-l-谷氨酰胺晶型b的x-ray粉末衍射图谱图10、12、14分别为实施例二至实施例四制备获得的n(2)-l-丙氨酰-l-谷氨酰胺晶型b的差示扫描量热测定及热重分析图谱具体实施方式本发明所使用的n(2)-l-丙氨酰-l-谷氨酰胺湿品为从含乙醇/水体系结晶,经过滤或离心获得。具体可参考以下任一文献制备:[1]_cn101519428a、[2]_cn101062938a、[3]_cn1679531a、[4]_cn102698247a、[5]_organicprocessresearch&development(2000),4(3),147-152、[6]_王如帆.l-丙氨酰-l-谷氨酰胺结晶过程研究.天津大学硕士学位论文。实施例一将n(2)-l-丙氨酰-l-谷氨酰胺湿品30g平铺于玻璃表面皿中,放置于减压干燥箱内,控制温度60±2℃,真空度≥-0.096mpa,减压干燥2小时。然后升温至80±2℃,通过调节排空阀控制真空度-0.088mpa~-0.090mpa,减压干燥6小时,降至室温,出料得n(2)-l-丙氨酰-l-谷氨酰胺22.8g,乙醇残留:0.18%,干燥失重0.20%。x-ray粉末衍射和差示扫描量热测定及热重分析测试图谱分别见附图1和附图2。表1实施例一所得n(2)-l-丙氨酰-l-谷氨酰胺的x-ray粉末衍射特征吸收峰2θd-值i/io13.7636.4287100(1)18.7264.734646.0(4)19.6714.509241.5(5)20.7484.277590.3(2)21.3784.152950.3(3)22.5333.942621.9(8)24.1353.684417.7(10)25.4233.500524.1(7)27.6813.220021.2(9)34.8502.572228.5(6)实施例二在无菌条件下,将基于垂直物流系统所得n(2)-l-丙氨酰-l-谷氨酰胺结晶液经无菌级卧式刮刀离心机离心后所得湿品转入单锥干燥器中。开启搅拌,控制热水箱温度55±2℃,真空度≥-0.092mpa,减压干燥2小时。然后升温至65±2℃,通过调节进气阀门,通入氮气与水蒸气的混合物,控制真空度-0.084mpa~-0.088mpa,减压干燥13小时,关闭进气阀门,关闭热水泵。开启夹套循环水降温至25±2℃,关闭真空泵,排空,出料得n(2)-l-丙氨酰-l-谷氨酰胺186kg,乙醇残留:0.10%,干燥失重0.14%。x-ray粉末衍射和差示扫描量热测定及热重分析测试图谱分别见附图3、附图4、附图9和附图10。表2实施例二所得n(2)-l-丙氨酰-l-谷氨酰胺晶型a的x-ray粉末衍射特征吸收峰2θd-值i/io13.7106.4534100(1)18.6214.761145.3(3)19.5934.527017.8(7)20.6694.293867.8(2)21.3804.152625.3(5)22.4553.956118.4(6)24.0573.696212.6(10)25.4503.497014.6(8)27.6543.223013.0(9)34.8242.574125.9(4)实施例三将一般生产区离心所得n(2)-l-丙氨酰-l-谷氨酰胺湿品251kg投入双锥干燥器中。点动双锥,控制热水箱温度40±2℃,真空度≥-0.096mpa,减压干燥5小时。然后升温至85±2℃,通过调节排空阀门,控制真空度-0.085mpa~-0.090mpa,减压干燥8小时,关闭排空阀门,继续干燥2小时。关闭热水泵,开启夹套循环水降温至25±2℃,关闭真空泵,排空,出料得n(2)-l-丙氨酰-l-谷氨酰胺188kg,乙醇残留:0.04%,干燥失重0.09%.x-ray粉末衍射和差示扫描量热测定及热重分析测试图谱分别见附图5、附图6、附图11和附图12。表3实施例三所得n(2)-l-丙氨酰-l-谷氨酰胺晶型a的x-ray粉末衍射特征吸收峰2θd-值i/io13.7906.4164100(1)18.7524.728143.4(3)19.6984.503335.0(6)20.7234.282879.0(2)21.4584.137640.2(4)22.5343.942427.5(9)24.1103.688229.0(8)25.5543.483024.3(10)27.7343.213930.4(7)34.8772.570339.1(5)实施例四在无菌条件下,将基于垂直物流系统所得n(2)-l-丙氨酰-l-谷氨酰胺结晶液经无菌级卧式刮刀离心机离心后所得湿品转入单锥干燥器中。开启搅拌,控制热水箱温度45±2℃,真空度≥-0.094mpa,减压干燥3小时。然后升温至67±2℃,通过调节氮气(经无菌过滤)阀门,控制真空度-0.082mpa~-0.086mpa,减压干燥9小时,关闭氮气阀门,继续干燥2小时。关闭热水泵,开启夹套循环水降温至25±2℃,关闭真空泵,排空,出料得n(2)-l-丙氨酰-l-谷氨酰胺193kg,乙醇残留:0.08%,干燥失重0.12%.x-ray粉末衍射和差示扫描量热测定及热重分析测试图谱分别见附图7、附图8、附图13和附图14。表4实施例四所得n(2)-l-丙氨酰-l-谷氨酰胺晶型a的x-ray粉末衍射特征吸收峰2θd-值i/io13.6846.4656100(1)18.5944.767944.9(4)19.5414.539029.3(6)20.6424.299373.5(2)21.3264.162954.1(3)22.4023.965423.2(8)24.0053.704119.2(9)25.3973.504117.3(10)27.5763.231924.8(7)34.7462.579742.3(5)当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1